Biyoortogonal kimya - Bioorthogonal chemistry
Dönem biyoortogonal kimya herhangi birini ifade eder Kimyasal reaksiyon içinde meydana gelebilir yaşayan sistemler doğal biyokimyasal süreçlere müdahale etmeden.[1][2][3] Terim tarafından icat edildi Carolyn R. Bertozzi 2003'te.[4] Girişinden bu yana, biyoortogonal reaksiyon kavramı, aşağıdaki gibi biyomoleküllerin çalışılmasına olanak sağlamıştır. glikanlar, proteinler,[5] ve lipidler[6] hücresel toksisite olmaksızın canlı sistemlerde gerçek zamanlı olarak. Biyoortogonalite gereksinimlerini karşılayan bir dizi kimyasal ligasyon stratejisi geliştirilmiştir. 1,3-çift kutuplu döngü arasında azidler ve siklooktitler (ayrıca adlandırılır bakır içermeyen tıklama kimyası ),[7] arasında nitronlar ve siklooktitler,[8] oksim /hidrazon dan oluşumu aldehitler ve ketonlar,[9] tetrazin ligasyon[10] izosiyanür tabanlı tıklama tepkisi,[11] ve son zamanlarda, quadricyclane ligasyonu.[12]
Biyoortogonal kimyanın kullanımı tipik olarak iki adımda ilerler. İlk olarak, bir hücresel substrat, bir biyo-ortogonal fonksiyonel grupla (kimyasal raportör) modifiye edilir ve hücreye verilir; substratlar arasında metabolitler, enzim inhibitörleri, vb. yer alır. Kimyasal raportör, substratın biyolojik aktivitesini etkilemekten kaçınmak için substratın yapısını önemli ölçüde değiştirmemelidir. İkinci olarak, substratı reaksiyona sokmak ve etiketlemek için tamamlayıcı fonksiyonel grubu içeren bir sonda eklenir.
Bakır içermeyen tıklama kimyası gibi etkili biyo-ortogonal reaksiyonlar geliştirilmiş olmasına rağmen, yeni reaksiyonların geliştirilmesi, aynı biyosistemlerde birden fazla etiketleme yönteminin kullanılmasına izin vermek için etiketleme için ortogonal yöntemler üretmeye devam etmektedir.
Biyoortogonalite için gereksinimler
Biyoortogonal olarak kabul edilebilmesi için, bir reaksiyonun bir dizi gereksinimi karşılaması gerekir:
- Seçicilik: Biyolojik bileşiklerle yan reaksiyonlardan kaçınmak için reaksiyon, endojen fonksiyonel gruplar arasında seçici olmalıdır.
- Biyolojik inertlik: Reaktif partnerler ve sonuçta ortaya çıkan bağlantı, incelenen organizmanın doğal kimyasal işlevselliğini bozabilecek herhangi bir reaktivite moduna sahip olmamalıdır.
- Kimyasal inertlik: Kovalent bağ güçlü ve biyolojik reaksiyonlara karşı inert olmalıdır.
- Kinetik: Prob metabolizması ve klirensinden önce kovalent ligasyonun sağlanması için reaksiyon hızlı olmalıdır. Reaksiyon, daha az miktarda bulunan türlerin küçük sinyallerini azaltabilecek reaksiyonlarda rekabeti önlemek için hücresel işlemlerin zaman ölçeğinde (dakika) hızlı olmalıdır. Hızlı reaksiyonlar, dinamik süreçleri doğru bir şekilde izlemek için gerekli olan hızlı bir yanıt da sunar.
- Reaksiyon biyouyumluluğu: Reaksiyonlar toksik olmamalı ve pH, sulu ortamlar ve sıcaklık dikkate alınarak biyolojik koşullarda işlev görmelidir. Biyoortogonal kimya canlı hayvan modellerine genişledikçe, farmakokinetik artan bir endişe kaynağıdır.
- Erişilebilir mühendislik: Kimyasal haberci, bir tür metabolik veya protein mühendisliği yoluyla biyomoleküllere dahil edilebilmelidir. Optimal olarak, işlevsel gruplardan biri de çok küçüktür, böylece yerel davranışı bozmaz.
Staudinger ligasyonu
Staudinger ligasyonu 2000 yılında Bertozzi grubu tarafından geliştirilen ve klasiklere dayanan bir tepkidir. Staudinger reaksiyonu triarilfosfinli azidlerin.[13] Artık yaygın olarak kullanılmamasına rağmen, tamamen abiyotik fonksiyonel gruplarla ilk reaksiyon olarak biyoortogonal kimya alanını başlattı. Staudinger ligasyonu hem canlı hücrelerde hem de canlı farelerde kullanılmıştır.[4]
Biyoortogonalite
Azid, yumuşak elektrofil gibi yumuşak nükleofilleri tercih eden fosfinler. Bu, tipik olarak sert nükleofiller olan çoğu biyolojik nükleofilin tersidir. Reaksiyon, kararlı bir ürün üretmek için suya toleranslı koşullar altında seçici olarak ilerler.
Fosfinler canlı sistemlerde tamamen yoktur ve hafif indirgeme potansiyeline rağmen disülfür bağlarını azaltmaz. Azidlerin, azidotimidin gibi FDA onaylı ilaçlarda ve çapraz bağlayıcılar olarak diğer kullanımlar yoluyla biyolojik olarak uyumlu olduğu gösterilmiştir. Ek olarak, küçük boyutları, hücresel metabolik yollarla biyomoleküllere kolayca dahil edilmelerine izin verir.
Mekanizma
Bu bölüm Mayıs konudan sapmak makalenin. (2014 Eylül) |
Klasik Staudinger Reaksiyonu

Nükleofilik fosfin, azide elektrofilik terminal nitrojende saldırır. Dört üyeli bir geçiş durumu aracılığıyla, N2 bir aza-ilid oluşturmak için kaybolur. Kararsız ilide fosfin oksit ve bir birincil amin oluşturmak üzere hidrolize edilir. Bununla birlikte, bu reaksiyon hemen biyoortogonal değildir çünkü hidroliz, aza-iliddeki kovalent bağı kırar.
Staudinger Ligasyonu

Reaksiyon, lokal konsantrasyonu arttırmak için esteri konumlandırarak ani hidrolizi aşmak için aza-ylidi yeni bir reaktivite yolu boyunca yönlendirmek için aril halkalarından birinde fosfor atomuna orto bir ester grubu içerecek şekilde modifiye edildi. Azide ilk nükleofilik saldırı, hız sınırlayıcı adımdır. İlid, beş üyeli bir halka oluşturmak için molekül içi siklizasyon yoluyla elektrofilik ester tuzağı ile reaksiyona girer. Bu halka hidrolize uğrar ve kararlı bir amide bağ.
Sınırlamalar
Fosfin reaktifleri, canlı sistemlerde yavaşça hava oksidasyonuna uğrar. Ek olarak, metabolize olmaları muhtemeldir. laboratuvar ortamında tarafından sitokrom P450 enzimler.
Reaksiyonların kinetiği, ikinci derece hız sabitleri yaklaşık 0.0020 M ile yavaştır.−1• s−1. Fosfinlere elektron veren gruplar ekleyerek nükleofilik saldırı oranlarını artırma girişimleri kinetiği geliştirdi, ancak aynı zamanda hava oksidasyon oranını da artırdı.
Zayıf kinetikler, görüntüleme uygulamalarında yüksek arka plan sinyali ile sorunlara yol açan yüksek konsantrasyonlarda fosfin kullanılmasını gerektirir. Bir florojenik fosfin reaktiflerinin geliştirilmesi yoluyla yüksek arka plan sorunuyla mücadele etmek için girişimlerde bulunulmuştur. floresan ve lusiferin ama içsel kinetik bir sınırlama olarak kalır.[14]
Bakırsız tıklama kimyası
Bakır içermeyen tıklama kimyası ilk olarak Carolyn Bertozzi tarafından geliştirilmiş bir biyoortogonal reaksiyondur. azid alkin Huisgen cycloaddition tarafından yapılan çalışmaya göre Karl Barry Sharpless et al. CuAAC'den farklı olarak, Cu-free click kimyası, bir sitotoksik bakır katalizörü ortadan kaldırarak, reaksiyonun hızlı ve canlı hücre toksisitesi olmadan ilerlemesine izin vererek biyoortogonal olacak şekilde modifiye edilmiştir. Bakır yerine reaksiyon, suş destekli bir alkin-azid siklo-ilavedir (SPAAC). Staudinger ligasyonuna daha hızlı bir alternatif olarak geliştirildi ve ilk nesiller altmış katın üzerinde daha hızlı tepki verdi. Reaksiyonun inanılmaz biyo-ortogonalitesi, Cu içermeyen tıklama reaksiyonunun kültürlenmiş hücreler, canlı zebra balığı ve farelerde uygulanmasına izin verdi.

Bakır toksisitesi
Klasik bakırla katalize edilmiş azid-alkin siklokatlama, biyo-konjugasyon için son derece hızlı ve etkili bir tıklama reaksiyonu olmuştur, ancak Cu (I) iyonlarının toksisitesinden dolayı canlı hücrelerde kullanım için uygun değildir. Toksisite, bakır katalizörlerin oluşturduğu reaktif oksijen türlerinden kaynaklanan oksidatif hasara bağlıdır. Bakır komplekslerinin hücresel metabolizmada değişikliklere neden olduğu ve hücreler tarafından alındığı da bulunmuştur.
Biyomolekül hasarını önlemek ve bölgeden uzaklaştırmayı kolaylaştırmak için ligandlarda bazı gelişmeler olmuştur. laboratuvar ortamında uygulamalar. Bununla birlikte, komplekslerin farklı ligand ortamlarının, metabolizmayı ve alımı hala etkileyebildiği ve hücresel işlevde istenmeyen bir karışıklığa neden olduğu bulunmuştur.[15]
Biyoortogonalite
Azid grubu özellikle biyo-ortogonaldir çünkü son derece küçüktür (hücre geçirgenliği için elverişlidir ve pertürbasyonları önler), metabolik olarak stabildir ve hücrelerde doğal olarak mevcut değildir ve dolayısıyla rekabet eden biyolojik yan reaksiyonları yoktur. Azidler reaksiyon için mevcut en reaktif 1,3-dipol olmasalar da, tipik sentetik koşullarda görece yan reaksiyon eksiklikleri ve stabiliteleri nedeniyle tercih edilirler.[16] alkin kadar küçük değil, ancak yine de için gerekli olan kararlılık ve ortogonaliteye sahip in vivo etiketleme. Siklooktitler, en küçük kararlı alkin halkası oldukları için etiketleme çalışmaları için geleneksel olarak en yaygın sikloalkindir.
Mekanizma

Reaksiyon standart bir 1,3-dipolar siklo-katlama olarak ilerler, bir tür asenkron, uyumlu perisiklik vardiya. kararsız 1,3-dipolün doğası, azid üzerindeki bir elektrofilik veya nükleofilik merkezin tanımlanmasını imkansız hale getirmelidir, öyle ki döngüsel elektron akışının yönü anlamsızdır. [p] Ancak, hesaplama, nitrojenler arasındaki elektron dağılımının en içteki nitrojen atomunun en büyük negatif yükü taşımasına neden olduğunu göstermiştir.[17]
Bölge seçiciliği
Reaksiyon, triazollerin rejyoizomerik bir karışımını oluştursa da, bölge seçiciliği Tepki, çoğu güncel uygulama için büyük bir endişe değildir. Daha fazla bölgeye özgü ve daha az biyo-ortogonal gereksinimler, özellikle gergin bir siklooktin sentezlemesinin sentetik zorluğu (bir terminal alkin ilavesine kıyasla) göz önüne alındığında, bakırla katalize edilmiş Huisgen siklo katlama ile en iyi şekilde karşılanır.
Cyclooctynes Gelişimi
| Siklooktin | İkinci dereceden oran sabiti (M−1s−1) |
|---|---|
| OCT | 0.0024 |
| HDS | 0.0013 |
| MOFO | 0.0043 |
| DIFO | 0.076 |
| DIBO | 0.057 |
| BARAC | 0.96 |
| DIBAC (ADIBO) | 0.31 |
| DIMAC | 0.0030 |

OCT Cu içermeyen tıklama kimyası için geliştirilen ilk siklooktindir. Doğrusal alkinler fizyolojik sıcaklıklarda reaktif olmamakla birlikte, OCT hiçbir toksisite göstermezken biyolojik koşullarda azidlerle kolayca reaksiyona girebildi. Bununla birlikte, suda çözünürlüğü zayıftı ve kinetik, Staudinger ligasyonuna göre zar zor geliştirildi. HDS (arilsiz oktin) suda çözünürlüğü iyileştirmek için geliştirildi, ancak yine de zayıf kinetiğe sahipti.
Monoflorlu (MOFO) ve diflorlu (DIFO) siklooktiler, elektron çeken florin ikame edicilerinin eklenmesiyle oranı artırmak için oluşturuldu. proparjik durum. Flor sentetik erişilebilirlik ve biyolojik eylemsizlik açısından iyi bir elektron çekme grubudur. Özellikle elektrofilik oluşturamaz Michael alıcı biyolojik nükleofillerle yan reaksiyona girebilir.[7]DIBO (dibenzocyclooctyne), iki aril halkasına bir füzyon olarak geliştirildi ve çok yüksek gerilim ve bozulma enerjilerinde bir azalma ile sonuçlandı. Biaril ikamesinin halka suşunu arttırdığı ve reaktiviteyi iyileştirmek için alkin ile konjugasyon sağladığı öne sürüldü. Hesaplamalar, mono-aril ikamesinin sterik çatışma (azid molekülü ile) ve suş arasında optimal bir denge sağlayacağını tahmin etmesine rağmen,[18] monoarilatlı ürünlerin kararsız olduğu görülmüştür.
BARAC (biarylazacyclooctynone) ve ardından bir sp ekleyen bir amid bağı ilavesi2distorsiyonla oranı artırmak için benzeri merkez. Amide rezonans kararsız bir moleküle yol açacak ek doymamışlık yaratmadan ek suşa katkıda bulunur. Ek olarak, siklooktin halkasına bir heteroatomun eklenmesi molekülün hem çözünürlüğünü hem de farmakokinetiğini geliştirir. BARAC, arka planı azaltmak için fazla probu yıkamak gereksiz olduğu ölçüde yeterli hıza (ve hassasiyete) sahiptir. Bu, gerçek zamanlı görüntüleme veya tam hayvan görüntüleme gibi yıkamanın imkansız olduğu durumlarda son derece yararlıdır. BARAC son derece kullanışlı olmasına rağmen, düşük stabilitesi 0 ° C'de, ışık ve oksijenden korunarak saklanmasını gerektirir.[19]

BARAC'ta üretilecek diğer ayar varyasyonları DIBAC / ADIBO reaktiviteyi daha da artırmak için distal halka suşu eklemek ve alkin çevresindeki sterikleri azaltmak için yapıldı. Hidroksil grubunun bir ketona dönüştürüldüğü Keto-DIBO, halka konformasyonundaki bir değişiklik nedeniyle hızda üç kat artışa sahiptir. Diflorobenzocyclooctyne yapma girişimleri (DIFBO) istikrarsızlık nedeniyle başarısız oldu.
DIFO ile ilgili sorunlar in vivo fare çalışmaları, biyoortogonal reaksiyonlar üretmenin zorluğunu göstermektedir. DIFO, hücrelerin etiketlenmesinde son derece reaktif olmasına rağmen, seruma bağlanması nedeniyle fare çalışmalarında zayıf performans gösterdi. albümin. Siklooktinin hidrofobikliği, membranlar ve serum proteinleri tarafından sekestrasyonu teşvik ederek biyolojik olarak kullanılabilir konsantrasyonları azaltır. Cevap olarak, DIMAC (dimethoxyazacyclooctyne) suda çözünürlüğü, polariteyi ve farmakokinetiği artırmak için geliştirilmiştir,[20] fare modellerinin biyo-ortogonal etiketlenmesine yönelik çabalar hala geliştirme aşamasındadır.
Reaktivite
Reaksiyonu iyileştirmeye devam etmede hayati bir rol oynayan bu döngüsel katılma reaksiyonlarının termodinamiğini ve kinetiğini açıklamada hesaplama çabaları hayati önem taşımaktadır. Alkinleri stabiliteden ödün vermeden aktive etmenin iki yöntemi vardır: geçiş durumu enerjisini düşürmek veya reaktan stabilitesini azaltmak.

Azalan reaktan stabilitesi: Houk [21] enerjideki farklılıkların (Ed ‡) azit ve alkin'i, geçiş durumu geometrilerine dönüştürmek için gerekli olan reaksiyon için bariyer yüksekliklerini kontrol eder. Aktivasyon enerjisi (E ‡) istikrarsızlaştırıcı çarpıklıkların ve dengeleyici etkileşimlerin toplamıdır (Eben ‡). En önemli distorsiyon, alkin distorsiyonunun daha az katkısı olan azid fonksiyonel grubundadır. Bununla birlikte, daha yüksek reaktivite için kolayca modifiye edilebilen sadece siklooktindir. Fenil azit için hesaplanan reaksiyon engelleri ve asetilen (16,2 kcal / mol) ile siklooktin (8,0 kcal / mol), 10'luk bir öngörülen hız artışı ile sonuçlanır.6. Siklooktin daha az distorsiyon enerjisi gerektirir (1,4 kcal / mol'e karşı 4,6 kcal / mol), daha küçük etkileşim enerjisine rağmen daha düşük aktivasyon enerjisi ile sonuçlanır.

Azalan geçiş durumu enerjisi: Flor gibi elektron çeken gruplar azalarak oranını artırır LUMO enerji ve HOMO-LUMO boşluğu. Bu, geçiş durumunda azidden florlanmış siklooktine daha büyük bir yük transferine, artan etkileşim enerjisine (daha düşük negatif değer) ve genel aktivasyon enerjisine yol açar.[22] LUMO'nun düşürülmesi sonucu hiperkonjugasyon alkin π verici orbitalleri ve CF σ * alıcıları arasında. Bu etkileşimler, tahvillerin bozuldukça artan verici / alıcı yeteneklerinin bir sonucu olarak öncelikle geçiş durumunda istikrar sağlar. NBO hesaplamaları, geçiş durumu distorsiyonunun etkileşim enerjisini 2.8 kcal / mol artırdığını göstermiştir.
Düzlem dışı π bağları arasındaki hiperkonjugasyon daha büyüktür çünkü düzlem içi π bağları zayıf bir şekilde hizalanmıştır. Bununla birlikte, geçiş durumu eğilmesi, düzlem içi π bağlarının etkileşimi kolaylaştıran daha ters düzlemsel bir düzenlemeye sahip olmasına izin verir. Ek hiper-konjügatif etkileşim enerjisi stabilizasyonu, oluşan CN bağı nedeniyle σ * elektronik popülasyonundaki bir artışla elde edilir. Σ * CF bağlarıyla negatif hiperkonjugasyon, bu stabilize edici etkileşimi artırır.[17]
Bölge seçiciliği
olmasına rağmen bölge seçiciliği bakırsız tıklama kimyasının mevcut görüntüleme uygulamalarında büyük bir sorun değil, ilaç tasarımı veya peptidomimetik gibi alanlarda gelecekteki uygulamaları engelleyen bir sorundur.[23]
Şu anda çoğu siklooktit, rejyoizomerik karışımlar oluşturmak için reaksiyona girer. [m] Hesaplama analizi, gaz fazı bölgesel seçiciliğinin, aktivasyon enerjisinde 2,9 kcal / mol'e kadar 1,4 ilaveye göre 1,5 eklemeyi tercih edecek şekilde hesaplanırken, çözme düzeltmelerinin her iki rejyoizomer için aynı enerji bariyerleri ile sonuçlandığını bulmuştur. DIFO'nun siklo-ilavesindeki 1,4 izomer, daha büyük dipol momenti tarafından beğenilmezken, solvasyon onu 1,5 izomerden daha güçlü bir şekilde stabilize ederek bölge seçiciliğini aşındırır.[22]

Gibi simetrik sikloositler BCN (bisiklo [6.1.0] nonyne) siklo ilave üzerine tek bir bölge izomer oluşturur[24] ve gelecekte bu sorunu çözmeye hizmet edebilir.
Başvurular
Bakır içermeyen tıklama kimyasının en yaygın uygulaması, azid etiketli bir biyomolekül ve bir görüntüleme ajanı taşıyan bir siklooktin kullanılarak canlı hücrelerde veya hayvanlarda biyolojik görüntülemedir.
DIBO'nun floresan keto ve oksim varyantları, siklooktinin floresansının reaksiyonda oluşan triazol tarafından söndürüldüğü floro-anahtar tıklama reaksiyonlarında kullanılır.[25] Öte yandan, kumarinle konjuge sikloositler coumBARAC Alkin floresanı bastırırken triazol oluşumu floresansı artıracak şekilde geliştirilmiştir. kuantum verimi on kat.[26]

Substrat etiketlemesinin uzaysal ve zamansal kontrolü, foto-aktifleştirilebilir siklooktiler kullanılarak araştırılmıştır. Bu, konsantrasyon gradyanlarının bir sonucu olarak artefaktları azaltmak için reaksiyondan önce alkin dengesine izin verir. Maskeli sikloositler karanlıkta azidlerle reaksiyona giremez, ancak ışıkla ışınlandığında reaktif alkinler haline gelir.[27]

Bakır içermeyen tıklama kimyası sentezlemede kullanılmak üzere araştırılıyor PET görüntüleme bileşikler uygulanmadan önce izotopik bozunmayı en aza indirmek için hızlı bir şekilde yüksek saflıkta ve verimde yapılması gereken maddeler. SPAAC'ın hem yüksek oran sabitleri hem de biyo-ortogonalitesi PET kimyasına uygundur.[28]
Diğer bioorthogonal reaksiyonlar
Nitron dipol siklo ilave
Bakır içermeyen tıklama kimyası, nitronları azidler yerine 1,3-dipol olarak kullanmak üzere uyarlanmıştır ve peptidlerin modifikasyonunda kullanılmıştır.[8]

Bir nitron ve bir siklooktin arasındaki bu siklo-ekleme, N-alkile edilmiş izoksazolinleri oluşturur. Reaksiyon hızı suyla artar ve 12 ila 32 M arasında değişen ikinci dereceden hız sabitleriyle son derece hızlıdır.−1• s−1nitronun ikamesine bağlı olarak. Reaksiyon son derece hızlı olmasına rağmen, nitronun metabolik etiketleme yoluyla biyomoleküllere dahil edilmesinde sorunlarla karşılaşır. Etiketleme, yalnızca translasyon sonrası peptid modifikasyonu yoluyla elde edilmiştir.
Norbornene siklo katılma
1,3-dipol olarak bir nitril oksit kullanarak bir biyo-ortogonal reaksiyon olarak 1,3 dipolar siklo-ilaveler geliştirilmiştir ve Norbornene bir dipolarofil olarak. Birincil kullanımı, otomatik oligonükleotid sentezleyicilerinde DNA ve RNA'nın etiketlenmesidir.[29]

Norbornenler, suşun teşvik ettiği reaktivite ve stabilite arasındaki dengeleri nedeniyle dipolarofiller olarak seçildi. Bu reaksiyonun dezavantajları, nitril oksidin güçlü elektrofilisite ve yavaş reaksiyon kinetiğine bağlı çapraz reaktivitesini içerir.
Oksanorbornadien siklo katılma
Oxanorbornadiene siklokatlama 1,3-çift kutuplu bir siklokasyondur ve bunu bir retro-Diels Kızılağaç bir triazole bağlı bir konjugat oluşturmak için reaksiyon ile bir Furan molekül.[30] Ön çalışma, peptid etiketleme deneylerinde yararlılığını ortaya koymuştur ve ayrıca üretilmesinde de kullanılmıştır. SPECT görüntüleme bileşikleri.[31] Daha yakın zamanlarda, bir oksanorbornadienin kullanımı, biyoortogonal reaksiyonlara yeni bir yaklaşımda, bir model amino asidin metal kısma bağlandığı, katalizörsüz bir oda sıcaklığında "iClick" reaksiyonunda tarif edilmiştir.[32]

Oksanorbornadien'deki halka suşu ve elektron eksikliği, siklo katma hızı sınırlama adımına doğru reaktiviteyi artırır. Retro-Diels Alder reaksiyonu, kararlı 1,2,3 triazol oluşturmak için daha sonra hızla gerçekleşir. Sorunlar arasında, oksanorbornadienin elektroniğini değiştirebilen ikame ediciler için zayıf tolerans ve düşük oranlar (10 mertebesinde ikinci dereceden hız sabitleri) bulunmaktadır.−4).
Tetrazin ligasyonu
tetrazin ligasyonu bir trans-siklooktenin reaksiyonu ve bir s-tetrazin ters talepli bir Diels Alder reaksiyonunda ve ardından nitrojen gazını ortadan kaldırmak için bir retro-Diels Alder reaksiyonunda.[33] Reaksiyon, ikinci derece hız sabiti 2000 M ile son derece hızlıdır.−1–S−1 (9: 1 metanol / su içinde) biyomoleküllerin son derece düşük konsantrasyonlarda modifikasyonuna izin verir.

Bach'ın hesaplamalı çalışmasına dayanarak, Z-siklooktenler için gerinim enerjisi, iki transannüler etkileşim kaybından dolayı siklooktan için 12.4 kcal / mol ile karşılaştırıldığında 7.0 kcal / mol'dür. E-siklookten, oldukça bükülmüş bir çift bağa sahiptir ve 17.9 kcal / mol'lük bir gerinim enerjisi ile sonuçlanır.[34] Bu nedenle, yüksek derecede gergin trans-siklookten, reaktif olarak kullanılır. dienofil. Dien suyla ani reaksiyona direnmek için ikame edilmiş bir 3,6-diaril-s-tetrazindir. Reaksiyon, N2 ve reaksiyonun tersine çevrilebilirliğini önler.[10]
Suya sadece reaksiyon toleranslı olmakla kalmaz, sulu ortamda hızın arttığı da bulunmuştur. Reaksiyonlar ayrıca 1 M düzeyinde ikinci dereceden oranlarda dienofiller olarak norbornenler kullanılarak gerçekleştirilmiştir.−1• s−1 sulu ortamda. Reaksiyon, canlı hücrelerin etiketlenmesinde uygulandı[35] ve polimer birleştirme.[36]
[4 + 1] Çevrimsel yükleme
Bu izosiyanür tıklama reaksiyonu bir [4 + 1] siklo-katma ve ardından N'nin retro-Diels Alder eliminasyonu2.[11]

Reaksiyon, bir başlangıç [4 + 1] siklo-katma ve ardından bir termodinamik çukuru ortadan kaldırmak ve tersinirliği önlemek için bir ters çevirme ile devam eder. Üçüncül bir amin veya izosiyanopropanoat kullanılırsa bu ürün stabildir. İkincil veya birincil bir izosiyanür kullanılırsa, ürün bir imine etmek hızla hidrolize olur.
İzosiyanür, küçük boyutu, stabilitesi, toksik olmaması ve memeli sistemlerinde bulunmaması nedeniyle tercih edilen bir kimyasal raportördür. Bununla birlikte, reaksiyon yavaştır, ikinci dereceden hız sabitleri 10 mertebesindedir.−2 M−1• s−1.
Tetrazol fotoclick kimyası
Photoclick kimyası, N'yi serbest bırakmak için foto indüklenmiş bir sikloreversion kullanır.2. Bu, nitrojen gazı kaybı yoluyla kısa ömürlü bir 1,3 nitril imin ara ürünü üretir ve bu, pirazolin sikloaddüktleri oluşturmak için bir alken ile 1,3-dipolar siklo-eklemeye maruz kalır.[11]

Fotoindüksiyon, hücrelere foton zararını en aza indirmek için kısa bir süre ışığa maruz bırakılarak (dalga boyu tetrazole bağlıdır) gerçekleşir. Reaksiyon sulu koşullarda geliştirilir ve tek bir rejyoizomer oluşturur.
Geçici nitril imin, distorsiyon enerjisini azaltan bükülmüş bir yapı nedeniyle 1,3-dipolar siklokatlama için oldukça reaktiftir. Fenil halkalarında elektron veren gruplarla ikame, 1,3 nitril imine yerleştirildiğinde HOMO enerjisini artırır ve reaksiyon hızını artırır.
Bu yaklaşımın avantajları arasında, reaksiyonu uzaysal veya zamansal olarak kontrol etme yeteneği ve hem alkenleri hem de tetrazolleri, genetik kodlama gibi basit biyolojik yöntemler kullanılarak biyomoleküllere dahil etme yeteneği yer alır.[37] Ek olarak, reaksiyonun ilerleyişini izlemek için tetrazol florojenik olacak şekilde tasarlanabilir.[38]
Quadricyclane ligasyonu
quadricyclane ligasyonu π sistemleri ile [2 + 2 + 2] döngüsel yüke tabi tutulması için oldukça gergin bir dört tekerlekli uçağı kullanır.[12]
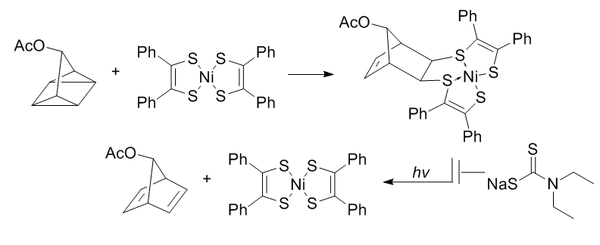
Quadricyclane abiyotiktir, biyomoleküllerle reaktif değildir (tam doygunluk nedeniyle), nispeten küçük ve oldukça gergindir (~ 80 kcal / mol). Bununla birlikte, oda sıcaklığında ve fizyolojik pH'ta sulu koşullarda oldukça kararlıdır. Seçici olarak elektron açısından fakir π sistemleriyle reaksiyona girebilir ancak basit alkenler, alkinler veya siklooktinler ile reaksiyona giremez.
Bis (ditiobenzil) nikel (II), reaktiviteye dayalı bir aday ekrandan bir reaksiyon ortağı olarak seçildi. Norbornadiene ışığın neden olduğu dönüşümü önlemek için, üründeki nikeli şelatlamak için dietilditiokarbamat eklenir.

Bu reaksiyonlar, 0.25 M'lik ikinci dereceden hız sabiti ile sulu koşullar ile güçlendirilir.−1• s−1. Özellikle ilgi çekici olan, hem oksim oluşumu hem de bakır içermeyen klik kimyası için biyo-ortogonal olduğunun kanıtlanmış olmasıdır.
Kullanımlar
Biyoortogonal kimya, aşağıdaki ülkelerde ön hedefleme deneyleri için çekici bir araçtır. nükleer görüntüleme ve radyoterapi.[39]
Referanslar
- ^ Sletten, Ellen M .; Bertozzi Carolyn R. (2009). "Biyoortogonal Kimya: İşlevsellik Denizinde Seçicilik için Balıkçılık". Angewandte Chemie Uluslararası Sürümü. 48 (38): 6974–98. doi:10.1002 / anie.200900942. PMC 2864149. PMID 19714693.
- ^ Prescher, Jennifer A .; Dube, Danielle H .; Bertozzi Carolyn R. (2004). "Canlı hayvanlarda hücre yüzeylerinin kimyasal olarak yeniden şekillenmesi". Doğa. 430 (7002): 873–7. Bibcode:2004Natur.430..873P. doi:10.1038 / nature02791. PMID 15318217. S2CID 4371934.
- ^ Prescher, Jennifer A; Bertozzi, Carolyn R (2005). "Canlı sistemlerde kimya". Doğa Kimyasal Biyoloji. 1 (1): 13–21. doi:10.1038 / nchembio0605-13. PMID 16407987. S2CID 40548615.
- ^ a b Sletten, Ellen M .; Bertozzi Carolyn R. (2011). "Mekanizmadan Fareye: İki Biyoortogonal Reaksiyonun Hikayesi". Kimyasal Araştırma Hesapları. 44 (9): 666–676. doi:10.1021 / ar200148z. PMC 3184615. PMID 21838330.
- ^ Plass, Tilman; Milles, Sigrid; Koehler, Christine; Schultz, Carsten; Lemke, Edward A. (2011). "Genetik Olarak Kodlanmış Bakır İçermeyen Tıklama Kimyası". Angewandte Chemie Uluslararası Sürümü. 50 (17): 3878–3881. doi:10.1002 / anie.201008178. PMC 3210829. PMID 21433234.
- ^ Neef, Anne B .; Schultz, Carsten (2009). "Canlı Hücrelerde Lipitlerin Seçici Floresan Etiketlemesi". Angewandte Chemie Uluslararası Sürümü. 48 (8): 1498–500. doi:10.1002 / anie.200805507. PMID 19145623.
- ^ a b Baskin, J. M .; Prescher, J. A .; Laughlin, S. T .; Agard, N. J .; Chang, P. V .; Miller, I. A .; Lo, A .; Codelli, J. A .; Bertozzi, C.R. (2007). "Dinamik in vivo görüntüleme için bakır içermeyen tıklama kimyası". Ulusal Bilimler Akademisi Bildiriler Kitabı. 104 (43): 16793–7. Bibcode:2007PNAS..10416793B. doi:10.1073 / pnas.0707090104. PMC 2040404. PMID 17942682.
- ^ a b Ning, Xinghai; Temming, Rinske P .; Dommerholt, Ocak; Guo, Jun; Blanco-Ania, Daniel; Borçlar, Marjoke F .; Wolfert, Margreet A .; Boons, Geert-Jan; Van Delft, Floris L. (2010). "Gerilim Destekli Alkin-Nitron Siklokatlama ile Protein Modifikasyonu". Angewandte Chemie Uluslararası Sürümü. 49 (17): 3065–8. doi:10.1002 / anie.201000408. PMC 2871956. PMID 20333639.
- ^ Yarema, K. J .; Mahal, LK; Bruehl, RE; Rodriguez, EC; Bertozzi, CR (1998). "Keton Gruplarının Sialik Asit Kalıntılarına Metabolik Taşınması. HÜCRE YÜZEY GLYCOFORM MÜHENDİSLİĞİNE UYGULAMA". Biyolojik Kimya Dergisi. 273 (47): 31168–79. doi:10.1074 / jbc.273.47.31168. PMID 9813021.
- ^ a b Blackman, Melissa L .; Royzen, Maksim; Tilki Joseph M. (2008). "Tetrazin Ligasyonu: Ters elektron talepli Diels-Alder Reaktivitesine dayalı Hızlı Biyokonjugasyon". Amerikan Kimya Derneği Dergisi. 130 (41): 13518–9. doi:10.1021 / ja8053805. PMC 2653060. PMID 18798613.
- ^ a b c Stöckmann, Henning; Neves, André A .; Merdivenler, Shaun; Brindle, Kevin M .; Leeper, Finian J. (2011). "Biyomoleküllerle ligasyon için izonitril bazlı tıklama kimyasını keşfetme". Organik ve Biyomoleküler Kimya. 9 (21): 7303–5. doi:10.1039 / C1OB06424J. PMID 21915395.
- ^ a b Sletten, Ellen M .; Bertozzi Carolyn R. (2011). "Bioorthogonal Quadricyclane Ligasyonu". Amerikan Kimya Derneği Dergisi. 133 (44): 17570–3. doi:10.1021 / ja2072934. PMC 3206493. PMID 21962173.
- ^ Saxon, E .; Bertozzi, CR (2000). "Modifiye Staudinger Reaksiyonu ile Hücre Yüzey Mühendisliği". Bilim. 287 (5460): 2007–10. Bibcode:2000Sci ... 287.2007S. doi:10.1126 / science.287.5460.2007. PMID 10720325. S2CID 19720277.
- ^ Pamela, Chang .; Prescher, Jennifer A .; Hangauer, Matthew J .; Bertozzi Carolyn R. (2008). "Biyoortogonal Kimyasal Raporlayıcılarla Hücre Yüzeyi Glikanlarını Görüntüleme". J Am Chem Soc. 129 (27): 8400–8401. doi:10.1021 / ja070238o. PMC 2535820. PMID 17579403.
- ^ Kennedy, David C .; McKay, Craig S .; Legault, Marc C. B .; Danielson, Dana C .; Blake, Jessie A .; Pegoraro, Adrian F .; Stolow, Albert; Mester, Zoltan; Pezacki, John Paul (2011). "Biyoortogonal Tıklama Reaksiyonlarını Katalize Etmek İçin Kullanılan Bakır Komplekslerinin Hücresel Sonuçları". Amerikan Kimya Derneği Dergisi. 133 (44): 17993–8001. doi:10.1021 / ja2083027. PMID 21970470.
- ^ Huisgen, Rolf. (1976). "1,3-Dipolar siklokatlanmalar. 76. 1,3-dipolar siklo-ilavelerin uyumlu doğası ve diradikal ara maddeler sorunu". Organik Kimya Dergisi. 41 (3): 403–419. doi:10.1021 / jo00865a001.
- ^ a b Altın, Brian; Shevchenko, Nikolay E .; Bonus, Natalie; Dudley, Gregory B .; Alabugin, Igor V. (2011). "Hiperkonjügatif ve Eşlenik Yardım yoluyla Seçici Geçiş Durumu Stabilizasyonu: Bakırsız Click Kimyası için Stereoelektronik Konsept". Organik Kimya Dergisi. 77 (1): 75–89. doi:10.1021 / jo201434w. PMID 22077877.
- ^ Chenoweth, Kimberly; Chenoweth, David; Goddard Iii, William A. (2009). "Katalize edilmemiş tıklama kimyası için siklooktin bazlı reaktifler: Hesaplamalı bir anket" (PDF). Organik ve Biyomoleküler Kimya. 7 (24): 5255–8. doi:10.1039 / B911482C. PMID 20024122.
- ^ Jewett, John C .; Sletten, Ellen M .; Bertozzi, Carolyn R. (2010). "Kolayca Sentezlenen Biarilazasiklooktinonlarla Hızlı Cu İçermeyen Click Kimyası". Amerikan Kimya Derneği Dergisi. 132 (11): 3688–90. doi:10.1021 / ja100014q. PMC 2840677. PMID 20187640.
- ^ Sletten, Ellen M .; Bertozzi Carolyn R. (2008). "Cu İçermeyen Tıklama Kimyası için Hidrofilik Bir Azasiklooktin". Organik Harfler. 10 (14): 3097–9. doi:10.1021 / ol801141k. PMC 2664610. PMID 18549231.
- ^ Ess, Daniel H .; Jones, Gavin O .; Houk, K.N (2008). "Gerilim Destekli Metal İçermeyen Klik Kimyasının Geçiş Durumları: Fenil Azit ve Siklooktilerin 1,3-Dipolar Döngü Koşulları". Organik Harfler. 10 (8): 1633–6. doi:10.1021 / ol8003657. PMID 18363405.
- ^ a b Schoenebeck, Franziska; Ess, Daniel H .; Jones, Gavin O .; Houk, K.N (2009). "Azitlerin Gerilmiş Alkinlere ve Alkenlere 1,3-Dipolar Döngüsel Koşullarında Reaktivite ve Regioseçicilik: Hesaplamalı Bir Çalışma". Amerikan Kimya Derneği Dergisi. 131 (23): 8121–33. doi:10.1021 / ja9003624. PMID 19459632.
- ^ Lutz, Jean-François (2008). "Bakır İçermeyen Azide Alkyne Cycloadditions: Yeni Görüşler ve Perspektifler". Angewandte Chemie Uluslararası Sürümü. 47 (12): 2182–4. doi:10.1002 / anie.200705365. PMID 18264961.
- ^ Dommerholt, Ocak; Schmidt, Samuel; Temming, Rinske; Hendriks, Linda J. A .; Rutjes, Floris P. J. T .; Van Hest, Jan C. M .; Lefeber, Dirk J .; Friedl, Peter; Van Delft, Floris L. (2010). "Biyoortogonal Etiketleme ve Canlı Hücrelerin Üç Boyutlu Görüntülenmesi için Kolayca Erişilebilen Bisiklononinler". Angewandte Chemie Uluslararası Sürümü. 49 (49): 9422–5. doi:10.1002 / anie.201003761. PMC 3021724. PMID 20857472.
- ^ Mbua, Ngalle Eric; Guo, Jun; Wolfert, Margreet A .; Steet, Richard; Boons, Geert-Ocak (2011). "Gerilme Destekli Alkin-Azid Siklokasyonları (SPAAC) Glikokonjugat Biyosentezinin Yeni Özelliklerini Ortaya Çıkarıyor". ChemBioChem. 12 (12): 1912–21. doi:10.1002 / cbic.201100117. PMC 3151320. PMID 21661087.
- ^ Jewett, John C .; Bertozzi Carolyn R. (2011). "Cu içermeyen klik kimyası ile aktive edilen florojenik bir siklooktinin sentezi". Organik Harfler. 13 (22): 5937–9. doi:10.1021 / ol2025026. PMC 3219546. PMID 22029411.
- ^ Polukhtine, Andrei A .; Mbua, Ngalle Eric; Wolfert, Margreet A .; Boons, Geert-Jan; Popik, Vladimir V. (2009). "Canlı Hücrelerin Fotoğrafla Tetiklenen Tıklama Reaksiyonu ile Seçmeli Etiketlenmesi". Amerikan Kimya Derneği Dergisi. 131 (43): 15769–76. doi:10.1021 / ja9054096. PMC 2776736. PMID 19860481.
- ^ Carpenter, Richard D .; Hausner, Sven H .; Sutcliffe, Julie L. (2011). "PET için Bakır İçermeyen Tıklama: Bir Flor-18 Siklooktin ile Hızlı 1,3-Dipolar Döngü Koşulları". ACS Tıbbi Kimya Mektupları. 2 (12): 885–889. doi:10.1021 / ml200187j. PMC 4018166. PMID 24900276.
- ^ Gutsmiedl, Katrin; Wirges, Christian T .; Ehmke, Veronika; Carell, Thomas (2009). "Bakır İçermeyen" Tıklayın "Nitril Oksit Norbornen 1,3-Dipolar Döngüleme Yoluyla DNA Modifikasyonu". Organik Harfler. 11 (11): 2405–8. doi:10.1021 / ol9005322. PMID 19405510.
- ^ Van Berkel, Sander S .; Dirks, A. (Ton) J .; Borçlar, Marjoke F .; Van Delft, Floris L .; Cornelissen, Jeroen J. L. M .; Nolte, Roeland J. M .; Rutjes, Floris P.J.T (2007). "Biyokonjugasyon Aracı Olarak Metal İçermeyen Triazol Oluşumu". ChemBioChem. 8 (13): 1504–8. doi:10.1002 / cbic.200700278. PMID 17631666.
- ^ Van Berkel, Sander S .; Dirks, A. (Ton) J .; Meeuwissen, Silvie A .; Pingen, Dennis L. L .; Boerman, Otto C .; Laverman, Peter; Van Delft, Floris L .; Cornelissen, Jeroen J. L. M .; Rutjes, Floris P.J.T (2008). "Siklik RGD DTPA Konjugatlarının Sentezinde Metalsiz Triazol Oluşumunun Uygulanması". ChemBioChem. 9 (11): 1805–15. doi:10.1002 / cbic.200800074. PMID 18623291.
- ^ Henry, Lucas; Schneider, Christopher; Mützel, Benedict; Simpson, Peter V .; Nagel, Christoph; Kahretsin, Katharina; Schatzschneider, Ulrich (2014). "Oksanorbornadien maskeli bir alkin ile MnI (bpy) (CO) 3 koordinatlı azitin iClick reaksiyonu yoluyla amino asit biyokonjugasyonu" (PDF). ChemComm. 50 (99): 15692–95. doi:10.1039 / C4CC07892F. PMID 25370120.
- ^ Row, R. David; Prescher, Jennifer A. (2016). "Tetrazin Noktayı İşaretler". ACS Merkez Bilimi. 2 (8): 493–494. doi:10.1021 / acscentsci.6b00204. PMC 4999966. PMID 27610408.
- ^ Bach, Robert D. (2009). "Siklooktil Sisteminde Halka Gerinim Enerjisi. Gerinim Enerjisinin Azidlerle [3 + 2] Devir Katılma Tepkimelerine Etkisi". Amerikan Kimya Derneği Dergisi. 131 (14): 5233–43. doi:10.1021 / ja8094137. PMID 19301865.
- ^ Devaraj, Neal K .; Weissleder, Ralph; Hilderbrand, Scott A. (2008). "Tetrazin Tabanlı Döngüsel Koşullar: Ön Hedefli Canlı Hücre Görüntülemesine Uygulama". Biyokonjugat Kimyası. 19 (12): 2297–9. doi:10.1021 / bc8004446. PMC 2677645. PMID 19053305.
- ^ Hansell, Claire F .; Espeel, Pieter; Stamenovic, Milan M .; Barker, Ian A .; Dove, Andrew P .; Du Prez, Filip E .; o Reilly, Rachel K. (2011). "Tetrazin Norbornene Chemistry ile Polimer İşlevselleştirme ve Bağlama için Katkısız Tıklama". Amerikan Kimya Derneği Dergisi. 133 (35): 13828–31. doi:10.1021 / ja203957h. PMID 21819063.
- ^ Lim, Reyna K. V .; Lin, Qing (2011). "Işıkla indüklenebilir Biyoortogonal Kimya: Canlı Hücrelerdeki Proteinleri Görselleştirmek ve Perturb Etmek İçin Uzamsal Olarak Kontrol Edilebilir Bir Araç". Kimyasal Araştırma Hesapları. 44 (9): 828–839. doi:10.1021 / ar200021p. PMC 3175026. PMID 21609129.
- ^ Song, Wenjiao; Wang, Yizhong; Qu, Jun; Lin, Qing (2008). "Genetik Olarak Kodlanmış Alken İçeren Proteinin Bakteriyel Hücrelerde" Fotoklik Kimyası "Yoluyla Seçici İşlevselleştirilmesi". Amerikan Kimya Derneği Dergisi. 130 (30): 9654–5. doi:10.1021 / ja803598e. PMID 18593155.
- ^ Knight, James C .; Cornelissen, Bart (2014). "Biyo-ortogonal kimya: ön hedefli nükleer (PET / SPECT) görüntüleme ve tedavi için çıkarımlar". Amerikan Nükleer Tıp ve Moleküler Görüntüleme Dergisi. 4 (2): 96–113. ISSN 2160-8407. PMC 3992206. PMID 24753979.
