DPPH - DPPH
 | |
 | |
| İsimler | |
|---|---|
| IUPAC adı di (fenil) - (2,4,6-trinitrofenil) iminoazanyum | |
| Diğer isimler 2,2-difenil-1-pikrilhidrazil 1,1-difenil-2-pikrilhidrazil radikali 2,2-difenil-1- (2,4,6-trinitrofenil) hidrazil Difenilpikrilhidrazil | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| Kısaltmalar | DPPH |
| ChemSpider | |
| ECHA Bilgi Kartı | 100.015.993 |
PubChem Müşteri Kimliği | |
| UNII | |
CompTox Kontrol Paneli (EPA) | |
| |
| |
| Özellikleri | |
| C18H12N5Ö6 | |
| Molar kütle | 394,32 g / mol |
| Görünüm | Siyahtan yeşile toz, çözelti içinde mor |
| Yoğunluk | 1,4 g / cm3 |
| Erime noktası | 135 ° C (275 ° F; 408 K) (ayrışır) |
| çözülmez | |
| Çözünürlük içinde metanol | 10 mg / mL |
| Tehlikeler | |
| Güvenlik Bilgi Formu | MSDS |
| NFPA 704 (ateş elması) | |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
DPPH organik için yaygın bir kısaltmadır kimyasal bileşik 2,2-difenil-1-pikrilhidrazil. Kararlı, koyu renkli kristal bir tozdur. serbest radikal moleküller. DPPH'nin her ikisi de laboratuar araştırmalarında iki ana uygulaması vardır: Birincisi, radikalleri içeren kimyasal reaksiyonların izlenmesi, en önemlisi de yaygın antioksidan tahlil[1] ve diğeri, konum ve yoğunluğunun bir standardıdır elektron paramanyetik rezonans sinyaller.
Özellikler ve uygulamalar
DPPH, kafes simetrisi ile farklılık gösteren birkaç kristal formuna sahiptir ve erime noktası (m.p.). Ticari toz, ~ 130 ° C'de eriyen bir faz karışımıdır. DPPH-I (m.p. 106 ° C) ortorombik, DPPH-II (m.p. 137 ° C) şekilsizdir ve DPPH-III (m.p. 128–129 ° C) triklinik.[2]
DPPH, iyi bilinen bir radikal ve diğer radikaller için bir tuzaktır ("çöpçü"). Bu nedenle, DPPH eklendikten sonra bir kimyasal reaksiyonun hız azalması, bu reaksiyonun radikal doğasının bir göstergesi olarak kullanılır. Yaklaşık 520 nm'de merkezlenmiş güçlü bir absorpsiyon bandı nedeniyle, DPPH radikali solüsyonda koyu mor renge sahiptir ve nötralize edildiğinde renksiz veya soluk sarı olur. Bu özellik, reaksiyonun görsel olarak izlenmesine izin verir ve ilk radikallerin sayısı, 520 nm'de optik absorpsiyondaki veya DPPH'nin EPR sinyalindeki değişiklikten sayılabilir.[3]
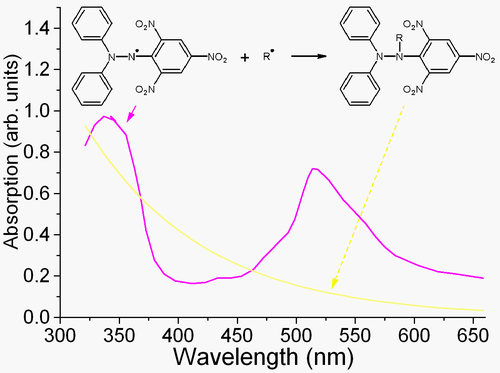
DPPH etkili bir radikal tuzak olduğundan, aynı zamanda güçlü bir inhibitörüdür. radikal aracılı polimerizasyon.[4]

Kararlı ve iyi karakterize edilmiş bir katı radikal kaynağı olan DPPH, geleneksel ve belki de en popüler konum standardıdır (g-işaretçisi) ve elektron paramanyetik rezonans (EPR) sinyalleri - yeni hazırlanmış bir numune için radikal sayısı tartılarak belirlenebilir ve DPPH için EPR bölme faktörü g = 2.0036'da kalibre edilir. DPPH sinyali, normalde yoğunluğu daha geniş güç aralığında mikrodalga gücünün karekökü ile doğrusal olarak artan tek bir hatta yoğunlaştığı için uygundur. DPPH radikallerinin seyreltik yapısı (41 atom başına bir eşleşmemiş dönüş), nispeten küçük bir hat genişliğine (1.5-4.7 Gauss) neden olur. Bununla birlikte, çözücü molekülleri kristalde kalırsa ve ölçümler, DPPH'nin hafif g-anizotropisinin saptanabilir hale geldiği yüksek frekanslı EPR kurulumu (~ 200 GHz) ile gerçekleştirilirse, hat genişliği artabilir.[5][6]
DPPH normalde paramanyetik bir katı iken, bir antiferromanyetik 0.3 K mertebesinde çok düşük sıcaklıklara soğuduktan sonra durumu. Alexander Prokhorov 1963'te.[7][8][9][10]
Referanslar
- ^ DPPH antioksidan tahlili yeniden ziyaret edildi. Om P. Sharma ve Tej K. Bhat, Gıda Kimyası, Cilt 113, Sayı 4, 15 Nisan 2009, Sayfa 1202–1205, doi:10.1016 / j.foodchem.2008.08.008
- ^ Kiers, C. T .; De Boer, J. L .; Olthof, R .; Spek, A.L. (1976). "2,2-difenil-1-pikrilhidrazil (DPPH) modifikasyonunun kristal yapısı". Acta Crystallographica Bölüm B. 32 (8): 2297. doi:10.1107 / S0567740876007632.
- ^ Mark S.M. Alger (1997). Polimer bilim sözlüğü. Springer. s. 152. ISBN 0-412-60870-7.
- ^ Cowie, J. M. G .; Arrighi Valeria (2008). Polimerler: Modern Malzemelerin Kimyası ve Fiziği (3. baskı). İskoçya: CRC Press. ISBN 978-0-8493-9813-1.
- ^ M.J. Davies (2000). Elektron Paramanyetik Rezonans. Kraliyet Kimya Derneği. s. 178. ISBN 0-85404-310-1.
- ^ Charles P. Poole (1996). Elektron spin rezonansı: deneysel teknikler üzerine kapsamlı bir inceleme. Courier Dover Yayınları. s. 443. ISBN 0-486-69444-5.
- ^ A. M. Prokhorov ve V.B. Fedorov, Sovyet Phys. JETP 16 (1963) 1489.
- ^ Teruaki Fujito (1981). "Solventsiz DPPH ve DPPH - Solvent Komplekslerinde Manyetik Etkileşim". Japonya Kimya Derneği Bülteni. 54 (10): 3110. doi:10.1246 / bcsj.54.3110.[kalıcı ölü bağlantı ]
- ^ Stig Lundqvist (1998). "A. M. Prokhorov". Nobel fizik dersleri, 1963-1970. World Scientific. s. 118. ISBN 981-02-3404-X.
- ^ Aleksandr M.Prokhorov, 1964 Nobel Fizik Ödülü

