Kurşun stifnat - Lead styphnate
 | |
| İsimler | |
|---|---|
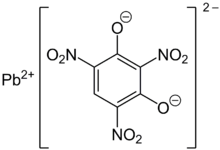
| Tercih edilen IUPAC adı Kurşun (II) 2,4,6-trinitrobenzen-1,3-bis (olate) | |
| Diğer isimler Kurşun 2,4,6-trinitrobenzen-1,3-diolat Kurşun 2,4,6-trinitro-m-fenilen dioksit 1,3-Benzenediol, 2,4,6-trinitro-, kurşun (2+) tuzu (1: 1) Kurşun tricinate Trinitroresorcinate kurşun Tricinat[1] | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| ChemSpider | |
| ECHA Bilgi Kartı | 100.035.703 |
| EC Numarası |
|
PubChem Müşteri Kimliği | |
| UNII |
|
| BM numarası | 0130 |
CompTox Kontrol Paneli (EPA) | |
| |
| |
| Özellikleri | |
| C6HN3Ö8Pb | |
| Molar kütle | 450.288 g / mol |
| Yoğunluk | 3,06 ila 3,1 g cm−3 |
| Patlayıcı veriler | |
| Şok hassasiyeti | Yüksek |
| Sürtünme hassasiyeti | Yüksek |
| Patlama hızı | 5200 m / saniye |
| Tehlikeler | |
| Güvenlik Bilgi Formu | Oxford MSDS |
| Zararlı (X), Çevre için tehlikeli (N), Patlayıcı (E) | |
| NFPA 704 (ateş elması) | |
| 330 ° C (626 ° F; 603 K) | |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
Kurşun stifnat (2,4,6-trinitroresorcinate, C6HN3Ö8Pb), adı türetilen stifnik asit, bir patlayıcı bileşen olarak kullanılır astar ve patlayıcı daha az hassas karışımlar ikincil patlayıcılar. Kurşun stifnat, Su ve metanol.[2] Kurşun stifnat örnekleri sarıdan altın rengine, turuncudan kırmızımsı kahverengiye ve kahverengiye değişir. Kurşun stifnat, çeşitli polimorflarda, hidratlarda ve bazik tuzlarda bilinir. Normal kurşun stifnat monohidrat, monobazik kurşun stifnat, tribazik kurşun stilat dihidrat ve pentabazik kurşun stilat dehidratın yanı sıra kurşun stifnatın α, polimorfları mevcuttur.
Kurşun stifnat altı yüzlü kristalleri oluşturur. monohidrat ve küçük dikdörtgen kristaller. Kurşun stifnat özellikle yangına ve Statik elektrik. Uzun ince kristaller özellikle hassastır. Kurşun stifnat diğer metallerle reaksiyona girmez ve şoka ve sürtünmeye göre daha az hassastır. cıva fulminat veya kurşun azid. Yüksek sıcaklıklarda bile depolamada stabildir. Diğerlerinde olduğu gibi öncülük etmek -içeren bileşikler, kurşun stifnat nedeniyle toksiktir ağır metal zehirlenme.
Hazırlık
Asla doğrulanmamış olmasına rağmen, kurşun stifnat, Peter Griess (nın-nin Griess testi 1919'da Edmund Herz, magnezyum stifnatın nitrik asit varlığında kurşun asetat ile reaksiyona sokulmasıyla ilk olarak susuz normal kurşun stilat preparatı oluşturdu.[3][4]
- {C6N3Ö8} MgH2O + Pb (CH3CO2)2 → {C6N3Ö8} PbH2O + Mg (CH3CO2)2
Yapısı
Normal kurşun stifnat, her ikisi de monoklinik kristaller olan α ve β polimorfları olarak bulunur. Lider merkezler yedi koordinatlıdır ve oksijen köprüleriyle köprülenmiştir. Su molekülü metale koordine edilir ve ayrıca anyona hidrojen ile bağlıdır. Pb-O mesafelerinin çoğu kısadır ve bir dereceye kadar kovalentlik gösterir. Styfnat iyonları, Pb atomları ile bağlanmış yaklaşık olarak paralel düzlemlerde bulunur.[5][6]
Özellikleri
Kurşun stifnatın oluşum ısısı −835 kJ mol−1. Su kaybı, 2,9 g cm yoğunluğa sahip hassas susuz bir malzemenin oluşumuna yol açar.−3. Renklerin değişimi açıklanamıyor.[7] Kurşun stifnatın patlama hızı 5,2 km / s'dir ve patlama sıcaklığı beş saniye sonra 265–280 ° C'dir.[8]
Başvurular
Kurşun stifnat esas olarak küçük kollarda kullanılır cephane askeri ve ticari uygulamalar için. Bir birincil patlayıcı basit bir darbede tutuşmayan ateşli silah itici ile.[9] Kurşun stifnat ayrıca küçük uydu istasyonlarının tutulması için mikro iticilerde astar olarak kullanılır.[10]
Referanslar
- ^ ECHA, Avrupa Kimyasallar Ajansı "Arşivlenmiş kopya" (PDF). Arşivlenen orijinal (PDF) 2014-10-22 tarihinde. Alındı 2014-10-17.CS1 Maint: başlık olarak arşivlenmiş kopya (bağlantı)
- ^ Jacques Boileau, Claude Fauquignon, Bernard Hueber ve Hans H. Meyer (2009). "Patlayıcılar". Ullmann'ın Endüstriyel Kimya Ansiklopedisi. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a10_143.pub2.CS1 Maint: birden çok isim: yazarlar listesi (bağlantı)
- ^ J.R. Payne (1994). "Kurşun stifnatın termokimyası". Thermochimica Açta. 242: 13–21. doi:10.1016/0040-6031(94)85003-8.
- ^ Jacques Boileau; Claude Fauquignon; Bernard Hueber; Hans H. Meyer (2009). Patlayıcılar. Ullmann'ın Endüstriyel Kimya Ansiklopedisi. doi:10.1002 / 14356007.a10_143.pub2. ISBN 978-3527306732.
- ^ Pierce-Butler, MA (1984). "2,4,6-trinitro-1,3-benzenediol monohidratın (alfa-polimorf) kurşun tuzunun yapısı". Açta Crystallogr. 40: 63–65. doi:10.1107 / S0108270184003036.
- ^ Pierce-Butler, MA (1982). "2,4,6-trinitro-1,3-benzenediol monohidratın baryum tuzunun yapıları ve izomorf kurşun tuzu (beta-polimorf)". Açta Crystallogr. 38 (12): 3100–3104. doi:10.1107 / S0567740882010966.
- ^ Robert Matyáš; Ji í Pachman (2013). Birincil Patlayıcılar. Springer Science & Business Media. doi:10.1007/978-3-642-28436-6. ISBN 978-3-642-28435-9. S2CID 199492549.
- ^ Hyman Henkin; Russell McGill (1952). "Patlayıcıların Patlayıcı Parçalanma Hızları. Sıcaklığın Bir Fonksiyonu Olarak Deneysel ve Teorik Kinetik Çalışma". San. Müh. Kimya. 44 (6): 1391–1395. doi:10.1021 / ie50510a054.
- ^ Gri, Theodore (2009). "Flaş Patlama". Popüler Bilim.
- ^ Daniel W. Youngner; et al. (2000). "Küçük Uydu İstasyon Koruması için MEMS Mega Piksel Mikro İtici Dizileri". Honeywell Technology 14. Yıllık / USU Küçük Uydular Konferansı.

