Metal alkoksialuminyum hidrürlerle indirgeme - Reductions with metal alkoxyaluminium hydrides
Metal alkoksiyaluminyum hidrürlerle indirgeme doymamış bir bileşiğin net hidrojenasyonunu veya indirgenebilir bir bileşiğin değiştirilmesini içeren kimyasal reaksiyonlardır. fonksiyonel grup metal alkoksialuminyum hidrit reaktifleri ile hidrojen ile.[1][2]
Giriş
Sodyum borohidrid ve lityum alüminyum hidrit yaygın olarak organik bileşiklerin indirgenmesi için kullanılır.[3][4] Bu iki reaktif reaktivitenin uç noktasındadır - lityum alüminyum hidrit neredeyse tüm indirgenebilir fonksiyonel gruplarla reaksiyona girerken, sodyum borohidrit çok daha sınırlı bir aralıkta reaksiyona girer. fonksiyonel gruplar. Azalmış veya artırılmış reaktivite, bu reaktiflerdeki bir veya daha fazla hidrojenin alkoksi grupları ile değiştirilmesiyle gerçekleştirilebilir.
Ek olarak, bu reaktiflerde şiral alkoksi grupları için hidrojenin ikame edilmesi asimetrik indirgeme sağlar.[5] Her ne kadar içeren yöntemler stokiyometrik Modern zamanlarda şiral metal hidrit miktarları yerini enantiyoselektif katalitik indirgemeler, stereoselektif reaksiyonların erken örnekleri olarak tarihsel ilgi konusudur.
Aşağıdaki tablo, çeşitli metal alüminyum hidrürler ve borohidrürler ile gerçekleştirilebilecek indirgemeleri özetlemektedir. "+" Sembolü, indirgemenin gerçekleştiğini, "-" indirgemenin olmadığını, "±" indirgemenin substratın yapısına bağlı olduğunu ve "0", literatür bilgisi eksikliğini belirtir.

(1)
Mekanizma ve Stereokimya
Hakim Mekanizma
Alkoksiyalüminyum hidritlerle indirgemenin çoğu durumda kutupsal bir mekanizma ile ilerlediği düşünülmektedir.[6] Organik substrata hidrit transferi, protik çözücü ile veya asidik çalışma üzerine nötralize edilen organik bir anyon üretir.

(2)
A, β-doymamış karbonil bileşiklerinin indirgenmeleri 1,2 anlamda (doğrudan ekleme) veya 1,4 anlamda (eşlenik ekleme) meydana gelebilir. 1,4 anlamında ekleme eğilimi, Pearson'un sert-yumuşak asit-baz teorisine göre hidrit reaktifinin yumuşaklığı ile ilişkilidir.[7] Deneysel sonuçlar teoriyle uyumludur - daha yumuşak hidrit reaktifleri, konjugat indirgeme ürününden daha yüksek verimler sağlar.[8]

(3)
Diaril ketonlar dahil birkaç substrat,[9] diarilalkenler[10] ve antrasen,[11] lityum alüminyum hidrit ile tek elektron transfer yollarıyla indirgemeye uğradığı bilinmektedir.
Metal alkoksilaluminyum hidrit reaktifleri sınırlı sayıda durumda iyi karakterize edilir.[12] Bazı durumlarda, alkoksiyalüminyum hidrürleri alkoksialüminatlara ve metal alüminyum hidrüre dönüştüren orantısızlık nedeniyle kesin karakterizasyon karmaşıktır:[13]
- LiAlHn(VEYA)4-n ⇌ (4-n) LiAlH4 + n LiAlH (OR)4
(4)
Stereokimya
Kökeni diastereo seçicilik Kiral ketonların azaltılmasında kapsamlı bir şekilde analiz edilmiş ve modellenmiştir.[14][15] Felkin'in geliştirdiği bir modele göre,[16] diastereo seçicilik, üç geçiş durumunun göreceli enerjisi tarafından kontrol edilir ben, II, ve III. Geçiş durumu ben a karbon üzerinde polar grupların yokluğunda tercih edilir ve aşiral keton ikame edicisinin (R) boyutu arttıkça stereoselektiflik artar. Geçiş durumu III alkil ketonların azaltılması için tercih edilir, burada RM bir elektron çeken gruptur, çünkü nükleofil ve elektron çeken ikame edici birbirlerinden mümkün olduğunca uzak olmayı tercih ederler.

(5)
Siklik ketonların indirgenmesindeki diastereo seçicilik de incelenmiştir. Konformasyonel olarak esnek ketonlar, hidrit reaktifi tarafından eksenel saldırıya uğrayarak ekvatoral alkole yol açar. Öte yandan sert siklik ketonlar, eksenel alkol sağlamak için öncelikle ekvatoral saldırıya uğrar. Rijit ketonlar üzerindeki tercihli ekvatoral saldırı, "sterik yaklaşım kontrolü" başlatılarak rasyonelleştirilmiştir - hidrit reaktifinin ekvator yaklaşımı, eksenel yaklaşıma göre sterik olarak daha az engellenmiştir.[17] Konformasyonel olarak esnek halkalı ketonlara eksenel saldırı tercihi, Felkin ve Anh tarafından ortaya konan bir model tarafından ele alınmıştır.[18][19] Eksenel saldırı için geçiş durumu (IV) herhangi bir eksenel ikame edici ile gelen hidrit reaktifi arasındaki sterik gerilmeden muzdariptir. Ekvator saldırısı için geçiş durumu (V) gelen hidrit reaktifi ve bitişik ekvatoral hidrojenler arasındaki burulma geriliminden muzdariptir. Bu iki gerinim enerjisi arasındaki fark, hangi saldırı yönünün tercih edildiğini belirler ve R küçük olduğunda burulma gerinimi V hakimdir ve ekvatoral alkol ürünü tercih edilir.

(6)
Kapsam ve Sınırlamalar
Alkoksialuminyum ve yakından ilişkili hidrit reaktifleri, çok çeşitli fonksiyonel gruplar, genellikle iyi seçicilikle. Fonksiyonel gruba göre düzenlenen bu bölüm, alkoksiyalüminyum hidritin indirgenmesi için en yaygın veya sentetik olarak yararlı yöntemleri kapsar. organik bileşikler.
Birçok seçici azaltma karbonil bileşikleri metal alkoksilaluminyum hidrürlerin benzersiz reaktivite profillerinden yararlanılarak gerçekleştirilebilir. Örneğin, lityum tri-tert-butoksi) alüminyum hidrit (LTBA), son derece yavaş reaksiyona girdiği esterlerin varlığında aldehitleri ve ketonları seçici olarak azaltır.[20]

(8)
α,-Doymamış ketonlar, makul bir indirgeme ajanı seçimi ile 1,2 veya 1,4 anlamda seçici olarak azaltılabilir. Nispeten engellenmemiş lityum trimetoksiyalüminyum hidrit kullanımı, karbonil grubuna neredeyse kantitatif doğrudan ilaveyle sonuçlanır (Denklem.9)).[21] Öte yandan, hacimli reaktif LTBA'nın kullanılması, yüksek bir konjugat ekleme ürünü verimine yol açar (Denk. (10)).[22]

(9)
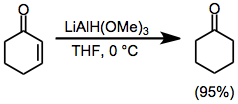
(10)
Çoğu hidrit reaktifiyle eter klivajının gerçekleştirilmesi zordur. Bununla birlikte, benzil aril eterlerin benzilden arındırılması SMEAH ile gerçekleştirilebilir.[23] Bu protokol, asit veya hidrojenoliz gerektiren yöntemlere (örneğin, Pd / C ve hidrojen gazı) faydalı bir alternatiftir.

(11)
Epoksitler genellikle daha az ikame edilmiş pozisyonda alkoksiyalüminyum hidritler tarafından saldırıya uğrar. Yakındaki bir hidroksil grubu, hidroksil grubuna daha yakın konumda 1,2-disübstitüe epoksitlerin seçici olarak açılmasına izin vererek hidrit reaktifinin molekül içi iletimini kolaylaştırabilir.[24] El değmemiş epoksit karbondaki konfigürasyon korunur.

(12)
Doymamış karbonil bileşikleri, alkoksiyalüminyum hidrit reaktifleri ile doymuş veya doymamış alkollere indirgenebilir. Bir Red-Al solüsyonuna doymamış bir aldehit eklenmesi, doymuş alkolü verdi; ters ekleme, doymamış alkol ürününü vermiştir.[25]

(13)
Alkenler, bazı alkoksiyaluminyum hidrürlerin varlığında hidroalüminasyona uğrar.[26] İlgili bir uygulamada, NaAlH2(OCH2CH2OCH3)2 (sodyum bis (metoksietoksi) alüminyum dihidrit, SMEAH veya Red-Al), zirkonosen klorür hidrit (Schwartz reaktifi) vermek üzere zirkonosen diklorür ile reaksiyona girer. Alkenler, bu reaktifin mevcudiyetinde hidrozirkonasyona uğrayarak, bir elektrofil ile söndürüldükten sonra işlevselleştirilmiş ürünler sağlar.[27]

(14)
Oksijenden başka heteroatomlar içeren fonksiyonel gruplar, bir alkoksiyalüminyum hidrit reaktifi varlığında karşılık gelen hidrokarbonlara indirgenebilir. Birincil alkil halojenürler, NaAlH (OH) (OCH) varlığında karşılık gelen alkanlara indirgenir.2CH2OCH3)2. İkincil halojenürler daha az reaktiftir ancak makul verimde alkan sağlar.[28]

(15)
Sülfoksitler, SMEAH varlığında iyi verimle karşılık gelen sülfitlere indirgenir.[29]

(16)
İminler, metal alkoksiyalüminyum hidritler tarafından karşılık gelen aminlere indirgenir. Aşağıdaki örnekte, ekzo yüksek diastereo seçiciliği olan amin formları. Bu durumda hidrit indirgemesinin seçiciliği, katalitik hidrojenasyondan daha yüksektir.[30]

(16)
Deneysel Koşullar ve Prosedür
Hidrit Reaktiflerinin Hazırlanması
Alkoksialuminyum hidritler tipik olarak lityum alüminyum hidrürün karşılık gelen alkol ile işlenmesiyle hazırlanır.[31] Hidrojen evrimi, alkoksiyalüminyum hidrit ürünlerinin oluşumunu gösterir. Lityum tri- gibi engellenmiş hidritler (tert-butoksi) alüminyum hidrit (LTBA) inert atmosfer altında uzun süre stabildir, ancak lityum trimetoksiyaluminyum hidrit (LTMA) orantısızlaşmaya uğrar ve hazırlandıktan hemen sonra kullanılmalıdır. Saf, katı Red-Al, inert atmosfer altında birkaç saat stabildir ve ticari olarak Vitride veya Synhydrid ticari adı altında toluen içinde% 70'lik bir çözelti halinde mevcuttur.
İndirgeme Koşulları
İndirgeme tipik olarak, bir kurutma tüpü kapaklı geri akış kondansatörü, cıva ile kapatılmış bir mekanik karıştırıcı, bir termometre, bir nitrojen girişi ve bir basınç dengeleme yan kolu olan ek bir huni ile donatılmış yuvarlak tabanlı bir şişede gerçekleştirilebilir. Kullanılan en yaygın çözücüler şunlardır: tetrahidrofuran ve dietil eter. Hangi çözücü kullanılırsa kullanılsın susuz ve saf olmalıdır. Alkoksialuminyum hidritler olabildiğince kuru tutulmalı ve özellikle aşırı hidrit kullanıldığında (çalışma sırasında hidrojen gelişir) önemli bir yangın tehlikesi oluşturmalıdır.
Örnek Prosedür[32]
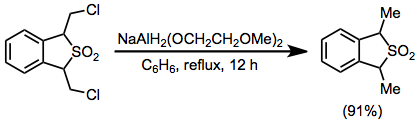
(17)
50 mL kuru içinde bir 1,3-dihidro-1,3-bis (klorometil) benzo [c] tiofen 2,2-dioksit (0,584 g, 2,2 mmol) çözeltisine benzen % 70'lik bir NaAlH benzen çözeltisinden 0.80 mL (2.8 mmol)2(OCH2CH2OCH2)2 şırınga yoluyla ve çözelti, 12 saat geri akıtıldı. Karışım 0 ° 'ye soğutuldu ve% 20 ile ayrıştırıldı sülfürik asit. Benzen tabakası ayrıldı, 10 mL su ile yıkandı, üzerinde kurutuldu. potasyum karbonat ve konsantre edilerek ürün% 91 verimle (0.480 g) sarı bir yağ olarak elde edildi; IR (film) 770, 1140 ve 1320 cm-1; NMR (CDCl3) δ 4.22 (q, 2 H), 1.61 ve 1.59 (2 d, 6 H, J = 7 Hz), 7.3 (s, 4 H); m / e (göreli yoğunluk) 196 (M +) (14), 132 (M-S02) (100); MS analizi 196.055796 (hesaplanan), 196.057587 (gözlem.).
Referanslar
- ^ Málek, J. Org. Tepki. 1985, 34, 1. doi:10.1002 / 0471264180.or034.01
- ^ Málek, J. Org. Tepki. 1988, 36, 249. doi:10.1002 / 0471264180.or036.03
- ^ Brown, G. Org. Tepki. 1951, 6, 469.
- ^ Schenker, E. in Daha Yeni Hazırlayıcı Organik Kimya Yöntemleri, Cilt. IV., W. Foerst, Ed., Academic Press, New York, 1968, s. 163–335.
- ^ Itsuno, S. Org. Tepki. 1998, 52, 395.
- ^ House, O. Modern Sentetik Reaksiyonlar, 2. baskı, W.A. Benjamin, Menlo Park, Kaliforniya, 1972.
- ^ Pearson, G. J. Chem. Educ. 1968, 45, 581.
- ^ Bottin, J .; Eisenstein, O .; Minot, C .; Anh, T. Tetrahedron Lett., 1972, 3015.
- ^ Cerný, M .; Málek, J. Toplamak. Çek. Chem. Commun.. 41, 119 (1976).
- ^ Málek, J .; Cerný, M. J. Organomet. Chem. 1975, 84, 139.
- ^ Málek, J .; Cerný, M .; Rericha, R. Toplamak. Çek. Chem. Commun. 1974, 39, 2656.
- ^ Bec, M .; Huet, J. Boğa. Soc. Chim. Fr., 1972, 1636.
- ^ Brown, C .; Shoaf, J. J. Am. Chem. Soc. 1964, 86, 1079.
- ^ Cram, J .; Abd Elhafez, A. J. Am. Chem. Soc. 1952, 74, 5828.
- ^ Chérest, M .; İhtiyatlı, N. Tetrahedron 1980, 36, 1599.
- ^ Chérest, M .; Felkin, H .; İhtiyatlı, N. Tetrahedron Lett., 1968, 2199.
- ^ Dauben, W. G .; Fonken, G. J .; Noyce, D. S. J. Am. Chem. Soc. 1956, 78, 2579.
- ^ Chérest, M .; Felkin, H. Tetrahedron Lett., 1971, 383.
- ^ Huet, J .; Maroni-Barnaud, Y .; Anh, N. T .; Seyden-Penne, J. Tetrahedron Lett., 1976, 159.
- ^ Torii, S .; Tanaka, H .; Inokuchi, T .; Tomozane, K. Boğa. Chem. Soc. Jpn. 1982, 55, 3947.
- ^ Danh, N. C .; Arnaud, C .; Huet, J. Boğa. Soc. Chim. Fr. 1974, 1071.
- ^ Durand, J .; Anh, N. T .; Huet, J. Tetrahedron Lett. 1974, 2397.
- ^ Kametani, T .; Huang, S. P .; Ihara, M .; Fukumoto, K. J. Org. Chem. 1976, 41, 2545.
- ^ Finan, M .; Kishi, Y. Tetrahedron Lett. 1982, 23, 2719.
- ^ Bazant, V .; Capka, M .; Cerny, M .; Chvalovský, V .; Kochloefl, K .; Kraus, M .; Málek, J. Tetrahedron Lett., 1968, 3303.
- ^ Ashby, C .; Başını salladı, A. J. Org. Chem. 1980, 45, 1035.
- ^ Hart, W .; Schwartz, J. J. Am. Chem. Soc. 1974, 96, 8115.
- ^ Capka, M .; Chvalovský, V. Toplamak. Çek. Chem. Commun. 1969, 34, 3110.
- ^ Weber, L. Chem. Ber. 1983, 116, 2022.
- ^ Law, J .; Lewis, H .; Borne, F. J. Heterocycl. Chem. 1978, 15, 273.
- ^ Véle, I .; Fusek, J .; Ştrouf, O. Toplamak. Çek. Chem. Commun. 1972, 37, 3063.
- ^ Barton, T. J .; Kippenhan, R. C. J. Org. Chem. 1972, 37, 4194.
















