Taban - Arsole - Wikipedia
| |||
| İsimler | |||
|---|---|---|---|
| Tercih edilen IUPAC adı 1H-Arsole | |||
| Diğer isimler Arsenol Arsacyclopentadiene | |||
| Tanımlayıcılar | |||
3 boyutlu model (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
PubChem Müşteri Kimliği | |||
CompTox Kontrol Paneli (EPA) | |||
| |||
| |||
| Özellikleri | |||
| C4H4Kül | |||
| Molar kütle | 128.00 g mol−1 | ||
| Bağıntılı bileşikler | |||
Bağıntılı bileşikler | Pirol, fosfol, bizmol, stibole | ||
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için standart durum (25 ° C'de [77 ° F], 100 kPa). | |||
| Bilgi kutusu referansları | |||
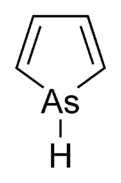
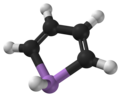
Taban, olarak da adlandırılır cephane[1] veya arsasiklopentadien, bir organoarsenik bileşik ile formül C4H4Kül. Olarak sınıflandırılır metalol ve izoelektroniktir ve bunlarla ilgilidir pirol bunun dışında bir arsenik atom yerine azot atom. Pirol molekülü düzlemsel iken, taban molekülü değildir ve arseniğe bağlı hidrojen atomu moleküler düzlemin dışına uzanır. Taban sadece orta derecede aromatik yaklaşık% 40 pirol aromatikliği ile.[2] Arsole'nin kendisi saf biçimde rapor edilmedi, ancak birkaç ikame analoglar denir arsoles var olmak. Arsoles ve daha karmaşık taban türevleri, benzer yapıya ve kimyasal özelliklere sahiptir. fosfol türevler. Taban astarı bir benzen halka, bu moleküle denir Arsindoleveya benzarsol.[3]
İsimlendirme
Arsole heterosiklik serisine aittir. piktojen Bileşikler. Döngüsel adlandırma organoarsenik bileşikler arsole gibi bir uzantıya dayanır Hantzsch – Widman isimlendirme sistemi[4] tarafından onaylandı IUPAC, aşağıda özetlendiği gibi:[5]
| Yüzük boyutu | Doymamış yüzük | Doymuş yüzük |
|---|---|---|
| 3 | Arsirene | Arsirane |
| 4 | Arsete | Arsetane |
| 5 | Taban | Arsolane |
| 6 | Arsinin | Arsinane |
| 7 | Arsepin | Arsepane |
| 8 | Arsocine | Arsocane |
| 9 | Kundakçılık | Kundakçılık |
| 10 | Arsecine | Arsecane |
İngilizce argo kelimeye benzerliği nedeniyle "göt deliği "(Kuzey Amerika dışında yaygın kullanımda)," arsole "adı bir eğlence hedefi," aptalca bir isim "olarak kabul edildi,[6][7] ve birkaç tanesinden biri alışılmadık bir ada sahip kimyasal bileşikler. Ancak bu "aptalca isim" tesadüfü, detaylı bilimsel çalışmaları da teşvik etmiştir.[2][başarısız doğrulama ][şüpheli ]
Özellikleri
| M | d (M-C), Å | d (M-H), Å | α (C-M-C), ° | E, kJ / mol |
|---|---|---|---|---|
| N | 1.37 | 1.01 | 110 | 0 |
| P | 1.81 | 1.425 | 90.5 | 67 |
| Gibi | 1.94 | 1.53 | 86 | 125 |
| Sb | 2.14 | 1.725 | 80.5 | 160 |
| Bi | 2.24 | 1.82 | 78 | 220 |
Arsole henüz deneysel olarak izole edilmedi, ancak moleküler geometri ve tabanlığın elektronik konfigürasyonu teorik olarak incelendi. Hesaplamalar ayrıca, hidrojen atomlarının diğer atomlar veya küçük hidrokarbon grupları ile ikame edildiği basit ayakkabı tabanlığı türevlerinin özelliklerini de ele aldı ve daha karmaşık taban türevlerinin kimyasal özellikleri hakkında deneysel raporlar var. Durum diğer C için benzer4H4MH metaloller burada M = P, As, Sb ve Bi.
Düzlemsellik
Hesaplamalar, pirol (C4H4NH) molekülü düzlemsel, fosfol (C4H4PH) ve daha ağır metaloller değildir ve piktojen bağlı hidrojen atomu düzlemin dışına uzanır.[9] Florlu C için de benzer bir eğilim tahmin edilmektedir.4F4MH türevleri (M = N, P, As, ..), ancak ters çevirme engelleri yaklaşık% 50-100 daha yüksektir. Düzlemsellik, nitrojene bağlı hidrojen atomu ikame edildiğinde, örneğin pirolde kaybolur. flor. Bununla birlikte, düzlemsellik, M-H bağının moleküler düzlemden sola veya sağa uzandığı iki konfigürasyon arasında dönüştürmek için gereken enerji ile hesaplamada değerlendirilir. Bununla birlikte, bu enerjinin sıfır olmayan (küçük) değeri, molekülün düşük simetriye sahip olduğu anlamına gelmez, çünkü termal veya kuantum tünelleme iki konfigürasyon arasında.[8]
Aromatiklik
Aromatiklik ayakkabı tabanının içinde kendini gösterir yerelleştirme ve rezonans halka elektronlarının. Düzlemsellik ile yakından ilgilidir, çünkü molekül ne kadar düzlemselse aromatikliği o kadar güçlüdür.[10] Taban ve türevlerinin aromatikliği hem deneysel hem de teorik açıdan yıllardır tartışılmaktadır. Kuantum kimyasal hesaplamalarla birleştirilmiş bir 2005 incelemesi, halka akımının aromatik olduğu bilinen pirolinkinin% 40'ı olduğu için, tabanlığın kendisinin "orta derecede" aromatik olduğu sonucuna varmıştır. Bununla birlikte, karşılaştırılabilir halka akımı hesaplanmıştır. siklopentadien, uzun zamandır aromatik olarak kabul edilmeyen.[2] Diğer raporlar, aromatikliğin (ve düzlemselliğin) taban türevleri arasında değişebileceğini ileri sürmektedir.[9]
Kimyasal özellikler (taban türevleri)
Taban türevlerinin kimyasal özellikleri deneysel olarak incelenmiştir; bunlara benzerler fosfol ve türevleri.[1] Tabanındaki tüm hidrojen atomlarının ikame edilmesi fenil gruplar sarı kristal iğneler verir pentafenil taban215 ° C erime noktasına sahiptir. Bu kompleks 1,4-diiyodo-1,2,3,4-tetrafenilbutadien reaksiyona sokularak% 50-93 verimle hazırlanabilir.[11] veya 1,4-dilithio-1,2,3,4-tetraphenylbutadiene with phenylarsenous dichloride (C6H5AsCl2) içinde eter.
Bu reaksiyonda ikame arsenik triklorür fenillarsenli diklorür için 1-kloro-2,3,4,5-tetrafenilol verir, bu da sarı iğneler oluşturur, ancak daha düşük erime noktası 182–184 ° C'dir. Pentafeniler taban ayrıca oksitlenebilir hidrojen peroksit erime noktası 252 ° C olan sarı kristaller ile sonuçlanır. Aynı zamanda reaksiyona girebilir demir pentakarbonil (Fe (CO)5) içinde izooktan 150 ° C'de formül C'ye sahip katı bir organoarsenik bileşik elde etmek için34H25Fe (CO)3.[1] Pentafenilolün metalik lityum veya potasyum verimi ile reaksiyona sokulması 1,2,3-trifenil naftalen.[12]
Fenilarsenik diklorürün doğrusal difeniller ile reaksiyonu, erime noktası yaklaşık 170 ° C olan bir katı olan 1,2,5-trifenil arolle (aşağıya bakınız) sonuçlanır.[13] Bu bileşik çeşitli oluşturur anyonlar alkali metallerle muamele üzerine.[14]
Ayrıca bakınız
- Pirol, bir azot analog.
- Furan, bir oksijen analog.
- Tiyofen, bir kükürt analog.
- Basit aromatik halkalar
- Varsol, bir petrol damıtmak Birlikte Kaynama aralığı 150–200 ° C arasında.
Referanslar
- ^ a b c Frederick George Mann (1970). Fosfor, arsenik, antimon ve bizmutun heterosiklik türevleri. John Wiley and Sons. s. 357–360. ISBN 978-0-471-37489-3. Alındı 21 Mart 2011.
İngilizcede bu halka sistemi sık sık arsenole 'for euphony' adını almıştır.
- ^ a b c M. P. Johansson; J. Juselius (2005). "Arsole Aromaticity Revisited". Lett. Org. Kimya. 2: 469–474. doi:10.2174/1570178054405968.
Kuantum kimyasal metodolojisini kullanarak, yeni geliştirilen gösterge dahil manyetik olarak indüklenen akımlar (GIMIC) yöntemini kullanarak çok tartışılan tabanının aromatikliğini yeniden araştırıyoruz. GIMIC, tabanlığın orta derecede aromatik olduğunu gösteren, indüklenen halka akımı gücünün nicel bir ölçümünü sağlar.
- ^ A. Muranaka; S. Yasuike; C-Y. Liu; J. Kurita; N. Kakusawa; T. Tsuchiya; M. Okuda; N. Kobayashi; Y. Matsumoto; K. Yoshida; D. Hashizume; M. Uchiyama (2009). "Heteroatomun Periyodik Değiştirilmesinin Indol ve Benzofuran Türevlerinin Spektroskopik Özellikleri Üzerindeki Etkisi". J. Phys. Chem. Bir. 113 (2): 464–473. doi:10.1021 / jp8079843. PMID 19099440.
- ^ "Heteromonosikller için Genişletilmiş Hantzsch-Widman İsimlendirme Sisteminin Revizyonu "IUPAC'ta, 29 Eylül 2008'de alındı
- ^ Nicholas C. Norman (1998). Arsenik, antimon ve bizmut kimyası. Springer. s. 235. ISBN 978-0-7514-0389-3. Alındı 15 Mart 2011.
- ^ Richard Watson Todd (25 Mayıs 2007). İngilizce hakkında çok fazla konuşma: büyüleyici bir dilin tuhaf yan yollarında yukarı ve aşağı. Nicholas Brealey Yayınları. s. 138. ISBN 978-1-85788-372-5. Alındı 15 Mart 2011.
- ^ Paul W May, Aptalca veya Alışılmadık İsimli Moleküller, publ. 2008 Imperial College Press, ISBN 978-1-84816-207-5(pbk). Ayrıca Web sayfasına bakın "Aptalca veya Alışılmadık İsimli Moleküller "School of Chemistry, University of Bristol, (29 Eylül 2008'de alındı)
- ^ a b Pelzer, Silke; Wichmann, Karin; Wesendrup, Ralf; Schwerdtfeger, Peter (2002). "Ters Çevirme Engellerindeki Eğilimler IV. Grup 15 Pirol Benzeşimi". Fiziksel Kimya Dergisi A. 106: 6387. doi:10.1021 / jp0203494.
- ^ a b Tadeusz Marek Krygowski; Michal K. Cyrański; M. Agostinha R. Matos (2009). Heterosiklik Bileşiklerde Aromatiklik. Springer. s. 47–. ISBN 978-3-540-68329-2. Alındı 21 Mart 2011.
- ^ Pelloni, Stefano; Lazzeretti, Paolo (2007). "Fosfolün manyetotropisitesi ve arsenik analogu". Teorik Kimya Hesapları. 118: 89. doi:10.1007 / s00214-007-0247-0.
- ^ Braye, E. H .; Hubel, W .; Caplier, I. (1961). "Yeni Doymamış Heterosiklik Sistemler. I". Amerikan Kimya Derneği Dergisi. 83: 4406. doi:10.1021 / ja01482a026.
- ^ C. W. Bird; Gordon William Henry Cheeseman (31 Aralık 1973). Aromatik ve Heteroatomik Kimya. Kraliyet Kimya Derneği. s. 23–. ISBN 978-0-85186-753-3. Alındı 23 Mart 2011.
- ^ Gottfried Märkl & Hagen Hauptmann (1972). "Bir Taban Halkasında Olağandışı Değişiklik" (PDF). Angewandte Chemie International Edition İngilizce. 11: 441. doi:10.1002 / anie.197204411.
- ^ Märkl, G (1983). "Synthese von 1-fenil-2,5-diaril (dialkil) -arsolen; umsetzung der arsole mit alkalimetallen ve lithiumorganylen". Organometalik Kimya Dergisi. 249: 335. doi:10.1016 / S0022-328X (00) 99433-6.