Kadmiyum iyodür - Cadmium iodide
 | |
 | |
 | |
| İsimler | |
|---|---|
| IUPAC adı Kadmiyum (II) iyodür | |
| Diğer isimler Kadmiyum diiyodür | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| ChemSpider | |
| ECHA Bilgi Kartı | 100.029.294 |
| EC Numarası |
|
PubChem Müşteri Kimliği | |
| UNII | |
CompTox Kontrol Paneli (EPA) | |
| |
| |
| Özellikleri | |
| CdI2 | |
| Molar kütle | 366,22 g / mol |
| Görünüm | beyazdan soluk sarı kristaller |
| Yoğunluk | 5,640 g / cm3, sağlam |
| Erime noktası | 387 ° C (729 ° F; 660 K) |
| Kaynama noktası | 742 ° C (1.368 ° F; 1.015 K) |
| 787 g / L (0 ° C) 847 g / L (20 ° C) 1250 g / L (100 ° C) | |
| Çözünürlük | içinde çözünür etanol, aseton, eter ve amonyak |
| -117.2·10−6 santimetre3/ mol | |
| Yapısı | |
| Üçgen, hP3, uzay grubu P3m1, No. 164 | |
| sekiz yüzlü | |
| Tehlikeler | |
| GHS piktogramları |    |
| GHS Sinyal kelimesi | Tehlike |
| H301, H331, H351, H373, H400, H410 | |
| P260, P280, P301 + 330 + 331, P310, P304 + 340, P311, P403 + 233 | |
| NFPA 704 (ateş elması) | |
| NIOSH (ABD sağlık maruziyet sınırları): | |
PEL (İzin verilebilir) | [1910.1027] TWA 0,005 mg / m3 (Cd olarak)[1] |
REL (Önerilen) | CA[1] |
IDLH (Ani tehlike) | Ca [9 mg / m3 (Cd olarak)][1] |
| Bağıntılı bileşikler | |
Diğer anyonlar | kadmiyum florür kadmiyum klorür kadmiyum bromür |
Diğer katyonlar | çinko iyodür cıva (II) iyodür |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
Kadmiyum iyodür, CdI2kimyasal bir bileşiktir kadmiyum ve iyot. Onun için dikkate değer kristal yapı MX formundaki bileşikler için tipik olan2 güçlü polarizasyon Etkileri.
Hazırlık
Kadmiyum iyodür, kadmiyum metali veya oksidi, hidroksiti veya karbonatının eklenmesiyle hazırlanır. hidroiyodik asit.
Ayrıca, bileşik kadmiyumun iyot ile ısıtılmasıyla da yapılabilir.
Kristal yapı

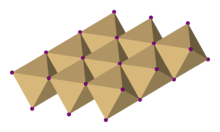
Kadmiyum iyodürde iyodür anyonlar kadmiyum ise altıgen kapalı paketli bir düzenleme oluşturur katyonlar tüm oktahedral alanları alternatif katmanlarda doldurun. Ortaya çıkan yapı, katmanlı bir kafesten oluşur. Bu aynı temel yapı, diğer birçok tuzlar ve mineraller. Kadmiyum iyodür çoğunlukla iyonik bağlı ama kısmi kovalent karakter.[2]
Kadmiyum iyodürün kristal yapısı, diğer birçok bileşiğin kristal yapılarının dayandığı düşünülebilecek prototiptir. Aşağıdaki özelliklerden herhangi birine sahip bileşikler, CdI'yi benimseme eğilimindedir.2 yapı:[kaynak belirtilmeli ]
- İyodürler orta derecede polarize katyonlar; bromürler ve klorürler güçlü polarizasyon katyonlarının
- Hidroksitler dikasyonlar, yani M (OH) genel formülüne sahip bileşikler2
- Sülfitler, Selenidler ve Tellurides (kalkojenitler ) tetrakasyonlar, yani MX genel formülüne sahip bileşikler2, burada X = S, Se, Te
Referanslar
- ^ a b c Kimyasal Tehlikeler için NIOSH Cep Rehberi. "#0087". Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü (NIOSH).
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Elementlerin Kimyası (2. baskı). Butterworth-Heinemann. sayfa 1211–1212. ISBN 978-0-08-037941-8.

