İzotopik etiketleme - Isotopic labeling
İzotopik etiketleme (veya izotopik etiketleme) bir kanalın geçişini izlemek için kullanılan bir tekniktir. izotop (bir atom nötron sayısında tespit edilebilir bir varyasyon ile) bir reaksiyon, metabolik yol veya hücre. reaktan belirli atomları izotopları ile değiştirerek 'etiketlenir'. Reaktantın daha sonra reaksiyona girmesine izin verilir. İzotopların konumu Ürün:% s reaksiyonda izotopik atomun izlediği diziyi veya hücrenin metabolik yolunu belirlemek için ölçülür. çekirdekler izotopik etiketlemede kullanılan olabilir kararlı çekirdekler veya radyonüklitler. İkinci durumda, etiketleme denir radyo etiketleme.
İzotopik etiketlemede, etiketleme izotoplarının varlığını tespit etmenin birçok yolu vardır; Onların aracılığıyla kitle, titreşim modu veya radyoaktif bozunma. Kütle spektrometrisi bir izotopun kütlesindeki farkı tespit ederken kızılötesi spektroskopi izotopun titreşim modlarındaki farkı algılar. Nükleer manyetik rezonans farklı jiromanyetik oranlara sahip atomları algılar. Radyoaktif bozunma, bir iyonlaşma odası veya otoradyograflar jellerin.
İzotopik etiketlemenin kullanımına bir örnek, fenol (C6H5OH) suyun içinde ortak hidrojen (protium ) ile döteryum (döteryum etiketleme). Fenol ekledikten sonra döteryumlanmış su (D içeren su2O normal H'ye ek olarak2O), döteryumun hidrojen yerine ikame edilmesi fenollerin Hidroksil grubu (C ile sonuçlanır6H5OD), fenolün su ile kolayca hidrojen değişim reaksiyonlarına girdiğini gösterir. Sadece hidroksil grubu etkilenir, bu da diğer 5 hidrojen atomunun değişim reaksiyonlarına katılmadığını gösterir.[kaynak belirtilmeli ]
İzotopik izleyici
Bir izotopik izleyici, (ayrıca "izotopik işaretleyici" veya "izotopik etiket") kullanılır kimya ve biyokimya kimyasalı anlamaya yardımcı olmak için tepkiler ve etkileşimler. Bu teknikte, bir veya daha fazla atomlar of molekül ilgilenilen aynı atomun yerine ikame edilir kimyasal element ama farklı izotop (bir radyoaktif kullanılan izotop radyoaktif izleme ). Etiketli atom aynı sayıda protona sahip olduğu için, neredeyse tamamen etiketlenmemiş muadili ile aynı şekilde davranacak ve birkaç istisna dışında, araştırılan reaksiyona müdahale etmeyecektir. Sayısındaki fark nötronlar ancak aynı elementin diğer atomlarından ayrı olarak tespit edilebileceği anlamına gelir.
Nükleer manyetik rezonans (NMR) ve kütle spektrometrisi (MS), kimyasal reaksiyonların mekanizmalarını araştırmak için kullanılır. NMR ve MS, izotopik farklılıkları tespit ederek, etiketlenmiş atomların ürünlerin yapısındaki konumu hakkında bilgi verilmesine olanak tanır. Ürünlerdeki izotopik atomların konumlandırılmasına ilişkin bilgilerle, ilk metabolitlerin ürünlere dönüştürmek için kullandıkları reaksiyon yolu belirlenebilir. Radyoaktif izotoplar, aşağıdakiler kullanılarak test edilebilir: otoradyograflar içindeki jel sayısı jel elektroforezi. Radyoaktif izotopları içeren bileşiklerin yaydığı radyasyon bir parça karartır. fotoğrafik film, etiketlenmiş bileşiklerin jel içinde birbirlerine göre konumlarının kaydedilmesi.
İzotop izleyiciler, genellikle izotop oranları şeklinde kullanılır. Aynı elementin iki izotopu arasındaki oranı inceleyerek, genellikle izotopik bolluklardaki çok daha küçük varyasyonları batıran, elementin genel bolluğunu içeren etkilerden kaçınıyoruz. İzotopik izleyiciler, en önemli araçlardan bazılarıdır. jeoloji çünkü toprak sistemlerinde karmaşık karıştırma süreçlerini anlamak için kullanılabilirler. Jeolojide izotopik izleyicilerin uygulamasına ilişkin daha fazla tartışma, başlığı altında ele alınmıştır. izotop jeokimyası.
İzotopik izleyiciler genellikle iki kategoriye ayrılır: kararlı izotop izleyiciler ve radyojenik izotop izleyiciler. Kararlı izotop izleyiciler yalnızca radyojenik olmayan izotopları içerir ve genellikle kütleye bağlıdır. Teorik olarak, iki kararlı izotoplu herhangi bir element, izotopik izleyici olarak kullanılabilir. Bununla birlikte, en yaygın olarak kullanılan kararlı izotop izleyiciler, doğal sistemlerde kolayca fraksiyonlaşmaya uğrayan nispeten hafif izotopları içerir. Ayrıca bakınız izotopik imza. Radyojenik bir izotop izleyici [2] tarafından üretilen bir izotop içerir radyoaktif bozunma Genellikle radyojenik olmayan bir izotop ile orantılı olan (yeryüzündeki bolluğu radyoaktif bozunma nedeniyle değişmeyen).
Kararlı izotop etiketleme
Bu bölüm için ek alıntılara ihtiyaç var doğrulama. (Kasım 2011) (Bu şablon mesajını nasıl ve ne zaman kaldıracağınızı öğrenin) |
Kararlı izotop etiketleme, radyoaktif olmayanların kullanılmasını içerir. izotoplar Bu, birkaç kimyasal ve biyokimyasal sistemi modellemek için kullanılan bir izleyici görevi görebilir. Seçilen izotop, bu bileşik üzerinde şu şekilde tanımlanabilen bir etiket görevi görebilir. nükleer manyetik rezonans (NMR) ve kütle spektrometrisi (HANIM). En yaygın kararlı izotoplardan bazıları 2H, 13C ve 15N, ayrıca üretilebilir NMR çözücüler, amino asitler, nükleik asitler, lipidler, Yaygın metabolitler ve hücre büyümesi medya.[4] Kararlı izotoplar kullanılarak üretilen bileşikler ya etiketlenmiş izotopların yüzdesi ile belirtilir (yani% 30 eşit şekilde etiketlenmiş 13C glikoz% 30 ile etiketlenmiş bir karışım içerir. 13 karbon izotopu ve% 70 doğal olarak etiketlenmiş karbon) veya bileşik üzerindeki özel olarak etiketlenmiş karbon pozisyonları (yani 1-13Glikozun ilk karbon konumunda etiketlenmiş olan C glukoz).
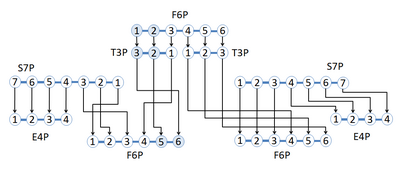
Bir tepkiler ağı benimsendi glikoliz yolu ve pentoz fosfat yolu etiketli karbon izotopunun reaksiyon ağı boyunca farklı karbon pozisyonlarına yeniden düzenlendiği gösterilmiştir. Ağ şununla başlar: fruktoz 6-fosfat (F6P), etiketli 6 karbon atomuna sahip 131. ve 2. karbon konumunda C. 1,2-13C F6P iki olur gliseraldehit 3-fosfat (G3P), bir 2,3-13C T3P ve bir etiketlenmemiş T3P. 2,3-13C T3P artık aşağıdakilerle reaksiyona sokulabilir: sedoheptuloz 7-fosfat (S7P) etiketlenmemiş bir eritroz 4-fosfat (E4P) ve 5,6-13C F6P. Etiketsiz T3P, etiketlenmemiş ürünleri sentezlemek için S7P ile reaksiyona girecektir.[3] Şekil, pozisyona özel etiketli bileşikler kullanılarak reaksiyonlar yoluyla karbon atomu yeniden düzenlenmesini keşfetmek için kararlı izotop etiketlemesinin kullanımını göstermektedir.
Kararlı izotop etiketleme kullanarak metabolik akı analizi

Metabolik akı analizi (MFA) kararlı kullanarak izotop etiketleme, belirli elementlerin akışını açıklamak için önemli bir araçtır. metabolik yollar ve tepkiler içinde hücre. Hücreye bir izotopik etiket verilir, ardından etiketli yem kullanılarak hücrenin büyümesine izin verilir. Sabit metabolik akı analizi için hücrenin bir kararlı hal (hücreye giren ve çıkan izotoplar zamanla sabit kalır) veya yarı kararlı durum (belirli bir süre boyunca kararlı duruma ulaşılır).[5] Çıkışın izotop modeli metabolit belirlendi. Çıkış izotop modeli, büyüklüğünü bulmak için kullanılabilecek değerli bilgiler sağlar. akı, dönüşüm oranı reaktanlar -e Ürün:% s her tepkiyle.[6]
Şekil, belirli bir reaksiyon yoluyla akıyı belirlemek için farklı etiketler kullanma yeteneğini gösterir. Üç karbonlu bir bileşik olan orijinal metabolitin, bir reaksiyonda iki karbonlu bir metabolit ve bir karbon metabolitine bölünme ve sonra yeniden birleştirme veya üç karbonlu bir metabolit olarak kalma yeteneğine sahip olduğunu varsayalım. Reaksiyon, eşit oranda metabolitin iki izotopu ile sağlanırsa, biri tamamen etiketlenmiş (mavi daireler), genellikle tek tip olarak etiketlenmiş olarak bilinir ve biri tamamen etiketlenmemiş (beyaz daireler). Diyagramın sol tarafındaki yol, metabolitlerde herhangi bir değişiklik göstermezken, sağ taraf bölünmeyi ve rekombinasyonu gösterir. Gösterildiği gibi, metabolit sadece sol taraftaki yolu alıyorsa, 50–50 oranında üniform olarak etiketlenmiş ve etiketlenmemiş metabolit oranında kalır. Metabolit yalnızca sağ tarafı alırsa, hepsi eşit oranlarda yeni etiketleme modelleri oluşabilir. Orijinal metabolitin ne kadarının yolun sağ tarafına karşı yolun sol tarafını takip ettiğine bağlı olarak başka oranlar oluşabilir. Burada, metabolitlerin yarısının sol tarafı ve yarısının sağ tarafını aldığı, ancak diğer oranların oluşabileceği bir durum için oranlar gösterilmiştir.[7] Bir bileşikteki bu etiketlenmiş atomlar ve etiketlenmemiş atomlar, izotopomerler. Farklı etiketlenmiş metabolitlerin izotopomer dağılımını ölçerek, her reaksiyon boyunca akı belirlenebilir.[8]
MFA, izotop etiketlemeden toplanan verileri, stokiyometri her reaksiyonun kısıtlamalar ve bir optimizasyon prosedürü bir akı haritasını çözer. İrtersinir reaksiyonlar Akıları bulmak için gereken termodinamik kısıtlamaları sağlar. Bir matris reaksiyonların stokiyometrisini içeren inşa edilmiştir. hücre içi akılar, bir yinelemeli yöntem simüle edilmiş akıların stokiyometrik modele takıldığı. Simüle edilen akılar, her reaksiyon için ürünlere dönüştürülen reaktanların oranını gösteren bir akı haritasında görüntülenir.[6] Çoğu akı haritasında, ok ne kadar kalınsa, reaksiyonun akı değeri o kadar büyük olur.[9]
İzotop etiketleme ölçüm teknikleri
Arasındaki farkı ölçmek için herhangi bir teknik izotopomerler kullanılabilir. İki temel yöntem, nükleer manyetik rezonans (NMR) ve kütle spektrometrisi (MS), kararlı izotop etiketlemede kütle izotopomerlerini ölçmek için geliştirilmiştir.
Proton NMR için kullanılan ilk teknikti 13C-etiketleme deneyleri. Bu yöntemi kullanarak, her bir protonlanmış karbon konumu belirli bir metabolit havuzu diğer pozisyonlardan ayrı olarak gözlemlenebilir.[10] Bu, belirli bir konumda etiketlenen izotopomerlerin yüzdesinin bilinmesini sağlar. Proton NMR'nin sınırı, eğer varsa n bir metabolitte karbon atomları, ancak en fazla n toplam izotopomer bilgisinin sadece küçük bir kısmı olan farklı konumsal zenginleştirme değerleri. Proton NMR etiketlemesinin kullanımı sınırlayıcı olsa da, saf proton NMR deneylerini değerlendirmek, daha fazla izotopomer bilgisine sahip deneylerden çok daha kolaydır.
Ek olarak Proton NMR, kullanma 13C NMR teknikler, izotopomerlerin dağılımının daha ayrıntılı bir görünümünü sağlayacaktır. Etiketli bir karbon atomu, moleküldeki doğrudan komşularının etiketleme durumuna bağlı olarak farklı aşırı ince bölme sinyalleri üretecektir.[10] Komşu karbon atomları etiketlenmemişse tekli bir tepe ortaya çıkar. Yalnızca bir komşu karbon atomu etiketlenirse çift tepe ortaya çıkar. İkili bölünmenin boyutu, komşu karbon atomunun fonksiyonel grubuna bağlıdır. İki komşu karbon atomu etiketlenirse, ikili bölünmeler eşitse, bir ikili çift üçlü bir üçlü olarak dejenere olabilir.
NMR tekniklerini kullanmanın sakıncaları metabolik akı analizi amacı, diğer NMR uygulamalarından farklı olmasıdır çünkü oldukça özel bir disiplintir. Bir NMR spektrometresi, tüm araştırma ekipleri için doğrudan mevcut olmayabilir. NMR ölçüm parametrelerinin optimizasyonu ve tepe yapılarının doğru analizi, yetenekli bir NMR uzmanı gerektirir. Bazı metabolitler ayrıca ek izotopomer verileri elde etmek için özel ölçüm prosedürleri gerektirebilir. Ek olarak, pik alanların kesin miktarını belirlemek ve dolaşık tekli, ikili ve üçlü piklerin ayrışmasını belirlemek için özel olarak uyarlanmış yazılım araçlarına ihtiyaç vardır.
Nükleer manyetik rezonansın aksine, kütle spektrometresi (MS) metabolik akı analizi deneylerine daha uygulanabilir ve duyarlı olan başka bir yöntemdir. MS cihazları farklı varyantlarda mevcuttur. İki boyutlu nükleer manyetik rezonanstan farklı (2D-NMR ), MS cihazları doğrudan hidrolizat.[10]
Gaz kromatografisi-kütle spektrometrisinde (GC-MS ) MS, hidrolizatın bileşiklerini ayırmak için bir gaz kromatografına bağlanır. GC kolonundan ayrıştırılan bileşikler daha sonra iyonize edilir ve eşzamanlı olarak parçalanır. GC-MS kullanmanın yararı, yalnızca ölçülen moleküler iyonun kütle izotopomerlerinin değil, aynı zamanda birkaç parçanın kütle izotopomer spektrumunun da ölçülen bilgiyi önemli ölçüde artırmasıdır.
Sıvı kromatografi-kütle spektrometrisinde (LC-MS ), GC bir sıvı kromatograf ile değiştirilir.[11] Temel fark, kimyasal türevlendirmenin gerekli olmamasıdır. Bununla birlikte, LC-MS'nin MFA'ya uygulamaları nadirdir.
Her durumda, MS cihazları belirli bir izotopomer dağılımını moleküler ağırlığına böler. Aynı sayıda etiketli karbon atomu içeren belirli bir metabolitin tüm izotopomerleri, bir tepe sinyalinde toplanır. Her izotopomer MS spektrumunda tam olarak bir pike katkıda bulunduğundan, yüzde değeri daha sonra her pik için hesaplanabilir ve böylece kütle izotopomer fraksiyonu elde edilir.[10] N karbon atomlu bir metabolit için n + 1 ölçüm üretilir. Normalleştirmeden sonra, tam olarak n bilgilendirici kütle izotopomer miktarları kalır.[10]
MS tekniklerini kullanmanın dezavantajı, gaz kromatografisi için numunenin, yüklü moleküller elde etmek için kimyasal türevlendirme ile hazırlanmasının gerekmesidir. Örnekleri türetmek için kullanılan çok sayıda bileşik vardır. N, N-Dimetilformamid dimetil asetal (DMFDMA)[12] ve N- (tert-butildimetilsilil) -N-metiltrifloroasetamid (MTBSTFA) [13] amino asitleri türevlendirmek için kullanılan bileşiklerin iki örneğidir.
Ek olarak, gözlenen güçlü izotop etkileri, GC kolonundaki farklı şekilde etiketlenmiş izotopomerlerin tutulma süresini etkiler. GC kolonunun aşırı yüklenmesi de önlenmelidir.[13]
Son olarak, karbon dışındaki diğer atomların doğal bolluğu da kütle izotopomer spektrumunda bir bozukluğa yol açar. Örneğin moleküldeki her oksijen atomu aynı zamanda bir 17O izotopu ve bir 18O izotopu. İzotopların doğal bolluğunun daha önemli bir etkisi, izotopların doğal bolluğuna sahip silikonun etkisidir. 29Si ve 30Si. Si, MS teknikleri için ajanların türevlendirilmesinde kullanılır.[10]
İnsan mineral beslenmesi araştırmalarındaki uygulamalar
Çalışmak için kararlı izotop izleyicilerinin kullanılması mineral insanlarda beslenme ve metabolizma ilk olarak 1960'larda rapor edildi.[14] Radyoizotoplar, insan beslenme araştırmalarında birkaç on yıl önce kullanılmış olsa da, kararlı izotoplar, özellikle radyasyona maruz kalma konusunda yüksek endişelerin olduğu deneklerde daha güvenli bir seçenek sunmuştur, örn. hamile ve emziren kadınlar ve çocuklar. Kararlı izotopların sunduğu diğer avantajlar arasında, uygun radyoizotopları olmayan elementleri inceleme ve uzun vadeli izleyici davranışını inceleme yeteneği bulunur.[15][16] Bu nedenle, kararlı izotopların kullanımı, izotopik olarak zenginleştirilmiş malzemelerin ve inorganik kütle spektrometrelerinin artan bulunabilirliği ile sıradan hale geldi. Radyoizotoplar yerine kararlı izotopların kullanımının birkaç dezavantajı vardır: doğal olarak var olan minerali bozma potansiyeline sahip olan daha büyük miktarlarda izleyici gereklidir; analitik numune hazırlama daha karmaşıktır ve kütle spektrometrisi enstrümantasyon daha maliyetli; tüm vücutta veya belirli dokularda izleyicinin varlığı harici olarak ölçülemez.[17] Bununla birlikte, insan çalışmalarında kararlı izotopları standart hale getirmenin avantajları galip geldi.
İnsan sağlığı için gerekli olan ve özellikle beslenme araştırmacılarının ilgisini çeken minerallerin çoğu, düşük doğal bolluklarından dolayı biyolojik izleyiciler olarak çok uygun olan kararlı izotoplara sahiptir.[15][17] Demir, çinko, kalsiyum, bakır, magnezyum, selenyum ve molibden izotop izleme yöntemlerinin uygulandığı kararlı izotoplara sahip temel mineraller arasındadır. Özellikle demir, çinko ve kalsiyum kapsamlı bir şekilde incelenmiştir.
İncelenen mineral beslenme / metabolizma yönleri arasında emilim ( gastrointestinal sistem vücuda), dağıtım, depolama, boşaltım ve bu işlemlerin kinetiği. İzotop izleyiciler, deneklere ağızdan (yiyecekle birlikte veya yemeksiz veya bir mineral takviyesi ile) ve / veya intravenöz olarak uygulanır. İzotop zenginleşmesi daha sonra kan plazması, eritrositler, idrarda ve / veya dışkıda ölçülür.[18][19] Anne sütünde de zenginleşme ölçülmüştür[20] ve bağırsak içeriği. İzleyici deney tasarımı bazen metabolizmalarındaki farklılıklar nedeniyle mineraller arasında farklılık gösterir. Örneğin, demir emilimi genellikle izleyicinin eritrositlere dahil edilmesiyle belirlenirken, çinko veya kalsiyum emilimi, plazma, idrar veya dışkıda izleyici görünümden ölçülür.[21][22] Birden fazla izotop izleyicinin tek bir çalışmada uygulanması yaygındır, daha güvenilir ölçüm yöntemlerinin kullanımına ve metabolizmanın birden çok yönünün eşzamanlı olarak incelenmesine izin verir.
Diyetten mineral emiliminin ölçümü, genellikle şu şekilde düşünülür: biyoyararlanım izotop izleyici yöntemlerinin beslenme araştırmalarında en yaygın uygulamasıdır. Bu tür çalışmaların amaçları arasında, emilimin gıda türünden (ör. Bitki ve hayvan kaynağı, anne sütü ve formül) ve diyetin diğer bileşenlerinden (ör. fitat ), hastalık ve metabolik bozukluklar (örn. çevresel enterik disfonksiyon ), üreme döngüsü, diyetteki mineral miktarı, kronik mineral eksikliği, denek yaşı ve homeostatik mekanizmalar. Bir mineral için bu tür çalışmalardan elde edilen sonuçlar mevcut olduğunda, mineralin insan fizyolojik ve diyet gereksinimlerinin tahminlerine temel oluşturabilirler.[23][24]
İzleyici, mineral emilimini ve metabolizmasını gözlemlemek amacıyla gıda ile birlikte uygulandığında, içsel veya dışsal bir etiket şeklinde olabilir.[25][26] İçsel bir etiket, gıdaya üretimi sırasında eklenen izotoptur, böylece gıdanın doğal mineral içeriğini zenginleştirirken, dışsal etiketleme, çalışma sırasında yiyeceğe izotop eklenmesini ifade eder. Çok zaman alan ve pahalı bir yaklaşım olduğu için, içsel etiketleme rutin olarak kullanılmamaktadır. Çeşitli gıdaların içsel ve dışsal etiketlemesini kullanarak emilim ölçümlerini karşılaştıran çalışmalar, genel olarak iki etiketleme yöntemi arasında iyi bir uyum gösterdi ve dışsal ve doğal minerallerin insan gastrointestinal sisteminde benzer şekilde ele alındığı hipotezini destekledi.
Zenginleştirme, ölçümünden ölçülür. izotop oranları izotopun bir referans izotop oranı, kütle spektrometresi ile. Farklı araştırmacılar tarafından çoklu zenginleştirme tanımları ve hesaplamaları benimsenmiştir.[27] Aynı anda birden çok izleyici kullanıldığında zenginleştirme hesaplamaları daha karmaşık hale gelir. Zenginleştirilmiş izotop preparatları hiçbir zaman izotopik olarak saf olmadığından, yani doğal olmayan bolluklarda elementin tüm izotoplarını içerdiklerinden, çoklu izotop izleyicilerinin zenginleştirilmesine ilişkin hesaplamalar, her izotop oranının diğer izleyiciler tarafından bozulmasını hesaba katmalıdır.[27]
Kaynak kıtlığı olan ülkelerde mineral eksikliklerinin yaygınlığı ve insan sağlığı ve refahı üzerindeki kritik etkileri nedeniyle, Uluslararası Atom Enerjisi Ajansı yakın zamanda, bu bilginin batılı akademik merkezlerin ötesinde araştırmacılara yayılmasını kolaylaştırmak için kararlı izotop yöntemlerinin ayrıntılı ve kapsamlı açıklamalarını yayınladı.[21][28]
Radyoizotopik etiketleme
Radyoizotopik etiketleme, bir madde örneğinin bir sistemden geçişini izlemek için kullanılan bir tekniktir. Madde dahil edilerek "etiketlenir" radyonüklitler kimyasal bileşiminde. Bunlar ne zaman çürüme, varlığı tespit edilerek belirlenebilir. radyasyon onlar tarafından yayılır. Radyoizotopik etiketleme, özel bir izotopik etiketleme durumudur.
Bu amaçlar için, özellikle yararlı bir radyoaktif bozunma türü, pozitron emisyonu. Bir pozitron bir elektronla çarpıştığında, iki yüksek enerjili açığa çıkarır. fotonlar taban tabana zıt yönlerde seyahat. Pozitron katı bir nesne içinde üretilirse, bunu bir milimetreden fazla seyahat etmeden önce yapması muhtemeldir.[kaynak belirtilmeli ] Bu fotonların her ikisi de tespit edilebilirse, bozunma olayının yeri çok kesin bir şekilde belirlenebilir.
Kesin konuşursak, radyoizotopik etiketleme yalnızca radyoaktivitenin deneyciler tarafından yapay olarak tanıtıldığı durumları içerir, ancak bazı doğal fenomenler benzer analizlerin yapılmasına izin verir. Özellikle, radyometrik tarihleme yakından ilgili bir ilke kullanır.
Proteomikteki uygulamalar
İçinde proteomik, tam setin çalışması proteinler ile ifade edilen genetik şifre, tanımlama hastalıklar biyobelirteçler kullanımını içerebilir hücre kültüründe amino asitlerle kararlı izotop etiketlemesi (SILAC), protein seviyelerini tahmin etmek için kullanılan izotopik etiketli amino asit formları sağlar.[29] Protein rekombinantında, manipüle edilmiş proteinler büyük miktarlarda üretilir ve izotop etiketleme, ilgili proteinleri test etmek için bir araçtır. Yöntem, çekirdeklerin seçici olarak zenginleştirilmesi hakkındaydı. 13C veya 15N veya tükenmek 1H onlardan. Rekombinant şu şekilde ifade edilecektir: E. coli içeren medya ile 15N-Amonyum Klorür bir nitrojen kaynağı olarak.[30] Sonuç 15N etiketli proteinler daha sonra hareketsizleştirilmiş metal afinitesi ile saflaştırılır ve yüzdeleri tahmin edilir. Etiketli proteinlerin verimini artırmak ve izotop etiketli ortamın maliyetini azaltmak için alternatif bir prosedür, minimum miktarda etiketli ortama sokmadan önce etiketlenmemiş ortamı kullanarak hücre kütlesini öncelikle artırır.[31] İzotop etiketlemenin başka bir uygulaması, DNA sentezini, yani hücre proliferasyonunu ölçmek olacaktır. laboratuvar ortamında. H kullanır3-Hücrelerdeki sentez (veya sekans) modelini karşılaştırmak için timidin etiketlemesi.[32]
Ekosistem süreç analizi için uygulamalar
İzotopik izleyiciler, doğal sistemlerdeki, özellikle karasal ve su ortamlarındaki süreçleri incelemek için kullanılır. Toprak biliminde 15N izleyici, nitrojen döngüsünü incelemek için yaygın olarak kullanılırken 13C ve 14C, kararlı karbon ve radyoizotoplar, organik bileşiklerin cirosunu ve fiksasyonunu incelemek için kullanılır. CO
2 tarafından ototroflar. Örneğin, Marsh ve ark. (2005) çift etiketli (15N- ve 14C) üre bileşiğin kullanımını göstermek için amonyak hem enerji kaynağı (amonyak oksidasyonu) hem de karbon kaynağı (kemoototrofik karbon fiksasyonu) olarak oksitleyiciler.[33]
Oşinografi için başvurular
İzleyiciler de yaygın olarak kullanılmaktadır. oşinografi çok çeşitli süreçleri incelemek. Kullanılan izotoplar tipik olarak iyi kurulmuş kaynaklarla ve oluşum ve bozulma hızlarıyla doğal olarak meydana gelir. Bununla birlikte, antropojenik izotoplar da büyük başarı ile kullanılabilir. Araştırmacılar, okyanusun fiziksel süreçleri hakkında bilgi elde etmek için farklı konum ve zamanlarda izotopik oranları ölçüyor.
Partikül taşıma
Okyanus, geniş bir parçacık taşıma ağıdır. Toryum izotopları, araştırmacıların maddenin dikey ve yatay hareketini deşifre etmelerine yardımcı olabilir. 234Okyanusta sabit, iyi tanımlanmış bir üretim oranına ve 24 günlük bir yarı ömre sahiptir. Bu doğal olarak oluşan izotopun derinlikle doğrusal olarak değiştiği gösterilmiştir. Bu nedenle, bu doğrusal modeldeki herhangi bir değişiklik, 234Parçacıklar. Örneğin, birkaç metre aşağıda çok yüksek değerlere sahip yüzey suyundaki düşük izotopik oranlar, aşağı yönde dikey bir akıyı gösterir. Ayrıca, partiküllerin yanal taşınmasını deşifre etmek için toryum izotopu belirli bir derinlikte izlenebilmektedir.[34]
Dolaşım
Körfezler, haliçler ve yeraltı suyu gibi yerel sistemlerdeki dolaşım radyum izotopları ile incelenebilir. 223Ra'nın yarı ömrü 11 gündür ve nehirler ve yeraltı suyu kaynaklarındaki belirli yerlerde doğal olarak meydana gelebilir. Radyumun izotopik oranı, kaynak nehirden gelen su bir körfeze veya haliç girdikçe azalacaktır. Miktarını ölçerek 223Ra, bir dizi farklı yerde, bir dolaşım düzeni deşifre edilebilir.[35] Aynı süreç, yeraltı suyunun hareketini ve deşarjını incelemek için de kullanılabilir.[36]
Küresel ölçekte dolaşımı incelemek için çeşitli kurşun izotopları kullanılabilir. Farklı okyanusların (yani Atlantik, Pasifik, Hint vb.) Farklı izotopik imzaları vardır. Bu, farklı okyanuslardaki çökeltilerin ve kayaların izotopik oranlarındaki farklılıklardan kaynaklanmaktadır.[37] Farklı kurşun izotoplarının 50–200 yıllık yarı ömürleri olduğundan, izotopik oranların tüm okyanus boyunca homojenize olması için yeterli zaman yoktur. Bu nedenle, farklı okyanusların dolaşımını incelemek için Pb izotopik oranlarının kesin analizi kullanılabilir.[38]
Tektonik süreçler ve iklim değişikliği
Son derece uzun yarı ömre sahip izotoplar ve bozunma ürünleri, tektonik ve aşırı iklim değişikliği gibi milyonlarca yıllık süreçleri incelemek için kullanılabilir. Örneğin, rubidyum-stronsiyum yaş tayini, stronsiyumun izotopik oranı (87Sr /86Sr), dünyanın ömrü boyunca meydana gelen değişiklikleri incelemek için buz çekirdeklerinde analiz edilebilir. Buz çekirdeği içindeki bu orandaki farklılıklar, dünyanın jeokimyasında önemli değişikliklere işaret edecektir.[38]
Yukarıda bahsedilen işlemler, doğal olarak oluşan izotoplar kullanılarak ölçülebilir. Bununla birlikte, antropojenik izotoplar, oşinografik ölçümler için son derece faydalıdır. Nükleer silah testleri, dünya okyanuslarına çok sayıda nadir izotop bıraktı. 3H, 129Ben ve 137Cs deniz suyunda çözünmüş halde bulunurken 241Am ve 238Pu parçacıklara bağlanır. Suda çözünen izotoplar, küresel dolaşımın incelenmesinde özellikle yararlıdır. Örneğin, bir okyanus içindeki yanal izotopik oranlardaki farklılıklar, güçlü su cephelerini veya girdapları gösterebilir.[39] Tersine, parçacıklara bağlanan izotoplar, su kolonları içindeki kütle taşınmasını incelemek için kullanılabilir. Örneğin, yüksek Am veya Pu seviyeleri, downwelling büyük derinliklerde gözlemlendiğinde veya yükselen yüzeyde görüldüğünde.[40]
İzotopik etiketleme yöntemleri
- Kimyasal sentez
- Enzim aracılı değişim
- Rekombinant protein ifadesi izotopik etiketli ortamda.
Ayrıca bakınız
- Radyonüklitlerin kullanımı
- Biyolojide radyoaktivite
- Radyoaktif izleyici
- İzotopomer
- İzotopolog
- İzobarik etiketleme
- İzotop seyreltme
- Metal karbonillerin kızılötesi spektroskopisi
- Organel proteinlerinin izotop yöntemi etiketleme ile lokalizasyonu
Referanslar
- ^ Blake, Michael E .; Bartlett, Kevin L .; Jones, Maitland (2003). "Bir Fenil Grubunun 1,2-Kayması Yoluyla Am-Benzyne To-Benzyne Dönüşümü". Amerikan Kimya Derneği Dergisi. 125 (21): 6485–6490. doi:10.1021 / ja0213672. ISSN 0002-7863. PMID 12785789.
- ^ Dickin, A.P., 2005. Radyojenik İzotop Jeolojisi, Cambridge University Press.
- ^ a b Kruger, Nicholas; Antje von Schaewen (2003). "Oksidatif pentoz fosfat yolu: yapı ve organizasyon" (PDF). Bitki Biyolojisinde Güncel Görüş. 6 (3): 236–246. doi:10.1016 / s1369-5266 (03) 00039-6. PMID 12753973. Arşivlenen orijinal (PDF) 15 Nisan 2012.
- ^ [1] Arşivlendi 4 Nisan 2012, Wayback Makinesi
- ^ Wiechert, Wolfgang (2001). "13C Metabolik Akı Analizi". Metabolik Mühendislik. 3 (3): 195–206. doi:10.1006 / mben.2001.0187. PMID 11461141.
- ^ a b Lee, Sang Yup; Park, Jong Myoung ve Kim, Tae Yong (2011). Dördüncü Bölüm: Metabolik Akı Analizinin Metabolik Mühendisliğinde Uygulaması. Enzimolojide Yöntemler. 498. sayfa 67–93. doi:10.1016 / B978-0-12-385120-8.00004-8. ISBN 9780123851208. PMID 21601674.CS1 bakım: birden çok isim: yazarlar listesi (bağlantı)
- ^ Stephanopoulos, Gregory; Aristos A. Aristidou (1998). "Bölüm 9: Metabolik Akıların İzotop Etiketleme ile Deneysel Belirlenmesine Yönelik Yöntemler". Metabolik mühendislik: ilkeler ve metodolojiler. San Diego: Akademik Basın. s. 356–404. ISBN 978-0-12-666260-3.
- ^ Stephanopoulos Gregory (1999). "Metabolik Akılar ve Metabolik Mühendisliği". Metabolik Mühendislik. 1 (1): 1–11. doi:10.1006 / mben.1998.0101. PMID 10935750.
- ^ Klamt, Steffen; Jorg Stelling, Martin Ginkel ve Ernst Dieter Gilles (2003). "FluxAnalyzer: etkileşimli akı haritalarında metabolik ağlardaki yapıyı, yolları ve akı dağılımlarını keşfetmek". Biyoinformatik. 19 (2): 261–269. doi:10.1093 / biyoinformatik / 19.2.261. PMID 12538248.CS1 bakım: birden çok isim: yazarlar listesi (bağlantı)
- ^ a b c d e f Wiechert, Wolfgang (2001). "13C Metabolik Akı Analizi". Metabolik Mühendislik. 3 (3): 195–206. doi:10.1006 / mben.2001.0187. PMID 11461141.
- ^ de Graaf, A.A. (2000c). Metabolik akı analizinde 13C etiketleme ve NMR spektroskopisinin kullanımı. İçinde Biyoteknolojide NMR: Teori ve Uygulamalar (J.-N. Barbotin ve J.-C. Portais, Eds.), Horizon Scientific Press.
- ^ Christensen, B. ve Nielsen, J. (2000). 13C etiketli glukoz kullanılarak Penicillium chrysogenum'un metabolik ağ analizi. Biotechnol. Bioeng. 68, 652-659.
- ^ a b Dauner, M. ve Sauer, U. (2000). Amino asitlerin GC-MS analizi, izotopomer dengelemesi için hızla zengin bilgi sağlar. Biotechnol. Prog. 16, 642-649.
- ^ Turnlund Judith (1989). "Sabit izotopların mineral beslenme araştırmalarında kullanımı". Beslenme Dergisi. 119 (1): 7–14. doi:10.1093 / jn / 119.1.7. PMID 2643698.
- ^ a b Woodhouse, Leslie; Abrams Steven (2001). "Kararlı-izotop Metodolojisindeki Gelişmeler". Lowe, Nicola'da; Jackson, Malcolm (editörler). İnsandaki Eser Elementlerin Analizi için İzotop Yöntemlerindeki Gelişmeler. Boca Raton, FL: CRC Press. s. 1–22. ISBN 0-8493-8730-2. OCLC 44579072.CS1 Maintenance: tarih ve yıl (bağlantı)
- ^ Patterson, Kristine; Veillon, Claude (2001). "İnsan beslenme araştırmalarında metabolik izleyiciler olarak minerallerin kararlı izotopları". Deneysel Biyoloji ve Tıp. 226 (4): 271–282. doi:10.1177/153537020122600403. PMID 11368418. S2CID 41966154.
- ^ a b Sandstrom, Brittmarie (1996). "İzotop yöntemlerine ve inorganik besin metabolizmasına genel bakış". Mellon'da, Fred; Sandstrom, Brittmarie (editörler). İnsan beslenmesinde kararlı izotoplar: inorganik besin metabolizması. Londra: Harcourt Brace. s. 3–9. ISBN 0-12-490540-4. OCLC 35224694.CS1 Maintenance: tarih ve yıl (bağlantı)
- ^ van Dokkum, Wim; Fairweather-Tait, Susan; Hurrell, Richard; Sandstrom, Brittmarie (1996). "Çalışma Teknikleri". Mellon'da, Fred; Sandstrom, Brittmarie (editörler). İnsan Beslenmesinde Kararlı İzotoplar: İnorganik Besin Metabolizması. Londra: Akademik Basın. sayfa 23–42. ISBN 0-12-490540-4.
- ^ Fairweather-Tait, Susan; Fox, Tom; Harvey, L; Zarif Jack (2001). "Eser Element Soğurma Analiz Yöntemleri". Lowe, Nicola'da; Jackson, Malcolm (editörler). İnsandaki Eser Elementlerin Analizi için İzotop Yöntemlerindeki Gelişmeler. Boca Raton, FL: CRC Press. s. 59–80. ISBN 0-8493-8730-2.
- ^ Davidsson, Lena (2001). "Bebeklerde ve Hamile veya Emziren Kadınlarda Eser Element Çalışmaları". Lowe, Nicola'da; Jackson, Malcolm (editörler). İnsandaki Eser Elementlerin Analizi için İzotop Yöntemlerindeki Gelişmeler. Boca Raton, FL: CRC Press. s. 167–186. ISBN 0-8493-8730-2.
- ^ a b Davidsson, L. (Lena), 1957- (2012). Stabil demir izotop teknikleri kullanılarak insanlarda demir biyoyararlanımının değerlendirilmesi. Uluslararası Atom Enerjisi Ajansı. Viyana: Uluslararası Atom Enerjisi Ajansı. ISBN 978-92-0-126510-4. OCLC 819377220.CS1 bakım: birden çok isim: yazarlar listesi (bağlantı)
- ^ Krebs, Nancy; Miller, Leland; Naake, Vernon; Lei, Sian; Westcott, Jamie; Fennessey, Paul; Hambidge, Michael (1995). "Çinko metabolizmasını değerlendirmek için kararlı izotop tekniklerinin kullanılması". Beslenme Biyokimyası Dergisi. 6 (6): 292–301. doi:10.1016 / 0955-2863 (95) 00043-Y.
- ^ DRI: A vitamini, K vitamini, arsenik, bor, krom, bakır, iyot, demir, manganez, molibden, nikel, silikon, vanadyum ve çinko için beslenme referans alımları: Mikrobesinler ... ve Daimi Üzerine Panel raporu Diyet Referans Alımlarının Bilimsel Değerlendirme Komitesi, Gıda ve Beslenme Kurulu, Tıp Enstitüsü. Tıp Enstitüsü (ABD). Mikro Besinler Paneli. Washington, D.C .: National Academy Press. 2001. ISBN 0-309-51199-2. OCLC 52777031.CS1 Maint: diğerleri (bağlantı)
- ^ Avrupa Gıda Güvenliği Kurumu (2014). "Çinko için Diyet Referans Değerleri Üzerine Bilimsel Görüş". EFSA Dergisi. 12 (10): 3844. doi:10.2903 / j.efsa.2014.3844. ISSN 1831-4732.
- ^ Fairweather-Tait, Susan; Tilki, Tom (1996). "Gıda Çalışmalarında İnorganik Besinlerin İçsel ve Dışsal Etiketlenmesi". Mellon'da, Fred; Sandstrom, Brittmarie (editörler). İnsan Beslenmesinde Kararlı İzotoplar: İnorganik Besin Metabolizması. Londra: Akademik Basın. s. 15–21. ISBN 0-12-490540-4.
- ^ IAEA. (2018). Stabil Çinko İzotop Teknikleri Kullanılarak İnsanlarda Çinko Metabolizmasının Değerlendirilmesi. Viyana: IAEA. sayfa 34–36. ISBN 978-92-0-108418-7. OCLC 1108521498.
- ^ a b IAEA. (2018). Stabil Çinko İzotop Teknikleri Kullanılarak İnsanlarda Çinko Metabolizmasının Değerlendirilmesi. Viyana: IAEA. s. 50–58. ISBN 978-92-0-108418-7. OCLC 1108521498.
- ^ IAEA. (2018). Stabil Çinko İzotop Teknikleri Kullanılarak İnsanlarda Çinko Metabolizmasının Değerlendirilmesi. Viyana: IAEA. ISBN 978-92-0-108418-7. OCLC 1108521498.
- ^ "Hücre Kültüründe Amino Asit ile Kararlı İzotop Etiketleme." SILAC. Paydey Lab, n.d. Ağ. 23 Kasım 2011.
- ^ Ranza David M. "Klinik Protein Biyobelirteçlerinin Kütle Spektrometrik Kantitasyonu için Dahili Standartlar Olarak Kullanım için Kararlı İzotopik Olarak Etiketlenmiş Proteinlerin İfadesi." NIST, malzeme ölçüm laboratuvarı. Ulusal Standartlar ve Teknoloji Enstitüsü (NIST), ABD Ticaret Bakanlığı'nın bir ajansıdır, 30 Mart 2009. Web. 19 Kasım 2011.
- ^ Marley, Jonathan; Lu, Min; Bracken, Clay (2001). "Etkili izotopik etiketleme ve rekombinent protein için bir yöntem". Biyomoleküler Etiketleme Dergisi. 20 (1): 71–75. doi:10.1023 / a: 1011254402785. PMID 11430757. S2CID 7811948.
- ^ Alman, James. "İnsan kan hücrelerinin kromozomlarındaki DNA sentezinin modeli." Rockefeller üniversite basını. 20.1 37–65. Yazdır.
- ^ Marsh, K. L., G. K. Sims ve R. L. Mulvaney. 2005. Toprağa eklenen 14C- ve 15N-etiketli ürenin akıbetiyle ilgili olarak üreyi ototrofik amonyak oksitleyen bakteriler için mevcudiyet. Biol. Fert. Toprak. 42: 137-145.
- ^ Coppola, L .; Roy-Barman, M .; et al. (2006). "Güney Okyanusu'nun Hint bölümünde parçacık dinamiği ve derin su sirkülasyonunun izleyicileri olarak toryum izotopları (ANTARES IV)". Deniz Kimyası. 100 (3–4): 299–313. doi:10.1016 / j.marchem.2005.10.019.
- ^ Hougham, A. L .; Moran, S. B .; et al. (2008). "İzleyici olarak 226Ra ve 228Ra kullanılarak tahmin edilen kıyı tuz havuzlarına denizaltı yeraltı suyu deşarjındaki mevsimsel değişiklikler". Deniz Kimyası. 109 (3–4): 268–278. doi:10.1016 / j.marchem.2007.08.001.
- ^ Swarzenski, P. W .; Reich, C .; et al. (2007). "Florida, Tampa Körfezi'ndeki denizaltı yeraltı suyu deşarjının doğal izleyicileri olarak Ra ve Rn izotopları". Deniz Kimyası. 104 (1–2): 69–84. doi:10.1016 / j.marchem.2006.08.001.
- ^ Hickey-Vargas, R .; Bizimis, M .; Deschamps, A. (2008). "Filipin Deniz Levhasında Hint Okyanusu izotopik imzasının başlangıcı: Erken Kretase terranlarından Hf ve Pb izotop kanıtı". Dünya ve Gezegen Bilimi Mektupları. 268 (3–4): 255–267. Bibcode:2008E ve PSL.268..255H. doi:10.1016 / j.epsl.2008.01.003.
- ^ a b Haley, B. A .; Frank, M .; et al. (2008). "Arktik Okyanusu sirkülasyonunun radyojenik izotop kaydı ve son 15 milyon yılın ayrışma girdileri". Paleo oşinografi. 23 (1): PA1S13. Bibcode:2008PalOc..23.1S13H. doi:10.1029 / 2007PA001486.
- ^ Povinec, P. P .; Breier, R .; et al. (2011). "Güney Hint Okyanusu'nda çoklu izotop yaklaşımı kullanarak su kütlelerinin izini sürmek". Dünya ve Gezegen Bilimi Mektupları. 302 (1–2): 14–26. Bibcode:2011E ve PSL.302 ... 14P. doi:10.1016 / j.epsl.2010.11.026.
- ^ Lee, S.-H .; Povinec, P. P .; et al. (2009). "Güney Hint Okyanusu'nda su cephelerinin izleyicileri olarak radyonüklitler - ANTARES IV Sonuçları". Oşinografi Dergisi. 65 (3): 397–406. doi:10.1007 / s10872-009-0035-7. S2CID 131348352.
Dış bağlantılar
| Kütüphane kaynakları hakkında İzotopik etiketleme |

