Metagenomik - Metagenomics - Wikipedia

Metagenomik çalışması genetik doğrudan geri kazanılan malzeme çevre örnekler. Geniş alan ayrıca şu şekilde de ifade edilebilir: çevresel genomik, ekojenomik veya topluluk genomiği.
Geleneksel iken mikrobiyoloji ve mikrobiyal genom dizileme ve genomik ekili güvenmek klonal kültürler, erken çevresel gen dizilimi klonlanmış spesifik genleri (genellikle 16S rRNA gen) doğal bir numunede bir çeşitlilik profili oluşturmak için. Bu tür çalışmalar, büyük çoğunluğunun mikrobiyal biyolojik çeşitlilik ekime dayalı yöntemlerle kaçırılmıştı.[2]
Metagenomik, mikroskobik yaşamın daha önce gizli olan çeşitliliğini ortaya çıkarma yeteneği nedeniyle, tüm canlı dünyanın anlayışında devrim yaratma potansiyeline sahip mikrobiyal dünyayı görüntülemek için güçlü bir mercek sunar.[3] DNA dizilemesinin fiyatı düşmeye devam ederken, metagenomikler artık mikrobiyal ekoloji eskisinden çok daha büyük ölçekte ve ayrıntılı olarak incelenecek. Son araştırmalar "pompalı tüfek "veya PCR örneklenen toplulukların tüm üyelerinden tüm genlerin büyük ölçüde tarafsız örneklerini almak için yönlendirilmiş dizileme.[4]
Etimoloji
"Metagenomik" terimi ilk olarak Jo Handelsman, Jon Clardy, Robert M. Goodman, Sean F. Brady ve diğerleri ve ilk olarak 1998'de yayında çıktı.[5] Metagenom terimi, çevreden dizilenen bir gen koleksiyonunun, tek bir araştırmanın çalışmasına benzer bir şekilde analiz edilebileceği fikrine atıfta bulundu. genetik şifre. 2005 yılında Kevin Chen ve Lior Pachter (araştırmacılar California Üniversitesi, Berkeley ) metagenomikleri "türlerin izolasyonuna ve laboratuvarda yetiştirilmesine gerek kalmadan modern genomik tekniğinin uygulanması" olarak tanımladı.[6]
Tarih
Konvansiyonel sıralama bir kaynak olarak aynı hücrelerden oluşan bir kültürle başlar DNA. Bununla birlikte, erken metagenomik çalışmalar, birçok ortamda muhtemelen büyük mikroorganizma grupları olduğunu ortaya çıkarmıştır. kültürlü ve bu nedenle sıralanamaz. Bu erken çalışmalar 16S'ye odaklandı ribozomal RNA (rRNA) nispeten kısa diziler, genellikle korunmuş bir tür içinde ve genellikle türler arasında farklıdır. Birçok 16S rRNA bilinen herhangi bir kültüre ait olmayan diziler bulundu Türler, çok sayıda izole edilmemiş organizma olduğunu gösterir. Doğrudan çevreden alınan ribozomal RNA genlerinin bu araştırmaları, yetiştirme temelli yöntemler bakteriyelin% 1'den azını bulur ve arkayal bir örnekteki türler.[2] Metagenomiklere olan ilginin çoğu, mikroorganizmaların büyük çoğunluğunun daha önce fark edilmediğini gösteren bu keşiflerden geliyor.
erken moleküler çalışma sahada tarafından yapıldı Norman R. Pace ve iş arkadaşları PCR ribozomal RNA dizilerinin çeşitliliğini keşfetmek.[7] Bu çığır açan çalışmalardan elde edilen içgörüler, Pace'i 1985 gibi erken bir tarihte doğrudan çevresel örneklerden DNA klonlama fikrini önermeye yöneltti.[8] Bu, ilk izolasyon raporuna yol açtı ve klonlama Pace ve arkadaşları tarafından 1991'de yayınlanan çevresel bir numuneden toplu DNA[9] Pace, Biyoloji Bölümü'ndeyken Indiana Üniversitesi. Önemli çabalar bunların olmamasını sağladı. PCR yanlış pozitifler ve keşfedilmemiş türlerden oluşan karmaşık bir topluluğun varlığını destekledi. Bu metodoloji yüksek oranda korunmuş olanları keşfetmekle sınırlı olsa da, protein kodlamayan genler, çeşitliliğin kültürleme yöntemleriyle bilinenden çok daha karmaşık olduğuna dair erken mikrobiyal morfoloji tabanlı gözlemleri destekledi. Bundan kısa bir süre sonra Healy, laboratuvarda kurutulmuş olarak yetiştirilen karmaşık bir çevresel organizma kültüründen oluşturulan "zoolibraries" den işlevsel genlerin metagenomik izolasyonunu bildirdi. çimen 1995'te.[10] Pace laboratuvarından ayrıldıktan sonra, Edward DeLong alanında devam etti ve 16S imza dizilerine dayanan çevresel soyoluşların temelini oluşturan çalışmalar yayınladı. deniz örnekler.[11]
2002 yılında, Mya Breitbart, Rohwer Ormanı ve meslektaşları, 200 litre deniz suyunun 5000'den fazla farklı virüs içerdiğini göstermek için çevresel av tüfeği sıralamayı (aşağıya bakın) kullandı.[12] Daha sonraki çalışmalar, binden fazla olduğunu gösterdi viral türler insan dışkısında ve muhtemelen kilogram deniz tortusu başına bir milyon farklı virüs bakteriyofajlar. Esasen bu çalışmalardaki tüm virüsler yeni türlerdi. 2004'te Gene Tyson, Jill Banfield ve California Üniversitesi, Berkeley ve Ortak Genom Enstitüsü bir asit maden drenajı sistemi.[13] Bu çaba, bir avuç bakteri için tam veya neredeyse tamamlanmış genomlarla sonuçlandı ve Archaea daha önce onları kültür girişimlerine direnen.[14]
2003'ten itibaren, Craig Venter, özel olarak finanse edilen paralelin lideri İnsan Genom Projesi, yol açtı Küresel Okyanus Örnekleme Gezisi (GOS), dünyanın etrafını dolaşıyor ve yolculuk boyunca metagenomik örnekler topluyor. Bu örneklerin tümü, yeni genomların (ve dolayısıyla yeni organizmaların) tanımlanacağı umuduyla, av tüfeği dizilimi kullanılarak dizilir. Pilot proje, Sargasso Denizi, yaklaşık 2000 farklı Türler 148 tür dahil bakteri daha önce hiç görülmedi.[15] Venter, dünyanın çevresini dolaştı ve Amerika Birleşik Devletleri'nin Batı Kıyısı ve iki yıllık bir keşif gezisini tamamladı. Baltık, Akdeniz ve Siyah Denizler. Bu yolculuk sırasında toplanan metagenomik verilerin analizi, biri 'bayram ya da kıtlık' gibi çevresel koşullara uyarlanmış taksonlardan oluşan iki grup organizma ortaya çıkardı ve ikincisi, nispeten daha az ancak daha bol ve yaygın olarak dağılmış taksonlardan oluşuyor: plankton.[16]
2005 yılında Stephan C. Schuster Penn Eyalet Üniversitesi ve meslektaşları, bir çevresel numunenin ilk dizilerini yayınladı. yüksek verimli sıralama, bu durumda büyük ölçüde paralel Pyrosequencing tarafından geliştirilmiş 454 Yaşam Bilimleri.[17] Bu alandaki bir başka erken makale 2006'da Robert Edwards tarafından yayınlandı, Rohwer Ormanı ve şuradaki meslektaşlarım San Diego Eyalet Üniversitesi.[18]
Sıralama
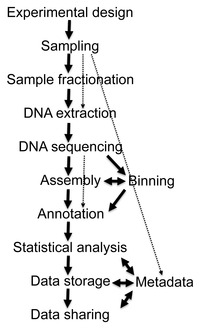
Birkaç binden uzun DNA dizilerinin geri kazanımı baz çiftleri çevreselden örnekler son gelişmelere kadar çok zordu moleküler biyolojik teknikler yapımına izin verdi kütüphaneler içinde bakteriyel yapay kromozomlar (BAC'ler), daha iyi vektörler için moleküler klonlama.[20]
Shotgun metagenomikleri
Gelişmeler biyoinformatik, DNA amplifikasyonunun iyileştirmeleri ve hesaplama gücünün çoğalması, çevresel örneklerden geri kazanılan DNA dizilerinin analizine büyük ölçüde yardımcı olmuş ve av tüfeği sıralaması metagenomik örneklere (tam metagenom shotgun veya WMGS sekanslama olarak da bilinir). Yaklaşım, birçok kültürlenmiş mikroorganizmayı sıralamak için kullanılır ve insan genomu, rastgele DNA keser, birçok kısa diziyi dizer ve yeniden inşa etmek onları bir konsensüs dizisi. Shotgun sıralaması, çevresel örneklerde bulunan genleri ortaya çıkarır. Tarihsel olarak, bu sıralamayı kolaylaştırmak için klon kitaplıkları kullanıldı. Bununla birlikte, yüksek verimli sıralama teknolojilerindeki ilerlemelerle, klonlama adımı artık gerekli değildir ve bu yoğun emek gerektiren darboğaz adımı olmadan daha fazla sıralama verisi verimi elde edilebilir. Shotgun metagenomics, hem hangi organizmaların mevcut olduğu hem de toplulukta hangi metabolik süreçlerin mümkün olduğu hakkında bilgi sağlar.[21] Bir ortamdan DNA toplanması büyük ölçüde kontrolsüz olduğundan, bir çevresel örnekte en bol bulunan organizmalar, sonuçta ortaya çıkan dizi verilerinde en yüksek oranda temsil edilir. Yeterince temsil edilmeyen topluluk üyelerinin genomlarını tam olarak çözmek için gereken yüksek kapsamı elde etmek için, çoğu zaman engelleyici bir şekilde büyük örneklere ihtiyaç vardır. Öte yandan, av tüfeği dizilemesinin rastgele doğası, aksi takdirde geleneksel kültür teknikleri kullanılarak fark edilmeyecek olan bu organizmaların çoğunun, en azından bazı küçük dizi bölümleriyle temsil edilmesini sağlar.[13]
Yüksek verimli sıralama
Yüksek verimli dizilemenin bir avantajı, bu tekniğin sıralanmadan önce DNA'nın klonlanmasını gerektirmemesi ve çevresel örneklemedeki ana önyargılardan ve darboğazlardan birini ortadan kaldırmasıdır. Kullanılarak yapılan ilk metagenomik çalışmalar yüksek verimli sıralama büyük ölçüde paralel kullanıldı 454 Pyrosequencing.[17] Çevresel örneklemede yaygın olarak uygulanan diğer üç teknoloji, Ion Torrent Kişisel Genom Makinesi, Illumina MiSeq veya HiSeq ve Uygulamalı Biyosistemler SOLiD sistemi.[22] DNA'nın sıralanması için bu teknikler, daha kısa fragmanlar oluşturur. Sanger sıralaması; Ion Torrent PGM System ve 454 pyrosequencing tipik olarak ~ 400 bp okuma üretir, Illumina MiSeq 400-700bp okuma üretir (eşleştirilmiş uç seçeneklerinin kullanılıp kullanılmadığına bağlı olarak) ve SOLiD 25-75 bp okuma üretir.[23] Tarihsel olarak, bu okuma uzunlukları, ~ 750 bp'lik tipik Sanger dizileme okuma uzunluğundan önemli ölçüde daha kısaydı, ancak Illumina teknolojisi hızla bu ölçüye yaklaşıyor. Bununla birlikte, bu sınırlama çok daha fazla sayıda dizi okuması ile telafi edilir. 2009'da, piroz dizili metagenomlar 200–500 megabaz üretir ve Illumina platformları yaklaşık 20–50 gigabaz üretir, ancak bu çıktılar son yıllarda büyük sırayla artmıştır.[24]
Ortaya çıkan bir yaklaşım, av tüfeği sıralaması ve kromozom konformasyon yakalama (Hi-C), mikrobiyal genom birleşimini yönlendirmek için aynı hücre içindeki herhangi iki DNA dizisinin yakınlığını ölçer.[25] PacBio RSII ve PacBio Sequel de dahil olmak üzere uzun okumalı sıralama teknolojileri Pasifik Biyolojik Bilimler ve Nanopore MinION, Grigion, PrometION by Oxford Nanopore Teknolojileri, montaj işlemini kolaylaştıracak uzun av tüfeği sıralama okumaları elde etmek için başka bir seçenektir.[26]
Biyoinformatik
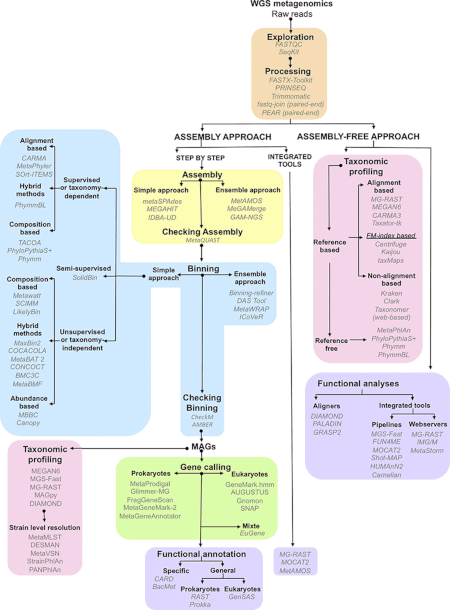
Metagenomik deneylerin ürettiği veriler hem muazzam hem de doğal olarak gürültülüdür ve 10.000 kadar türü temsil eden parçalanmış veriler içerir.[1] İnek dizilimi rumen üretilen metagenom 279 gigabazlar veya 279 milyar baz çift nükleotid dizisi verisi,[28] insan bağırsağı mikrobiyom gen kataloğu, sekans verilerinin 567.7 gigabazından toplanan 3.3 milyon geni tanımladı.[29] Bu büyüklükteki veri kümelerinden yararlı biyolojik bilgilerin toplanması, derlenmesi ve çıkarılması, araştırmacılar için önemli hesaplama zorluklarını temsil eder.[21][30][31][32]
Sıralı ön filtreleme
Metagenomik veri analizinin ilk adımı, gereksiz, düşük kaliteli dizilerin ve olası dizilerin kaldırılması dahil olmak üzere belirli ön filtreleme adımlarının yürütülmesini gerektirir. ökaryotik köken (özellikle insan kaynaklı metagenomlarda).[33][34] Kontamine edici ökaryotik genomik DNA dizilerinin çıkarılması için mevcut yöntemler arasında Eu-Detect ve DeConseq bulunur.[35][36]
Montaj
Genomik ve metagenomik projelerden elde edilen DNA dizisi verileri esasen aynıdır, ancak genomik dizi verileri daha yüksek kapsama metagenomik veriler genellikle fazlalık değildir.[31] Ayrıca, kısa okuma uzunluklarına sahip ikinci nesil dizileme teknolojilerinin artan kullanımı, gelecekteki metagenomik verilerin çoğunun hataya açık olacağı anlamına gelir. Kombinasyon halinde alındığında bu faktörler, metagenomik sekans okumalarının genomlara birleştirilmesini zor ve güvenilmez hale getirir. Yanlış montajlar, tekrarlayan DNA dizileri Bu, örnekte bulunan türlerin nispi bolluğundaki farklılık nedeniyle montajı özellikle zorlaştırır.[37] Yanlış montajlar, birden fazla türden dizilerin kimerik hale getirilmesini de içerebilir. contigs.[37]
Birçok montaj programı vardır ve bunların çoğu çift uçlu etiketler montajların doğruluğunu artırmak için. Gibi bazı programlar Phrap veya Celera Assembler, tekli montaj için kullanılmak üzere tasarlanmıştır. genomlar ancak metagenomik veri setlerini birleştirirken yine de iyi sonuçlar verir.[1] Gibi diğer programlar Kadife montajcı, ikinci nesil dizileme tarafından üretilen daha kısa okumalar için optimize edilmiştir. de Bruijn grafikleri.[38][39] Referans genomların kullanılması, araştırmacıların en bol bulunan mikrobiyal türlerin birleşimini geliştirmelerine olanak tanır, ancak bu yaklaşım, sıralı genomların mevcut olduğu küçük mikrobiyal filum alt kümesiyle sınırlıdır.[37] Bir montaj oluşturulduktan sonra, ek bir zorluk, "metagenomik ters evrişim" veya hangi dizilerin örnekteki hangi türlerden geldiğini belirlemektir.[40]
Gen tahmini
Metagenomik analiz boru hatları monte edilmiş bölümlerdeki kodlama bölgelerinin açıklamasında iki yaklaşım kullanın.[37] İlk yaklaşım, genleri temel alarak tanımlamaktır. homoloji halihazırda halka açık olan genlerle dizi veritabanları, genellikle tarafından ÜFLEME aramalar. Bu tür bir yaklaşım programda uygulanmaktadır MEGAN 4.[41] İkinci, ab initio, ilgili organizmalardan gen eğitim setlerine dayalı olarak kodlama bölgelerini tahmin etmek için dizinin kendine özgü özelliklerini kullanır. Bu gibi programlar tarafından benimsenen yaklaşım budur GeneMark[42] ve PARLAK. Ana avantajı ab initio Tahmin, dizi veri tabanlarında homologlardan yoksun kodlama bölgelerinin saptanmasını sağlamasıdır; bununla birlikte, karşılaştırma için geniş bitişik genomik DNA bölgeleri olduğunda en doğrudur.[1]
Türlerin çeşitliliği
Gen ek açıklamaları "ne" yi sağlarken, türlerin çeşitliliği "kim" i sağlayın.[43] Metagenomlarda topluluk kompozisyonu ve işlevi arasında bağlantı kurmak için diziler gruplanmalıdır. Binning belirli bir diziyi bir organizma ile ilişkilendirme sürecidir.[37] Benzerlik tabanlı gruplamada, aşağıdaki gibi yöntemler ÜFLEME filogenetik belirteçleri veya mevcut kamu veritabanlarında başka türlü benzer dizileri hızla aramak için kullanılır. Bu yaklaşım, MEGAN.[44] PhymmBL adlı başka bir araç, interpolasyonlu Markov modelleri okumaları atamak için.[1] MetaPhlAn ve AMPHORA Geliştirilmiş hesaplama performansları ile organizmaya ait göreli bollukları tahmin etmek için benzersiz sınıfa özgü belirteçlere dayalı yöntemlerdir.[45] Gibi diğer araçlar mOTU'lar[46][47] ve MetaPhyler,[48] prokaryotik türlerin profilini çıkarmak için evrensel işaretleyici genleri kullanın. İle mOTUs profil oluşturucu Mikrobiyal topluluk çeşitliliği tahminini geliştirerek, referans genomu olmayan türlerin profilini çıkarmak mümkündür.[47] Gibi yeni yöntemler SLIMM, yanlış pozitif isabetleri en aza indirmek ve güvenilir göreli bolluklar elde etmek için bireysel referans genomlarının kapsama alanını okuyun.[49] Bileşime dayalı gruplamada yöntemler, dizinin oligonükleotid frekansları gibi kendine özgü özelliklerini kullanır veya kodon kullanım eğilimi.[1] Diziler gruplandırıldıktan sonra, çeşitlilik ve zenginliğin karşılaştırmalı analizini yapmak mümkündür.
Veri entegrasyonu
Katlanarak büyüyen sıra verilerinin muazzam miktarı, veri tabanının karmaşıklığı nedeniyle karmaşık olan göz korkutucu bir sorundur. meta veriler metagenomik projelerle ilişkili. Meta veriler, numunenin üç boyutlu (derinlik veya yükseklik dahil) coğrafyası ve çevresel özellikleri hakkında ayrıntılı bilgileri, numune sahası hakkında fiziksel verileri ve numune alma metodolojisini içerir.[31] Bu bilgi hem sağlamak için gereklidir tekrarlanabilirlik ve aşağı akış analizi sağlamak için. Öneminden dolayı, meta veriler ve işbirliğine dayalı veri inceleme ve iyileştirme, Genomes OnLine Database (GOLD) gibi özel veritabanlarında bulunan standartlaştırılmış veri formatlarını gerektirir.[50]
Meta verileri ve sekans verilerini entegre etmek için çeşitli araçlar geliştirilmiştir, bu da bir dizi ekolojik indeks kullanılarak farklı veri kümelerinin aşağı akış karşılaştırmalı analizlerine olanak tanır. 2007'de Folker Meyer ve Robert Edwards ve bir ekip Argonne Ulusal Laboratuvarı ve Chicago Üniversitesi Subsystem Technology sunucusunu kullanarak Metagenomics Rapid Annotation'ı yayınladı (MG-RAST ) metagenom veri seti analizi için bir topluluk kaynağı.[51] Haziran 2012 itibarıyla 14,8 terabazın (14x1012 DNA bazları) analiz edildi ve MG-RAST içinde karşılaştırma için ücretsiz olarak sunulan 10.000'den fazla kamuya açık veri seti. Şu anda 8.000'den fazla kullanıcı MG-RAST'a toplam 50.000 metagenom göndermiştir. Entegre Mikrobiyal Genomlar / Metagenomlar (IMG / M) sistemi ayrıca, metagenom dizilerine dayalı olarak mikrobiyal toplulukların fonksiyonel analizi için bir araç koleksiyonu sağlar. Entegre Mikrobiyal Genomlar (IMG) sistemi ve Bakteri ve Arkeaların Genomik Ansiklopedisi (GEBA) proje.[52]
Yüksek verimli metagenom av tüfeği verilerini analiz etmek için ilk bağımsız araçlardan biri MEGAN (MEta Genom Analizörü).[41][44] Programın ilk versiyonu, bir dev kemiğinden elde edilen DNA dizilerinin metagenomik bağlamını analiz etmek için 2005 yılında kullanıldı.[17] Bir referans veritabanı ile BLAST karşılaştırmasına dayalı olarak, bu araç, okumaları NCBI taksonomisinin düğümlerine basit bir en düşük ortak ata (LCA) algoritması veya düğümlerin üzerine yerleştirerek hem taksonomik hem de işlevsel gruplamayı gerçekleştirir. TOHUM veya KEGG sırasıyla sınıflandırmalar.[53]
Hızlı ve ucuz dizileme araçlarının ortaya çıkmasıyla, DNA dizilerinin veri tabanlarının büyümesi artık üsteldir (örneğin, NCBI GenBank veri tabanı [54]). MG-RAST veya MEGAN gibi BLAST tabanlı yaklaşımlar, büyük numunelere açıklama eklemek için yavaş çalıştığından (örneğin, küçük / orta büyüklükte bir veri setini / numuneyi işlemek için birkaç saat), yüksek verimli sıralamanın hızına ayak uydurmak için daha hızlı ve verimli araçlara ihtiyaç vardır. [55]). Böylece, daha uygun fiyatlı güçlü sunucular sayesinde son zamanlarda ultra hızlı sınıflandırıcılar ortaya çıkmıştır. Bu araçlar taksonomik ek açıklamayı son derece yüksek hızda gerçekleştirebilir, örneğin CLARK [56] (CLARK'ın yazarlarına göre, "dakikada 32 milyon metagenomik kısa okumayı" doğru bir şekilde sınıflandırabilir). Böyle bir hızda, çok büyük bir veri kümesi / milyarlarca kısa okumadan oluşan örnek yaklaşık 30 dakika içinde işlenebilir.
Antik DNA içeren örneklerin artan bulunabilirliği ve bu örneklerin doğasıyla ilişkili belirsizlik nedeniyle (antik DNA hasarı),[57] muhafazakar benzerlik tahminleri üretebilen hızlı bir araç kullanıma sunulmuştur. FALCON'un yazarlarına göre, bellek ve hız performansını etkilemeden gevşetilmiş eşikler kullanabilir ve mesafeleri düzenleyebilir.
Karşılaştırmalı metagenomik
Metagenomlar arasındaki karşılaştırmalı analizler, karmaşık mikrobiyal toplulukların işlevi ve konakçı sağlığındaki rolleri hakkında ek bilgiler sağlayabilir.[58] Metagenomlar arasında ikili veya çoklu karşılaştırmalar, sekans kompozisyonu düzeyinde yapılabilir (karşılaştırma GC içeriği veya genom boyutu), taksonomik çeşitlilik veya fonksiyonel tamamlayıcı. Popülasyon yapısı ve filogenetik çeşitliliğin karşılaştırmaları 16S ve diğer filogenetik işaretçi genler temelinde veya - düşük çeşitlilikte topluluklar olması durumunda - metagenomik veri setinden genom rekonstrüksiyonu ile yapılabilir.[59] Metagenomlar arasındaki fonksiyonel karşılaştırmalar, dizileri aşağıdaki gibi referans veri tabanlarıyla karşılaştırarak yapılabilir. ÇARK DİŞİ veya KEGG ve bolluğu kategoriye göre tablo haline getirmek ve istatistiksel anlamlılık için herhangi bir farklılığı değerlendirmek.[53] Bu gen merkezli yaklaşım, topluluk taksonomik gruplardan ziyade bir bütün olarak ve fonksiyonel tamamlayıcıların benzer çevresel koşullar altında analog olduğunu gösterir.[59] Sonuç olarak, metagenomik örneğin çevresel bağlamına ilişkin meta veriler, araştırmacılara habitatın topluluk yapısı ve işlevi üzerindeki etkisini inceleme yeteneği sağladığından, karşılaştırmalı analizlerde özellikle önemlidir.[1]
Ek olarak, çeşitli çalışmalar, çeşitli mikrobiyal topluluklar arasındaki farklılıkları belirlemek için oligonükleotid kullanım modellerini de kullanmıştır. Bu tür metodolojilerin örnekleri, Willner ve diğerleri tarafından dinükleotid göreceli bolluk yaklaşımını içerir.[60] ve Ghosh ve diğerlerinin HabiSign yaklaşımı.[61] Bu son çalışma ayrıca, tetranükleotid kullanım şekillerindeki farklılıkların, belirli habitatlardan kaynaklanan genleri (veya metagenomik okumaları) tanımlamak için kullanılabileceğini gösterdi. Ayrıca TriageTools gibi bazı yöntemler[62] veya Compareads[63] iki okuma seti arasında benzer okumaları tespit edin. benzerlik ölçüsü Okumalara uygulanırlar, birkaç aynı uzunluktaki kelimeye dayanır k okuma çiftleri tarafından paylaşılır.
Karşılaştırmalı metagenomikteki temel amaç, belirli bir ortama belirli özellikler kazandırmaktan sorumlu mikrobiyal grup (lar) ı belirlemektir. Ancak, dizileme teknolojilerindeki sorunlar nedeniyle, yapay nesnelerin metagenomeSeq'deki gibi hesaba katılması gerekir.[30] Diğerleri, yerleşik mikrobiyal gruplar arasındaki mikrobiyal etkileşimleri karakterize etmiştir. Bir GUI Community-Analyzer adlı karşılaştırmalı metagenomik analiz uygulaması, Kuntal ve ark. [64] Bu, analiz edilen mikrobiyal topluluklardaki farklılıkların (taksonomik bileşimleri açısından) hızlı bir şekilde görselleştirilmesini kolaylaştırmakla kalmayıp, aynı zamanda burada meydana gelen içsel mikrobiyal etkileşimlere ilişkin içgörüler sağlayan korelasyon tabanlı bir grafik yerleşim algoritması uygular. Özellikle, bu düzen algoritması, çeşitli taksonomik grupların bolluk değerlerini basitçe karşılaştırmak yerine, olası mikrobiyal etkileşim modellerine dayalı olarak metagenomların gruplandırılmasını da sağlar. Ek olarak, araç, kullanıcıların mikrobiyomlar arasında standart karşılaştırmalı analizler gerçekleştirmesini sağlayan çeşitli etkileşimli GUI tabanlı işlevler uygular.
Veri analizi
Topluluk metabolizması
Pek çok bakteri topluluğunda, doğal veya işlenmiş (örn. biyoreaktörler ), metabolizmada önemli bir iş bölümü vardır (Syntrophy ), bazı organizmaların atık ürünleri diğerleri için metabolittir.[65] Böyle bir sistemde, metanojenik biyoreaktör, fonksiyonel stabilite birkaç tane varlığını gerektirir sözdizimsel Türler (Syntrophobacterales ve Sinerji ) ham kaynakları tamamen metabolize olmuş atığa dönüştürmek için birlikte çalışmak (metan ).[66] Karşılaştırmalı gen çalışmalarını ve ifade deneylerini kullanma mikro diziler veya proteomik araştırmacılar, tür sınırlarının ötesine geçen bir metabolik ağı bir araya getirebilirler. Bu tür çalışmalar, hangi proteinlerin hangi versiyonlarının hangi türler tarafından ve hatta hangi türlerin hangi suşları tarafından kodlandığı konusunda ayrıntılı bilgi gerektirir. Bu nedenle, topluluk genomik bilgisi başka bir temel araçtır ( metabolomik ve proteomik) metabolitlerin bir topluluk tarafından nasıl transfer edildiğini ve dönüştürüldüğünü belirleme arayışında.[67]
Metatranscriptomics
Metagenomik, araştırmacıların mikrobiyal toplulukların işlevsel ve metabolik çeşitliliğine erişmesine izin verir, ancak bu süreçlerden hangisinin aktif olduğunu gösteremez.[59] Metagenomik ekstraksiyon ve analizi mRNA ( Metatranscriptome) hakkında bilgi sağlar düzenleme ve ifade karmaşık toplulukların profilleri. Teknik zorluklar nedeniyle ( kısa yarı ömür Örneğin mRNA'nın) çevresel RNA'nın toplanmasında nispeten az yerinde mikrobiyal toplulukların bugüne kadarki metatranscriptomik çalışmaları.[59] Başlangıçta sınırlı iken mikrodizi teknoloji, metatranscriptomics çalışmaları yararlandı transkriptomik teknolojileri bir mikrobiyal topluluğun tüm genom ekspresyonunu ve miktarını ölçmek için,[59] ilk olarak topraktaki amonyak oksidasyonunun analizinde kullanılmıştır.[68]
Virüsler
Metagenomik sıralama, viral toplulukların incelenmesinde özellikle yararlıdır. Virüsler, paylaşılan bir evrensel filogenetik belirteçten yoksun olduğundan ( 16S RNA bakteri ve arkeler için ve 18S RNA Ökarya için), viral topluluğun genetik çeşitliliğine çevresel bir örnekten erişmenin tek yolu metagenomiktir. Viral metagenomlar (viromlar olarak da adlandırılır) bu nedenle viral çeşitlilik ve evrim hakkında giderek daha fazla bilgi sağlamalıdır.[69][70][71][72][73] Örneğin, metagenomik bir ardışık düzen olarak adlandırılan Dev Virüs Bulucu varlığının ilk kanıtını gösterdi dev virüsler tuzlu bir çölde[74] ve Antarktika'nın kuru vadilerinde.[75]
Başvurular
Metagenomik, çok çeşitli alanlarda bilgiyi geliştirme potansiyeline sahiptir. Aynı zamanda pratik zorlukları çözmek için de uygulanabilir. ilaç, mühendislik, tarım, Sürdürülebilirlik ve ekoloji.[31][76]
Tarım
topraklar İçinde bitkilerin büyüdüğü mikrobiyal toplulukların yaşadığı bir gram toprak yaklaşık 109-1010 yaklaşık bir gigabaz sekans bilgisi içeren mikrobiyal hücreler.[77][78] Topraklarda yaşayan mikrobiyal topluluklar, bilimin bildiği en karmaşık topluluklardır ve ekonomik önemlerine rağmen tam olarak anlaşılamamışlardır.[79] Mikrobiyal konsorsiyum, çok çeşitli ekosistem servisleri atmosferik nitrojenin sabitlenmesi dahil bitki büyümesi için gerekli, besin döngüsü, hastalık bastırma ve tecrit edici Demir ve diğeri metaller.[80] Fonksiyonel metagenomik stratejiler, bitkiler ve mikroplar arasındaki etkileşimleri, bu mikrobiyal toplulukların kültivasyondan bağımsız çalışmaları yoluyla keşfetmek için kullanılmaktadır.[81][82] Metagenomik yaklaşımlar, daha önce yetiştirilmemiş veya nadir topluluk üyelerinin besin döngüsündeki rolüne ve bitki büyümesinin desteklenmesine ilişkin içgörüler sağlayarak, mahsuller ve çiftlik hayvanları ve geliştirilmiş adaptasyon çiftçilik mikroplar ve bitkiler arasındaki ilişkiden yararlanarak mahsul sağlığını iyileştiren uygulamalar.[31]
Biyoyakıt
Biyoyakıtlar vardır yakıtlar elde edilen biyokütle dönüşümde olduğu gibi selüloz içerdiği Mısır sapları çimen ve diğer biyokütle selülozik etanol.[31] Bu süreç, selülozu dönüştüren mikrobiyal konsorsiyuma (birleşme) bağlıdır. şeker ve ardından mayalanma şekerlerin etanol. Mikroplar ayrıca çeşitli kaynaklar üretir. biyoenerji dahil olmak üzere metan ve hidrojen.[31]
verimli endüstriyel ölçekli yapıbozum biyokütlenin oranı yeni gerektirir enzimler daha yüksek verimlilik ve daha düşük maliyetle.[28] Karmaşık mikrobiyal toplulukların analizine yönelik metagenomik yaklaşımlar, hedeflenen tarama nın-nin enzimler biyoyakıt üretiminde endüstriyel uygulamalarla, örneğin glikozit hidrolazlar.[83] Dahası, bu mikrobiyal toplulukların nasıl çalıştığına dair bilgi, onları kontrol etmek için gereklidir ve metagenomik, anlayışlarında anahtar bir araçtır. Metagenomik yaklaşımlar arasında karşılaştırmalı analizlere izin verir yakınsak mikrobiyal sistemler gibi biyogaz mayalayıcılar[84] veya böcek otoburlar benzeri mantar bahçesi of yaprak kesici karıncalar.[85]
Biyoteknoloji
Mikrobiyal topluluklar, rekabet ve iletişimde kullanılan çok çeşitli biyolojik olarak aktif kimyasallar üretir.[80] Bugün kullanılan ilaçların çoğu mikroplarda ortaya çıkarıldı; Kültüre alınamayan mikropların zengin genetik kaynağını madencilikteki son gelişmeler, yeni genlerin, enzimlerin ve doğal ürünlerin keşfedilmesine yol açtı.[59][86] Metagenomiklerin uygulanması, emtia ve ince kimyasallar, zirai kimyasallar ve ilaç yararı nerede enzim katalizli kiral sentez giderek daha fazla kabul görmektedir.[87]
İki tür analiz kullanılır. Biyolojik inceleme Metagenomik veri: ifade edilen bir özellik için fonksiyon odaklı tarama ve ilgili DNA dizileri için sekans odaklı tarama.[88] Fonksiyon odaklı analiz, istenen bir özelliği veya faydalı aktiviteyi ifade eden klonları belirlemeyi ve ardından biyokimyasal karakterizasyon ve sekans analizini arar. Bu yaklaşım, uygun bir taramanın mevcudiyeti ve istenen özelliğin konakçı hücrede ifade edilmesi gerekliliği ile sınırlıdır. Dahası, düşük keşif oranı (taranan 1000 klonda birden az) ve emek yoğun doğası bu yaklaşımı daha da sınırlandırır.[89] Aksine, sıralı analiz kullanır korunmuş DNA dizileri -e tasarım PCR primerleri ilgili sekans için klonları taramak.[88] Klonlamaya dayalı yaklaşımlarla karşılaştırıldığında, yalnızca dizi yaklaşımının kullanılması, gerekli tezgah çalışması miktarını daha da azaltır. Büyük ölçüde paralel dizileme uygulaması, yüksek verimli biyoinformatik analiz ardışık düzenleri gerektiren üretilen dizi verisi miktarını da büyük ölçüde artırır.[89] Tarama için sekans güdümlü yaklaşım, genel sekans veritabanlarında bulunan gen fonksiyonlarının genişliği ve doğruluğu ile sınırlıdır. Pratikte deneyler, ilgilenilen işleve, taranacak örneğin karmaşıklığına ve diğer faktörlere dayalı olarak hem fonksiyonel hem de sekans temelli yaklaşımların bir kombinasyonunu kullanır.[89][90] İlaç keşfi için bir biyoteknoloji olarak metagenomiği kullanan bir başarı örneği, malasidin antibiyotikler.[91]
Ekoloji

Metagenomik, çevresel toplulukların işlevsel ekolojisine ilişkin değerli bilgiler sağlayabilir.[92] Avustralya deniz aslanlarının dışkılamalarında bulunan bakteri konsorsiyumunun metagenomik analizi, besin açısından zengin deniz aslanı dışkısının kıyı ekosistemleri için önemli bir besin kaynağı olabileceğini düşündürmektedir. Bunun nedeni, dışkılama ile eşzamanlı olarak atılan bakterilerin, dışkıdaki besin maddelerini, besin zincirine alınabilecek biyolojik olarak kullanılabilir bir forma ayırmada ustadır.[93]
DNA dizilimi, bir su kütlesinde bulunan türleri tanımlamak için daha geniş bir şekilde kullanılabilir.[94] havadan filtre edilmiş pislik veya kir örneği. Bu, aralığı oluşturabilir istilacı türler ve nesli tükenmekte olan türler ve mevsimsel popülasyonları izleyin.
Çevresel iyileştirme
Metagenomik, aşağıdakilerin etkisini izlemek için stratejileri geliştirebilir kirleticiler açık ekosistemler ve kirli ortamları temizlemek için. Mikrobiyal toplulukların kirleticilerle nasıl başa çıktığına dair artan anlayış, kirlenmiş alanların kirlilikten kurtulma potansiyeline ilişkin değerlendirmeleri iyileştirir ve olasılıkları artırır. biyoagmentasyon veya biyostimülasyon başarılı olmak için denemeler.[95]
Bağırsak mikrop karakterizasyonu
Mikrobiyal topluluklar insanı korumada kilit bir rol oynamak sağlık ancak kompozisyonları ve bunu yaptıkları mekanizma gizemini koruyor.[96] Metagenomik sıralama, en az 250 kişiden oluşan 15-18 vücut bölgesinden mikrobiyal toplulukları karakterize etmek için kullanılmaktadır. Bu, İnsan Mikrobiyom girişimi bir çekirdek olup olmadığını belirlemek için birincil hedeflerle insan mikrobiyomu insan mikrobiyomunda insan sağlığı ile ilişkilendirilebilecek değişiklikleri anlamak ve yeni teknolojik ve biyoinformatik bu hedefleri destekleyecek araçlar.[97]
MetaHit (İnsan Bağırsak Sisteminin Metagenomikleri) projesinin bir parçası olan başka bir tıbbi çalışma, Danimarka ve İspanya'dan sağlıklı, aşırı kilolu ve irritabl bağırsak hastalığı hastalarından oluşan 124 kişiden oluşuyordu. Çalışma, gastrointestinal bakterilerin derinliğini ve filogenetik çeşitliliğini kategorize etmeye çalıştı. Illumina GA sekans verilerini ve kısa okumaları derlemek için özel olarak tasarlanmış de Bruijn grafik tabanlı bir araç olan SOAPdenovo'yu kullanarak, 10,3 Gb toplam bitiş uzunluğu ve 2,2 kb N50 uzunluğu için 500 bp'den büyük 6,58 milyon bağlantı oluşturabildiler.
Çalışma, iki bakteri bölünmesinin, Bacteroidetes ve Firmicutes'in, distal bağırsak bakterilerine hakim olan bilinen filogenetik kategorilerin% 90'ından fazlasını oluşturduğunu gösterdi. Bağırsakta bulunan göreceli gen frekanslarını kullanarak bu araştırmacılar, bağırsak sisteminin sağlığı için kritik öneme sahip 1.244 metagenomik küme belirlediler. Bu aralık kümelerinde iki tür işlev vardır: temizlik ve bağırsağa özgü olanlar. Düzenleyici gen kümeleri tüm bakterilerde gereklidir ve genellikle merkezi karbon metabolizması ve amino asit sentezi dahil olmak üzere ana metabolik yollarda önemli oyunculardır. Bağırsağa özgü işlevler, konukçu proteinlere yapışmayı ve şekerlerin globoseries glikolipidlerinden toplanmasını içerir. İrritabl bağırsak sendromu olan hastaların, irritabl bağırsak sendromundan muzdarip olmayan bireylere göre% 25 daha az gen ve daha düşük bakteri çeşitliliği sergiledikleri gösterilmiştir, bu da hastaların bağırsak biyomu çeşitliliğindeki değişikliklerin bu durumla ilişkili olabileceğini göstermektedir.
Bu çalışmalar, potansiyel olarak değerli bazı tıbbi uygulamaları vurgulamakla birlikte, okumaların yalnızca% 31-48,8'i 194 genel insan bağırsağı bakteri genomuna ve% 7,6-21,2'si GenBank'ta bulunan bakteri genomlarına hizalanabilir ki bu, hala çok daha fazla araştırmanın gerekli olduğunu göstermektedir. yeni bakteri genomlarını yakalar.[98]
Bulaşıcı hastalık teşhisi
Bulaşıcı ve bulaşıcı olmayan hastalıkları ayırt etmek ve enfeksiyonun altında yatan etiyolojiyi belirlemek oldukça zor olabilir. Örneğin, vakaların yarısından fazlası ensefalit Son teknoloji klinik laboratuvar yöntemlerinin kullanıldığı kapsamlı testlere rağmen teşhis edilmemiş kalır. Metagenomik sıralama, bir hastanın örneğinde bulunan genetik materyali binlerce bakteri, virüs ve diğer patojenden oluşan bir veri tabanıyla karşılaştırarak enfeksiyonu teşhis etmek için hassas ve hızlı bir yöntem olarak umut vaat ediyor.
Ayrıca bakınız
Referanslar
- ^ a b c d e f g Wooley JC, Godzik A, Friedberg I (Şubat 2010). Bourne PE (ed.). "Metagenomik üzerine bir başlangıç". PLOS Hesaplamalı Biyoloji. 6 (2): e1000667. Bibcode:2010PLSCB ... 6E0667W. doi:10.1371 / journal.pcbi.1000667. PMC 2829047. PMID 20195499.
- ^ a b Hugenholtz P, Goebel BM, Pace NR (Eylül 1998). "Kültürden bağımsız çalışmaların, ortaya çıkan bakteri çeşitliliğinin filogenetik görüşüne etkisi". Bakteriyoloji Dergisi. 180 (18): 4765–74. doi:10.1128 / JB.180.18.4765-4774.1998. PMC 107498. PMID 9733676.
- ^ Marco, D, ed. (2011). Metagenomik: Güncel Yenilikler ve Gelecek Trendler. Caister Academic Press. ISBN 978-1-904455-87-5.
- ^ Eisen JA (Mart 2007). "Çevresel av tüfeği sıralaması: potansiyeli ve mikropların gizli dünyasını incelemenin zorlukları". PLOS Biyoloji. 5 (3): e82. doi:10.1371 / journal.pbio.0050082. PMC 1821061. PMID 17355177.
- ^ Handelsman J, Rondon MR, Brady SF, Clardy J, Goodman RM (Ekim 1998). "Molecular biological access to the chemistry of unknown soil microbes: a new frontier for natural products". Chemistry & Biology. 5 (10): R245-9. doi:10.1016/S1074-5521(98)90108-9. PMID 9818143..
- ^ Chen K, Pachter L (July 2005). "Bioinformatics for whole-genome shotgun sequencing of microbial communities". PLOS Hesaplamalı Biyoloji. 1 (2): 106–12. Bibcode:2005PLSCB...1...24C. doi:10.1371/journal.pcbi.0010024. PMC 1185649. PMID 16110337.
- ^ Lane DJ, Pace B, Olsen GJ, Stahl DA, Sogin ML, Pace NR (October 1985). "Rapid determination of 16S ribosomal RNA sequences for phylogenetic analyses". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 82 (20): 6955–9. Bibcode:1985PNAS...82.6955L. doi:10.1073/pnas.82.20.6955. PMC 391288. PMID 2413450.
- ^ Pace NR, Stahl DA, Lane DJ, Olsen GJ (1986). "The Analysis of Natural Microbial Populations by Ribosomal RNA Sequences". In Marshall KC (ed.). Mikrobiyal Ekolojideki Gelişmeler. 9. Springer ABD. s. 1–55. doi:10.1007/978-1-4757-0611-6_1. ISBN 978-1-4757-0611-6.
- ^ Schmidt TM, DeLong EF, Pace NR (July 1991). "Analysis of a marine picoplankton community by 16S rRNA gene cloning and sequencing". Bakteriyoloji Dergisi. 173 (14): 4371–8. doi:10.1128/jb.173.14.4371-4378.1991. PMC 208098. PMID 2066334.
- ^ Healy FG, Ray RM, Aldrich HC, Wilkie AC, Ingram LO, Shanmugam KT (1995). "Direct isolation of functional genes encoding cellulases from the microbial consortia in a thermophilic, anaerobic digester maintained on lignocellulose". Uygulamalı Mikrobiyoloji ve Biyoteknoloji. 43 (4): 667–74. doi:10.1007/BF00164771. PMID 7546604. S2CID 31384119.
- ^ Stein JL, Marsh TL, Wu KY, Shizuya H, DeLong EF (February 1996). "Characterization of uncultivated prokaryotes: isolation and analysis of a 40-kilobase-pair genome fragment from a planktonic marine archaeon". Bakteriyoloji Dergisi. 178 (3): 591–9. doi:10.1128/jb.178.3.591-599.1996. PMC 177699. PMID 8550487.
- ^ Breitbart M, Salamon P, Andresen B, Mahaffy JM, Segall AM, Mead D, et al. (Ekim 2002). "Genomic analysis of uncultured marine viral communities". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 99 (22): 14250–5. Bibcode:2002PNAS...9914250B. doi:10.1073/pnas.202488399. PMC 137870. PMID 12384570.
- ^ a b Tyson GW, Chapman J, Hugenholtz P, Allen EE, Ram RJ, Richardson PM, et al. (Mart 2004). "Community structure and metabolism through reconstruction of microbial genomes from the environment". Doğa. 428 (6978): 37–43. Bibcode:2004Natur.428...37T. doi:10.1038/nature02340. PMID 14961025. S2CID 4420754.(abonelik gereklidir)
- ^ Hugenholtz P (2002). "Exploring prokaryotic diversity in the genomic era". Genom Biyolojisi. 3 (2): REVIEWS0003. doi:10.1186/gb-2002-3-2-reviews0003. PMC 139013. PMID 11864374.
- ^ Venter JC, Remington K, Heidelberg JF, Halpern AL, Rusch D, Eisen JA, et al. (Nisan 2004). "Environmental genome shotgun sequencing of the Sargasso Sea". Bilim. 304 (5667): 66–74. Bibcode:2004Sci ... 304 ... 66V. CiteSeerX 10.1.1.124.1840. doi:10.1126 / bilim.1093857. PMID 15001713. S2CID 1454587.
- ^ Yooseph S, Nealson KH, Rusch DB, McCrow JP, Dupont CL, Kim M, et al. (Kasım 2010). "Genomic and functional adaptation in surface ocean planktonic prokaryotes". Doğa. 468 (7320): 60–6. Bibcode:2010Natur.468...60Y. doi:10.1038/nature09530. PMID 21048761.(abonelik gereklidir)
- ^ a b c Poinar HN, Schwarz C, Qi J, Shapiro B, Macphee RD, Buigues B, et al. (Ocak 2006). "Metagenomics to paleogenomics: large-scale sequencing of mammoth DNA". Bilim. 311 (5759): 392–4. Bibcode:2006Sci...311..392P. doi:10.1126/science.1123360. PMID 16368896. S2CID 11238470.
- ^ Edwards RA, Rodriguez-Brito B, Wegley L, Haynes M, Breitbart M, Peterson DM, et al. (Mart 2006). "Using pyrosequencing to shed light on deep mine microbial ecology". BMC Genomics. 7: 57. doi:10.1186/1471-2164-7-57. PMC 1483832. PMID 16549033.
- ^ Thomas T, Gilbert J, Meyer F (February 2012). "Metagenomics - a guide from sampling to data analysis". Mikrobiyal Bilişim ve Deneyleme. 2 (1): 3. doi:10.1186/2042-5783-2-3. PMC 3351745. PMID 22587947.
- ^ Béjà O, Suzuki MT, Koonin EV, Aravind L, Hadd A, Nguyen LP, et al. (Ekim 2000). "Construction and analysis of bacterial artificial chromosome libraries from a marine microbial assemblage". Çevresel Mikrobiyoloji. 2 (5): 516–29. doi:10.1046/j.1462-2920.2000.00133.x. PMID 11233160. S2CID 8267748.
- ^ a b Segata N, Boernigen D, Tickle TL, Morgan XC, Garrett WS, Huttenhower C (May 2013). "Computational meta'omics for microbial community studies". Moleküler Sistem Biyolojisi. 9 (666): 666. doi:10.1038/msb.2013.22. PMC 4039370. PMID 23670539.
- ^ Rodrigue S, Materna AC, Timberlake SC, Blackburn MC, Malmstrom RR, Alm EJ, Chisholm SW (July 2010). Gilbert JA (ed.). "Unlocking short read sequencing for metagenomics". PLOS ONE. 5 (7): e11840. Bibcode:2010PLoSO...511840R. doi:10.1371/journal.pone.0011840. PMC 2911387. PMID 20676378.
- ^ Schuster SC (January 2008). "Next-generation sequencing transforms today's biology". Doğa Yöntemleri. 5 (1): 16–8. doi:10.1038/nmeth1156. PMID 18165802. S2CID 1465786.
- ^ "Metagenomics versus Moore's law". Doğa Yöntemleri. 6 (9): 623. 2009. doi:10.1038/nmeth0909-623.
- ^ Stewart RD, Auffret MD, Warr A, Wiser AH, Press MO, Langford KW, et al. (Şubat 2018). "Assembly of 913 microbial genomes from metagenomic sequencing of the cow rumen". Doğa İletişimi. 9 (1): 870. Bibcode:2018NatCo...9..870S. doi:10.1038/s41467-018-03317-6. PMC 5830445. PMID 29491419.
- ^ Hiraoka S, Yang CC, Iwasaki W (September 2016). "Metagenomics and Bioinformatics in Microbial Ecology: Current Status and Beyond". Mikroplar ve Ortamlar. 31 (3): 204–12. doi:10.1264/jsme2.ME16024. PMC 5017796. PMID 27383682.
- ^ Pérez-Cobas AE, Gomez-Valero L, Buchrieser C (2020). "Metagenomic approaches in microbial ecology: an update on whole-genome and marker gene sequencing analyses". Mikrobiyal Genomik. 6 (8). doi:10.1099/mgen.0.000409. PMID 32706331.
- ^ a b Hess M, Sczyrba A, Egan R, Kim TW, Chokhawala H, Schroth G, et al. (Ocak 2011). "Metagenomic discovery of biomass-degrading genes and genomes from cow rumen". Bilim. 331 (6016): 463–7. Bibcode:2011Sci...331..463H. doi:10.1126/science.1200387. PMID 21273488. S2CID 36572885.
- ^ Qin J, Li R, Raes J, Arumugam M, Burgdorf KS, Manichanh C, et al. (Mart 2010). "A human gut microbial gene catalogue established by metagenomic sequencing". Doğa. 464 (7285): 59–65. Bibcode:2010Natur.464...59.. doi:10.1038/nature08821. PMC 3779803. PMID 20203603.(abonelik gereklidir)
- ^ a b Paulson JN, Stine OC, Bravo HC, Pop M (December 2013). "Differential abundance analysis for microbial marker-gene surveys". Doğa Yöntemleri. 10 (12): 1200–2. doi:10.1038/nmeth.2658. PMC 4010126. PMID 24076764.
- ^ a b c d e f g Committee on Metagenomics: Challenges and Functional Applications, National Research Council (2007). The New Science of Metagenomics: Revealing the Secrets of Our Microbial Planet. Washington, D.C.: The National Academies Press. doi:10.17226/11902. ISBN 978-0-309-10676-4. PMID 21678629.
- ^ Oulas A, Pavloudi C, Polymenakou P, Pavlopoulos GA, Papanikolaou N, Kotoulas G, et al. (2015). "Metagenomics: tools and insights for analyzing next-generation sequencing data derived from biodiversity studies". Bioinformatics and Biology Insights. 9: 75–88. doi:10.4137/BBI.S12462. PMC 4426941. PMID 25983555.
- ^ Mende DR, Waller AS, Sunagawa S, Järvelin AI, Chan MM, Arumugam M, et al. (23 Şubat 2012). "Assessment of metagenomic assembly using simulated next generation sequencing data". PLOS ONE. 7 (2): e31386. Bibcode:2012PLoSO...731386M. doi:10.1371/journal.pone.0031386. PMC 3285633. PMID 22384016.
- ^ Balzer S, Malde K, Grohme MA, Jonassen I (April 2013). "Filtering duplicate reads from 454 pyrosequencing data". Biyoinformatik. 29 (7): 830–6. doi:10.1093/bioinformatics/btt047. PMC 3605598. PMID 23376350.
- ^ Mohammed MH, Chadaram S, Komanduri D, Ghosh TS, Mande SS (September 2011). "Eu-Detect: an algorithm for detecting eukaryotic sequences in metagenomic data sets". Biosciences Dergisi. 36 (4): 709–17. doi:10.1007/s12038-011-9105-2. PMID 21857117. S2CID 25857874.
- ^ Schmieder R, Edwards R (March 2011). "Fast identification and removal of sequence contamination from genomic and metagenomic datasets". PLOS ONE. 6 (3): e17288. Bibcode:2011PLoSO...617288S. doi:10.1371/journal.pone.0017288. PMC 3052304. PMID 21408061.
- ^ a b c d e Kunin V, Copeland A, Lapidus A, Mavromatis K, Hugenholtz P (December 2008). "A bioinformatician's guide to metagenomics". Mikrobiyoloji ve Moleküler Biyoloji İncelemeleri. 72 (4): 557–78, Table of Contents. doi:10.1128/MMBR.00009-08. PMC 2593568. PMID 19052320.
- ^ Namiki T, Hachiya T, Tanaka H, Sakakibara Y (November 2012). "MetaVelvet: an extension of Velvet assembler to de novo metagenome assembly from short sequence reads". Nükleik Asit Araştırması. 40 (20): e155. doi:10.1093/nar/gks678. PMC 3488206. PMID 22821567.
- ^ Zerbino DR, Birney E (May 2008). "Velvet: algorithms for de novo short read assembly using de Bruijn graphs". Genom Araştırması. 18 (5): 821–9. doi:10.1101/gr.074492.107. PMC 2336801. PMID 18349386.
- ^ Burton JN, Liachko I, Dunham MJ, Shendure J (May 2014). "Species-level deconvolution of metagenome assemblies with Hi-C-based contact probability maps". G3. 4 (7): 1339–46. doi:10.1534/g3.114.011825. PMC 4455782. PMID 24855317.
- ^ a b Huson DH, Mitra S, Ruscheweyh HJ, Weber N, Schuster SC (September 2011). "Integrative analysis of environmental sequences using MEGAN4". Genom Araştırması. 21 (9): 1552–60. doi:10.1101/gr.120618.111. PMC 3166839. PMID 21690186.
- ^ Zhu W, Lomsadze A, Borodovsky M (July 2010). "Ab initio gene identification in metagenomic sequences". Nükleik Asit Araştırması. 38 (12): e132. doi:10.1093/nar/gkq275. PMC 2896542. PMID 20403810.
- ^ Konopka A (November 2009). "What is microbial community ecology?". ISME Dergisi. 3 (11): 1223–30. doi:10.1038/ismej.2009.88. PMID 19657372.
- ^ a b Huson DH, Auch AF, Qi J, Schuster SC (March 2007). "MEGAN analysis of metagenomic data". Genom Araştırması. 17 (3): 377–86. doi:10.1101/gr.5969107. PMC 1800929. PMID 17255551.
- ^ Segata N, Waldron L, Ballarini A, Narasimhan V, Jousson O, Huttenhower C (June 2012). "Metagenomic microbial community profiling using unique clade-specific marker genes". Doğa Yöntemleri. 9 (8): 811–4. doi:10.1038/nmeth.2066. PMC 3443552. PMID 22688413.
- ^ Sunagawa S, Mende DR, Zeller G, Izquierdo-Carrasco F, Berger SA, Kultima JR, et al. (Aralık 2013). "Metagenomic species profiling using universal phylogenetic marker genes". Doğa Yöntemleri. 10 (12): 1196–9. doi:10.1038/nmeth.2693. PMID 24141494. S2CID 7728395.
- ^ a b Milanese A, Mende DR, Paoli L, Salazar G, Ruscheweyh HJ, Cuenca M, et al. (Mart 2019). "Microbial abundance, activity and population genomic profiling with mOTUs2". Doğa İletişimi. 10 (1): 1014. Bibcode:2019NatCo..10.1014M. doi:10.1038/s41467-019-08844-4. PMC 6399450. PMID 30833550.
- ^ Liu B, Gibbons T, Ghodsi M, Treangen T, Pop M (2011). "Accurate and fast estimation of taxonomic profiles from metagenomic shotgun sequences". BMC Genomics. 12 Suppl 2: S4. doi:10.1186/1471-2164-12-S2-S4. PMC 3194235. PMID 21989143.
- ^ Dadi TH, Renard BY, Wieler LH, Semmler T, Reinert K (2017). "SLIMM: species level identification of microorganisms from metagenomes". PeerJ. 5: e3138. doi:10.7717/peerj.3138. PMC 5372838. PMID 28367376.
- ^ Pagani I, Liolios K, Jansson J, Chen IM, Smirnova T, Nosrat B, et al. (January 2012). "Genomes OnLine Veritabanı (GOLD) v.4: genomik ve metagenomik projelerin durumu ve bunlarla ilişkili meta veriler". Nükleik Asit Araştırması. 40 (Database issue): D571-9. doi:10.1093/nar/gkr1100. PMC 3245063. PMID 22135293.
- ^ Meyer F, Paarmann D, D'Souza M, Olson R, Glass EM, Kubal M, et al. (Eylül 2008). "The metagenomics RAST server - a public resource for the automatic phylogenetic and functional analysis of metagenomes". BMC Biyoinformatik. 9: 386. doi:10.1186/1471-2105-9-386. PMC 2563014. PMID 18803844.
- ^ Markowitz VM, Chen IM, Chu K, Szeto E, Palaniappan K, Grechkin Y, et al. (January 2012). "IMG/M: the integrated metagenome data management and comparative analysis system". Nükleik Asit Araştırması. 40 (Database issue): D123-9. doi:10.1093/nar/gkr975. PMC 3245048. PMID 22086953.
- ^ a b Mitra S, Rupek P, Richter DC, Urich T, Gilbert JA, Meyer F, et al. (Şubat 2011). "Functional analysis of metagenomes and metatranscriptomes using SEED and KEGG". BMC Biyoinformatik. 12 Suppl 1: S21. doi:10.1186/1471-2105-12-S1-S21. PMC 3044276. PMID 21342551.
- ^ Benson DA, Cavanaugh M, Clark K, Karsch-Mizrachi I, Lipman DJ, Ostell J, Sayers EW (January 2013). "GenBank". Nükleik Asit Araştırması. 41 (Database issue): D36-42. doi:10.1093 / nar / gks1195. PMC 3531190. PMID 23193287.
- ^ Bazinet AL, Cummings MP (May 2012). "A comparative evaluation of sequence classification programs". BMC Biyoinformatik. 13: 92. doi:10.1186/1471-2105-13-92. PMC 3428669. PMID 22574964.
- ^ Ounit R, Wanamaker S, Close TJ, Lonardi S (March 2015). "CLARK: fast and accurate classification of metagenomic and genomic sequences using discriminative k-mers". BMC Genomics. 16: 236. doi:10.1186/s12864-015-1419-2. PMC 4428112. PMID 25879410.
- ^ Pratas D, Pinho AJ, Silva RM, Rodrigues JM, Hosseini M, Caetano T, Ferreira PJ (February 2018). "FALCON: a method to infer metagenomic composition of ancient DNA". bioRxiv 10.1101/267179.
- ^ Kurokawa K, Itoh T, Kuwahara T, Oshima K, Toh H, Toyoda A, et al. (Ağustos 2007). "Comparative metagenomics revealed commonly enriched gene sets in human gut microbiomes". DNA Araştırması. 14 (4): 169–81. doi:10.1093/dnares/dsm018. PMC 2533590. PMID 17916580.
- ^ a b c d e f Simon C, Daniel R (February 2011). "Metagenomic analyses: past and future trends". Uygulamalı ve Çevresel Mikrobiyoloji. 77 (4): 1153–61. doi:10.1128/AEM.02345-10. PMC 3067235. PMID 21169428.
- ^ Willner D, Thurber RV, Rohwer F (July 2009). "Metagenomic signatures of 86 microbial and viral metagenomes". Çevresel Mikrobiyoloji. 11 (7): 1752–66. doi:10.1111/j.1462-2920.2009.01901.x. PMID 19302541.
- ^ Ghosh TS, Mohammed MH, Rajasingh H, Chadaram S, Mande SS (2011). "HabiSign: a novel approach for comparison of metagenomes and rapid identification of habitat-specific sequences". BMC Biyoinformatik. 12 Suppl 13 (Supplement 13): S9. doi:10.1186/1471-2105-12-s13-s9. PMC 3278849. PMID 22373355.
- ^ Fimereli D, Detours V, Konopka T (April 2013). "TriageTools: tools for partitioning and prioritizing analysis of high-throughput sequencing data". Nükleik Asit Araştırması. 41 (7): e86. doi:10.1093/nar/gkt094. PMC 3627586. PMID 23408855.
- ^ Maillet N, Lemaitre C, Chikhi R, Lavenier D, Peterlongo P (2012). "Compareads: comparing huge metagenomic experiments". BMC Biyoinformatik. 13 Suppl 19 (Suppl 19): S10. doi:10.1186/1471-2105-13-S19-S10. PMC 3526429. PMID 23282463.
- ^ Kuntal BK, Ghosh TS, Mande SS (October 2013). "Community-analyzer: a platform for visualizing and comparing microbial community structure across microbiomes". Genomik. 102 (4): 409–18. doi:10.1016/j.ygeno.2013.08.004. PMID 23978768.
- ^ Werner JJ, Knights D, Garcia ML, Scalfone NB, Smith S, Yarasheski K, et al. (Mart 2011). "Bacterial community structures are unique and resilient in full-scale bioenergy systems". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 108 (10): 4158–63. Bibcode:2011PNAS..108.4158W. doi:10.1073/pnas.1015676108. PMC 3053989. PMID 21368115.
- ^ McInerney MJ, Sieber JR, Gunsalus RP (December 2009). "Syntrophy in anaerobic global carbon cycles". Biyoteknolojide Güncel Görüş. 20 (6): 623–32. doi:10.1016/j.copbio.2009.10.001. PMC 2790021. PMID 19897353.
- ^ Klitgord N, Segrè D (August 2011). "Ecosystems biology of microbial metabolism". Biyoteknolojide Güncel Görüş. 22 (4): 541–6. doi:10.1016/j.copbio.2011.04.018. PMID 21592777.
- ^ Leininger S, Urich T, Schloter M, Schwark L, Qi J, Nicol GW, et al. (Ağustos 2006). "Arkeler, toprakta amonyak oksitleyen prokaryotlar arasında baskındır". Doğa. 442 (7104): 806–9. Bibcode:2006Natur.442..806L. doi:10.1038 / nature04983. PMID 16915287. S2CID 4380804.
- ^ Paez-Espino D, Eloe-Fadrosh EA, Pavlopoulos GA, Thomas AD, Huntemann M, Mikhailova N, et al. (Ağustos 2016). "Uncovering Earth's virome". Doğa. 536 (7617): 425–30. Bibcode:2016Natur.536..425P. doi:10.1038/nature19094. PMID 27533034. S2CID 4466854.
- ^ Paez-Espino D, Chen IA, Palaniappan K, Ratner A, Chu K, Szeto E, et al. (Ocak 2017). "IMG/VR: a database of cultured and uncultured DNA Viruses and retroviruses". Nükleik Asit Araştırması. 45 (D1): D457–D465. doi:10.1093/nar/gkw1030. PMC 5210529. PMID 27799466.
- ^ Paez-Espino D, Roux S, Chen IA, Palaniappan K, Ratner A, Chu K, et al. (Ocak 2019). "IMG/VR v.2.0: an integrated data management and analysis system for cultivated and environmental viral genomes". Nükleik Asit Araştırması. 47 (D1): D678–D686. doi:10.1093/nar/gky1127. PMC 6323928. PMID 30407573.
- ^ Paez-Espino D, Pavlopoulos GA, Ivanova NN, Kyrpides NC (August 2017). "Nontargeted virus sequence discovery pipeline and virus clustering for metagenomic data" (PDF). Doğa Protokolleri. 12 (8): 1673–1682. doi:10.1038/nprot.2017.063. PMID 28749930. S2CID 2127494.
- ^ Kristensen DM, Mushegian AR, Dolja VV, Koonin EV (January 2010). "New dimensions of the virus world discovered through metagenomics". Mikrobiyolojideki Eğilimler. 18 (1): 11–9. doi:10.1016/j.tim.2009.11.003. PMC 3293453. PMID 19942437.
- ^ Kerepesi C, Grolmusz V (March 2016). "Giant viruses of the Kutch Desert". Viroloji Arşivleri. 161 (3): 721–4. arXiv:1410.1278. doi:10.1007/s00705-015-2720-8. PMID 26666442. S2CID 13145926.
- ^ Kerepesi C, Grolmusz V (June 2017). "The "Giant Virus Finder" discovers an abundance of giant viruses in the Antarctic dry valleys". Viroloji Arşivleri. 162 (6): 1671–1676. arXiv:1503.05575. doi:10.1007/s00705-017-3286-4. PMID 28247094. S2CID 1925728.
- ^ Copeland CS (September–October 2017). "The World Within Us" (PDF). New Orleans Sağlık Dergisi: 21–26.
- ^ Jansson J (2011). "Towards "Tera-Terra": Terabase Sequencing of Terrestrial Metagenomes Print E-mail". Mikrop. 6 (7). s. 309. Archived from orijinal on 31 March 2012.
- ^ Vogel TM, Simonet P, Jansson JK, Hirsch PR, Tiedje JM, Van Elsas JD, Bailey MJ, Nalin R, Philippot L (2009). "TerraGenome: A consortium for the sequencing of a soil metagenome". Doğa İncelemeleri Mikrobiyoloji. 7 (4): 252. doi:10.1038/nrmicro2119.
- ^ "TerraGenome Homepage". TerraGenome international sequencing consortium. Alındı 30 Aralık 2011.
- ^ a b Committee on Metagenomics: Challenges and Functional Applications, National Research Council (2007). Understanding Our Microbial Planet: The New Science of Metagenomics (PDF). The National Academies Press.
- ^ Charles T (2010). "The Potential for Investigation of Plant-microbe Interactions Using Metagenomics Methods". Metagenomics: Theory, Methods and Applications. Caister Academic Press. ISBN 978-1-904455-54-7.
- ^ Bringel F, Couée I (22 May 2015). "Pivotal roles of phyllosphere microorganisms at the interface between plant functioning and atmospheric trace gas dynamics". Mikrobiyolojide Sınırlar. 6: 486. doi:10.3389/fmicb.2015.00486. PMC 4440916. PMID 26052316.
- ^ Li LL, McCorkle SR, Monchy S, Taghavi S, van der Lelie D (May 2009). "Bioprospecting metagenomes: glycosyl hydrolases for converting biomass". Biyoyakıtlar için Biyoteknoloji. 2: 10. doi:10.1186/1754-6834-2-10. PMC 2694162. PMID 19450243.
- ^ Jaenicke S, Ander C, Bekel T, Bisdorf R, Dröge M, Gartemann KH, et al. (Ocak 2011). Aziz RK (ed.). "Comparative and joint analysis of two metagenomic datasets from a biogas fermenter obtained by 454-pyrosequencing". PLOS ONE. 6 (1): e14519. Bibcode:2011PLoSO...614519J. doi:10.1371/journal.pone.0014519. PMC 3027613. PMID 21297863.
- ^ Suen G, Scott JJ, Aylward FO, Adams SM, Tringe SG, Pinto-Tomás AA, et al. (Eylül 2010). Sonnenburg J (ed.). "An insect herbivore microbiome with high plant biomass-degrading capacity". PLOS Genetiği. 6 (9): e1001129. doi:10.1371/journal.pgen.1001129. PMC 2944797. PMID 20885794.
- ^ Simon C, Daniel R (November 2009). "Achievements and new knowledge unraveled by metagenomic approaches". Uygulamalı Mikrobiyoloji ve Biyoteknoloji. 85 (2): 265–76. doi:10.1007/s00253-009-2233-z. PMC 2773367. PMID 19760178.
- ^ Wong D (2010). "Applications of Metagenomics for Industrial Bioproducts". Metagenomics: Theory, Methods and Applications. Caister Academic Press. ISBN 978-1-904455-54-7.
- ^ a b Schloss PD, Handelsman J (June 2003). "Biotechnological prospects from metagenomics" (PDF). Biyoteknolojide Güncel Görüş. 14 (3): 303–10. doi:10.1016/S0958-1669(03)00067-3. PMID 12849784. Arşivlenen orijinal (PDF) 4 Mart 2016 tarihinde. Alındı 20 Ocak 2012.
- ^ a b c Kakirde KS, Parsley LC, Liles MR (November 2010). "Size Does Matter: Application-driven Approaches for Soil Metagenomics". Soil Biology & Biochemistry. 42 (11): 1911–1923. doi:10.1016/j.soilbio.2010.07.021. PMC 2976544. PMID 21076656.
- ^ Parachin NS, Gorwa-Grauslund MF (May 2011). "Isolation of xylose isomerases by sequence- and function-based screening from a soil metagenomic library". Biyoyakıtlar için Biyoteknoloji. 4 (1): 9. doi:10.1186/1754-6834-4-9. PMC 3113934. PMID 21545702.
- ^ Hover BM, Kim SH, Katz M, Charlop-Powers Z, Owen JG, Ternei MA, et al. (Nisan 2018). "Culture-independent discovery of the malacidins as calcium-dependent antibiotics with activity against multidrug-resistant Gram-positive pathogens". Doğa Mikrobiyolojisi. 3 (4): 415–422. doi:10.1038/s41564-018-0110-1. PMC 5874163. PMID 29434326.
- ^ Raes J, Letunic I, Yamada T, Jensen LJ, Bork P (March 2011). "Toward molecular trait-based ecology through integration of biogeochemical, geographical and metagenomic data". Moleküler Sistem Biyolojisi. 7: 473. doi:10.1038/msb.2011.6. PMC 3094067. PMID 21407210.
- ^ Lavery TJ, Roudnew B, Seymour J, Mitchell JG, Jeffries T (2012). Steinke D (ed.). "High nutrient transport and cycling potential revealed in the microbial metagenome of Australian sea lion (Neophoca cinerea) faeces". PLOS ONE. 7 (5): e36478. Bibcode:2012PLoSO...736478L. doi:10.1371/journal.pone.0036478. PMC 3350522. PMID 22606263.
- ^ "What's Swimming in the River? Just Look For DNA". NPR.org. 24 Temmuz 2013. Alındı 10 Ekim 2014.
- ^ George I, Stenuit B, Agathos SN (2010). "Application of Metagenomics to Bioremediation". In Marco D (ed.). Metagenomics: Theory, Methods and Applications. Caister Academic Press. ISBN 978-1-904455-54-7.
- ^ Zimmer C (13 July 2010). "How Microbes Defend and Define Us". New York Times. Alındı 29 Aralık 2011.
- ^ Nelson KE and White BA (2010). "Metagenomics and Its Applications to the Study of the Human Microbiome". Metagenomics: Theory, Methods and Applications. Caister Academic Press. ISBN 978-1-904455-54-7.
- ^ Qin J, Li R, Raes J, Arumugam M, Burgdorf KS, Manichanh C, et al. (Mart 2010). "A human gut microbial gene catalogue established by metagenomic sequencing". Doğa. 464 (7285): 59–65. Bibcode:2010Natur.464...59.. doi:10.1038/nature08821. PMC 3779803. PMID 20203603.
Dış bağlantılar
- Focus on Metagenomics -de Doğa İncelemeleri Mikrobiyoloji journal website
- The “Critical Assessment of Metagenome Interpretation” (CAMI) initiative to evaluate methods in metagenomics
