N-Hidroksiftalimid - N-Hydroxyphthalimide - Wikipedia
 | |
| İsimler | |
|---|---|
| IUPAC adı 2-Hidroksiizoindol-1,3-dion | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| ChemSpider | |
| ECHA Bilgi Kartı | 100.007.600 |
| EC Numarası |
|
PubChem Müşteri Kimliği | |
| UNII | |
CompTox Kontrol Paneli (EPA) | |
| |
| |
| Özellikleri | |
| C8H5NÖ3 | |
| Molar kütle | 163.132 g · mol−1 |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
N-Hidroksiftalimid ... N-hidroksi türevi ftalimid. Bileşik kullanılır, diğerlerinin yanı sıra, gibi katalizör için oksidasyon reaksiyonları özellikle seçici oksidasyon için (örn. Alkanlar -e alkoller ) ile moleküler oksijen hafif koşullar altında.[1][2]
Oluşum ve üretim
Sentezi N-hidroksiftalimid ftaloil klorür ve hidroksilamin hidroklorür Sulu çözelti içinde sodyum karbonat mevcudiyetinde ilk olarak 1880'de Lassar Cohn ("Ftalilhidroksilamin" olarak anılacaktır) tarafından bildirilmiştir.[3]
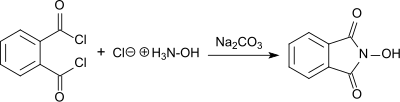
Ürün kırmızı olarak oluşur Sodyum tuzu temel koşullar altında, beyaz iken N-hidroksiftalimid, çözelti olduğu gibi% 55 verimle çökelir. asitlenmiş. N-hidroksiftalimid ayrıca hidroksilamin hidroklorürün reaksiyona girmesiyle üretilir. dietil ftalat huzurunda sodyum asetat,[4] veya ile ftalik anhidrit huzurunda sodyum karbonat ısıtma ile. Son durumda, aşağıdaki şekilde saflaştırmanın ardından% 76'lık bir toplam verim elde edilir. yeniden kristalleşme.[5]
Ftalik anhidrit ve hidroksilamin hidroklorürün mikrodalga ışınlaması piridin üretir N-hidroksiftalimid,% 81 verim.[6] Bir bazın yokluğunda bile, ftalik anhidrit ve hidroksilamin fosfat reaksiyona girerek N-hidroksiftalimid 130 ° C'ye ısıtıldığında% 86 verim.[7]

Özellikleri
N-Hydroxyphthalimide, suda ve organik çözücülerde çözülebilen renksizden sarıya, kokusuz bir kristal tozdur. asetik asit, Etil asetat ve asetonitril.[8] Bileşik iki farklı renkte mevcuttur monoklinik kristal formlar. Renksiz beyaz form olması durumunda, N-OH grubu molekül düzleminden yaklaşık 1.19 ° döndürülürken, sarı formda düzlemselliğe (0.06 ° dönüş) çok daha yakındır.[9]
Sentezlenen renk N-hidroksiftalimid, kullanılan çözücü tipine bağlıdır; beyazdan sarıya renk geçişi geri döndürülemez.[10] N-hidroksiftalimid, güçlü renkli, çoğunlukla sarı veya kırmızı tuzlar oluşturur. alkali ve ağır metaller, amonyak ve aminler.[11] Hidrolizi N-hidroksiftalimid güçlü bazların eklenmesiyle mono ftalik asit üretirhidroksamik asit tarafından su eklemek karbon-nitrojen bağlarından biri boyunca.[4] N-hidroksiftalimid eterler ise renksizdir ve Ö-alkilhidroksilaminler, alkalin hidroliz veya bölünme yoluyla hidrazin hidrat.
Cohn tarafından bildirilen "ftalilhidroksilamin", Moleküler formül nın-nin C
8H
5HAYIR
3 ancak kesin yapı bilinmiyordu.[3] Üç olasılık tartışıldı ve aşağıdaki Şekilde gösterildi: tekoksim ftalik anhidrit ("ftaloksim", ben), genişletilmiş bir iki heteroatomlu halka, (2,3-benzoksazin-1,4-dion, II), ve N-hidroksiftalimid (III).[10][12] 1950'lere kadar Cohn'un ürününün kesinlikle (III), N-hidroksiftalimid.[13]

Uygulamalar ve reaksiyonlar
Nefkens ve Tesser, üretmek için bir teknik geliştirdi. aktif esterler itibaren N-hidroksiftalimid[14] kullanmak için peptid sentezi,[15] daha sonra genişletilmiş bir yaklaşım N-hidroksisüksinimid.[16] Ester bağı arasında oluşur N-hidroksiftalimid ve a karboksilik asit tarafından eliminasyon su ile elde edilen bağlantı N,N '-disikloheksilkarbodiimid (DCC). Peptit sentezi için, N- büyüyen peptidin terminali korumalı ile tert-bütiloksikarbonil iken C-terminus (Z-NH-CH (R) -COOH), N-hidroksiftalimid. Bir Ester sonraki amino asit istenen peptid dizisinde, aktive ester ile çalkalanır, zincire eklenir ve yer değiştirir. N-hidroksiftalimid. Bu reaksiyon kantitatiftir ve 0 ° C'de neredeyse anlıktır.[15][17] Elde edilen ester, döngü tekrarlanmadan önce hidrolize edilmelidir.

N-hidroksiftalimid ile çalkalanarak uzaklaştırılabilir. sodyum bikarbonat,[15] ama N-hidroksisüksinimid yaklaşımı daha fazla reaktivite ve uygunluk gösterir ve genellikle tercih edilir.[16][17]
Esterleri N-hidroksiftalimid ve aktive sülfonik asitler gibi triflorometansülfonik anhidrit veya p-toluensülfonil klorür UV ışınlaması sırasında protonları ayıran fotoasitler olarak kullanılır.

Üretilen protonlar, aside duyarlılığın hedeflenen yerel bozunmasına hizmet eder. fotorezistler.[18]
N-hidroksiftalimid, paladyum (II) asetat varlığında vinil asetat ile N- kantitatif olarak hidrojene edilen viniloksiftalimid N-etoksiftalimid ve bölünme ile saflaştırıldıktan sonra, ürün Ö-etilhidroksilamin.[19]

Çeşitli farklı fonksiyonel gruplar ile oksitlenebilir aminoksil radikali (ftalimid-N-oksil, PINO)[20] bir hidrojen atomunun soyutlanmasıyla oluşur. N-hidroksiftalimid nazik koşullar altında (benzer TEMPO ):[1]
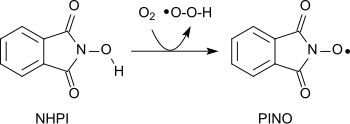
Moleküler oksijen alkanları kullanılarak alkoller, ikincil alkoller ketonlara, asetallerden esterlere ve alkenler için oksitlenebilir. epoksitler.[21][22][23] Amidler ile karbonil bileşiklerine dönüştürülebilir Nhafif koşullar altında hidroksiftalimid ve kobalt (II) tuzları.[24]

Önemli temel kimyasalların öncülerinin verimli oksidasyon reaksiyonları özellikle teknik ilgi konusudur. Örneğin, ε-kaprolaktam Sikloheksanın oksidasyonu sırasında elde edilen KA yağından ("keton-alkol" yağı, bir sikloheksanol ve sikloheksanon karışımı) NHPI kullanılarak hazırlanabilir. Reaksiyon, peroksidisikloheksilamin vermek üzere amonyak ile reaksiyona giren sikloheksanol hidroperoksit yoluyla devam eder, ardından katalitik miktarlarda lityum klorür varlığında yeniden düzenleme yapılır.[22][25]

Kullanımı NKA yağının oksidasyonunda bir katalizör olarak hidroksiftalimid, geleneksel-kaprolaktam sentezi ile üretilen istenmeyen yan ürün amonyum sülfat oluşumunu önler (Beckmann yeniden düzenlemesi siklohekzanon oksim ile sülfürik asit ).
Alkanlar, nitrojen dioksit varlığında nitroalkanlara dönüştürülür.[26]
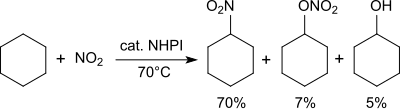
Siklohekzan nitrojen dioksit / hava ile 70 ° C'de nitrosikloheksan (% 70), sikloheksil nitrat (% 7) ve sikloheksanol (% 5) karışımına dönüştürülür.
Ayrıca, uygulamaları N-hidroksiftalimid, oksitleyici ajanlar olarak fotoğraf geliştiricileri[27] ve tonerlerde şarj kontrol ajanları olarak[28] patent literatüründe açıklanmıştır.
Ftalimido-N-oksil (PINO)
Bir H atomunun çıkarılmasıyla türetilen radikal N-hidroksiftalimid denir N-ftalimido-N-oksilkısaltma olmak PINO. Güçlü bir H atomu soyutlama ajanıdır.[1] NHPI'nin (yani PINO-H) bağ ayrışma enerjisi, çözücüye bağlı olarak 88-90 kcal / mol arasındadır.[29]
Referanslar
- ^ a b c Recupero, Francesco; Punta, Carlo (2007). "Tarafından Katalizlenen Organik Bileşiklerin Serbest Radikal İşlevselleştirilmesi N-Hydroxyphthalimide ". Chem. Rev. 107 (9): 3800–3842. doi:10.1021 / cr040170k. PMID 17848093.
- ^ Melone, Lucio; Punta, Carlo (2013). "Metal içermeyen aerobik oksidasyonların neden olduğu N-hidroksiftalimid. Kısa bir inceleme ". Beilstein J. Org. Chem. 9: 1296–1310. doi:10.3762 / bjoc.9.146. PMID 23843925.
- ^ a b Cohn, Lassar (1880). "Ftalilhidroksilamin: Salicylsäure'de Ueberführung der Phthalsäure" [N-hidroksiftalimid: Ftalik asidin salisilik aside dönüşümü]. Justus Liebigs Ann. Chem. (Almanca'da). 205 (3): 295–314. doi:10.1002 / jlac.18802050304.
- ^ a b Bauer, Ludwig; Miarka, Stanley V. (1957). "Kimyası N-Hydroxyphthalimide ". J. Am. Chem. Soc. 79 (8): 1983–1985. doi:10.1021 / ja01565a061.
- ^ Gross, H .; Keitel, I. (1969). "Zur Darstellung von N-Hydroxyphthalimid und N-Hydroxysuccinimid "[Hazırlanmasında N-hidroksiftalimid ve N-hidroksisüksinimid]. J. Prakt. Chem. (Almanca'da). 311 (4): 692–693. doi:10.1002 / prac.19693110424.
- ^ Sugamoto, Kazuhiro; Matsushita, Yoh-ichi; Kameda, Yu-hei; Suzuki, Masahiko; Matsui Takanao (2005). "Mikrodalga Destekli Sentez N‐Hydroxyphthalimide Türevleri ". Synth. Commun. 35 (1): 67–70. doi:10.1081 / SCC-200046498.
- ^ EP başvurusu 1085013, Elke Fritz-Langhals, "Verfahren zur Herstellung bisikletçi N-Hydroxy-dicarboximide (Siklik asitlerin hazırlanması için proses) N-hidroksidikarboksimidler) ", 2001-03-21'de yayınlanan, Consortium für elektrochemische Industrie GmbH'ye devredilmiştir.
- ^ Gambarotti, Cristian; Punta, Carlo; Recupero, Francesco; Zlotorzynska, Maria; Sammis Glenn (2013). "N-Hidroksiftalimid". N-Hidroftalimid. Organik Sentez için Reaktif Ansiklopedisi. doi:10.1002 / 047084289X.rn00598.pub2. ISBN 978-0471936237.
- ^ Reichelt, Hendrik; Faunce, Chester A .; Paradies, Henrich H. (2007). "Zor formlar ve yapılar N-hidroksiftalimid: Renksiz ve sarı kristal formları N-hidroksiftalimid ". J. Phys. Chem. Bir. 111 (13): 2587–2601. doi:10.1021 / jp068599y. PMID 17388355.
- ^ a b Ames, D. E .; Gri, T.F (1955). "N-Hydroxy-imides. Bölüm II. Homoftalik ve ftalik asit türevleri ". J. Chem. Soc.: 3518–3521. doi:10.1039 / JR9550003518.
- ^ Porcheddu, Andrea; Giacomelli, Giampaolo (2009). "Oksimlerin ve hidroksamik asitlerin sentezi". Rappaport, Zvi'de; Lieberman, Joel F. (editörler). Hidroksilaminlerin, Oksimlerin ve Hidroksamik Asitlerin Kimyası, Bölüm 1. Chichester: Wiley. sayfa 224–226. ISBN 978-0-470-51261-6.
- ^ Bradly, Oscar L .; Baker, Leslie C .; Goldstein, Richard F .; Harris, Samuel (1928). "LXVIII. — Oksimlerin izomerizmi. Kısım XXXIII. Opianik asit ve ftalik anhidritin oksimleri". J. Chem. Soc.: 529–539. doi:10.1039 / JR9280000529.
- ^ Hurd, Charles D .; Buess, Charles M .; Bauer, Ludwig (1954). "Süksino- ve ftalo-hidroksamik asitler". J. Org. Chem. 19 (7): 1140–1149. doi:10.1021 / jo01372a021.
- ^ Nefkens, G.H.L .; Tesser, G. I .; Nivard, R.J.F (1962). "Esterlerin sentezi ve reaksiyonları N-hidroksiftalimid ve N-korunmuş amino asitler". Recl. Trav. Chim. Bas öder. 81 (8): 683–690. doi:10.1002 / recl.19620810807.
- ^ a b c Nefkens, G.H.L .; Tesser, G.I. (1961). "Peptit Sentezinde Yeni Bir Aktifleştirilmiş Ester". J. Am. Chem. Soc. 83 (5): 1263. doi:10.1021 / ja01466a068.
- ^ a b Anderson, George W .; Zimmerman, Joan E .; Callahan, Francis M. (1964). "Esterlerin Kullanımı N-Hydroxysuccinimide in Peptide Synthesis ". J. Am. Chem. Soc. 86 (9): 1839–1842. doi:10.1021 / ja01063a037.
- ^ a b Bodanszky, Miklos (1993). "Aktivasyon ve Kuplaj". Peptid Sentezinin Prensipleri (2. baskı). Springer-Verlag. s. 9–61. doi:10.1007/978-3-642-78056-1_2. ISBN 9783642780561.
- ^ 0919867, K. Elian, E. Günther, R. Leuschner
- ^ 1995025090, D.M.C. Callant, A.M.C.F. Castelijns, J.G. De Vries
- ^ S. Coseri (2009), "Ftalimid ‐ N ‐ oksil (PINO) Radikal, Güçlü Bir Katalitik Ajan: Çeşitli Organik Substratlara Yönelik Üretimi ve Çok Yönlülüğü", Katal. Rev. Sci. Müh., 51 (2), sayfa 218–292, doi:10.1080/01614940902743841
- ^ Y. Ishii, K. Nakayama, M. Takeno, S. Sakaguchi, T. Iwahama, Y. Nishiyama (1995), "Novel Catalysis by N-Organik Substratların Moleküler Oksijenle Oksidasyonunda Hidroksiftalimid ", J. Org. Chem., 60 (13), s. 3934–3935, doi:10.1021 / jo00118a002CS1 bakimi: birden çok ad: yazarlar listesi (bağlantı)
- ^ a b "Karbon radikali üreten bir katalizörün keşfi ve organik senteze uygulanması" (PDF). TCIMAIL, Numara 116. Tokyo Chemical Industry Co. Ltd. Nisan 2003. Alındı 2016-08-11.
- ^ B.B. Wentzel, M.P.J. Donners, P.L. Alsters, M.C. Feiters, R.J.M. Nolte (2000), "N-Hydroxyphthalimide / kobalt (II), moleküler oksijen kullanılarak düşük sıcaklıkta benzilik oksidasyonla katalize edilmiş ", Tetrahedron, 56 (39), s. 7797–7803, doi:10.1016 / S0040-4020 (00) 00679-7CS1 bakimi: birden çok ad: yazarlar listesi (bağlantı)
- ^ F. Minisci, C. Punta, F. Recupero, F. Fontana, G.F. Pedulli (2002), "Aerobik Oksidasyonu N-Alkilamidler NHafif Koşullar Altında-Hidroksiftalimid. Polar ve Entalpik Etkiler ", J. Org. Chem., 67 (8), sayfa 2671–2676, doi:10.1021 / jo016398e, PMID 11950315CS1 bakimi: birden çok ad: yazarlar listesi (bağlantı)
- ^ O. Fukuda, S. Sakaguchi, Y. Ishii (2001), "KA-yağının katalitik Baeyer-Villiger oksidasyonu için moleküler oksijen kullanarak yeni bir strateji N-hidroksiftalimid ", Tetrahedron Lett., 42 (20), s. 3479–3481, doi:10.1016 / S0040-4039 (01) 00469-5CS1 bakimi: birden çok ad: yazarlar listesi (bağlantı)
- ^ S. Sakaguchi, Y. Nishiwaki, T. Kitamura, Y. Ishii (2001), "Hava destekli NO2 ile verimli katalitik alkan nitrasyon N-hidroksiftalmid ", Angew. Chem., Int. Düzenle., 40 (1), sayfa 222–224, doi:10.1002 / 1521-3773 (20010105) 40: 1 <222 :: AID-ANIE222> 3.0.CO; 2-WCS1 bakimi: birden çok ad: yazarlar listesi (bağlantı)
- ^ EP başvurusu 0664479, W. Ishikawa & T. Sampei, "Gümüş halojenür fotografik ışığa duyarlı malzemeyi işleme yöntemi", 1994-7-26'da yayınlanan, Konica Corp.
- ^ Bize 5332637 J.C. Wilson; S.M. Bonser ve H.W. Osterhoudt, "Elektrostatografik kuru toner ve hidroksiftalimidli geliştirici bileşimleri", 1994-7-26'da Eastman Kodak Co.
- ^ Coseri, Sergiu (2009). "Ftalimid-N-oksil (PINO) Radikal, Güçlü Bir Katalitik Ajan: Üretimi ve Çeşitli Organik Substratlara Yönelik Çok Yönlülüğü". Kataliz İncelemeleri. 51 (2): 218–292. doi:10.1080/01614940902743841.
