Fenilsodyum - Phenylsodium - Wikipedia
 | |
| İsimler | |
|---|---|
| Diğer isimler Sodyum benzenid, Sodyum fenil, sodiobenzen | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| Kısaltmalar | NaPh, PhNa |
| ChemSpider | |
PubChem Müşteri Kimliği | |
| UNII | |
| |
| |
| Özellikleri | |
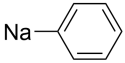
| C6H5Na | |
| Molar kütle | 100.096 g · mol−1 |
| Görünüm | Sarımsı beyaz toz[1] |
| Tepki verir | |
| Çözünürlük | Hidrokarbonlarda çözünmez, eterle reaksiyona girer |
| Tehlikeler | |
| Ana tehlikeler | Havada aşındırıcı, piroforik |
| Bağıntılı bileşikler | |
Bağıntılı bileşikler | Fenillityum, Benzilsodyum |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
Fenilsodyum C6H5Na bir organosodyum bileşiği. Katı fenilsodyum ilk olarak 1903 yılında Nef tarafından izole edilmiştir. Fenilsodyum ve fenil magnezyum bromür benzerdir, organosodyum bileşiği çok nadiren kullanılır.[2]
Sentez
Fenilsodyumun varlığı ilk olarak Kekulé oluşumunu gözlemledikten sonra sodyum benzoat tepkisinde bromobenzen ile sodyum altında karbon dioksit.
Transmetalasyon
Orijinal sentezde, difenil cıva ve sodyumun bir fenilsodyum süspansiyonu verdiği gösterilmiştir:
- (C6H5)2Hg + 3 Na → 2 C6H5Na + NaHg
Shorigen reaksiyonu, bir alkil sodyum bileşiğinin benzen ile muamele edildiği fenilsodyum oluşumunda da kullanılır:[3]:
- RNa + C6H6 → RH + C6H5Na
Yöntem ayrıca ikinci bir sodyum ilavesiyle de sonuçlanabilir. Bu dimetallasyon, meta ve para pozisyonlar. N-amil sodyum gibi belirli alkil sodyum bileşiklerinin kullanımının bu dimetallasyon etkisini büyük ölçüde artırdığı bilinmektedir.[4]
Metal-halojen değişimi
Fenilsodyum için ortak bir yol, toz halindeki sodyum ile birlikte bromobenzen:
- C6H5Br + 2 Na → C6H5Na + NaBr
Bu yöntemin verimi, fenilsodyumun aril halojenür başlangıç malzemesi ile reaksiyona girmesi nedeniyle difenil oluşumu ile azaltılır.[5]
Lityum Değişimi
Daha modern bir sentez, fenillityum ve NaOtBu:[6]
- C6H5Li + NaOtBu → C6H5Na + LiOtBu
Özellikler ve Yapı

Organomercury yolunu kullanan ilk fenilsodyum sentezleri açık kahverengi bir toz veriyor gibi görünüyordu.[7] Tarafından keşfedildi Schlenk bu ürünün bulaşmış olduğunu sodyum amalgum. Santrifüjleme, kolayca alevlere dönüşen sarımsı beyaz amorf bir toz olarak görünen saf fenilsodyumun izolasyonuna izin verdi.[1]
Fenillityum gibi, bileşiğin eklentileri ile PMDTA kristalize edilmiştir. Fenillityum, PMDTA ile bir monomerik eklenti oluştururken, fenilsodyum, daha büyük sodyum radyumunu yansıtan bir dimer olarak bulunur.[6]
Fenilsodyum ve magnezyum alkoksitlerin kompleksleri, özellikle magnezyum 2-etoksietoksit Mg (OCH2CH2OEt)2benzende çözünür. Kompleks, reaksiyonla oluşur:
- NaPh + Mg (OCH2CH2OEt)2 → Na2MgPh2(OCH2CH2OEt)2
Fenilsodyum kompleks olmasına rağmen, fenilasyon ve metalleşme kabiliyetini korur. Ek olarak, kompleks, bir aylık depolamadan sonra reaktivitesini koruyan benzen içinde oldukça kararlıdır.[8]
Fenillityum, fenilsodyumun özelliklerini değiştirmek için de kullanılabilir. Normalde, fenilsodyum ile şiddetli reaksiyona girer. dietil eter, fakat Georg Wittig PhNa'yı eterde PhLi ile sentezleyerek, kompleks (C6H5Li) (C6H5Na)n oluşturulmuştur. Kompleksin fenilsodyum bileşeni, fenillityumdan önce reaksiyona girerek, yüksek derecede reaktif sodyum bileşiğini stabilize etmek için etkili bir bileşik haline getirir. Bu kompleks, eter içinde çözülebilen ve birkaç gün oda sıcaklığında çözelti içinde stabil kalan katı kristaller olarak izole edilebildi. Fenillityum, fenilsodyumu 1:24 Li: Na kadar yüksek bir oranda stabilize edebilir, ancak bu, reaksiyonlar için hala kullanılabilecek çözünmez bir kütle üretir.[2]
Tepkiler
Fenilsodyum içeren reaksiyonlar, 1903'ten önce olmasına rağmen, 19. yüzyılın ortalarında kullanılmıştır. Tipik olarak fenilsodyum, in situ için kullanılan yöntemlere benzer şekilde hazırlanır. Grignard reaktifleri. Acree'nin çalışması, bileşiği içeren bir dizi reaksiyon örneği sağlar.[9]
Çapraz çiftleme
Etil bromür ile reaksiyon, etil benzen:
- NaPh + BrEt → PhEt + NaBr
Benzer bir reaksiyon, fenilsodyumun hazırlanmasında da meydana gelir. difenil:
- NaPh + PhBr → Ph-Ph + NaBr
Reaksiyonu benzil klorür ve fenilsodyum ile sonuçlanır difenilmetan ve stilbene. Difenilmetan, klorür ikamesinden beklenen üründür. Stilben oluşumu, Wurtz-Fittig reaksiyon mekanizmasında önerilenler gibi radikal ara maddeleri ima eder.
Fenilsodyumun reaksiyonu benzoil klorür hidrolizden sonra verim, trifenilkarbinol. Benzofenon bir ara ürün olarak önerilmektedir.
- 2NaPh + PhCOCl → Ph3CONa + NaCl
Metalleştirme
Fenilsodyum ile metalleşme reaksiyonları aşağıdaki genel biçimde gerçekleşir:
- PhNa + RH → C6H6 + RNa
Metalleşme, metalize bileşiğin karbon dioksit ile işlenmesiyle doğrulanır / tespit edilir, bu da karboksilik asit verecek şekilde asitleştirilebilen karşılık gelen sodyum karboksilatı verir:
- RNa + CO2 → RCO2Na
Metalleşme, genel olarak tahmin edilebilir bir reaktivite sırasını takip eder. Benzen, alkilsodyum bileşikleri tarafından metalleştirilerek fenilsodyum elde edilebilir. Fenilsodyum daha sonra diğer aromatik bileşikleri metalleştirebilir. Fenilsodyum ile metalleştirme için en yaygın kullanılan reaktif, benzilsodyum üreten toluendir. Toluen, benzen yerine toluen içinde fenilsodyum sentezlenerek metalleştirilebilir:
- C6H5Cl + 2Na + (C6H6) (CH3) → C6H6 + NaCl + (C6H6) (CH2Na
Benzilsodyum daha sonra nükleofilik bir eklemede kullanılabilir. Metalleştirmenin etkinliği, benzoik asit ürününün karbonatlanması ve izole edilmesiyle belirlenebilir.
Referanslar
- ^ a b Schlenk, W .; Holtz, Johanna (Ocak 1917). "Über die einfachsten metallorganischen Alkaliverbindungen". Berichte der Deutschen Chemischen Gesellschaft. 50 (1): 262–274. doi:10.1002 / cber.19170500142.
- ^ a b Seyferth, Dietmar (Ocak 2006). "Alkali Metallerin Alkil ve Aril Türevleri: Güçlü Bazlar ve Güçlü Nükleofiller Olarak Kullanışlı Sentetik Reaktifler. 1. Organik Halojenürlerin Organoalkali-Metal Bileşiklerine Dönüşümü". Organometalikler. 25 (1): 13. doi:10.1021 / om058054a.
- ^ Schorigin, Paul (Mayıs 1908). "Synthesen mittels Natrium ve Halogenalkylen". Berichte der Deutschen Chemischen Gesellschaft. 41 (2): 2114. doi:10.1002 / cber.190804102208.
- ^ Bryce-Smith, D .; Turner, E.E. (1953). "177. Alkali Metallerin Organometalik Bileşikleri. Bölüm II. Benzen Metalleştirmesi ve Boyutlandırılması". Journal of the Chemical Society (Resumed): 861–863. doi:10.1039 / jr9530000861.
- ^ Jenkins, William W. (Haziran 1942). "Fenil Sodyumun Hazırlanması Üzerine Bir Çalışma". Yüksek Lisans Tezleri (225).
- ^ a b Schümann, Uwe; Behrens, Ulrich; Weiss, Erwin (Nisan 1989). "Synthese ve Struktur von Bis [μ-fenil (pentametildietilentriamin) natrium], einem Fenilnatrium-Solvat". Angewandte Chemie. 101 (4): 481–482. doi:10.1002 / ange.19891010420.
- ^ Acree, S.F. (Ağustos 1903). "Sodyum Fenil ve Sodyumun Ketonlar Üzerindeki Etkisi Üzerine (John Ulric Nef'in çalışması hakkında rapor)". Amerikan Kimya Derneği Dergisi. 25 (8): 588–609. doi:10.1021 / ja02010a026.
- ^ Screttas, Constantinos G .; Micha-Screttas, Maria (Haziran 1984). "Hidrokarbonda çözünür organoalkali-metal reaktifler. Aril türevlerinin hazırlanması". Organometalikler. 3 (6): 904–907. doi:10.1021 / om00084a014.
- ^ Acree, Solomon, F (1903). Sodyum Fenil ve Sodyumun Ketonlar Üzerindeki Etkisi Üzerine. Easton, PA: Chemical Publishing Co.'nun Basını s. 1–23.
