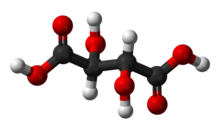
Tartarik asit - Tartaric acid
 | |
 | |
| İsimler | |
|---|---|
| Tercih edilen IUPAC adı 2,3-Dihidroksibutandioik asit | |
| Diğer isimler Tartarik asit 2,3-Dihidroksisüksinik asit Threarik asit Rasemik asit Üvik asit Paratartarik asit Winestone | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA Bilgi Kartı | 100.121.903 |
| KEGG | |
| MeSH | tartarik + asit |
PubChem Müşteri Kimliği | |
CompTox Kontrol Paneli (EPA) | |
| |
| |
| Özellikleri | |
| C4H6Ö6 (Temel formül) HO2CCH (OH) CH (OH) CO2H (Yapısal formül) | |
| Molar kütle | 150.087 g / mol |
| Görünüm | Beyaz toz |
| Yoğunluk | 1.79 g / mL (H2Ö) |
| Erime noktası | 171 - 174 ° C (340 - 345 ° F; 444 - 447 K) (Kral-tartarik; saf) 206 ° C (DL, rasemik) 165–166 ° C (mezo-susuz) 146–148 ° C (mezo-sulu)[3] |
| |
| Asitlik (pKa) | L (+) 25 ° C: pKa1= 2.89, pKa2= 4.40 meso 25 ° C: pKa1= 3.22, pKa2= 4.85 |
| Eşlenik baz | Bitartrate |
| −67.5·10−6 santimetre3/ mol | |
| Tehlikeler | |
| Tahriş edici (Xi) | |
| R cümleleri (modası geçmiş) | R36 |
| Bağıntılı bileşikler | |
Diğer katyonlar | Monosodyum tartrat Disodyum tartrat Monopotasyum tartrat Dipotasyum tartrat |
İlişkili karboksilik asitler | Bütirik asit Süksinik asit Dimerkaptosüksinik asit Malik asit Maleik asit Fumarik asit |
Bağıntılı bileşikler | 2,3-Butandiol Sikorik asit |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
Tartarik asit beyaz, kristal organik asit Bu, birçok meyvede doğal olarak, özellikle de üzüm ama aynı zamanda muz, demirhindi, ve narenciye.[4] Onun tuz, potasyum bitartrat, yaygın olarak bilinen tartar kremi, sürecinde doğal olarak gelişir mayalanma. Genellikle karıştırılır sodyum bikarbonat ve olarak satılır kabartma tozu olarak kullanılan mayalama ajanı yemek hazırlamada. Asidin kendisi gıdalara bir antioksidan E334 ve kendine özgü ekşi tadı vermek.
Tartarik asit, bir alfa-hidroksi-karboksilik asit, dır-dir diprotik ve aldar asit özelliklerinde ve bir dihidroksil türevidir süksinik asit.
Tarih
Tartarik asidin şarap üreticileri asırlardır. Şarap yapımı artıklarından ekstraksiyonunun yazılı kaydı yapıldı yaklaşık MS 800 simyacı Jābir ibn Hayyān.[5] Ekstraksiyon için kimyasal işlem 1769'da İsveççe eczacı Carl Wilhelm Scheele.[6]
Tartarik asitin keşfedilmesinde önemli bir rol oynadı. kimyasal kiralite. Tartarik asidin bu özelliği ilk olarak 1832'de Jean Baptiste Biot, dönme yeteneğini gözlemleyen polarize ışık.[7][8] Louis Pasteur 1847'de kiral olduğunu bulduğu sodyum amonyum tartrat kristallerinin şekillerini araştırarak bu araştırmaya devam etti. Farklı şekilli kristalleri manuel olarak ayırarak, Pasteur saf bir levotartarik asit numunesi üreten ilk kişi oldu.[9][10][11][12][13]
Stereokimya
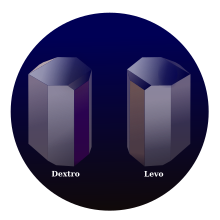
Doğal olarak meydana gelen tartarik asit kiral ve yararlı bir hammaddedir. organik kimyasal sentez. Asidin doğal olarak oluşan formu dekstrotartarik asit veya L- (+) - tartarik asit (eski ad d -tartarik asit). Doğal olarak mevcut olduğu için, olduğundan biraz daha ucuzdur. enantiyomer ve mezo izomer. dextro ve Levo önekler arkaik terimlerdir.[14] Modern ders kitapları doğal biçime (2R,3R)-tartarik asit (L- (+) - tartarik asit)ve enantiyomeri (2S,3S)-tartarik asit (D-(-)-tartarik asit). mezo diastereomer (2R,3S) -tartarik asit (‘(2S,3R)-tartarik asit').
Oysa iki kiral stereoizomerler düzlem polarize ışığı ters yönlerde döndürür, mezo-tartarik asit çözeltileri düzlem polarize ışığı döndürmez. Optik aktivitenin olmaması, moleküldeki bir ayna düzleminden kaynaklanmaktadır [aşağıdaki resimde bölümlenmiş çizgi].[15][16]
Tartarik asit Fehling'in çözümü bakır (II) iyonlarına bağlanarak çözünmez hidroksit tuzlarının oluşumunu engeller.
| DL-tartarik asit (rasemik asit ) (1: 1 oranında) | mezotartarik asit | |
|---|---|---|
| dekstrotartarik asit (L- (+) - tartarik asit) | levotartarik asit (D- (-) - tartarik asit) | |
 |  |  |
| Yaygın isim | Tartarik asit | Levotartarik asit | Dekstrotartarik asit | Mezotartarik asit | Rasemik asit |
|---|---|---|---|---|---|
| Eş anlamlı | (2S,3S)-tartarik asit (S,S)-tartarik asit (-) - tartarik asit l-tartarik asit (eski) levotartarik asit D-tartarik asit D- trearik asit ('doğal olmayan izomer')[17] | (2R,3R)-tartarik asit (R,R)-tartarik asit (+) - tartarik asit d-tartarik asit (eski) L-tartarik asit L- trearik asit ("Doğal izomer")[18] | (2R,3S)-tartarik asit mezo-tartarik asit eritrarik asit | ırk-(2R,3S)-tartarik asit (2RS,3SR)-tartarik asit (±) -tartarik asit DL-tartarik asit dl-tartarik asit (eski) paratartarik asit uvik asit | |
| PubChem | CID 875 itibaren PubChem | CID 439655 itibaren PubChem | CID 444305 itibaren PubChem | CID 78956 itibaren PubChem | CID 5851 itibaren PubChem |
| EINECS numarası | |||||
| CAS numarası | 526-83-0 | 147-71-7 | 87-69-4 | 147-73-9 | 133-37-9 |
Üretim
L- (+) - Tartarik asit
LTartarik asitin - (+) - tartarik asit izomeri endüstriyel olarak en büyük miktarlarda üretilir. Elde edilir Lees, fermantasyonların katı bir yan ürünü. Önceki yan ürünler çoğunlukla potasyum bitartrattan (KHC4H4Ö6). Bu potasyum tuzu, kalsiyum tartrata (CaC4H4Ö6) kireç sütü ile muamele üzerine (Ca (OH)2):[19]
- KO2CCH (OH) CH (OH) CO2H + Ca (OH)2 → Ca (O2CCH (OH) CH (OH) CO2) + KOH + H2Ö
Uygulamada, eklenmesi ile daha yüksek kalsiyum tartrat verimleri elde edilir. kalsiyum klorür. Kalsiyum tartrat daha sonra tuzun sulu sülfürik asit ile işlenmesiyle tartarik aside dönüştürülür:
- Ca (O2CCH (OH) CH (OH) CO2) + H2YANİ4 → HO2CCH (OH) CH (OH) CO2H + CaSO4
Rasemik tartarik asit
Rasemik tartarik asit (yani.: 50:50 karışımı D- (-) - tartarik asit ve L- (+) - tartarik asit molekülleri, rasemik asit ) çok aşamalı bir reaksiyonla hazırlanabilir maleik asit. İlk aşamada, maleik asit epoksitlenmiş tarafından hidrojen peroksit kullanma potasyum tungstat bir katalizör olarak.[19]
- HO2CC2H2CO2H + H2Ö2 → OC2H2(CO2H) 2
Bir sonraki adımda epoksit hidrolize edilir.
- OC2H2(CO2H)2 + H2O → (HOCH)2(CO2H)2
mezo-Tartarik asit
mezo-Tartarik asit oluşur üzerinden termal izomerizasyon. dextro-Tartarik asit yaklaşık 2 gün 165 ° C'de suda ısıtılır. mezo-Tartarik asit ayrıca gümüş hidroksit kullanılarak dibromosüksinik asitten hazırlanabilir:[20]
- HO2CCHBrCHBrCO2H + 2 AgOH → HO2CCH (OH) CH (OH) CO2H + 2 AgBr
mezo-Tartarik asit, artık rasemik asitten kristalleştirme ile ayrılabilir, rasemat daha az çözünürdür.
Reaktivite
L - (+) - tartarik asit, birkaç reaksiyona katılabilir. Aşağıdaki reaksiyon şemasında gösterildiği gibi, dihidroksimalaleik asit, L - (+) - tartarik asidin bir demir tuzunun varlığında hidrojen peroksit ile işlenmesi üzerine üretilir.
- HO2CCH (OH) CH (OH) CO2H + H2Ö2 → HO2CC (OH) C (OH) CO2H + 2 H2Ö
Dihidroksimaleik asit daha sonra okside edilebilir tartronik asit nitrik asit ile.[21]
Türevler


Tartarik asitin önemli türevleri arasında tuzları, tartar kremi (potasyum bitartrat ), Rochelle tuzu (potasyum sodyum tartrat, hafif müshil ), ve tartar emetik (antimon potasyum tartrat).[22][23][24] Diizopropil tartrat olarak kullanılır yardımcı katalizör asimetrik sentezde.
Tartarik asit bir kas toksin üretimini engelleyerek çalışan Malik asit yüksek dozlarda ise felç ve ölüme neden olur.[25] ortalama öldürücü doz (LD50) bir insan için yaklaşık 7.5 gram / kg, tavşanlar için 5.3 gram / kg ve fareler için 4.4 gram / kg'dır.[26] Bu rakam göz önüne alındığında, 70 kg (150 lb) ağırlığındaki bir kişiyi öldürmek 500 g'dan (18 ons) fazla zaman alır, bu nedenle pek çok yiyeceğe, özellikle ekşi tatlara güvenle dahil edilebilir. tatlılar. Olarak Gıda katkı maddesi tartarik asit, bir antioksidan ile E numarası E334; tartaratlar antioksidan görevi gören diğer katkı maddeleri veya emülgatörler.
Suya krem tartar eklendiğinde, bakırın temizlenmesine yarayan bir süspansiyon oluşur. madeni paralar tartrat çözeltisi madeni paranın yüzeyinde bulunan bakır (II) oksit tabakasını çözebildiğinden çok iyi. Elde edilen bakır (II) -tartrat kompleksi, suda kolayca çözünür.
Şarapta tartarik asit

Tartarik asit, şarap içenler tarafından en çok "şarap elmasları" nın kaynağı olarak hemen tanınabilir. potasyum bitartrat bazen üzerinde kendiliğinden oluşan kristaller mantar veya şişenin dibi. Bu "tartratlar", bazen kırık camla karıştırılmalarına rağmen zararsızdır ve birçok şarapta soğuk stabilizasyon (şarabın profilini değiştirebileceği için her zaman tercih edilmez). İçeride kalan tartratlar yaşlanan varil bir zamanlar potasyum bitartratın önemli bir endüstriyel kaynağıydı.
Tartarik asit kimyasal olarak önemli bir rol oynar, fermente "şıra" nın pH'ını birçok istenmeyen bozulma bakterisinin yaşayamayacağı bir seviyeye düşürür ve sonrasında koruyucu olarak işlev görür. mayalanma. Ağızda tartarik asit şarabın ekşiliğinin bir kısmını sağlar, ancak sitrik ve malik asitler ayrıca bir rol oynar.
Turunçgillerde tartarik asit
Bir çalışmanın sonuçları, narenciyede organik tarımda üretilen meyvelerin, geleneksel tarımda üretilen meyvelerden daha yüksek seviyelerde tartarik asit içerdiğini göstermiştir.[27]
Süperiletkenlerde
Tartarik asit, belirli durumlarda kritik sıcaklığı artırıyor gibi görünüyor süperiletkenler Bu fenomenin mekanizması hala tam olarak bilinmiyorken, sözde oksidasyon derecesini yükselterek.[28]
Başvurular
Tartarik asit ve türevleri, farmasötikler alanında çok sayıda kullanıma sahiptir. Örneğin, sitrik asit ile kombinasyon halinde efervesan tuzların üretiminde oral ilaçların tadını iyileştirmek için kullanılmıştır.[21] Tartar emetiği olarak bilinen asidin potasyum antimonil türevi, küçük dozlarda, öksürük şurubu olarak balgam söktürücü.
Tartarik asit ayrıca endüstriyel kullanım için çeşitli uygulamalara sahiptir. Asit gözlenmiştir Kıskaç kalsiyum ve magnezyum gibi metal iyonları. Bu nedenle asit, tarım ve metal endüstrilerinde, topraktaki mikro besinleri kompleks hale getirmek için bir şelatlama maddesi olarak hizmet etmiştir. gübre sırasıyla alüminyum, bakır, demir ve bu metallerin alaşımlarından oluşan metal yüzeylerin temizlenmesi için.[19]
Referanslar
- ^ Tartarik Asit - Bileşik Özeti, PubChem.
- ^ Dawson, R.M.C. ve diğerleri, Biyokimyasal Araştırma Verileri, Oxford, Clarendon Press, 1959.
- ^ Lide, D. R., ed. (2005). CRC El Kitabı Kimya ve Fizik (86. baskı). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ^ Duarte, A.M .; Caixeirinho, D .; Miguel, M.G .; Sustelo, V .; Nunes, C .; Fernandes, M.M .; Marreiros, A. (2012). "Geleneksel ve Organik Tarımdan Narenciye Suyunda Organik Asit Konsantrasyonu". Açta Horticulturae (933): 601–606. doi:10.17660 / actahortic.2012.933.78. ISSN 0567-7572.
- ^ Lisa Solieri, Paolo Giudici (2009). Dünya Sirkeleri. Springer. s. 29. ISBN 978-88-470-0865-6.
- ^ Retzius, Anders Cihan (1770) "Försök med vinsten och dess syra" (Tartar kremi ve asidi ile deneyler), Kungliga Vetenskapsakademiens Handlingar (Kraliyet Bilimler Akademisi Bildirileri), 31 : 207–213. S. 209: "§. 6. Dessa försök omtalte jag för Hr. Carl Wilhelm Scheele (en snabb och lårgirug Pharmaciæ Studiosus)…" (§. 6. Bu deneylerden Bay Carl Wilhelm Scheele (hızlı ve çalışkan bir farmakoloji öğrencisi) adına söz ediyorum…)
- ^ Biot (1835) "Kutuplaşma sirkülasyonu ve çevre uygulamaları gibi uygulamalar" (Dairesel polarizasyon ve organik kimyaya uygulamaları üzerine anı), Mémoires de l'Académie des sciences de l'Institut2. seri, 13 : 39–175. O tartarik asit (Acide tartarique cristallisé) düzlem polarize ışığı döndürür Tablo G aşağıdaki s. 168. (Not: Bu makale 5 Kasım 1832'de Fransız Kraliyet Bilimler Akademisi'ne okundu.)
- ^ Biot (1838) "Süzgeçleri ve birleşimleri dökün, kayıpsız, hızlı ve hızlı polarizasyonu; uygulamaların tatbikatları ve l'acide tartarique avec l'eau, l'alcool ve l'esprit de bois" (Polarize ışık üzerinde etkili olan tanımlanmış veya tanımlanmamış karışımları ve kimyasal kombinasyonları ayırt etmek için; ardından tartarik asitin su, alkol [yani etanol] ve odun ruhu [yani metanol] ile kombinasyonlarına uygulamaları takip eder), Mémoires de l'Académie des sciences de l'Institut2. seri, 15 : 93–279.
- ^ L. Pasteur (1848) "Kristalin ve kimyasal bileşimin bir araya gelmesiyle oluşan ilişki, ve sur la polarizasyon rotatoire neden olur" (Kristalin form ile kimyasal bileşim arasında var olabilen ilişki üzerine hatırat ve döner polarizasyonun nedeni), " Comptes rendus de l'Académie des sciences (Paris), 26 : 535–538.
- ^ L. Pasteur (1848) "Daha iyi ilişkiler, kristalin, bir bileşim ve daha iyi polarizasyon rotatoire" (Kristalin form ile kimyasal bileşim arasında var olabilecek ilişkiler ve dönel polarizasyon hissi üzerine), Annales de Chimie ve Physique3. seri, 24 : 442–459.
- ^ Pastör, Louis (1850) "Spécifiques des deux, qui composent l'acide racémique'i yeniden canlandırıyor" (Rasemik asidi oluşturan iki asidin spesifik özelliklerinin araştırılması), Annales de Chimie ve Physique3. seri, 28 (3): 56–99. Ayrıca bakınız Levha II. (Ayrıca Pasteur'ün bulgularını doğrulamak için atanan komisyonun raporuna bakın, s. 99-117.) [Fransızca]
- ^ George B. Kauffman ve Robin D. Myers (1998). "Pasteur'ün rasemik asit çözünürlüğü: Yüzüncü yıla ait bir geriye dönük inceleme ve yeni bir çeviri" (PDF). Kimya Eğitmeni. 3 (6): 1–4. doi:10.1007 / s00897980257a. S2CID 95862598. Arşivlenen orijinal (PDF) 2006-01-17 tarihinde.
- ^ H. D. Flack (2009). "Louis Pasteur'ün 1848'de moleküler kiralite ve kendiliğinden çözünürlüğü keşfi, kristalografik ve kimyasal çalışmalarının tam bir incelemesi ile birlikte" (PDF). Açta Crystallographica A. 65 (5): 371–389. doi:10.1107 / S0108767309024088. PMID 19687573. Arşivlenen orijinal (PDF) 2012-09-06 tarihinde.
- ^ J.M. McBride'ın tartarik asit stereokimyası tarihi, D / L ve R / S sistemleri üzerine Yale dersi
- ^ çeşitli (2007-07-23). Organik Kimya. Global Medya. s. 65. ISBN 978-81-89940-76-8. Alındı 2010-06-05.
- ^ "(WO / 2008/022994) Azabisiklo hekzan türevlerinin kullanımı".
- ^ "Tartarik Asit_1".
- ^ "Tartarik Asit_2".
- ^ a b c J.-M. Ullmann'ın Endüstriyel Kimya Ansiklopedisinde Kassaian "Tartarik asit"; VCH: Weinheim, Almanya, 2002, 35, 671-678. doi:10.1002 / 14356007.a26_163
- ^ Augustus Price West. Deneysel Organik Kimya. Dünya Kitap Şirketi: New York, 1920, 232-237.
- ^ a b Blair, G.T .; DeFraties, J. J. (2000). "Hidroksi Dikarboksilik Asitler". Kirk Othmer Kimyasal Teknoloji Ansiklopedisi. s. 1–19. doi:10.1002 / 0471238961.0825041802120109.a01. ISBN 0471238961.
- ^ Zalkin, Allan; Templeton, David H .; Ueki, Tatzuo (1973). "L-tris (1,10-fenatrolin) demir (II) bis (antimon (III) d-tartrat) oktahidratın kristal yapısı". İnorganik kimya. 12 (7): 1641–1646. doi:10.1021 / ic50125a033.
- ^ Haq, I; Khan, C (1982). "Geleneksel göz kozmetiklerinin tehlikeleri - SURMA". JPMA. Pakistan Tabipler Birliği Dergisi. 32 (1): 7–8. PMID 6804665.
- ^ McCallum, RI (1977). "Başkanın adresi. Antimon üzerine gözlemler". Kraliyet Tıp Derneği Bildirileri. 70 (11): 756–63. doi:10.1177/003591577707001103. PMC 1543508. PMID 341167.
- ^ Alfred Swaine Taylor, Edward Hartshorne (1861). Adli tıp. Blanchard ve Lea. s.61.
- ^ Joseph A. Maga, Anthony T. Tu (1995). Gıda katkı maddesi toksikolojisi. CRC Basın. s. 137–138. ISBN 0-8247-9245-9.
- ^ Duarte, A.M .; Caixeirinho, D .; Miguel, M.G .; Sustelo, V .; Nunes, C .; Fernandes, M.M .; Marreiros, A. (2012). "Geleneksel ve Organik Tarımdan Narenciye Suyunda Organik Asit Konsantrasyonu". Açta Horticulturae (933): 601–606. doi:10.17660 / actahortic.2012.933.78. ISSN 0567-7572.
- ^ arXiv,. "Kırmızı Şarap, Tartarik Asit ve Süperiletkenliğin Sırrı". MIT Technology Review. Alındı 2020-01-09.
