Geçiş metal klorür kompleksi - Transition metal chloride complex
İçinde kimya, bir geçiş metali klorür kompleksi bir koordinasyon kompleksi oluşur Geçiş metali bir veya daha fazla koordine klorür ligand. Kompleks sınıfı kapsamlıdır.[1]
Yapıştırma
Halojenürler X-tipidir ligandlar içinde koordinasyon kimyası. Hem σ hem de π donörleridir. Klorür, hem bir terminal ligand olarak hem de yaygın olarak bulunur. köprü ligandı. Halojenür ligandları zayıf alan ligandları. Daha küçük bir kristal alan bölme enerjisi nedeniyle, ilk geçiş serisinin homoleptik halojenür komplekslerinin tümü yüksek spinlidir. Yalnızca [CrCl6]3− değişim etkisizdir.
Homoleptik metal halojenür kompleksleri birkaç stokiyometri ile bilinir, ancak ana olanlar heksahalometalatlar ve tetrahalometalatlardır. Hexahalides benimser sekiz yüzlü koordinasyon geometrisi tetrahalidler genellikle dört yüzlüdür. Kare düzlemsel tetrahalidler Pd (II), Pt (II) ve Au (III) için bilinir. 2 ve 3 koordinasyonlu örnekler Au (I), Cu (I) ve Ag (I) için yaygındır.
Dolu p varlığı nedeniyleπ orbitaller, geçiş metalleri üzerindeki halojenür ligandları takviye edebilir π-backbonding π-asit üzerine. Ayrıca labilize oldukları biliniyor cisligandlar.[2]
Homoleptik kompleksler
Homoleptik kompleksler (sadece klorür ligandlı kompleksler) genellikle yaygın reaktiflerdir. Hemen hemen tüm örnekler anyonlardır.
1. sıra

| Karmaşık | renk | elektron yapılandırması. | geometri | yorumlar |
|---|---|---|---|---|
| TiCl4 | renksiz | (t2 g)0 | dört yüzlü | |
| [Ti2Cl10]2− | renksiz | d0d0 | biyoktahedral | |
| [Ti2Cl9]− | beyaz / renksiz | d0d0 | yüz paylaşımlı bioktahedron | Ti-Cl (terminal) = 2,23 Å, 2,45 (terminal) (N (PCl3)2)+ tuz)[3] |
| [Ti2Cl9]3- | turuncu | (t2 g)1(t2 g)1 | yüz paylaşımlı bioktahedron | Ti-Ti = 3.22 Å Ti-C1 (terminal) = 2.32-2.35 Å (terminal), Ti-Cl (köprü) = 2.42-2.55 Å ((Ağ4+)3)3 tuz)[4] |
| [Ti3Cl12]3- | yeşil | (t2 g)1(t2 g)1(t2 g)1 | yüz paylaşımlı trioktahedron | Ti-Ti = 3.19, 3.10 Å (terminal) Ti-C1 (terminal) = 2.36 Å (terminal), Ti-Cl (köprü) = 2.50 Å ((PPh4+)3)3 tuz)[5] |
| [TiCl6]2− | Sarı | d0 | sekiz yüzlü | |
| VCl4 | kırmızı | (t2 g)1 | dört yüzlü | V1 − Cl = 2.29 Å |
| VCl5 | menekşe | (t2 g)0 | kenar paylaşımlı bioktahedron | V1 − Cl (köprüleme) = 2.48 Å, V1 − Cl (terminal) = 2.16-2.21 Å[6] |
| [VCl6]2- | kırmızı | (t2 g)1 | sekiz yüzlü | V1 − Cl = 2.29 Å[7] |
| [CrCl6]3− | ?? | (t2 g)3 | sekiz yüzlü[8] | |
| [MnCl4]2−[9] | soluk pembe | (eg)2(t2 g)3 | dört yüzlü | Mn-Cl bağ uzunluğu = 2.3731-2.3830 Å[10] |
| [Mn2Cl6]2− | sarı yeşil | (eg)2(t2 g)3 | bitetrahedral | Mn-Cl (terminal) bağ uzunluğu = 2.24 Å Mn-Cl (terminal) bağ uzunluğu = 2.39 Å[11] (PPN+)2 tuz |
| [MnCl6]2− | koyu Kırmızı | (t2 g)3(eg)1 | sekiz yüzlü | Mn-Cl mesafesi = 2.28 Å K+ tuz[12]) tuz K ile izostrüktüreldir2PtCl6 |
| [Mn3Cl12]6− | pembe | (t2 g)3(eg)2 | eş yüzlü trioktahedron | Mn-Cl mesafesi = --- Å [(C (NH2)3]+6 tuz[13] |
| [FeCl4]2−[9] | krem ((Et4N+)2 tuz)[9] | (eg)3(t2 g)3 | dört yüzlü | |
| [FeCl4]− | (eg)2(t2 g)3 | dört yüzlü | Fe-Cl bağ uzunluğu = 2.19 Å[14] | |
| [Fe2Cl6]2− | soluk sarı | (eg)2(t2 g)3 | bitetrahedral | Fe-Cl (terminal) bağ uzunluğu = 2.24 Å Fe-Cl (terminal) bağ uzunluğu = 2.39 Å[11] (PPN+)2 tuz |
| [CoCl4]2−[9] | mavi[9] | (eg)4(t2 g)3 | dört yüzlü | |
| [Co2Cl6]2− | mavi[11] | (eg)4(t2 g)3 | bitetrahedral | Mn-Cl (terminal) bağ uzunluğu = 2.24 Å Co-Cl (terminal) bağ uzunluğu = 2.35 Å[11] (PPN+)2 tuz |
| [NiCl4]2−[9] | mavi[9] | (eg)4(t2 g)4 | dört yüzlü | Ni-Cl bağ uzunluğu = 2.28 Å (Et4N+)2 tuz[15] |
| [Ni3Cl12]6− | turuncu[16] | (t2 g)6(eg)2 | karşılıklı üç yüzlü | Ni-Cl bağ uzunluğu = 2.36-2.38 Å ((Ben mi2NH2+)2)8 tuz iki Cl ile çift tuz−[16] |
| [CuCl4]2−[9] | turuncu[17] | (t2 g)6(eg)3 | dört yüzlü | Cu-Cl bağ uzunluğu = 2.24 Å |
| [Cu2Cl6]2− | yeşil | (t2 g)6(eg)3 | kenar paylaşımlı bis (kare düzlemsel)[18] | |
| [ZnCl4]2− | beyaz / renksiz | d10 | dört yüzlü |

2. sıra
- Bazı Metal Klorürlerin Yapıları

[M2Cl10]n- M = Nb, Ta (n = 0); M = Ti, Zr, Hf (n = 2)
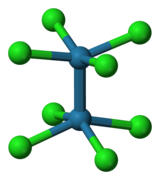
[M2Cl8]n− M = Mo (n = 4), Re (n = 2)

[M2Cl9]n− M = Ti (n = 1), Mo, Rh (n = 3) için.

M6Cl184− M = Nb, Ta için.
İkinci sıra geçiş metallerinin bazı homoleptik kompleksleri metal-metal bağlarına sahiptir.
| Karmaşık | renk | elektron yapılandırması. | geometri | yorumlar |
|---|---|---|---|---|
| [ZrCl6]2− | Sarı | (t2 g)0 | sekiz yüzlü | Zr-Cl mesafesi = 2.460 Å (Ben mi4N+)2 tuz[20] |
| [Zr2Cl10]2− | renksiz | (t2 g)0 | kenar paylaşımlı biyoktahedral | Zr-Cl = 2.36 Å (terminal), 2.43 Å (köprüleme) N (PCl3)2)+ tuz[3] |
| [NbCl5] | Sarı | (t2 g) | kenar paylaşımlı biyoktahedral [Nb2Cl10] | |
| [NbCl6]− | Sarı | (t2 g)0 | sekiz yüzlü | Nb-Cl = 2.34 Å N (PCl3)2)+ tuz[3] |
| [Nb6Cl18]2- | siyah | Nb-Cl = 2.92 Å (K+) 2 tuz[21] | ||
| MoCl6 | siyah | (t2 g)0 | sekiz yüzlü | Mo − Cl = 2.28 -2.31 Å[6]10.1524 / ncrs.2004.219.2.101 |
| [MoCl6]2- | Sarı | (t2 g)2 | sekiz yüzlü | Mo − Cl = 2.37, 2.38, 2.27 Å[22] |
| [MoCl6]3- | pembe | (t2 g)3 | sekiz yüzlü | |
| [Mo2Cl8]4- | mor[23] | d4 | Mo-Mo dörtlü bağ 10.1002 / zaac.19845080113 | |
| [Mo2Cl9]3- | d3 | Mo-Mo (üçlü) bağ uzunluğu = 2,65 Å Mo-Cl (terminal) bağ uzunluğu = 2.38 Å Mo-Cl (köprüleme) bağ uzunluğu = 2.49 Å[24] | ||
| [Mo2Cl10]2-[25][26] | d1d1 | |||
| [Mo5Cl13]2- | Kahverengi[23] | d2d2d2d2d3 | eksik oktahedron[27] | |
| [Mo6Cl14]2- | Sarı | d4 | oktahedral küme | |
| [RuCl6]2− | Kahverengi | (t2 g)4 | sekiz yüzlü | (EtPPh3+)2 tuz[28] |
| [Ru3Cl12]4− | yeşil | (d5)2(d6) | eş yüzlü üç yüzlü | Ru-Ru bağ uzunlukları = 2.86 Å Ru-Cl bağ uzunlukları = 2.37-2.39 Å (Et4N+)2(H7Ö3+)2 tuz[29] |
| [RhCl6]3− | kırmızı | (t2 g)6 | sekiz yüzlü | H2N+(CH2CH2NH3+)2 tuz)[30] |
| [Rh2Cl9]3− | kırmızı kahverengi | (t2 g)6 | sekiz yüzlü | Rh-Cl (terminal) = 2.30 Å, Rh-Cl (terminal) = 2.40 Å ((Ben mi3CH2Doktora)+)3 tuz)[24] |
| [PdCl4]2− | Kahverengi | d8 | kare düzlemsel | |
| [PdCl6]2− | Kahverengi | d6 | sekiz yüzlü | Olağandışı Pd (IV) örneği |
| [AgCl2]− | beyaz / renksiz | d10 | doğrusal | [K (2.2.2-crypt)] tuzu+[31] |
| [CdCl4]2− | beyaz / renksiz | d10 | dört yüzlü | Et4N+ tuz, Cd-Cl mesafesi 2.43 Å[19] |
| [CD2Cl6]2− | beyaz / renksiz | d10 | kenar paylaşımlı bitetrahedron | (C6N3(4-C5H4N)33+ tuz[32] |
| [CD3Cl12]6− | beyaz / renksiz | d10 | oktahedral (merkezi Cd) beş koordinat (terminal Cd'ler) ortak işlevli üç yüzlü | (C6N3(4-C5H4N)33+ tuz[32] (3,8-Diamonyum-6-fenilfenantridin3+)2[33] |
| [CD6Cl19]7− | beyaz / renksiz | d10 | oktahedranın sekiz yüzlü | 4,4 '- (C6H3(2-Et) NH3+)2 tuz[34] |
3. sıra
| Karmaşık | renk | elektron yapılandırması. | geometri | yorumlar |
|---|---|---|---|---|
| [HfCl6]2− | beyaz | (t2 g)0 | sekiz yüzlü | Hf-Cl mesafesi = 2.448 A ((Ben mi4N+)2 tuz)[20] |
| [Hf2Cl10]2− | renksiz / beyaz | (t2 g)0 | kenar paylaşımlı biyoktahedral[35] | |
| [Hf2Cl9]− | renksiz / beyaz | (t2 g)0 | yüz paylaşımlı biyoktahedral[36] | |
| [TaCl5] | beyaz | (t2 g)0 | kenar paylaşımlı biyoktahedral | |
| [TaCl6]− | beyaz / renksiz | (t2 g)0 | sekiz yüzlü | Ta-Cl = 2.34 Å (N (PCl3)2)+ tuz)[3] |
| [Ta6Cl18]2- | yeşil | d0 | sekiz yüzlü | Ta-Ta = 2.34 Å (H+2 tuz heksahidrat[37] |
| WCl6 | mavi | (t2 g)0 | sekiz yüzlü | 2.24–2.26 Å[38] |
| [WCl6]2− | (t2 g)2 | sekiz yüzlü | W-Cl mesafeleri 2,34 ila 2,37 Å arasındadır (PPh4+ tuz)[39] | |
| [WCl6]− | (t2 g)1 | sekiz yüzlü | W-Cl mesafesi = 2.32 Å (Et4N+ tuz)[40] | |
| [W2Cl9]2− | d3d2 | yüz paylaşımlı biyoktahedral | W-W mesafesi = 2,54 Å W-Cl (terminal) = 2,36 Å, W-Cl (köprü) = 2,45 Å ((PPN+)2 tuz)[41] | |
| [W2Cl9]3− | d3d3 | sekiz yüzlü | W-Cl mesafesi = 2.32 Å (Et4N+ tuz)[41] | |
| [W3Cl13]3− | d3, d3, d4 | [W3(μ3-Cl) (μ-Cl)3Cl9]3- | W-W mesafeleri = 2.84 Å[42] | |
| [W3Cl13]2− | d3, d4, d4 | [W3(μ3-Cl) (μ-Cl)3Cl9]3-[42] | W-W mesafeleri = 2.78 Å[42] | |
| [W6Cl14]2- | Sarı[43] | (d4)6 | Mo'ya bakın6Cl12 | |
| [ReCl6]− | kırmızı kahverengi | (t2 g)6 | sekiz yüzlü | Re-Cl mesafesi = 2.24-2.31 Å (PPh4+ tuz)[44] |
| [ReCl6] | (t2 g)1 | sekiz yüzlü | Re-Cl mesafesi = 226,3 (6) Å[6] | |
| [ReCl6]2− | yeşil | (t2 g)5 | sekiz yüzlü | Re-Cl mesafesi = 2.35-2.38 Å ((PPN+)2 tuz)[45] |
| [Yeniden2Cl9]2− | (t2 g)5 | yüz paylaşımlı biyoktahedral | Yeniden Re mesafesi = 2.48 Å Re-Cl mesafeleri = 2.42 Å (köprü), 2.33 Å (terminal) ((Et4N+)2 tuz)[46] | |
| [Yeniden2Cl9]− | (t2 g)5 | yüz paylaşımlı biyoktahedral | Yeniden Re mesafesi = 2.70 Å Re-Cl mesafeleri = 2.41 (köprü), 2.28 Å (terminal) (Bu4N+ tuz)[46] | |
| [İşletim sistemi2Cl10]2− | (t2 g)5 | sekiz yüzlü | (Et4N+)2 tuz [47] tuz | |
| [OsCl6]− | (t2 g)5 | sekiz yüzlü | Os-Cl mesafesi 2.28 Å | |
| [OsCl6]2− | (t2 g)4 | sekiz yüzlü[48] | Os-Cl mesafesi 2.33 Å | |
| [IrCl6]3− | kırmızı | (t2 g)6 | sekiz yüzlü | Ir-Cl = 2.36 Å[49] |
| [IrCl6]2− | Kahverengi | (t2 g)5 | sekiz yüzlü | Ir-Cl = 2.33 Å[50] |
| [PtCl4]2− | pembe | d8 | kare düzlemsel | |
| [PtCl6]2− | Sarı | d6 | sekiz yüzlü | Pt-Cl mesafesi = 2.32 Å Et4N+ tuz, ((Ben4N+)2 tuz)[20] |
| [AuCl2]− | beyaz / renksiz | d10 | doğrusal | Au-Cl mesafeleri 2,28 Å 4+ sal[51] |
| [AuCl4]− | Sarı | d8 | kare düzlemsel | Au-Cl mesafeleri 2,26 Å NBu4+ tuz[52] |
| [HgCl4]2− | beyaz / renksiz | d10 | dört yüzlü | Hg-Cl mesafesi 2.46 Å[19] Et4N+ tuz |
| [Hg2Cl6]2− | beyaz / renksiz | d10 | kenar paylaşımlı bitetrahedral | Hg-Cl mesafesi 2.46 Å[53] Bu4N+ tuz |
Heteroleptik kompleksler
Klorür içeren heteroleptik kompleksler çoktur. Hidratlı metal halojenürlerin çoğu bu sınıfın üyeleridir. Hexamminecobalt (III) klorür ve Cisplatin (cis-Pt (NH3)2Cl2) metal-ammin-klorürlerin önde gelen örnekleridir.
Hidratlar

Aşağıdaki tabloda belirtildiği gibi, birçok hidrat Metal klorürler moleküler komplekslerdir.[54][55] Bu bileşikler genellikle geçiş metali klorürlerinin önemli ticari kaynaklarıdır. Birkaç hidratlı metal klorür moleküler değildir ve bu nedenle bu tabloya dahil edilmemiştir. Örneğin, dihidratları manganez (II) klorür, nikel (II) klorür, bakır (II) klorür, demir (II) klorür, ve kobalt (II) klorür vardır koordinasyon polimerleri.
| Formülü hidratlı metal halojenürler | Koordinasyon metal küre |
|---|---|
| VCl3(H2Ö)6 | trans- [VCl2(H2Ö)4]+[56] |
| CrCl3(H2Ö)6 | trans- [CrCl2(H2Ö)4]+ |
| CrCl3(H2Ö)6 | [CrCl (H2Ö)5]2+ |
| CrCl2(H2Ö)4 | trans- [CrCl2(H2Ö)4] |
| CrCl3(H2Ö)6 | [Cr (H2Ö)6]3+[57] |
| MnCl2(H2Ö)6 | trans- [MnCl2(H2Ö)4] |
| MnCl2(H2Ö)4 | cis- [MnCl2(H2Ö)4][58] |
| FeCl2(H2Ö)6 | trans- [FeCl2(H2Ö)4] |
| FeCl2(H2Ö)4 | trans- [FeCl2(H2Ö)4] |
| FeCl3(H2Ö)6 | dört hidrattan biri Demir klorür,[59] |
| FeCl3(H2Ö)2.5 | cis- [FeCl2(H2Ö)4]+[60] |
| CoCl2(H2Ö)6 | trans- [CoCl2(H2Ö)4] |
| CoCl2(H2Ö)4 | cis- [CoCl2(H2Ö)4] |
| NiCl2(H2Ö)6 | trans- [NiCl2(H2Ö)4] |
| NiCl2(H2Ö)4 | cis- [NiCl2(H2Ö)4] |
Eter kompleksleri
Metal klorürler, eterlerle, özellikle tetrahidrofuran ile eklentiler oluşturur[61] ve şelatlayıcı eterler. Bu bileşikler, genellikle çözünür ve susuz oldukları için önemli reaktiflerdir.
| Formülü Metal-Klorür-eher Kompleksleri | Koordinasyon metal küre | renk |
|---|---|---|
| TiCl4(thf)2 | TiO2Cl4 | Sarı |
| TiCl3(thf)3 | TiO3Cl3 | mavi |
| ZrCl4(thf)2 | ZrO2Cl4 | beyaz |
| HfCl4(thf)2 | HfO2Cl4 | beyaz |
| VCl3(thf)3 | SES3Cl3 | pembe |
| NbCl4(thf)2 | NbO2Cl4 | Sarı |
| NiCl2(dimetoksietan)2 | NiCl2Ö4 | Sarı[62] |
Referanslar
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Elementlerin Kimyası (2. baskı). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ^ J.F. Hartwig (2009). "4: Metal-Heteroatom Bağlarıyla Bağlanan Kovalent (X-Tipi) Ligandlar". Organotransisyon Metal Kimyası. ISBN 978-1-891389-53-5.
- ^ a b c d Rivard, Eric; McWilliams, Andrew R .; Lough, Alan J .; Görgü, Ian (2002). "Bis (triklorofosfin) iminyum tuzları, [Cl3P = N = PCl3]+geçiş metali halojenür karşı iyonları ile ". Acta Crystallographica C Bölümü Kristal Yapı İletişimi. 58 (9): i114 – i118. doi:10.1107 / S0108270102012532. PMID 12205363.
- ^ Castro, Stephanie L .; Streib, William E .; Huffmann, John C .; Christou George (1996). "Karışık bir değer (TiIIITiIV) Karboksilat Kompleksi: Kristal Yapıları ve [Ti2OCl3(Ö2CPh)2(THF)3] ve [NEt4] 3 [Ti2Cl9]". Kimyasal İletişim (18): 2177. doi:10.1039 / CC9960002177.
- ^ Chen, Linfeng; Pamuk, F.Albert (1998). "Yüz paylaşımlı Ti (III) komplekslerinin sentezi, reaktivite ve X-ışını yapıları; yeni üç çekirdekli iyon, [Ti3Cl12] 3−". Çokyüzlü. 17 (21): 3727–3734. doi:10.1016 / S0277-5387 (98) 00171-5.
- ^ a b c Tamadon, Farhad; Seppelt, K. (2012). "Zor Halides VCl5, MoCl6ve ReCl6". Angewandte Chemie Uluslararası Sürümü. 52 (2): 767–769. doi:10.1002 / anie.201207552. PMID 23172658.CS1 Maint: yazar parametresini kullanır (bağlantı)
- ^ Hayton, Trevor W .; Patrick, Brian O .; Legzdins, Peter (2004). "Nitrik Oksitin Vanadyum Tetraklorürle Reaksiyonlarına İlişkin Yeni Detaylar". İnorganik kimya. 43 (22): 7227–7233. doi:10.1021 / ic0491534. PMID 15500362.
- ^ O. S. Filipenko, D. D. Makitova, O. N. Krasochka, V. I. Ponomarev, L. O. Atovmyan (1987). Koord. Khim. 13: 669. Eksik veya boş
| title =(Yardım)CS1 bakım: birden çok isim: yazar listesi (bağlantı) - ^ a b c d e f g h Gill, N. S .; Taylor, F.B. (1967). "İlk Geçiş Serisindeki Dipozitif Metallerin Tetrahalo Kompleksleri". İnorganik Sentezler. 9: 136–142. doi:10.1002 / 9780470132401.ch37. ISBN 9780470132401.
- ^ Chang, Jui-Cheng; Ho, Wen-Yueh; Sun, I-Wen; Chou, Yu-Kai; Hsieh, Hsin-Hsiu; Wu, Tzi-Yi (2011). "Yeni tetraklorokobaltat (II) ve tetrakloromanganat (II) anyon tuzlarının dikasyonik karşı iyonlarla sentezi ve özellikleri". Çokyüzlü. 30 (3): 497–507. doi:10.1016 / j.poly.2010.11.009.
- ^ a b c d Sun, Jui-Sui; Zhao, Hanhua; Ouyang, Xiang; Clérac, Rodolphe; Smith, Jennifer A .; Clemente-Juan, Juan M .; Gómez-Garcia, Carlos; Coronado, Eugenio; Dunbar, Kim R. (1999). "Dinükleer Anyon [M2Cl6] 2- (M = Mn, Fe, Co) İçeren Tuzların Yapıları, Manyetik Özellikleri ve Reaktivite Çalışmaları". İnorganik kimya. 38 (25): 5841–5855. doi:10.1021 / ic990525w.
- ^ Moews, P.C. (1966). "Potasyum Heksakloromanganatın (IV) Kristal Yapısı, Görünür ve Ultraviyole Spektrumları". İnorganik kimya. 5: 5–8. doi:10.1021 / ic50035a002.
- ^ Sen, Abhijit; Swain, Diptikanta; Guru Row, Tayur N .; Sundaresan, A. (2019). "Parlak bir parlak organik-inorganik halojenür (CH6N3) 2MnCl4 içinde değiştirilebilir dielektrik ve manyetik özelliklerde eşi görülmemiş 30 K histerezis" (PDF). Malzeme Kimyası C Dergisi. 7 (16): 4838–4845. doi:10.1039 / C9TC00663J.
- ^ Lutz, Martin; Huang, Yuxing; Moret, Marc-Etienne; Klein Gebbink, Robertus J.M. (2014). "Faz geçişleri ve ikiz düşük sıcaklık yapıları tetraetilamonyum tetrakloridoferrat (III)". Acta Crystallographica Bölüm C Yapısal Kimya. 70 (5): 470–476. doi:10.1107 / S2053229614007955. hdl:1874/307900. PMID 24816016.
- ^ Stucky, G. D .; Folkers, J. B .; Kistenmacher, T.J. (1967). "Tetraetilamonyum tetrakloronikelatın (II) kristal ve moleküler yapısı". Açta Crystallographica. 23 (6): 1064–1070. doi:10.1107 / S0365110X67004268.
- ^ a b Gerdes, Allison; Bond, Marcus R. (2009). "Octakis (dimetilamonyum) heksa-μ2-klorido-heksakloridotrinikelat (II) diklorür: Asimetrik köprülü bir doğrusal trinikel kompleksi". Acta Crystallographica C Bölümü Kristal Yapı İletişimi. 65 (10): m398 – m400. doi:10.1107 / S0108270109036853. PMID 19805875.
- ^ Mahoui, A .; Lapasset, J .; Moret, J .; Saint Grégoire, P. (1996). "Tetraetilamonyum Tetrametilamonyum Tetraklorokuprat (II), [(C2H5) 4N] [(CH3) 4N] [CuCl4]". Acta Crystallographica C Bölümü Kristal Yapı İletişimi. 52 (11): 2674–2676. doi:10.1107 / S0108270196009031.
- ^ Willett, Roger D .; Kasap, Robert E .; Landee, Christopher P .; Twamley, Brendan (2006). "Bakır (II) Halojenür Dimerlerinde İki Halojenür Değişimi: (4,4′-Bipiridinyum) Cu2Cl6 − x BRX". Çokyüzlü. 25 (10): 2093–2100. doi:10.1016 / j.poly.2006.01.005.
- ^ a b c Mahoui, A .; Lapasset, J .; Moret, J .; Saint Grégoire, P. (1996). "Bis (tetraetilamonyum) Tetraklorometalatlar, [(C2H5) 4N] 2 [MC14], burada M = Hg, Cd, Zn". Acta Crystallographica C Bölümü Kristal Yapı İletişimi. 52 (11): 2671–2674. doi:10.1107 / S010827019600666X.
- ^ a b c Autillo, Matthieu; Wilson, Richard E. (2017). "Tetrametilamonyum Heksaklorometalat Bileşiklerinde (TMA) Faz Geçişleri2MCI6 (M = U, Np, Pt, Sn, Hf, Zr) ". Avrupa İnorganik Kimya Dergisi. 2017 (41): 4834–4839. doi:10.1002 / ejic.201700764.
- ^ Simon, Arndt; von Schnering, Hans-Georg; Schäfer, Harald (1968). "Beiträge zur Chemie der Elemente Niob und Tantal. LXIX K4Nb6Cl18 Darstellung, Eigenschaften und Struktur ". Zeitschrift für anorganische und allgemeine Chemie. 361 (5–6): 235–248. doi:10.1002 / zaac.19683610503.
- ^ Rabe, Susanne; Bubenheim, Wilfried; Müller, Ulrich (2004). "Bis (tetrafenilfosfonyum) Tetraklorooksovanadat (IV), Hekzaklorostannat (IV) ve -Molibdat (IV) Asetonitril Solvatlarının Kristal Yapıları, [P (C6H5)4] 2 [VOCl4] · 4CH3CN, [P (C6H5)4] 2 [MCl6] · 4CH3CN (M = Sn, Mo) ". Zeitschrift für Kristallographie - Yeni Kristal Yapılar. 219 (2): 101–105. doi:10.1524 / ncrs.2004.219.2.101. S2CID 201122319.
- ^ a b Brignole, A. B .; Cotton, F. A .; Dori, Z. (1972). Dörtlü Bağ İçeren Renyum ve Molibden Bileşikleri. Inorg. Synth. 13. sayfa 81–89. doi:10.1002 / 9780470132449.ch15.
- ^ a b Pamuk, F.A; Ucko, David A. (1972). "Trimetilfenilamonyum Nonaklorodirhodat'ın (III) Yapısı ve Konfasiyal Bioctahedra'da Metal-Metal Etkileşimleri Üzerine Bir Araştırma". İnorganika Chimica Açta. 6: 161–172. doi:10.1016 / S0020-1693 (00) 91778-X.
- ^ . doi:10.1524 / ncrs.2004.219.2.101. Alıntı dergisi gerektirir
| günlük =(Yardım); Eksik veya boş| title =(Yardım) - ^ Hey E .; Weller, F .; Dehnicke, K. (1984). "Synthese ve Kristallstruktur von (PPh4)2[Mo2Cl10]". Zeitschrift für anorganische und allgemeine Chemie. 508: 86–92. doi:10.1002 / zaac.19845080113.
- ^ Ahmed, Ejaz; Ruck, Michael (2011). "İyonik Sıvılarda Polinükleer Geçiş-Metal Komplekslerinin Kimyası". Dalton İşlemleri. 40 (37): 9347–57. doi:10.1039 / c1dt10829h. PMID 21743925.
- ^ Sharutin, V. V .; Sharutina, O. K .; Senchurin, V. S .; Andreev, P.V. (2018). "Rutenyum Komplekslerinin Sentezi ve Yapısı $$ rm [{Ph_ {3} PR] _2 ^ + [RuCl6] ^ {2 -}} $$ [Doktora3PR] 2 + [RuCl6] 2 - (R = C2H5, CH = CHCH3, CH2CH = CHCH3, CH2OCH3) ve $$ rm [{Ph_ {3PCH2CH = CHCH2{PPh3}] _ 2 ^ {2 +} [Ru_2Cl_ {10} O] ^ {4 -}} $$ [Telefon3PCH2CH = CHCH2PPh3 ] 2 2 + [Ru2Cl10Ö]4− · 4H2Ö". Rus İnorganik Kimya Dergisi. 63 (9): 1178–1185. doi:10.1134 / S0036023618090188. S2CID 105746627.
- ^ Bino, Avi; Cotton, F.Albert (1980). "Rutenyumun Doğrusal, Trinükleer, Karışık Değerli Kloro Kompleksi, [Ru3Cl12]4-". Amerikan Kimya Derneği Dergisi. 102 (2): 608–611. doi:10.1021 / ja00522a027.
- ^ Frank, Walter; Reiß, Guido J .; Kleinwächter, Ingo (1996). "Spezielle Alkylammoniumhexachlorometallate. I. Kristallisationsverhalten und Kristallstruktur von Dietilentriammoniumhexachlororhodat, [H3N (CH2)2NH2(CH2)2NH3] [RhCl6]". Zeitschrift für anorganische und allgemeine Chemie. 622 (4): 729–733. doi:10.1002 / zaac.19966220428.
- ^ Helgesson, Goeran; Jagner Susan (1991). "Olağandışı koordinasyon geometrilerine sahip Halojenoargentat (I). Katı Haldeki İki Koordineli Kloroargentatın (I) İlk Örneği Dahil Kloro-, Bromo- ve İyodoargentatların (I) Potasyum-kript Tuzlarının Sentezi ve Yapısı". İnorganik kimya. 30 (11): 2574–2577. doi:10.1021 / ic00011a024.
- ^ a b Hao, Pengfei; Guo, Chunyu; Shen, Junju; Fu, Yunlong (2019). "Üç çekirdekli [Cd3Cl12] 6− kümeleri ve protonlanmış tripiridil-triazinler içeren yeni bir fotokromik hibrit". Dalton İşlemleri. 48 (44): 16497–16501. doi:10.1039 / C9DT03494C. PMID 31559400.
- ^ Costin-Hogan, Christina E .; Chen, Chun-Long; Hughes, Emma; Pickett, Austin; Valencia, Richard; Rath, Nigam P .; Beatty, Alicia M. (2008). ""Tersine "mühendislik: 0-D kadmiyum halojenür kümelerine doğru". CrystEngComm. 10 (12): 1910. doi:10.1039 / b812504j.
- ^ Chen, Chun-Long; Beatty, Alicia M. (2007). "Kristal mühendisliğinden küme mühendisliğine: Kadmiyum klorür 2-D'den 0-D'ye nasıl dönüştürülür". Chem. Commun. (1): 76–78. doi:10.1039 / B613761J. PMID 17279266.
- ^ Neumüller, Bernhard; Dehnicke Kurt (2004). "Die Kristallstrukturen von (Doktora4P)2[HfCl6] 2CH2Cl2 und (Ph4P)2[Hf2Cl10] CH2Cl2". Zeitschrift für anorganische und allgemeine Chemie. 630 (15): 2576–2578. doi:10.1002 / zaac.200400370.
- ^ Dötterl, Matthias; Haas, Isabelle; Alt, Helmut G. (2011). "TiCl'nin Çözünürlük Davranışı4, ZrCl4ve HfCl4 Kloroalüminat İyonik Sıvılarda ". Zeitschrift für anorganische und allgemeine Chemie. 637 (11): 1502–1506. doi:10.1002 / zaac.201100244.
- ^ Jacobson, Robert A .; Thaxton, Charles B. (1971). "H2 [Ta6Cl18] .6H2O'nun kristal yapısı". İnorganik kimya. 10 (7): 1460–1463. doi:10.1021 / ic50101a029.
- ^ J.C. Taylor, P.W. Wilson (1974). "Toz Nötron ve X-ışını Kırınımı ile β-Tungsten Heksaklorürün Yapısı". Açta Crystallographica. B30 (5): 1216–1220. doi:10.1107 / S0567740874004572.CS1 Maint: yazar parametresini kullanır (bağlantı)
- ^ Lau, C .; Dietrich, A .; Plate, M .; Dierkes, P .; Neumüller, B .; Wocadlo, S .; Massa, W .; Harms, K .; Dehnicke, K. (2003). "Kristallstrukturen der Hexachlorometallate NH4[SbCl6], NH4[WCl6], [K (18-Krone-6) (CH2Cl2)]2[WCl6] · 6CH2Cl2 und (PPh4)2[WCl6] · 4CH3CN ". Zeitschrift für Anorganische und Allgemeine Chemie. 629 (3): 473–478. doi:10.1002 / zaac.200390078.
- ^ Eichler, W .; Seifert, H.-J. (1977). "Strukturelle und magnetische Untersuchungen an Hexachlorowolframaten (V)". Zeitschrift für anorganische und allgemeine Chemie. 431: 123–133. doi:10.1002 / zaac.19774310112.
- ^ a b Cotton, F. Albert; Falvello, Larry R .; Mott, Graham N .; Schrock, Richard R .; Sturgeoff, Lynda G. (1983). "Nonakloroditungsten (II, III) İyonunun Yapısal Karakterizasyonu". İnorganik kimya. 22 (18): 2621–2623. doi:10.1021 / ic00160a031.
- ^ a b c Kolesnichenko, Vladimir; Luci, Jeffrey J .; Swenson, Dale C .; Messerle, Louis (1998). "W3 (μ3-Cl) (μ-Cl) 3Cl9n- (n = 2, 3), Yeni Bir İkili Tungsten Klorürden Türetilen Ayrık Monokaplı Tritungsten Kümeleri, W3Cl10: Elektron Sayısının İzostrukturaltrianguloM3X13 Kümelerdeki Bağlanma Üzerindeki Etkisi". Amerikan Kimya Derneği Dergisi. 120 (50): 13260–13261. doi:10.1021 / ja9831958.
- ^ Kolesnichenko, Vladimir; Messerle, Louis (1998). "Tungsten Halojenürlerin Geleneksel Olmayan, Hafif İndirgeyicilerle Kolayca İndirgenmesi. 2. Heksatungsten Dokaklorür Kümesi W6Cl12 ve Küme Asitinin (H3O) 2 [W6 (μ3-Cl) 8Cl6] (OH2) x, Dört Uygun, Yüksek Verimli Katı Hal Sentezi, Yeni Katyon Destekli Üçlü Yollar Dahil ". İnorganik kimya. 37 (15): 3660–3663. doi:10.1021 / ic980232n. PMID 11670462.
- ^ Arp, O .; Preetz, W. (1994). "Darstellung, Schwingungsspektren ve Normalkoordinatenanalyse von Hexachlororhenat (V) sowie Kristallstruktur von [P (C6H5)4] [ReCl6]". Zeitschrift für anorganische und allgemeine Chemie. 620 (8): 1391–1396. doi:10.1002 / zaac.19946200811.
- ^ "Di [bis (trihenylphosphine) iminium] Hexachlororhenate (IV)" yapısı. Acta Crystallographica C Bölümü Kristal Yapı İletişimi. 44 (4): 751–753. 1988. doi:10.1107 / S0108270187011910.
- ^ a b Heath, Graham A .; McGrady, John E .; Raptis, Raphael G .; Willis, Anthony C. (1996). "Değerliğe Bağlı Metal − Metal Bağları ve Konfasiyal Biyoktahedralde Optik Spektrumlar [Re2Cl9]z-(z = 1, 2, 3). [Re'nin Kristalografik ve Hesaplamalı Karakterizasyonu2Cl9]−ve [Re2Cl9]2-". İnorganik kimya. 35 (23): 6838–6843. doi:10.1021 / ic951604k. PMID 11666851.
- ^ B.Krebs, G.Henkel, M.Dartmann, W. Preetz, M.Bruns (1984). "Reaktionen und Strukturen von [(C2H5) 4N] [OsCl6] ve [(n-C4H9) 4N] 2 [Os2Cl10] / Reaksiyonlar ve [(C2H5) 4N] [OsCl Yapıları6] ve [(n-C4H9) 4N] 2 [Os2Cl10] ". Z. Naturforsch. 39 (7): 843. doi:10.1515 / znb-1984-0701. S2CID 95254820.CS1 bakım: birden çok isim: yazar listesi (bağlantı)
- ^ Kim, Eunice E .; Eriks, Klaas; Magnuson Roy (1984). "Hexachloroosmate (V) ve Hexachloroosmate (IV) Tetrafenilfosfonyum tuzlarının Kristal Yapıları, [(C6H5)4P] OsCl6 ve C6H5)4P]2OsCl6". İnorganik kimya. 23 (4): 393–397. doi:10.1021 / ic00172a003.
- ^ Rankin, DA; Penfold, BR; Fergusson, JE (1983). "İridyum (III) ve iridyum (IV) 'ün kloro ve bromo kompleksleri. II. IrIII komplekslerinin yapısal kimyası". Avustralya Kimya Dergisi. 36 (5): 871. doi:10.1071 / CH9830871.
- ^ Sanchis-Perucho, Adrián; Martínez-Lillo, José (2019). "Heksakloroiridat (IV) Anyonuna Dayalı Yeni Ir (IV) -Cu (II) Zincirinde Ferromanyetik Değişim Etkileşimi". Dalton İşlemleri. 48 (37): 13925–13930. doi:10.1039 / C9DT02884F. PMID 31411207.
- ^ Helgesson, Göran; Jagner, Susan; Vicentini, G .; Rodellas, C .; Niinistö, L. (1987). "Tetraetilamonyum Dikloroaurat (I) ve Tetraetilamonyum Diiyodoauratın (I) Kristal Yapıları". Acta Chemica Scandinavica. 41a: 556–561. doi:10.3891 / acta.chem.scand.41a-0556.
- ^ Buckley, Robbie W .; Healy, Peter C .; Loughlin, Wendy A. (1997). "[NBu'nun4] [AuCl4] [NBu'ya4] [AuCl2] Sodyum Asetilasetonat ile ". Avustralya Kimya Dergisi. 50 (7): 775. doi:10.1071 / C97029.
- ^ Goggin, Peter L .; Kral Paul; McEwan, David M .; Taylor, Graham E .; Woodward, Peter; Sandström Magnus (1982). "Tetra-n-bütilamonyum trihalojenomerküratların titreşimli spektroskopik çalışmaları; [NBun4] (HgCl3) ve [NBun4] - (HgI3) kristal yapıları". J. Chem. Soc., Dalton Trans (5): 875–882. doi:10.1039 / dt9820000875.
- ^ Waizumi, K .; Masuda, H .; Ohtaki, H. (1992). "FeBr'nin X-ışını Yapısal Çalışmaları2 • 4H2O, CoBr2 • 4H2O, NiCl2 • 4H2O ve CuBr2 • 4H2O. cis / trans Geçiş Metalinde (II) dihalid Tetrahidratta Seçicilik ". İnorganika Chimica Açta. 192: 173–181. doi:10.1016 / S0020-1693 (00) 80756-2.
- ^ Morosin, B. (1967). "Nikel (II) Klorür Dihidrat Üzerine Bir X-ışını Kırınım Çalışması". Açta Crystallogr. 23 (4): 630–634. doi:10.1107 / S0365110X67003305.
- ^ Donovan, William F .; Smith, Peter W. (1975). "Aquahalogenovanadium (III) Komplekslerinin Kristal ve Moleküler Yapıları. Bölüm I. X-Işını Kristal Yapısı trans-Tetrakisaquadibromo-Vanadium (III) Bromide Dihydrate ve Isomorphous Chloro- Compound ". Kimya Derneği Dergisi, Dalton İşlemleri (10): 894. doi:10.1039 / DT9750000894.
- ^ Andress, K.R .; Carpenter, C. "Kristallhydrate. II.Die Struktur von Chromchlorid- und Aluminiumchloridhexahydrat" Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie 1934, cilt 87, p446-p463.
- ^ Zalkin, Allan; Forrester, J. D .; Templeton, David H. (1964). "Manganez diklorür tetrahidratın kristal yapısı". İnorganik kimya. 3 (4): 529–33. doi:10.1021 / ic50014a017.
- ^ Lind, M.D. (1967). "Demir Klorür Heksahidratın Kristal Yapısı". Kimyasal Fizik Dergisi. 47 (3): 990–993. Bibcode:1967JChPh..47..990L. doi:10.1063/1.1712067.
- ^ Simon A. Cotton (2018). "Demir (III) klorür ve koordinasyon kimyası". Koordinasyon Kimyası Dergisi. 71 (21): 3415–3443. doi:10.1080/00958972.2018.1519188. S2CID 105925459.
- ^ Manzer, L. E. (1982). Seçilmiş Erken Geçiş Metallerinin Tetrahidrofuran Kompleksleri. İnorganik Sentezler. 21. s. 135–140. doi:10.1002 / 9780470132524.ch31.
- ^ Ward, Laird G.L. (1972). "Susuz Nikel (II) Halojenürler ve bunların Tetrakis (etanol) ve 1,2-Dimetoksietan Kompleksleri". İnorganik Sentezler. İnorganik Sentezler. 13. s. 154–164. doi:10.1002 / 9780470132449.ch30. ISBN 9780470132449.




