Hidrojen izotop biyojeokimyası - Hydrogen isotope biogeochemistry - Wikipedia
Hidrojen izotop biyojeokimyası dağılımını ve göreceli bolluğunu kullanarak çevredeki biyolojik, jeolojik ve kimyasal süreçlerin bilimsel çalışmasıdır. hidrojen izotopları. İki kararlı hidrojen izotopu vardır, protium 1El döteryum 2Yüzlerce mertebesine göre göreceli bollukta değişen H permil. Bu iki tür arasındaki oran hidrojen olarak düşünülebilir izotopik parmak izi bir maddenin. İzotopik parmak izlerini ve kaynaklarını anlamak fraksiyonlama bunlar arasında farklılıklara yol açan, aşağıdakilerden farklı bir dizi soruyu ele almak için uygulanabilir: ekoloji ve hidroloji -e jeokimya ve paleoiklim rekonstrüksiyonlar. Doğal hidrojen izotop bolluk oranlarını ölçmek için özel teknikler gerekli olduğundan, hidrojen izotop alanı biyojeokimya ekoloji ve jeokimya gibi daha geleneksel alanlar için benzersiz şekilde özelleştirilmiş araçlar sağlar.
Hidrojen izotoplarının tarihi
İlk çalışma
Çalışma hidrojen kararlı izotoplar keşfi ile başladı döteryum kimyager tarafından Harold Urey[1] ünlü Urey ve Miller deneyi. Olsa bile nötron 1932 yılına kadar gerçekleşmedi,[2] Urey, 1931'de "ağır hidrojen" aramaya başladı. Urey ve meslektaşı George Murphy, kırmızıya kayma ağır hidrojen Balmer serisi ve bir spektrografik ders çalışma. Yayınlanabilir veriler için spektroskopik çizgileri yoğunlaştırmak için Murphy ve Urey, Ferdinand Brickwedde ve bugün olarak bilinen daha konsantre bir ağır hidrojen havuzunu damıttı döteryum. Hidrojen izotopları üzerindeki bu çalışma 1934'te Urey'i kazandı Nobel Kimya Ödülü.[3]

Ayrıca 1934'te bilim adamları Ernest Rutherford, Mark Oliphant, ve Paul Harteck, radyoaktif izotop üretti trityum döteryuma yüksek enerjili çekirdeklerle vurarak. Deneyde kullanılan döteryum, Cömert bir ağır su armağanıydı. Berkeley fizikçi Gilbert N Lewis.[4] Döteryumun bombalanması, önceden tespit edilmemiş iki izotop, helyum-3 ve hidrojen-3 üretti. Rutherford ve meslektaşları başarılı bir şekilde trityumu yarattılar, ancak yanlışlıkla helyum-3'ün radyoaktif bileşen olduğunu varsaydılar. İşi Luis Walter Alvarez ve Robert Cornog[5] ilk izole trityum ve Rutherford'un yanlış fikrini tersine çevirdi. Alvarez, trityumun radyoaktif olduğunu düşündü, ancak yarı ömrü ölçmedi, ancak o zamanki hesaplamalar on yıldan fazla olduğunu gösteriyordu. Sonunda Dünya Savaşı II, fiziksel kimyager Willard Libby kalıntı tespit edildi radyoaktivite bir trityum numunesinin gayger sayacı,[4] daha doğru bir anlayış sağlamak yarım hayat, şimdi 12,3 yılda kabul edildi.[6]
Fiziksel kimyaya etkisi
Hidrojen izotoplarının keşfi aynı zamanda fizik 1940'larda Nükleer Manyetik Rezonans (NMR) spektroskopisi ilk icat edildi. Bugün, organik kimyagerler kullanmak NMR haritalamak için protein etkileşimleri[7] veya küçük bileşikleri tanımlamak,[8] ancak NMR ilk önce fizikçilerin tutkulu bir projesiydi. Her üç hidrojen izotopunun da manyetik özellikler NMR spektroskopisi için uygundur. NMR'nin bir uygulamasını tam olarak ifade eden ilk kimyager, George Pake, kim ölçtü alçıtaşı () bir kristal ve toz olarak.[9] Gözlenen sinyal İkili pake, sudaki manyetik olarak aktif hidrojenlerdendi. Pake daha sonra proton-protonu hesapladı bağ mesafesi. 1960'larda ticari makineler piyasaya sürüldüğünde NMR ölçümlerinde daha fazla devrim yapıldı. Bundan önce NMR deneyleri, büyük projeler inşa etmeyi, büyük mıknatısları yerleştirmeyi ve bakır bobinin elle kablolanmasını içeriyordu.[10] Proton NMR sonraki yıllarda gelişmeler boyunca en popüler teknik olarak kaldı, ancak döteryum ve trityum NMR spektroskopisinin diğer aromalarında kullanıldı. Döteryum farklı bir manyetik moment ve çevirmek protiumdan, ancak genellikle çok daha küçük bir sinyal. Tarihsel olarak, döteryum NMR proton NMR'ye zayıf bir alternatiftir, ancak davranışını incelemek için kullanılmıştır. lipidler açık zarlar.[11] Son zamanlarda, bir döteryum NMR varyasyonu 2H-SNIF, konuma özgü izotop bileşimlerini anlamak ve biyosentetik yolları anlamak için potansiyel göstermiştir.[12] Trityum ayrıca NMR'da da kullanılır,[13] protiumdan daha hassas olan tek çekirdek olduğu için çok büyük sinyaller üretir. Ancak trityum radyoaktivite T-NMR ile ilgili birçok çalışmayı caydırdı.
Trityum radyoaktivite, spektroskopi çürümeden gelen enerji, nükleer silahlar. Bilim adamları anlamaya başladı nükleer enerji 1800'lü yılların başlarında, ancak araştırmalarda büyük ilerlemeler kaydedildi. atom bombası 1940'ların başında. Savaş zamanı araştırması, özellikle Manhattan projesi büyük ölçüde hızlandırılmış bilimsel anlayış radyoaktivite. Trityum bir yan üründür reaktörler vurmanın bir sonucu lityum-6 ile nötronlar, neredeyse 5 MeV enerji üretir.

İçinde artırılmış fisyon nükleer silahlar döteryum ve trityum karışımı olana kadar ısıtılır. termonükleer fisyon helyum üretmek ve serbest bırakmak nötronlar.[14] Telaş hızlı nötron parçacıklar daha sonra daha da heyecanlanır fisyon reaksiyonları ile uranyum, "güçlendirilmiş" oluşturma atom bombası. 1951'de Sera Operasyonu George adlı bir prototip, böyle bir silah için konsept kanıtını başarıyla doğruladı.[15] Ancak, ilk doğru güçlendirilmiş fisyon nükleer cihazı, Sera Öğesi, 1952'de başarıyla test edildi ve 45,5 kilotonluk patlayıcı verimi, neredeyse güçlendirilmemiş bir sistemin değerini iki katına çıkardı.[15] Amerika Birleşik Devletleri trityum üretimini durdurdu nükleer reaktörler 1988'de[16] fakat nükleer silah testleri 1950'lerde büyük artışlar ekledi radyoaktif elementler atmosfere, özellikle radyokarbon ve trityum.[17][18] Jeologlar için bu karmaşık ölçümler karbonun radyometrik tarihlemesi. Ancak bazıları oşinograflar İzlemek için sudaki sinyali kullanarak trityum artışından yararlandı fiziksel karıştırma su kütleleri.[19]
Biyojeokimya üzerindeki etkisi
Biyojeokimyada, bilim adamları öncelikle çevresel süreçler için bir izleyici olarak döteryumun kararlı izotopuna, özellikle de Su döngüsü. Amerikalı jeokimyacı Harmon Craig, bir zamanlar Urey's yüksek lisans öğrencisi, yağmur suyunun hidrojeni ile oksijen izotopu oranlar. doğrusal korelasyon iki ağır izotop arasında dünya çapında korunur ve Küresel Meteorik Su Hattı.[20] 1960'ların sonunda, hidrojen izotoplarının odağı sudan uzaklaştı ve organik moleküller. Bitkiler oluşturmak için su kullanır biyokütle, ancak Zebrowski, Ponticorvo ve Rittenberg tarafından yapılan 1967 araştırması, bitkilerdeki organik materyalin su kaynağına göre daha az döteryuma sahip olduğunu buldu.[21] Zebrowski'nin araştırması, döteryum konsantrasyonunu ölçtü. yağ asitleri ve amino asitler tortulardan türetilmiştir Mohole sondaj projesi. Bruce Smith ve Samuel Epstein 1970 yılında, çevresel suya kıyasla organiklerdeki döteryumun tükendiğini doğruladı.[22] 1970'teki bir başka ikili, Schiegl ve Vogel, biyokütle haline geldikçe su biyokütle haline geldikçe hidrojen izotoplarının bileşimini analiz ettiler. kömür ve sıvı yağ ve petrol haline geldikçe doğal gaz.[23] Her adımda döteryumun daha da tükendiğini gördüler. 1980'de Marilyn Epstep, şimdiki M. Fogel ve Thomas Hoering tarafından "Kararlı hidrojen izotoplarının biyojeokimyası" başlıklı dönüm noktası niteliğindeki bir makale, organik malzemeler ve kaynaklar arasındaki bağları rafine etti.[24]
Hidrojene kararlı izotop çalışmasının bu erken aşamasında, çoğu izotop bileşimi veya fraksiyonları, hepsinin toplu ölçümleri olarak rapor edildi. organik materyal ya da hepsi inorganik malzeme. Bazı istisnalar şunları içerir: selüloz[25][26] ve metan,[27] bu bileşikler kolayca ayrıldığından. Metanın bileşiğe özgü ölçümler için bir başka avantajı, hidrojen değişiminin olmamasıdır. Selüloz değiştirilebilir hidrojene sahiptir, ancak kimyasal türevlendirme selüloz hidrojenin su veya mineral hidrojen kaynakları ile değiş tokuşunu önleyebilir. 1970'ler ve 1980'lerdeki selüloz ve metan çalışmaları, modern hidrojen izotop jeokimyası için standardı belirledi.
Bireysel bileşiklerin ölçümleri, 1990'ların sonlarında ve 2000'lerin başlarında, kütle spektrometrisi.[28] Termo Delta + XL, bileşiğe özgü izotop analizi yapabilen ilk cihaz olarak ölçümleri dönüştürdü. Daha sonra daha küçük numunelere daha hassas bir şekilde bakmak mümkün oldu. Hidrojen izotop uygulamaları hızla ortaya çıktı petrol jeokimyası yağı ölçerek, paleoklimatoloji gözlemleyerek lipit biyobelirteçler, ve ekoloji inşa ederek trofik dinamik. Şu anda kümelenmiş izotop bileşiminde modern ilerlemeler devam etmektedir. metan[29] geliştirildikten sonra karbonat termometre.[30][31] Hassas ölçümler ayrıca mikrobiyal odaklanma sağlar biyosentetik yollar hidrojen içeren.[32] Ekolojistler ders çalışıyor trofik seviyeler özellikle geçmiş diyetlerin oluşturulması ve avcı-av ilişkilerinin izlenmesi için bileşiğe özgü ölçümlerle ilgileniyor.[33] Son derece gelişmiş makineler şimdi, pozisyona özgü hidrojen izotop analizi için umut veriyor. biyomoleküller ve doğal gazlar.[34]
Önemli kavramlar
Radyoaktif izotoplara karşı kararlı
Bir kimyasal elementin tüm izotopları, değişen sayıda nötron içeren aynı sayıda proton içerir. Hidrojen elementinin doğal olarak oluşan üç izotoplar, 1H, 2El 3Bazen sırasıyla protium (H), döteryum (D) ve trityum (T) olarak anılan H. Her ikisi de 1El 2H süresiz olarak kararlıdır 3H kararsız ve oluşturmak için beta bozunmasına uğrar 3O. Bazı önemli uygulamaları varken 3Jeokimyada H (örneğin bir okyanus sirkülasyon izleyicisi ) bunlar burada daha fazla tartışılmayacaktır.
İzotop gösterimi
Kararlı izotop biyojeokimyası çalışması, belirli bir kimyasal havuzdaki çeşitli izotopların nispi bolluğunun tanımlanmasının yanı sıra, fizikokimyasal işlemlerin bir havuzda diğerine göre bu izotopların fraksiyonunu nasıl değiştirdiğini içerir. Bu süreçlerde izotopların bolluğunu ve bolluğundaki değişimi açıklamak için çeşitli tipte gösterim türleri geliştirilmiştir ve bunlar aşağıda özetlenmiştir. Çoğu durumda, bir izotopun yalnızca nispi miktarları söz konusudur, herhangi bir izotopun mutlak konsantrasyonu çok az önemlidir.
İzotop oranı ve kesirli bolluk
Bir sistemdeki hidrojen izotoplarının en temel tanımı döteryum ve protiumun göreceli bolluğudur. Bu değer, izotop oranı olarak bildirilebilir 2R veya kesirli bolluk 2F şöyle tanımlanır:
ve
nerede 2El 1H sırasıyla döteryum ve protium miktarlarıdır. Fraksiyonel bolluk, mol fraksiyonuna eşdeğerdir ve 100 ile çarpıldığında atom yüzdesi verir. Bazı durumlarda, bir numunenin atom yüzdesini eksi bir standardın atom yüzdesini bildiren atom yüzdesi fazlalığı kullanılır.
Delta (δ) gösterimi
Belirli bir madde için izotop oranları, genellikle bilinen izotopik bileşimli bir standarda kıyasla rapor edilir ve bağıl kütlelerin ölçümleri her zaman bir standardın ölçülmesiyle birlikte yapılır. Hidrojen durumunda Viyana Standart Ortalama Okyanus Suyu 155.76 ± 0.1 ppm izotop oranına sahip standart kullanılır. Bu standarda kıyasla delta değeri şu şekilde tanımlanır:
Bu delta değerleri genellikle oldukça küçüktür ve genellikle yukarıdaki denklemin 1000 faktörü ile çarpılmasından gelen mil değerlerine (‰) göre rapor edilir.
Fraksiyonasyon ölçüleri
Hidrojen izotop biyojeokimyası çalışması, çeşitli fizikokimyasal işlemlerin protyuma göre döteryumu tercihli olarak zenginleştireceği veya tüketeceği gerçeğine dayanır (kinetik izotop etkisine bakınız, vb.). Genellikle bir fizyokimyasal işlemin ürünü ve reaktanı olmak üzere iki havuz arasındaki bir izotopta fraksiyonlaşmayı açıklamak için geliştirilmiş çeşitli önlemler vardır. α notasyonu, iki hidrojen havuzu A ve B arasındaki farkı aşağıdaki denklemle açıklar:
nerede δ2HBir VSMOW'a göre A havuzunun delta değeridir. Birçok delta değeri birbirinden çok farklı olmadığından, a değeri genellikle birliğe çok yakındır. Epsilon (ε) adı verilen ilgili bir ölçü genellikle basitçe şu şekilde verilir:
Bu değerler genellikle sıfıra çok yakındır ve α-1'i 1000 ile çarparak değirmen başına değerler olarak rapor edilir. Son bir ölçü Δ'dir ve "cap delta" olarak telaffuz edilir, bu basitçe:
Karıştırma hesaplamalarında kütlenin korunumu
Yukarıda tartışıldığı gibi döteryum ve protium, radyoaktif bozunmaya asla uğramayan kararlı izotoplardır. Bu nedenle, hidrojen içeren bir havuzun D / H oranı, sisteme hidrojen eklenmediği veya sistemden çıkarılmadığı sürece sabit kalacaktır. kütlenin korunumu. İki hidrojen A ve B havuzu molar miktarlarda hidrojen m ile karıştığındaBir ve MB, her biri kendi başlangıç fraksiyonel döteryum bolluğuna (FBir ve FB), sonra ortaya çıkan karışımın fraksiyonel bolluğu aşağıdaki tam denklemle verilir:
Σ olan terimler, birleşik havuzların değerlerini temsil eder. Bilinen bir izotopik bileşime sahip iki havuzun karıştırılmasına ilişkin hesaplamalarda kullanılan aşağıdaki tahmini bulmak genellikle yaygındır:
Bu yaklaşım, doğal süreçlerden hidrojen havuzları ile uğraşmak zorunda kalan çoğu uygulamada küçük bir hata ile uygun ve uygulanabilir. Hesaplanan delta değeri ile yaklaşık ve kesin denklemler arasındaki maksimum fark aşağıdaki denklemde verilmiştir:
Bu hata, delta değerlerinde oldukça büyük doğal varyasyonlara sahip olabilen hidrojen için bile, doğal olarak oluşan izotop değerlerinin neredeyse tüm karışımları için oldukça küçüktür.[35] Doğal olmayan büyük izotop delta değerleriyle karşılaşıldığında tahmin genellikle kaçınılır, ki bu özellikle izotopik etiketleme deneyler.
Doğal olarak oluşan izotop varyasyonu
Doğal süreçler, farklı hidrojen havuzlarında bulunan D / H oranında geniş varyasyonlara neden olur. Kinetik izotop etkileri ve yağış ve buharlaşma gibi fiziksel değişiklikler bu gözlemlenen değişikliklere yol açar. Okyanus suyu, mil başına 0 ile −10 arasında çok az değişiklik gösterirken, atmosferik suyun mil başına yaklaşık −200 ila +100 arasında değiştiği bulunabilir. Organizmalar tarafından sentezlenen biyomoleküller, üzerinde büyüdükleri suyun D / H imzasının bir kısmını ve ayrıca mil başına birkaç yüz kadar büyük olabilen büyük bir fraksiyonlama faktörünü koruyacaktır. Dünya ile Mars gibi diğer gezegensel cisimler arasında, muhtemelen gezegen oluşumu sırasında izotop fraksiyonasyonundaki varyasyonlar ve uzaya hidrojenin fiziksel kaybı nedeniyle, mil başına binlerce değerinde büyük D / H farklılıkları bulunabilir.
İyi bilinen fraksiyonasyon etkilerinin listesi
Doğada bulunan izotop varyasyonlarını üretmek için bir dizi yaygın işlem hidrojen izotoplarını parçalara ayırır. Yaygın fiziksel süreçler arasında çökeltme ve buharlaşma bulunur. Kimyasal reaksiyonlar ayrıca havuzlar arasında ağır ve hafif izotopların bölünmesini büyük ölçüde etkileme potansiyeline sahiptir. Bir kimyasal reaksiyonun hızı, kısmen reaksiyonda oluşan ve kırılan kimyasal bağların enerjilerine bağlıdır. Farklı izotopların farklı kütleleri olduğundan, bağ enerjileri farklıdır. izotopologlar bir kimyasal türün. Bu, farklı izotopologlar için bir reaksiyon hızında bir farka yol açacak ve bir kimyasal reaksiyonda reaktan ile ürün arasında farklı izotopların fraksiyonlanmasına neden olacaktır. Bu, kinetik izotop etkisi olarak bilinir. Böyle bir izotop etkisinin klasik bir örneği, H arasındaki dengede D / H oranı farkıdır.2O ve H2 alfa değeri 3-4 kadar olabilir.[36]
Parmak izi için izleyici olarak izotop oranı
Pek çok çalışma alanında, bir kimyasalın veya bir grup kimyasalın kaynağı merkezi öneme sahiptir. Çevresel kirleticilerin kaynağı, bir sporcunun vücudundaki hormonların kaynağı veya yiyeceklerin ve aromaların gerçekliği gibi soruların tümü, kimyasal bileşiklerin tanımlanması ve kaynaklanması gereken örneklerdir. Hidrojen izotopları, bu ve diğer birçok farklı çalışma alanında kullanım alanları bulmuştur. Birçok işlem, belirli bir kimyasal bileşiğin D / H oranını etkileyebileceğinden, bu oran bir teşhis imzası belirli bir yerde veya belirli bir işlemle üretilen bileşikler için. Bir dizi kaynağın D / H oranları bilindiğinde, kaynağı bilinmeyen bir numune için bu oranın ölçümü, onu belirli bir kaynağa veya üretim yöntemine geri bağlamak için sıklıkla kullanılabilir.
Fiziksel kimya
Hidrojen izotop oluşumu
Protium veya hidrojen-1, bir proton ve hayır nötronlar, en bol olan element içinde Güneş Sistemi, ilk turlarda oluşmuş yıldız patlamaları sonra Büyük patlama.[37] Sonra Evren yaşama patladı, sıcak ve yoğun parçacık bulutu soğumaya başladı, önce atomaltı parçacıklar sevmek kuarklar ve elektronlar, daha sonra oluşturmak için yoğunlaştı protonlar ve nötronlar. Şundan büyük öğeler hidrojen ve helyum sırasında açığa çıkan enerjiden oluşan ardışık yıldızlarla üretildi. süpernova.
Döteryum veya bir proton ve bir nötron içeren hidrojen-2'nin de kozmik kökene sahip olduğu bilinmektedir. Protium gibi döteryum da evren tarihinin çok erken dönemlerinde üretildi. Big Bang nükleosentezi. Protonlar ve nötronlar birleştikçe, helyum-4 ile üretildi döteryum orta düzey. Alfa reaksiyonları helyum-4 ile günümüzün güneş sistemine hakim olan büyük elementlerin çoğunu üretir. Ancak, evren soğumadan önce, yüksek enerji fotonlar herhangi bir döteryumu yok ederek daha büyük element oluşumunu engelledi. Bu, döteryum darboğazı için zaman çizelgesinde bir kısıtlama nükleosentez. Günümüz döteryumunun tamamı bundan kaynaklandı proton-proton füzyonu yeterli soğutmadan sonra.[38]
Trityum veya bir proton ve iki nötron içeren hidrojen-3, erken evrende proton ve nötron çarpışmalarıyla da üretildi, ancak o zamandan beri radyoaktif olarak bozulmuş -e helyum-3. Modern trityum, trityumun kısa olması nedeniyle Big Bang nükleosentezi ile açıklanamaz. yarım hayat 12,3 yıl. Bugünün trityum konsantrasyonu bunun yerine aşağıdakiler tarafından yönetilmektedir: nükleer reaksiyonlar ve kozmik ışınlar. Trityumun helyuma radyoaktif beta bozunması, ortalama 18.6 MeV enerji salımı ile bir elektron ve bir antinötrino açığa çıkarır. Bunun nispeten zayıf bir beta reaksiyonu olarak sınıflandırıldığına dikkat etmek önemlidir, bu nedenle radyoaktivite cilde nüfuz edemez. Trityum bu nedenle yalnızca doğrudan yutulduğunda veya solunduğunda tehlikelidir.[39]
Kuantum özellikleri
Protium bir döndür-½ atom altı parçacık ve bu nedenle bir fermiyon. Diğer fermiyonlar şunları içerir: nötronlar, elektronlar, ve radyoaktif izotop trityum. Fermiyonlar tarafından yönetilir Pauli'nin dışlama ilkesi, hiçbir iki parçacığın aynı olamayacağı kuantum sayısı.[40][41] Bununla birlikte, döteryum ve fotonlar gibi bozonlar dışlama ile bağlı değildir ve birden çok parçacık aynı enerji durumunu işgal edebilir. Bu temel fark 1El 2H birçok fiziksel özellikte kendini gösterir. Döteryum gibi tamsayı spin parçacıkları takip eder Bose-Einstein istatistikleri yarım tam sayı dönüşlü fermiyonlar takip ederken Fermi-Dirac istatistikleri. Dalga fonksiyonları Bozon dalga fonksiyonları simetrikken, çoklu fermiyonları tanımlayan, parçacıkların değiş tokuşuna göre antisimetrik olmalıdır.[42] Bozonlar ayırt edilemez oldukları ve aynı durumda olabildikleri için, bozon koleksiyonları daha düşük sıcaklıklardaki fermiyonlardan çok farklı davranır. Bozonlar soğutulup en düşük enerji durumuna kadar gevşetilirken, aşırı akışkanlık ve süperiletkenlik meydana gelir.[43]
Kinetik ve denge izotop etkileri
İzotoplar sayılarına göre farklılık gösterir. nötronlar, fiziksel özellikleri kütle ve boyuta göre doğrudan etkileyen. Tipik hidrojene hidrojen-1 veya protium denir ve nötron içermez. Döteryum veya hidrojen-2 bir nötron ve trityum veya hidrojen-3 iki nötron içerir. Bu ek nötronlar, elementin kütlesini önemli ölçüde etkiler ve farklı kimyasal fiziksel özellikler. Bu etki özellikle hidrojen izotoplarında yaygındır, çünkü bir nötron eklenmesi kütleyi protiumdan döteryuma iki katına çıkarır. Daha yüksek düzey öğeler için karbon, oksijen, azot veya kükürt kütle farkı seyreltilir.
Fiziksel kimyagerler genellikle model yapıştırma ile kuantum harmonik osilatör, bir hidrojen-hidrojen bağını bir yayla birbirine bağlanmış iki top olarak basitleştiriyor.[41][44] Kuantum harmonik osilatörünün kendisi temel alır Hook kanunu ve iyi bir yaklaşım olarak hareket eder. Mors potansiyeli bu, bağlanmayı doğru bir şekilde tanımlar. Hidrojen ve döteryumun modellenmesi Kimyasal reaksiyon İzotopların ürünlerde ve reaktanlarda enerji dağılımlarını gösterir. Daha ağır izotop döteryum için daha düşük enerji seviyeleri, harmonik osilatörün tersine bağımlılığı ile matematiksel olarak açıklanabilir. azaltılmış kütle, μ ile gösterilir. Böylece, daha büyük bir azaltılmış kütle, daha büyük payda ve dolayısıyla daha küçük sıfır noktası enerjisi ve daha düşük enerji durumu içinde kuantum kuyusu.

- Döteryum-döteryum bağına karşı hidrojen-hidrojen bağının indirgenmiş kütlesini hesaplamak şunları verir:
- Kuantum harmonik osilatör aşağıdaki biçimde enerji seviyelerine sahiptir, burada k yay sabiti ve h Planck sabitidir.[41]
Bu enerji dağılımının etkileri, kinetik izotop etkisi ve denge izotopu etki.[45] İçinde tersinir reaksiyon denge koşulları altında, reaksiyon, termodinamik serbest enerjiyi en aza indirmek için izotopları dağıtarak ileri ve geri ilerleyecektir. Bir süre sonra, dengede, ürün tarafında daha ağır izotoplar olacaktır. Düşük enerjinin kararlılığı, ürünlerin reaktanlara göre döteryum bakımından zenginleşmesini sağlar. Tersine, kinetik koşullar altında reaksiyonlar genellikle geri çevrilemez. sınırlayıcı adım tepkide üstesinden gelmek aktivasyon enerjisi ara bir duruma ulaşma engeli. Daha hafif izotop, kuantum kuyusunda daha yüksek bir enerji durumuna sahiptir ve bu nedenle, tercihen ürünler haline getirilecektir. Dolayısıyla kinetik koşullar altında ürün döteryumda nispeten tükenecektir.
Kinetik izotop etkileri biyolojik sistemlerde yaygındır ve hidrojen izotop biyojeokimyası için özellikle önemlidir. Kinetik etkiler genellikle daha büyük kesirler denge reaksiyonlarından daha fazla. Herhangi bir izotop sisteminde, kinetik etkiler daha büyük kütle farklılıkları için daha güçlüdür. Çoğu sistemdeki ışık izotopları da daha hızlı hareket etme eğilimindedir, ancak daha zayıf bağlar oluşturur. Yüksek sıcaklıklarda, entropi izotop bileşiminde büyük bir sinyali açıklar. Bununla birlikte, sıcaklık düştüğünde izotop etkileri daha fazla ifade edilir ve rastgelelik daha az rol oynar. Bu genel eğilimler, bağ kırılmasının daha iyi anlaşılmasında ortaya çıkar. yayılma veya efüzyon, ve yoğunlaşma veya buharlaşma reaksiyonlar.
Hidrojen değişiminin kimyası
Hidrojen izotoplarının incelenmesindeki en büyük komplikasyonlardan biri değiştirilebilirlik sorunudur. Bilim adamları, saatlerden jeolojik çağlara kadar değişen birçok zaman ölçeğinde, incelenen moleküllerdeki hidrojen parçalarının orijinal türler olup olmadığını veya yakınlarda su veya mineral hidrojen ile alışverişi temsil edip etmediklerini düşünmek zorundadır. Bu alandaki araştırmalar, döviz kurları açısından hala yetersizdir, ancak genel olarak hidrojen değişiminin izotop çalışmalarında bilginin korunmasını zorlaştırdığı anlaşılmaktadır.
Hızlı değişim
Hidrojen atomları elektronegatif gibi tahviller hidroksil bağlar (O-H), azot bağlar (N-H) ve tiol /Merkapto tahviller (S-H) saatten güne uzun zaman ölçeklerinde. Bu hızlı değişim, özellikle yığın ölçümleri için sorunludur organik materyal bunlarla fonksiyonel gruplar çünkü izotop bileşimlerinin izotop etkisini değil kaynak suyu yansıtması daha olasıdır. Bu nedenle kayıtları paleoiklim Antik suları ölçmeyen diğer izotopik işaretlere güvenirler. 1990'lardaki gelişmeler, bu sorunu çözmek için umut verici bir potansiyele sahipti: numuneler, iki ağır su çeşidi ile dengelendi ve karşılaştırıldı. Oranları bir değişim faktörünü temsil eder. kalibre etmek hidrojen ve döteryum değişimini düzeltmek için ölçümler.[46]
Karbona bağlı hidrojen değişimi
Bir süredir araştırmacılar, hidrokarbon molekülleri hidrojen değişimine karşı dayanıklıydı, ancak son çalışmalar izotopların yeniden düzenlenmesine izin veren birçok reaksiyonu tanımladı. İzotopik değişim, jeolojik zaman ölçekleri ve biyologların çalışmalarını etkiledi lipit biyobelirteçler antik çağda çalışan jeologların yanı sıra sıvı yağ. Değişimden sorumlu reaksiyonlar şunları içerir:[46][47]

- Radikal reaksiyonlar C-H bağlarını ayıran.
- İyon değişimi üçüncül ve aromatik hidrojeninki.
- Enolizasyonlar Hidrojenleri aktive eden keton alfa karbonları.
- Stereokimyasal neden olan değişim stereokimyasal ters çevirme.
- Anayasal değişim gibi metil vardiya çift bağ göçler ve karbon omurgası yeniden düzenlemeleri.
Bu reaksiyonların ayrıntılı kinetiği belirlenmemiştir. Ancak biliniyor ki kil mineralleri iyonik hidrojen değişimini diğer minerallerden daha hızlı katalize eder.[48] Böylece hidrokarbonlar oluşur kırıntılı ortamlarda bulunanlardan daha fazla değiş tokuş karbonat ayarlar. Aromatik ve üçüncül hidrojen ayrıca birincil hidrojenden daha yüksek döviz kurlarına sahiptir. Bu, ilişkili olanın artan kararlılığından kaynaklanmaktadır. karbokatyonlar.[49] Birincil karbokatyonlar, fiziksel olarak var olamayacak kadar kararsız olarak kabul edilir ve hiçbir zaman FT-ICR spektrometre.[50] Öte yandan, üçüncül karbokatyonlar nispeten kararlıdır ve genellikle ara maddeler içinde organik Kimya reaksiyonlar. Proton kaybı olasılığını artıran bu kararlılık, elektron bağışı yakındaki karbon atomlarının. Rezonans ve yakınlarda yalnız çiftler ayrıca karbokatyonları stabilize edebilir elektron bağışı. Aromatik karbonlar dolayısıyla değiştirilmesi nispeten kolaydır.
Bu reaksiyonların çoğu, yüksek sıcaklıklar tipik olarak değişimi hızlandıran güçlü bir sıcaklık bağımlılığına sahiptir. Bununla birlikte, her sıcaklık aralığında farklı mekanizmalar geçerli olabilir. İyon değişimi örneğin, düşük sıcaklıklarda en önemli olanıdır. Bu kadar düşük sıcaklık ortamlarında, orijinal hidrojen izotop sinyalini yüz milyonlarca yıl boyunca koruma potansiyeli vardır.[51] Ancak, birçok kayalık jeolojik zaman önemli ulaştı termal olgunluk. Petrol penceresinin başlangıcında bile, hidrojenin çoğunun değiştiği görülüyor. Son zamanlarda, bilim adamları bir gümüş astarı keşfettiler: hidrojen değişimi bir sıfır dereceden kinetik reaksiyon (80–100 ° C'de karbona bağlı hidrojen için, yarım zamanlar muhtemelen 104 – 105 yıl).[51] Matematiğini uygulamak hız sabitleri izin verirdi ekstrapolasyon orijinal izotopik kompozisyonlara. Bu çözüm umut vaat ederken, literatürde sağlam kalibrasyonlar için çok fazla anlaşmazlık var.
Buhar izotop etkileri
Protium, döteryum ve trityum için buhar izotop etkileri meydana gelir, çünkü her izotop sıvı ve gaz fazlarında farklı termodinamik özelliklere sahiptir.[52] Su molekülleri için, yoğunlaştırılmış faz daha zenginleşirken, buhar daha azdır. Örneğin, bir buluttan yoğunlaşan yağmur, buharın başlangıç noktasından daha ağır olacaktır. Genel olarak, döteryum su konsantrasyonlarındaki büyük farklılıklar sıvı, buhar ve katı rezervuarlar arasındaki fraksiyonlardan kaynaklanmaktadır. Suyun fraksiyonlaşma modelinin aksine, yağlar ve lipitler gibi polar olmayan moleküller, sıvıya göre döteryum ile zenginleştirilmiş gaz halindeki benzerlerine sahiptir.[28] Bunun, uzun zincirli hidrokarbonlara müdahale etmeyen sudaki hidrojen bağından kaynaklanan polarite ile ilişkili olduğu düşünülmektedir.
İzotop bolluğundaki gözlemlenen varyasyonlar
Bu makale olabilir gerek Temizlemek Wikipedia'yla tanışmak için kalite standartları. Spesifik sorun şudur: δD tanımlanmadan defalarca kullanılır; daha az teknik okuyucular için daha basit bir göreli veya mutlak bolluk ölçüsüne çevrilmeye değer olabilir. (Mayıs 2019) (Bu şablon mesajını nasıl ve ne zaman kaldıracağınızı öğrenin) |

Fiziksel ve kimyasal fraksiyonlama süreçleri nedeniyle, elementlerin izotopik bileşimlerindeki varyasyonlar rapor edilir ve standart atom ağırlıkları Hidrojen izotoplarının, Atom Ağırlıkları ve İzotopik Bollukları Komisyonu tarafından yayınlandı. IUPAC. Kararlı H izotoplarının oranları, Uluslararası Atom Enerjisi Ajansı (IAEA) referans su. Genel olarak Hidrojen ve Döteryum'un denge izotop reaksiyonlarında, daha yüksek olan bileşikte ağır izotopun zenginleşmesi gözlenir. paslanma durumu. Bununla birlikte, doğal çevremizde, hidrojen izotoplarının izotopik bileşimi, dengesizlik hallerinde etkileşen elementlerin karmaşıklığından dolayı kaynaklara ve organizmalara bağlı olarak büyük ölçüde değişir. Bu bölümde, Güneş sistemindeki su kaynakları (hidrosfer), canlı organizmalar (biyosfer), organik maddeler (jeosfer) ve dünya dışı materyallerin hidrojen izotop bolluklarında gözlemlenen varyasyonlar açıklanmaktadır.
Hidrosfer
Okyanuslar
Farklı su kaynaklarının ve buzulların δD değerinde farklılıklar görülmüştür. buharlaşma ve yoğunlaşma süreçler. [Daha fazla ayrıntı için bölüm 6'ya bakın] Okyanus suyu iyi karıştırıldığında, dengedeki δD, 0,00015576 D / H oranıyla 0 ‰ (‰ SMOW) 'a yakındır. Bununla birlikte, δD değerlerindeki sürekli değişimler, buharlaşma veya yağış fraksiyonasyon süreçlerinde dengesizliğe yol açan süreçler. Okyanusların yüzey sularında büyük bir H izotopik gradyan (δD değerlerinde varyasyonlar) ve dalgalanma değeri gözlenir. Kuzeybatı Atlantik yüzey suyu 20 ‰ civarındadır. Denizin güneydeki üst bölümünü inceleyen verilere göre Pasifik Okyanusu, enlem (˚S) −65˚S'den −40˚S'ye düştükçe, δD değeri yaklaşık −50 ‰ ve −70 ‰ arasında dalgalanır.[54]
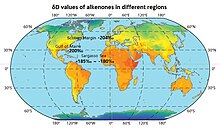
Deniz suyunun izotop bileşimi (sadece yüzey suyunun değil) çoğunlukla 0 - (- 10) range aralığındadır. Dünya genelinde okyanusların farklı kısımları için δD değerlerinin tahminleri haritada gösterilmektedir.[55]
Buzullar
Kutup bölgelerindeki buz tabakaları için tipik δD değerleri yaklaşık −400 ‰ ila −300 ‰ (‰ SMOW) arasındadır.[57] Buz örtüleri için δD değerleri açık okyanustan uzaklık, enlem, atmosferik sirkülasyon ve ayrıca güneşlenme miktarı ve sıcaklıktan etkilenir. The temperature change affects the deuterium content of ice caps, so the H/D isotopic composition of ice can give estimates for the historical climate cycles such as the timelines for interglacial ve buzul dönemleri. [See section 7.2. Paleo-reconstruction for more details]
The δD values of ice caps from 70 km south of Vostok Station and in East Antarktika are −453.7‰ and −448.4‰ respectively, and are shown on the map.[58]
Atmosphere
The analysis done based on satellite measurement data estimates the δD values for the atmosphere in various regions of the world. The general trend is that the δD values are more negative at higher-latitude regions, so the atmosphere above the Antarctica and the arctic regions is observed to be highly D-depleted to around −230‰ to −260‰ or even lower.
The estimates of the atmospheric δD values are shown on the map.[60]
A vast portion of the global atmospheric water vapor comes from the western Pacific Ocean near the tropical zone, (mean 2009) and the H/D isotopic composition of atmosphere varies depending on the temperature and humidity. In general, higher δD values are observed in humid regions with a high temperature.[61] Water vapor in the atmosphere is in general more depleted than the terrestrial water sources, since the rate of evaporation for 1H16
2O is faster than 1HD16O due to a higher vapor pressure. On the other hand, the rain water (precipitation) is in general more enriched than the atmospheric water vapor.[62][63]
Yağış
The δD values of the annual yağış in different regions of the world are shown on the map.[65] The precipitation is more D-enriched near the equator in the Tropical regions. The values of δD generally fall in the range of around −30~-150‰ in the northern hemisphere and −30~+30‰ over the land areas of the southern hemisphere. In North America, the δD values of average monthly precipitation across regions are more negative in January (ranging up to around −300‰ in Canada) compared to July (up to around −190‰).[66]
The overall mean precipitation is determined by balance between the evaporation of water from the oceans and surface water sources and the condensation of the atmospheric water vapor in the form of rain. The net evaporation should equal the net precipitation, and the δD value for the mean isotopic composition of global precipitation is around −22‰ (global average).[67] The Global Network of Isotopes in Precipitation (GNIP) investigates and monitors the isotopic composition of precipitation at various sites all over the world. The mean precipitation can be estimated by the equation, δ2H = 8.17(±0.07) δ18O + 11.27(±0.65)‰ VSMOW. (Rozanski et al., 1993) This equation is the slightly modified version from the general 'Global Meteoric Water Line (GMWL)' equation, δ2H = 8.13δ18O + 10.8, which provides the average relationship between δ2H and δ18O of natural terrestrial waters.[67][68]
Göller ve nehirler
The δD values vs. VSMOW of lakes in different regions are shown on the map.[70] The general pattern observed indicates that the δD values of the surface waters including lakes and rivers are similar to that of local precipitation.[71]
Soil water
The isotopic composition of soil is controlled by the input of yağış. Therefore, the δD values of soil across regions are similar to that of local precipitation. However, due to evaporation, soil tends to be more D-enriched than precipitation. The degree of enrichment varies greatly depending on the atmospheric humidity, local temperature as well as the depth of the soil beneath the surface. According to the study done by Meinzer et al. (1999), as the depth in the soil increases, the δD of soil water decreases.[71]
| Kaynak | δD | Referans |
|---|---|---|
| Surface ocean | −70‰ to −50‰ | Clog et al. (2013) |
| Deep ocean | −10‰ to 0‰ | Englebrecht and Sachs (2005) |
| Ice caps | −450‰ to −300‰ | Lecuyer et al. (1998), Masson-Delmotte et al. (2008) |
| Atmosphere | −260‰ to −80‰ | Frankenberg et al. (2009) |
| Yağış | −270‰ to +30‰ | waterisotopes.org |
| Göller | −130‰ to +50‰ | Sachse et al. (2012) |
| Soil water | −270‰ to +30‰ | waterisotopes.org |
Biyosfer
Marine algae
The factors affecting δD values of algal lipidler are the following: δD of water, algal species (up to 160%), lipid type (up to 170%), tuzluluk (+0.9±0.2% per PSU), growth rate (0 ~ -30% per day) and temperature (−2 ~ -8% per °C).
In the study done by Zhang et al. (2009), the δD values of fatty acids in Thakassiosira pseudonana chemostat cultures were −197.3‰, −211.2‰ and −208.0‰ for C14, C16 and C18 fatty acids respectively. Moreover, the δD value of C16 yağ asidi in an algal species named A. E. unicocca at 25 °C was determined using the empirical equation y = 0.890x – 91.730 where x is the δD of water at harvest. For another algal species named B. V. aureus, the equation was y = 0.869x −74.651.[72]
The degree of D/H fractionation in most algal lipids increases with increasing temperature and decreases with increasing salinity. The growth rates have different impacts on the D/H fractionation depending on the species types.[73]
Phytoplankton and Bacteria
The δD values of lipids from fitoplankton is largely affected by δD of water, and there seems to be a linear correlation between those two values. The δD of most other biosynthetic products found in phytoplankton or cyanobacteria are more negative than that of the surrounding water.[74] The δD values of yağ asitleri içinde methanotrophs living in seawater lie between −50 and −170‰, and that of steroller ve hopanols range between −150 and −270‰.[75][76]
The H isotopic composition of foto ototroflar can be estimated using the equation below:
- Rl = Xwαl/wRw + (1 – Xw)αl/sRs,[75]
nerede Rl, Rw, ve Rs are the D/H ratios of lipids, water, and substrates, respectively. Xw is the mole fraction of lipid H derived from external water, whereas αl/w ve αl/s denote the net isotopic fractionations associated with uptake and utilization of water and substrate hydrogen, respectively.
İçin Fototroflar, Rl is calculated assuming that Xw equals to 1. The isotopic fractionation between lipids and methane (αl/m) is 0.94 for fatty acids and 0.79 for isoprenoid lipids. The isotopic fractionation between lipids and water (αl/w) is 0.95 for fatty acids and 0.85 for isoprenoid lipids. For plants and yosun, the isotopic fractionation between lipids and methane (αl/m) is 0.94 for fatty acids and 0.79 for isoprenoid lipids.[75]
The δD values for lipids in bacterial species[72]
- Lipids in organisms growing on heterotrofik substrates:
- Growing on sugar: depletion of 200‰ ~ 300‰ relative to water
- Growing on direct precursor of TCA döngüsü (Örneğin. asetat (δDs = -76‰) or succinate ): enrichment of −50‰ ~ +200‰ relative to water
- αl/w: -150‰ ~ +200‰
- Lipids in organisms growing photoautotrophically:
- Depletion of 50‰ ~ 190‰ relative to water
- αl/w: -150‰ ~ -250‰
- Lipids in organisms growing chemoautotrophically:
- αl/w: -200‰ ~ -400‰
Bitkiler
δD values for n-C29 alkan (‰) vs. VSMOW for different plant groups are the following. In the equations, y represents δD values for n-C29 alkane(‰) vs. VSMOW, and x represents δD values for mean annual precipitation (‰) vs. VSMOW).[78]
| Plant Group | Equation for Estimating δD |
|---|---|
| Çalılar | y = 0.867x - 112 |
| Ağaçlar | y = 0.524x - 134 |
| Forbs | y = 1.158x - 120 |
| C3 graminoids | y = 1.209x – 129 |
| C4 graminoids | y = 0.777x – 142 |
For plant leaf balmumu, the relative humidity, the timing of leaf wax formation and the growth conditions including light levels affect the D/H fractionation of plant wax. From the Craig–Gordon model, it can be understood that leaf water in the growth chamber gasses is significantly D-enriched due to transpiration.[79]
Şeker
The relative global abundance of D in plants is in the following order: fenilpropanoidler > karbonhidratlar > bulk material > hydrolysable lipids > steroids.[80] In plants, δD values of carbohydrates, which typically range around -70‰ to -140‰, are good indicators of the photosynthetic metabolism. Photosynthetically produced Hydrogens which are bound to carbon backbones are around 100–170‰ more D-depleted than the water found in plant tissues.
The heterotrophic processing of carbohydrates involves izomerleştirme nın-nin triose phosphates and interconversion between fructose-6-phosphate ve glucose-6-phosphate. These cellular processes promote the exchange between organic H and H2O within the plant tissues leading to around 158‰ of D-enrichment of those exchanged sites.[81] The δD of C3 tesisleri gibi Şekerpancarı, orange and grape ranges from −132‰ to −117‰, and that of C4 bitkiler gibi şeker kamışı ve maize ranges from −91‰ to −75‰. The δD of KAM such as pineapple is estimated to be around −75‰.[80] Sugar beet and sugar cane contain sucrose, and maize contain glucose. Orange and pineapple are the sources of glikoz ve fructose.
The deuterium content of the sugars from the above plant species are not distinctive. In C3 plants, Hydrogens attached to Carbons in 4 and 5 positions of the glucose typically come from NADPH in the photosynthetic pathway, and are found to be more D-enriched. Whereas in C4 plants, Hydrogens attached to Carbons 1 and 6 positions are more D-enriched. D-enrichment patterns in CAM species tend to be closer to that in C3 species.[82]
Toplu organik Önemli olmak
The H/D isotopic composition of the leaf water is variable during the biosynthesis, and the enrichment in the whole leaf can be described by the equation, △Dleaf = △De * ((1-e−p)/P) [83][84]
The typical δD value of bulk plant is around −160‰ where δD values for selüloz ve lignin are −110‰ and −70‰ respectively.[80]
Hayvanlar
The hydrogen isotopic composition in animal tissues are difficult to estimate due to complexities in the diet intake and the isotopic composition of surrounding water sources. When fish species were investigated, average hydrogen isotopic composition of proteins was in a large range of −128 ‰ ~ +203 ‰. In the bulk tissue of organisms, all lipids were found to be D-depleted, and the values of δD for lipids tend to be lower than that for proteins. The average δD for Chironomid and fish protein was estimated to be in the range of −128‰ to +203‰.[85]
Most hydrogens in heterotrofik tissues come from water not from diet sources, but the proportion coming from water varies. In general, Hydrogen from water is transferred to NADPH and then taken up to the tissues. An apparent trofik effect (compounding effect) can be observed for δD in heterotrophs, so significant D-enrichments result from the intake of surrounding water the in aquatic food webs. The δD of proteins in animal tissues are in cases affected more by diet sources than by surrounding water.[85]
Although different δD values for the same class of compounds may arise in different organisms growing in water with the same δD value, those compounds generally have the same δD value within each organism itself. [See Section 7.5. Ecology for more details]
Lipidler
The δD values of fatty acids found in living organisms typically range from −73‰ to −237‰. The values of δD for individual fatty acids vary widely between cultures (−362‰ to +331‰), but typically by less than around 30‰ between different fatty acids from the same species.[72]
The differences in δD for the compounds within the same lipid class is generally smaller than 50‰, whereas the difference falls in the range of 50–150‰ for the compounds in different lipid classes.[72]
δD values for typical lipid groups are determined using the following equation:
- εl/w = (D/H)l/(D/H)w−1 = [(δDl + 1)/(δDw + 1)]−1[78] nerede εl/w = net or apparent fractionation, δDl = lipid product and δDw = source water.
- The δD for common lipid classes found in living organisms are the following:
- n-alkil: -170 ± 50‰ (113–262‰ more D-depleted than growth water)
- izoprenoit: -270 ± 75‰ (142–376‰ more D-depleted than growth water)
- fitol: -360 ± 50‰ (more depleted than the other two categories)
Polyisoprenoid lipids are more depleted than acetogenic (n-alkyl) lipids with more negative δD values.
| Tür | Kaynak | δD | Referans |
|---|---|---|---|
| Lipid | Marine Sediment | −470‰ to −30‰ | Zhang vd. (2008) |
| Marine Algae | −211‰ to −197‰ | Zhang vd. (2008) | |
| Methanotrophs | −170‰ to −50‰ | Sessions (2002) | |
| Heterotrophs | Enrichment of −50‰ to +200‰ relative to water | Zhang vd. (2008) | |
| Photoautotrophs | Enrichment of +50‰ to +190‰ relative to water | Zhang vd. (2008) | |
| Bitkiler | −270‰ to −120‰ | Sachse et al. (2012) | |
| Şeker | Carbohydrates | −140‰ to −70‰ | Schmidt et al. (2003) |
| C3 tesisleri | −132‰ to −117‰ | Schmidt et al. (2003) | |
| C4 bitkiler | −91‰ to −75‰ | Schmidt et al. (2003) | |
| KAM | around −75‰ | Schmidt et al. (2003) | |
| Toplu | Bitkiler | around −160‰ | Schmidt et al. (2003) |
| Animals (e.g. fish) | −128‰ to +203‰ | Soto et al. (2013) |
Jeosfer
Sıvı yağ[86]
- Oil samples from northeast Japan: from −130‰ to around −110‰ with higher maturity.[87]
- Oil samples from Portiguar Basin: -90‰ (lancustrine environment), -120‰ to -135‰ (marine-evaporitic environment),[88]
Alkenones[89]
The isotopic composition of alkenones often reflect the isotopic enrichment or depletion of the surrounding environment, and the δD values of alkenones in different regions are shown on the map.[91]
Coals[92]
According to the studies done by Reddings et al., δD for coals from various sources range from around −90‰ to −170‰.[94]
The δD values of coals in different regions are shown on the map.[95][96]
Doğal gaz[97]
Metan
Metan produced from marine metanojenler is typically more D-enriched than methane produced from methanogens grown in freshwater. The δD values for termojenik methane range from −275‰ to −100‰, and from −400‰ to −150‰ for mikrobiyal methane.[98]
H2 Gaz
The δD value observed for atmospheric H2 is around +180‰, which is the biggest delta value observed for natural terrestrials. (The mole fraction of 2H: 0.0001838) The δD value for doğal gaz from a Kansas well is around −836‰ (The mole fraction of Deuterium is 0.0000255)[99]Süreci sırasında elektroliz of water, hydrogen gas is produced at the cathode, but an incomplete electrolysis of water may cause isotopic fractionation leading to enrichment of D in the sample water and the production of hydrogen gas with deuterium components.
Mineral H
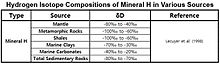
The δD values of hydroxyl-bearing minerals of mantle were estimated to be −80‰ ~ -40‰ through the analysis of the isotopic composition for juvenile water. Hydrogen Minerals generally have large isotope effects, and the isotopic composition often follows the pattern observed for precipitation.
Clay minerals
The D/H fractionations in clays such as kaolinite, illite, smectite are in most cases consistent when no significant external forces are applied under constant temperature and pressure.
The following is an empirically determined equation for estimating the D/H fractionation factor: 1000 In αkaolinite-water = -2.2 × 106 × T−2 – 7.7.[101]
The δD values vs. ‰SMOW for Hydrogen minerals found in örtü, Metamorfik Kaya, şeyller, deniz killer, deniz karbonatlar ve tortul rocks are shown in the table.[57]
| Kaynak | δD | Referans |
|---|---|---|
| Sıvı yağ | −135‰ to −90‰ | Waseda (1993), dos Santos Neto and Hayes (1999) |
| Alkenones | −204‰ to −181‰ | Englebrecht and Sachs (2005) |
| Coals | −170‰ to −50‰ | Redding (1980), Rigby and Smith (1981), Smith (1983) |
| Natural Gas (Methane) | −400‰ to −100‰ | Whiticar (1999) |
| H2 Gaz | −836‰ to +180‰ | Hoefs (2009) |
| Mineral H | −100‰ to −20‰ | Lecuyer et al. (1998) |
Extraterrestrial Objects
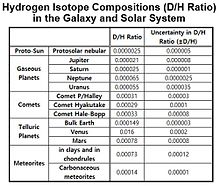
Variations of D/H ratio in the solar system[102]
- Dünya
- The H isotope composition of örtü rocks on earth is highly variable, and that of örtü water is around −80‰ ~ −50‰ depending on its states such as fluid, hydrous phase, hydroxyl point defect, Juvenile water (from degassing of the mantle), magmatic water (water equilibrated with a magma ).
- Güneş
- The D/H ratio of the sun is around 21 ± 5 × 10−6.[104]
- Mars
- The current Hydrogen isotope composition is enriched by a factor of 5 relative to terrestrial ocean water due to continual losses of H in Martian atmosphere. Therefore, the δD value is estimated to be around +4000‰.
The D/H ratios for Jüpiter ve Satürn is nearly in the order of 10−5, and the D/H ratios of Uranüs ve Neptün is closer to the order of 10−4.[105]
Hidrojen, evrende en bol bulunan elementtir. Variations in isotopic composition of extraterrestrial materials stem from planetary birikme or other planetary processes such as atmosferik escape, and are larger for H and N than for C and O. The preservation of D-enrichment is observed in kondritik göktaşları, interplanetary dust particles and kuyruklu yıldız volatiles.
İtibaren Helyum isotope abundance data, the cosmic D/H value is estimated to be around 20 ppm which is much lower than the terrestrial D/H ratio of 150 ppm. The enrichment of D/H from the proto-solar reservoir occurs for most of the planets except for Jupiter and Saturn, the massive gaseous planets. The D/H ratios of the atmospheres of Venüs and Mars are ~2 × 10−2 and ~8 × 10−4 sırasıyla. The D/H ratios of Uranus and Neptune is larger than that of protosolar reservoir by a factor of around 3 due to their Deuterium-rich icy cores. The D/H ratios for comets are much larger than the values for the planets in the solar system with δD value of around 1000‰.[106]
The Hydrogen isotope compositions in the galaxy and the solar system are shown in the table.
Measurement techniques
Determination of D/H ratio can be performed with a combination of different preparation techniques and instruments for different purposes. There are several basic categories of hydrogen isotope measurements: (i) organic hydrogen or water are converted to H2 first, followed by high precision IRMS (Isotope-ratio mass spectrometry ) measurement with high precisions; (ii) D/H and 18Ö/16O are directly measured as H2O by laser spectroscopy also with high precisions; (iii) the intact molecules are directly measured by NMR veya kütle spektrometrisi with relatively lower precision than IRMS.
Offline combustion and reduction
The conversion to simple molecules (i.e. H2 for hydrogen) is required prior to IRMS measurement for stable isotopes. This is due to several reasons with regard to hydrogen:
- organic molecules and some inorganic ones (e.g. CO2 + H2O) can have proton-exchange reactions with ion source of mass spectrometer and produce the products such as ve that cannot be distinguished;
- isotope effects due to ionization and transmission in the mass spectrometer can vary with different molecular forms.[107] It would require standards in every different molecular form that is being measured, which is not convenient.
The classical offline preparation for the conversion is combustion over CuO at > 800 °C in sealed quartz tubes, followed by the isolation of resulting water and the reduction to H2 over hot metal at 400 ~1000 °C on a vacuum line.[108] The produced gas is then directly injected into the dual-inlet mass spectrometer for measurement.[107] The metals used for the reduction to H2 includes U, Zn, Cr, Mg and Mn, etc. U and Zn had been widely used since the 1950s[25][109][110][111][112][113] until Cr[114] was successfully employed in the late 1990s.
The offline combustion/reduction has the highest accuracy and precision for hydrogen isotope measurement without limits for sample types. The analytical uncertainty is typically 1~2‰ in δD. Thus it is still being used today when highest levels of precision are required. However, the offline preparation procedure is very time-consuming and complicated. It also requires large sample size (several 102 mg). Thus the online preparation based on combustion/reduction coupled with the subsequent continuous flow-IRMS (CF-IRMS) system has been more commonly used nowadays. Chromium reduction or high temperature conversion are the dominant online preparation methods for the detection of hydrogen isotope by IRMS.
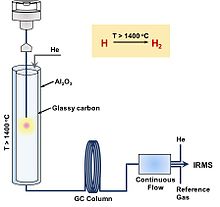
High temperature conversion/Elemental Analyzer (TC/EA)
TC/EA (or HTC, high temperature conversion; HTP, high temperature piroliz; HTCR, high temperature carbon reduction) is an 'online' or 'continuous flow' preparation method typically followed by IRMS detection. This is a "bulk" technique that measures all of the hydrogen in a given sample and provides the average isotope signal. The weighed sample is placed in a tin or silver capsule and dropped into a pyrolysis tube of TC/EA. The tube is made of glassy carbon with glassy carbon filling in which way oxygen isotope can be measured simultaneously without the oxygen exchange with ceramic (Al2Ö3) surface.[116] The molecules are then reduced into CO and H2 at high temperature (> 1400 °C) in the reactor. The gaseous products are separated through gas chromatography (GC) using helium as the carrier gas, followed by a split-flow interface, and finally detected by IRMS. TC/EA method can be problematic for organic compounds with halogen or nitrogen due to the competition between the pyrolysis byproducts (e.g. HCl and HCN) and H2 formation.[117][118] In addition, it is susceptible to contamination with water, so samples must be scrupulously dried.
An adaption of this method is to determine the non-exchangeable (C-H) and exchangeable hydrogen (bounds to other elements, e.g. O, S and N) in organic matter. The samples are equilibrated with water in sealed autosampler carousels at 115 °C and then transferred into pyrolysis EA followed by IRMS measurement.[119]
TC/EA method is quick with a relatively high precision (~ 1‰). It was limited to solid samples, however, liquid sample recently can also be measured in TC/EA-IRMS system by adapting an autosampler for liquids. The drawback of TC/EA is the relatively big sample size (~ mg), which is smaller than offline combustion/reduction but larger than GC/pyrolysis. It cannot separate different compounds as GC/pyrolysis does and thus only the average for the whole sample can be provided, which is also a drawback for some research.
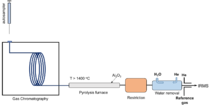
Gas chromatography/pyrolysis (GC/pyrolysis)
GC-interface (combustion or pyrolysis) is also an online preparation method followed by IRMS detection. This is a 'compound-specific' method, allowing separation of analytes prior to measurement and thus providing information about the isotopic composition of each individual compound. Following GC separation, samples are converted to smaller gaseous molecules for isotope measurements. GC/pyrolysis uses the pyrolysis interface between GC and IRMS for the conversion of H and O in the molecules into H2 and CO. GC-IRMS was first introduced by Matthews and Hayes in the late 1970s,[120] and was later used for δ13C, δ15N, δ18O and δ34S. Helium is used as the carrier gas in the GC systems. However, the separation of DH (m/z=3) signal from the tail of 4O+ beam was problematic due to the intense signal of 4O+.[121] During the early 1990s, intense efforts were made in solving the difficulties to measure δD by GC/pyrolysis-IRMS. In 1999, Hilkert et al. developed a robust method by integrating the high temperature conversion (TC) into GC-IRMS and adding a pre-cup electrostatic sector and a retardation lens in front of the m/z=3 cup collector. Several different groups were working on this at the same time.[121][122][123][124] This GC/pyrolysis-IRMS based on TC has been widely used for δD measurement nowadays. The commercial products of GC-IRMS include both combustion and pyrolysis interfaces so that δ13C and δD can be measured simultaneously.
The significant advantage of GC/pyrolysis method for hydrogen isotope measurement is that it can separate different compounds in the samples. It requires the smallest sample size (a typical size of ~ 200 ng[122]) relative to other methods and also has a high precision of 1~5 ‰. But this method is relatively slow and limited to the samples which can be applied in GC system.
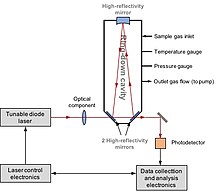
Laser spectroscopy
Lazer Spektroskopisi (veya Boşluk halka aşağı spektroskopisi, CRDS) is able to directly measure D/H, 17Ö/16O and 18Ö/16O isotope compositions in water or methane. The application of laser spectroscopy to hydrogen isotopes was first reported by Bergamaschi et al. 1994 yılında.[125] They directly measured 12CH3D/12CH4 içinde atmosferik metan using a lead salt tunable diode laser spectroscopy. The development of CRDS was first reported by O'Keefe et al. 1988'de.[126] In 1999, Kerstel et al. successfully applied this technique to determine D/H in water sample.[127] The system consists of a laser and a boşluk equipped with high finesse reflectivity mirrors. Laser light is injected into the cavity, at which the resonance takes place due to the constructive interference. The laser then is turn off. The decay of light intensity is measured. In the presence of a water sample, the photo-absorption by water isotopologues follows the kinetic law. The optical spectrum is obtained by recording ring-down time H'nin2O spectral features of interest at certain laser wavelength. The concentration of each isotopologue is proportional to the area under each measured isotopologue spectral feature.[128]
Laser Spectroscopy is a quick and simple procedure, relatively lower cost and the equipment is portable. So it can be used in the field for measuring water samples. D/H and 18Ö/16O can be determined simultaneously from a single injection. It requires a small sample size of < 1 μL for water. The typical precision is ~ 1‰. However, this is the compound-specific instrument, i.e. only one specific compound can be measured. And coexisting organic compounds (i.e. ethanol ) could interfere with the optical light absorption features of water, resulting in cross-contamination.
SNIF-NMR
2H-Site-specific Natural Isotope Fractionation-Nuclear Magnetic Resonance(2H-SNIF-NMR ) is a type of NMR specialized in measuring the deuterium concentration of organic molecules at natural abundances. The NMR spectra distinguishes hydrogen atoms in different chemical environments (e.g. The order of carbon that hydrogen binds to, adjacent functional groups, and even geminal positions of methylene groups), making it a powerful tool for position-specific isotope analysis. kimyasal kayma (in frequency units) of 2H is 6.5 times lower than that of 1H. Thus, it is difficult to resolve 2H peaks. To provide high-enough resolution to separate 2H peaks, high strength magnetic field instruments (~11.4T)[129] are applied. Application of NMR to study hydrogen isotopes of natural products was pioneered by G'erard Martin and his co-workers in the 1980s.[130] For several decades it has been developed and expanded. The D/H NMR measurement is sometimes coupled with IR-MS measurement to create a referential standard.[131] The sensitivity of SNIF-NMR is relatively low, typically requiring ~1 mmol of samples for each measurement.[132] The precision with respect to isotope ratio is also relatively poor compared with mass spectrometry. Even the state-of-art instruments can only measure D/H ratios with around 50~200‰ error depending on the compound.[133][134][135] Therefore, so far technique can only distinguish the large D/H variations in preserved materials. In 2007, Philippe Lesot and his collezzes advanced this technique with a 2-Dimensional NMR using chiral sıvı kristaller (CLCs) instead of isotropic solvents to dissolve organic molecules.[136] This enables the measurements of quadrupolar doublets for each nonequivalent deuterium atom. Thus reduces peak overlaps and provides more detailed information of hydrogen chemical environment.[134]
Ana akım applications of 2H-SNIF-NMR have been in source attribution, adli ve biyosentetik yol studies. (See also Gray's section "Source attribution and Forensics") When measuring şeker compounds, a timesaving strategy is to convert them into ethanol through fermentation because 2H-SNIF NMR for ethanol is well established.[131] Several studies[131][137] have proved that hydrogen isotopes on the methyl and methylene position of the resulting ethanol is not affected by either fermentation rate or media. Another example is the study of monoterpenes. since the 1980s SNIF-NMR study of α-pinene has found large variations in D/H ratios among its sites. Particularly ex-C2 position has a strong depletion (~-750‰), which was in disagreement with accepted biosynthetic mechanism (mevalonate mechanism) at that time, and lead to new development in pathways. More recently, Ina Ehlers published their work on the D6S/D6R ratios of glucose molecules. The stereochemical diteterium distribution was found to correlate to photorespiration/photosynthesis ratios. Photorespiration/photosynthesis ratios are driven by CO2 fertilization,[135] thus this might lead to new proxies in reconstructing paleo-CO2 concentration. Work has also been done for long-chain fatty acids and found that even-numbered sites, which are thought to be derived from C2 position of the acetyl group, are more enriched in deuterium than odd-numbered hydrogen that come from C1 position of the acetyl group.[132] Duan et al. reported a strong kinetik izotop etkisi (KIE) during the desaturation from oleic acid to linoleic acid.[138]
In summary, the underlying physics of the SNIF-NMR makes it capable of measuring isotopomers. Another advantage of doing NMR measurements over mass spectrometry is that it analyzes samples non-destructively. 2H SNIF-NMR has been well industrialized in source identification and forensics, and has contributed much to biochemical pathway studies. The application of 2H SNIF-NMR to geological records is sporadic and still needs exploring.
Intact molecular isotope ratio mass spectrometry
Conventionally, mass spectrometry, such as Gas Chromatography-Mass Spectrometry(GC-MS ) and Gas Chromatography -Time Of Flight(GC-TOF ), is a common technique for analyzing isotopically labeled molecules.[139][140] This method involves ionizing and analyzing isotopologues of an intact organic molecule of interest rather than its products of piroliz or conversion. However, it does not work for natural abundance hydrogen isotopes because conventional mass spectrometers do not have enough mass-resolving power ölçmek için 13CD isotopologues of intact organic molecules or molecular fragments at natural abundance. For example, to resolve the single D substituted isotopologue peak of any hydrocarbons en azından tek kişiyi dışlayabilmen gerekecek 13Yine de 0,0029 aynı kardinal kütlede oturan C ikameli izotopolog tepe noktası AMU daha hafiftir ve daha büyük miktarlarda daha fazladır.
Analitik cihazlardaki son gelişmeler, organik moleküllerdeki doğal bolluk D / H oranlarının doğrudan ölçülmesini sağlar. Yeni cihazlar, herhangi bir geleneksel gaz kaynağıyla aynı çerçeveye sahiptir IRMS, ancak daha büyük manyetik sektör, çift odaklama sektörleri, dört kutuplu kütle filtresi ve çoklu toplayıcılar gibi yeni özellikler içerir. İki ticari örnek Nu Panorama'dır[141] ve Thermo Scientific 253 Ultra.[142] Bu enstrümanlar genellikle iyi hassasiyet ve hassasiyete sahiptir. Yalnızca onlarca nanomol metan kullanan Ultra, δD'de yaklaşık 0,1 ‰ hata gibi sabit yüksek hassasiyete ulaşabilir.[143] Bu tür ölçümlerin ilk örneklerinden biri metanın kümelenmiş izotoplarıdır. (Fosil yakıtlarda "doğal gaz" bölümüne bakın) Bu tür aletlerin bir diğer gücü, sahaya özgü izotopik oran ölçümleri yapabilme kabiliyetidir. Bu teknik, parçaların D / H oranlarının ölçülmesine dayanmaktadır. iyon kaynağı (ör. CH3CH+
2 (propan molekülü) molekülün farklı bölümlerinden hidrojen atomlarını örnekleyen.[144]
Özet olarak, doğrudan moleküler kütle spektrometrisi, laboratuar çivili izotop izleyicileri ölçmek için yaygın olarak kullanılmıştır. Son zamanlarda geliştirilen yüksek çözünürlüklü gaz kaynağı izotop oranı kütle spektrometreleri, organik moleküllerin hidrojen izotoplarını doğrudan ölçebilir. Bu kütle spektrometreleri, yüksek hassasiyet ve yüksek hassasiyet sağlayabilir. Bu tür aletlerin dezavantajı yüksek maliyet ve standardizasyon zorluğunu içerir. Ayrıca, kütle spektrometresi ile sahaya özgü izotopları çalışmak daha az basittir ve SNIF-NMR yönteminden daha fazla kısıtlamaya ihtiyaç duyar ve yalnızca ayırt edebilir izotopologlar Ama değil izotopomerler.
Hidrolojik döngü
Hidrolojik döngüde izotop fraksiyonasyonu

Su tüm canlı organizmalar için birincil hidrojen kaynağıdır, bu nedenle çevresel suyun izotopik bileşimi, biyosferinki üzerinde birinci dereceden bir kontroldür. hidrolojik döngü Suyu, yeryüzündeki farklı rezervuarların etrafında hareket ettirir, bu sırada sudaki hidrojen izotopları önemli ölçüde bölünür.[145] Atmosfere birincil nem kaynağı olarak okyanus, 0 0 (VSMOW) civarında dünya genelinde nispeten tekdüze bir hidrojen izotop bileşimine sahiptir.[146] Okyanusta 10'dan büyük largerD varyasyonları genellikle buharlaşma, deniz buzu oluşumu ve yağış, nehirler veya buzdağları ile meteorik suların eklenmesi nedeniyle yüzey sularıyla sınırlıdır.[145] Hidrolojik döngüde, hidrojen izotoplarını okyanus suyundan ayıran iki ana süreç şunlardır: buharlaşma ve yoğunlaşma. Oksijen izotopik bileşiminin (18Ö/16O) su da hidrolojik döngüde önemli bir izleyicidir ve su ile ilişkili izotop fraksiyonlama süreçlerinden bahsettiğimizde hidrojen izotoplarından ayrılamaz.
Suyun okyanustan atmosfere buharlaşması sırasında, ortaya çıkan su buharının hidrojen ve oksijen izotopik bileşimini belirlemek için hem denge hem de kinetik izotop etkileri meydana gelir. Su-hava arayüzünde, durgun bir sınır tabakası su buharı ile doyurulur (% 100 bağıl nem ) ve sınır tabakasındaki su buharının izotopik bileşimi, sıvı su ile bir denge fraksiyonasyonunu yansıtır. Hidrojen ve oksijen izotopları için sıvı buhar denge fraksiyonları sıcaklığa bağlıdır:[147]
(‰)
(‰)
Hidrojen izotopları için sıvı-buhar denge fraksiyonasyonunun büyüklüğü, iki izotop sisteminin bağıl kütle farklarını yansıtan, toprak yüzey sıcaklıklarındaki oksijen izotoplarının yaklaşık 8 katıdır (2H% 100 daha ağırdır 1H, 18O,% 12,5 daha ağırdır. 16Ö). Sınır tabakasının üzerinde, bağıl nemi% 100'den az olan bir geçiş bölgesi vardır ve sınır tabakasından geçiş bölgesine su buharı difüzyonu ile ilişkili bir kinetik izotop fraksiyonasyonu vardır ve bu, deneysel olarak bağıl nem (h) ile ilgilidir. :[148]
‰
‰
Difüzyonla ilişkili kinetik izotop etkisi, ağır izotop ikame edilmiş su moleküllerinin (HD16O ve H18
2O) normal izotopoloğa göre (H16
2Ö).
Su atmosfere buharlaştırıldıktan sonra taşınarak yoğuşma ve çökelme yoluyla yüzeye geri döndürülür. Su buharının yoğunlaşması, daha düşük bir sıcaklık ve doymuş buhar basıncı geliştiren yükselen hava kütlelerinde meydana gelir. Soğutma ve yoğuşma nispeten yavaş hızlarda gerçekleştiği için denge izotop etkisi olan bir süreçtir. Bununla birlikte, nem taşınması sırasında su buharı aşamalı olarak yoğunlaştığı ve havadan kaybolduğu için, kalan buharın izotopik bileşimi ve ortaya çıkan çökelme, işlem nedeniyle büyük ölçüde tükenebilir. Rayleigh damıtma. Rayleigh damıtma denklemi şöyledir:[149]

Denklemde, R0 ilk su buharındaki izotop oranını temsil eder, Rr bir miktar yoğunlaşmadan sonra kalan su buharındaki izotop oranını, f havada kalan su buharının fraksiyonu ve α sıvı-buhar denge fraksiyonlama faktörüdür (α = 1 + ε). Ortaya çıkan çökeltinin izotopik bileşimi (Rp) kalan buharın bileşiminden türetilebilir:
F yoğunlaşma sırasında giderek azalırken, kalan buhar ağır izotoplardan gittikçe daha fazla tükenir ve tükenmenin büyüklüğü f sıfıra yaklaştıkça artar. Rayleigh damıtma işlemi, tropiklerden kutuplara izotopik tükenme, kıyıdan iç bölgelere izotopik tükenme ve bir dağ silsilesi üzerinde yükseklik ile izotopik tükenme dahil olmak üzere, yağışların izotopik bileşiminde gözlemlenen bazı birinci dereceden uzaysal kalıpları açıklayabilir. ,[2] bunların tümü nakliye sırasında artan nem kaybı ile ilişkilidir. Rayleigh damıtma modeli, δD ve δ arasındaki güçlü korelasyonu açıklamak için de kullanılabilir.18O, küresel yağışta gözlemlenen küresel meteorik su hattı (GMWL): δD = 8δ18O + 10[150] (daha sonra δD = 8.17 ± 0.07 δ olarak güncellendi18O + 11,27 ± 0,65[41]GMWL'nin eğimi, yoğunlaşma sırasında hidrojen ve oksijen izotop fraksiyonasyonunun nispi büyüklüğünü yansıtır. GMWL'nin kesişme noktası sıfırdan farklıdır (döteryum fazlalığı veya d-fazlalığı olarak adlandırılır), bu da okyanus suyunun GMWL'ye düştüğü anlamına gelir. Bu, su buharı doymuş sınır tabakasından doymamış geçiş bölgesine yayıldığında buharlaşma sırasında kinetik izotop etkisi ile ilişkilidir ve Rayleigh modeli ile açıklanamaz. Bununla birlikte, GMWL'deki sağlam model, tropikal batı Pasifik olan küresel atmosfere güçlü bir şekilde tek bir baskın nem kaynağı önermektedir. Ayrıca, yerel bir meteorik su hattının, farklı yerlerdeki nem ve buharlaşma yoğunluğundaki farklılıklar nedeniyle GMWL'den farklı bir eğime sahip olabileceği ve kesişebileceği belirtilmelidir.[148] Sudaki hidrojen ve oksijen izotopları bu nedenle hem küresel hem de yerel olarak hidrolojik döngünün mükemmel bir izleyicisi olarak hizmet eder.
Su izotopları ve iklim
Hidrolojik döngüde izotopları parçalayan süreçlere dayanarak, meteorik suyun izotopik bileşimi, hava sıcaklığı, yağış miktarı, geçmiş kotlar, göl seviyeleri gibi ilgili çevresel değişkenleri çıkarmak ve nem kaynaklarını izlemek için kullanılabilir. Bu çalışmalar izotop hidrolojisi alanını oluşturur. İzotop hidroloji uygulamalarının örnekleri aşağıdakileri içerir:
Sıcaklık rekonstrüksiyonu
Yağışın izotopik bileşimi, Rayleigh sürecine bağlı olarak hava sıcaklığındaki değişiklikleri anlamak için kullanılabilir. Daha düşük sıcaklık, daha düşük doyma buhar basıncına karşılık gelir, bu da artık buharı izotop tükenmesine doğru yönlendiren daha fazla yoğunlaşmaya yol açar. Ortaya çıkan yağış bu nedenle daha negatif bir δD ve δ'ye sahiptir.18Daha düşük sıcaklıkta O değeri. Bu çökelme izotop termometresi, düşük sıcaklıklarda daha hassastır ve yüksek enlemlerde yaygın olarak uygulanır. Örneğin, δD ve δ18O'nun Antarktik karda 8 ‰ / ° C ve 0,9 ‰ / ° C sıcaklık hassasiyetine ve Arktik bölgelerinde 5,6 ‰ / ° C ve 0,69 ‰ / ° C hassasiyete sahip olduğu bulundu.[151] δD ve δ18Grönland, Antarktika ve dağ buzullarındaki buz çekirdeklerinin O, jeolojik geçmişte sıcaklık değişiminin önemli arşivleridir.
Yağış miktarı etkisi
Yüksek enlemlerde sıcaklık kontrolünün aksine, tropik bölgelerdeki yağışların izotopik bileşimi esas olarak yağış miktarından (negatif korelasyon) etkilenir. Bu "miktar etkisi", subtropiklerde yaz yağışlarında da gözlenmektedir.[41][151] "Miktar etkisi" terimini ilk öneren Willi Dansgaard, korelasyon için birkaç olası neden öne sürdü: (1) Soğutma ve yoğunlaşma ilerledikçe, yağış izotopik bileşimi, Rayleigh süreci tarafından entegre bir izotopik tükenmeyi yansıtır; (2) Az miktarda yağışın buharlaşma ve çevredeki nem ile değişimden etkilenmesi daha olasıdır, bu da onu izotopik olarak daha zengin hale getirme eğilimindedir. Düşük enlemlerde, δ için miktar etkisi18O, ada istasyonlarında 100 mm yağış artışı başına yaklaşık -1,6 ‰ ve kıta istasyonlarında 100 mm başına −2,0 ‰ civarındadır.[151] Tropik bölgelerde farklı yerlerde aylık yağışların izotopik bileşimi karşılaştırıldığında miktar etkisinin en belirgin olduğu da kaydedildi.[151] Hidrojen izotopları için de miktar etkisi beklenir, ancak çok fazla kalibrasyon çalışması yoktur. Güneydoğu Asya genelinde, aylık yağış miktarına karşı δD hassasiyeti, yere bağlı olarak −15 ile −25 ‰ / 100 mm arasında değişmektedir.[152] Ilıman bölgelerde, yağışların izotopik bileşimine yazın yağış miktarı hakimdir, ancak kışın sıcaklık tarafından daha fazla kontrol edilir.[151] Miktar etkisi, bölgesel nem kaynaklarındaki değişikliklerle de karmaşık hale gelebilir.[153] Jeolojik geçmişte tropiklerde yağış miktarının yeniden yapılandırılması çoğunlukla δ18O speleothems[154][155] veya biyojenik lipitlerin δD'si,[156][157] her ikisi de çökeltinin izotopik bileşimi için vekiller olarak düşünülmektedir.
Başvurular
İzotop hidrolojisi
Hidrojen ve oksijen izotopları ayrıca göller, nehirler, yeraltı suları ve toprak suyu dahil olmak üzere karasal rezervuarlarda su bütçesi için izleyici görevi görür. Bir göl için, hem göldeki su miktarı hem de suyun izotopik bileşimi, girdiler (yağış, dere ve yer altı suyu girişi) ve çıktılar (buharlaşma, dere ve yer altı suyu çıkışı) arasındaki denge ile belirlenir.[145] Göl suyunun izotopik bileşimi genellikle buharlaşmayı izlemek için kullanılabilir, bu da göl suyunda izotop zenginleşmesine ve ayrıca bir δD-δ18O meteorik su hattından daha sığ olan eğim.[158] Nehir suyunun izotopik bileşimi oldukça değişkendir ve farklı zaman aralıklarında karmaşık kaynaklara sahiptir, ancak genellikle iki uçlu bir karıştırma problemi, bir taban akış uç elemanı (esas olarak yer altı suyu yeniden doldurma) ve bir karadan akış uç elemanı (çoğunlukla fırtına) olarak değerlendirilebilir. Etkinlikler). İzotop verileri, uzun vadeli entegre temel akış uç elemanının, yazın en yüksek akışlarda bile çoğu nehirde daha önemli olduğunu göstermektedir.[145] Sistematik nehir izotop verileri, Dünya çapında Nehirlerdeki Küresel İzotop Ağı (GNIR) tarafından toplanmıştır.[3] Yeraltı suyunun izotopik bileşimi, kaynaklarını ve akış yollarını izlemek için de kullanılabilir. Bir örnek, bir yeraltı suyu izotop haritalama çalışmasıdır. Sacramento, İnsan kullanımı için pompalama nedeniyle önemli bir su tablası çökmesi geliştiren yeraltı suyuna ayrı bir izotop bileşimi ile nehir suyunun yanal akışını gösteren California.[159] Aynı çalışma, Kaliforniya'nın Central Valley'deki dev alüvyon akiferine yeniden doldurulan tarımsal suyun izotopik bir sinyalini de gösterdi.[159] Son olarak, toprak suyunun izotopik bileşimi bitkilerin incelenmesi için önemlidir. Su tablasının altında, toprak, belirli bir izotopik bileşime sahip nispeten sabit bir su kaynağına sahiptir. Su tablasının üzerinde, toprak suyunun izotopik bileşimi, yüzeyde maksimuma kadar buharlaşma ile zenginleştirilir. Toprak suyunun izotopik bileşiminin dikey profili, hem sıvı hem de buharlı suyun difüzyonu ile korunur.[160] Toprak suyu ile bitki ksilem suyu δD'nin bir karşılaştırması, bitki köklerinin topraktan su aldığı derinliği anlamak için kullanılabilir.[161]
Paleo-yeniden yapılanma
Buz çekirdeği kayıtları

İzotopik bileşimi Buz çekirdekleri kıtasal buz tabakalarından ve Alp buzullarından 1950'lerden beri sıcaklık vekilleri olarak geliştirilmiştir. Samuel Epstein, Antarktika karda oksijen izotoplarını ölçerek bu vekilin uygulanabilirliğini ilk gösterenlerden biriydi ve ayrıca karın oluştuğu hava kütlelerinin geçmişinin neden olduğu kararlı izotop-sıcaklık korelasyonundaki komplikasyonlara dikkat çekti.[163] Grönland ve Antarktika'daki buz çekirdeklerinin kalınlığı binlerce metre olabilir ve son birkaç buzul-buzullararası döngünün kar izotopik bileşimini kaydedebilir. Buz çekirdekleri, üstte katman sayımı ve derinlikteki buz akışı modellemesi ile, volkanik külden kaynaklanan ek yaş kısıtlamaları ile tarihlenebilir.[164] Grönland ve Antarktika'dan gelen çekirdekler, küresel olarak iyi karışmış iz gazı (örn., CH4) çekirdeklerde hapsolmuş hava kabarcıklarındaki konsantrasyonlar.[165] Grönland ve Antarktika'daki yaş tahminleriyle birlikte ilk buz çekirdeği kayıtlarından bazıları son 100.000 yıl öncesine dayanıyor ve δD ve δ'de bir tükenme gösterdi.18O son buz çağında.[166][167] Buz çekirdeği rekoru Antarktika'da son 800.000 yıla kadar uzatıldı.[168] ve Grönland'da en az 250.000 yıl.[169] En iyi δD tabanlı buz çekirdek sıcaklığı kayıtlarından biri, Antarktika'daki 420.000 yıl öncesine dayanan Vostok buz çekirdeğinden alınmıştır.[162] ΔD sıcaklığı ( ters çevirme Kar oluştuğu katman) Doğu Antarktika'da modern uzaysal gradyan δD (9 ‰ / ° C) dayalı dönüşüm ΔTben= (ΔδDbuz-8Δδ18Ösw) / 9, küresel buz hacmi değişikliklerinin neden olduğu deniz suyu izotopik bileşimindeki değişiklikleri hesaba katar.[162] Birçok yerel etki, sıcaklığa ek olarak buz δD'yi de etkileyebilir. Bu etkiler, daha karmaşık modellerde açıklanabilecek nem kaynağı ve taşıma yolları, buharlaşma koşulları ve yağış mevsimselliğini içerir.[170] Bununla birlikte, Vostok buz çekirdeği kaydı bazı çok önemli sonuçlar göstermektedir: (1) Antarktika'da 8 ° C'lik bir soğumaya karşılık gelen buzullararası zamanlara kıyasla son dört buzul döneminde ~ 70 ‰ tutarlı bir δD tükenmesi; (2) Tutarlı bir atmosferik CO düşüşü2 100 ppmv ve CH ile konsantrasyon4 Buzul dönemlerinde buzullar arası döneme göre ~ 300 ppbv düşüş, küresel iklimi düzenlemede sera gazlarının rolünü düşündürmektedir; (3) Antarktika hava sıcaklığı ve sera gazı konsantrasyonu değişiklikleri, küresel buz hacminden ve Grönland hava sıcaklığı değişimlerinden önce buzul sonlandırmaları sırasında ortaya çıkar ve sera gazları, buzul-buzullararası döngüleri sırasında güneşe maruz kalma zorlamasının bir yükselticisi olabilir.[162] Grönland buz çekirdeği izotop kayıtları, buzul-buzullararası döngüleri göstermenin yanı sıra, buz eritme yüklerinin neden olduğu okyanus sirkülasyonundaki yeniden düzenlemeyi yansıtabilecek bin yıllık ölçekli iklim salınımlarını da gösteriyor.[169][171][172][173] Ayrıca, farklı kıtalardaki dağ buzullarında üretilen buz çekirdeği kayıtları da var. Bir kayıt And dağları Peru'da son buzul çağında tropik bölgelerde 5-6 ° C'lik bir sıcaklık düşüşü görülüyor.[174] Tibet platosundan alınan bir kayıt, son buz çağında benzer bir izotop kayması ve soğumasını gösteriyor.[175] Diğer mevcut dağ buzul izotop kayıtları arasında Tanzanya'daki Kilimanjaro Dağı, Rusya'daki Altay Dağı ve Batı Belukha Platosu, Kanada'daki Logan Dağı, Wyoming'deki Fremont Buzulu ve Bolivya'daki Illimani Buz Çekirdeği yer alır ve bunların çoğu bir aralığı kapsar. Holosen epoch.[4]
Biyomoleküller
İzotopik bileşimler biyomoleküller tortul kayıtta korunan bir vekil paleoenvironment rekonstrüksiyonları için. Su için birincil hidrojen kaynağı olduğu için foto ototroflar Biyokütlenin hidrojen izotop bileşimi, büyüme sularının bileşimi ile ilişkili olabilir ve bu nedenle eski ortamların bazı özelliklerine dair fikir edinmek için kullanılabilir.[176] Hidrojen, diğer kararlı izotop sistemlerinden daha doğrudan iklimle ilişkili olduğu için, hidrojen izotoplarının incelenmesi çok değerli olabilir. Bununla birlikte, oksijen, nitrojen veya sülfür atomlarına bağlı hidrojen atomları çevresel hidrojen ile değiştirilebilir, bu da bu sistemi daha az basit hale getirir.[177] [önceki H değişimi bölümüne ref]. Biyomoleküllerin hidrojen izotop bileşimini incelemek için, hidrojenin büyük ölçüde karbona bağlı olduğu ve bu nedenle deneysel zaman ölçeklerinde değiştirilemeyen bileşiklerin kullanılması tercih edilir. Bu kriterlere göre, lipidler hidrojen izotop çalışmaları için şeker veya amino asitlerden çok daha iyi bir konudur.
Kaynak su ve lipitler arasındaki net fraksiyonlama, ε olarak belirtilir.l / wve şu şekilde temsil edilebilir:
nerede w suyu ifade eder ve l lipitleri ifade eder.
Kaynak suyun δD'si lipidlerin δD'si üzerindeki en büyük etkiyken,[178] Eğimden ve regresyonun kesişmesinden elde edilen fraksiyonlama faktörü değerleri arasındaki tutarsızlıklar, ilişkinin iki havuzlu fraksiyonlamadan daha karmaşık olduğunu göstermektedir.[179] Başka bir deyişle, lipitlerin izotopik bileşiminin anlaşılmasında dikkate alınması gereken çok sayıda fraksiyonlama adımı vardır.
Selüloz
Karbona bağlı hidrojen izotopik bileşimi selüloz yaprak sudan miras alındığı şekliyle, orijinal meteorik su sinyalini koruma potansiyeline sahiptir. Bu ilk olarak 1970'lerde gösterildi.[25][180] Kuzey Amerika'da yapılan sistematik bir araştırmada ağaç selülozu δD'nin 5,6 / ° C yağış δD hassasiyetine benzer şekilde 5,8 ‰ / ° C sıcaklık hassasiyetine sahip olduğu bulunmuştur.[181] Bu mekansal korelasyon, toprak buharlaşması ve yaprak terlemesinin yerel etkileri nedeniyle karmaşık hale gelebilir.[181] ve uzaysal gradyan, tek bir yerde ağaç halkalı selülozdaki zamansal değişiklikleri temsil etmeyebilir. Meteorik sudan selülozda δD sinyalini oluşturan mekanizma tam olarak anlaşılmamıştır, ancak en azından yaprak suyu terlemesini, karbonhidratların sentezini, fotosentetik şekerlerden selüloz sentezini ve ksilem suyu ile şeker alışverişini içerir.[182] Modelleme çalışmaları, gözlenen ağaç halkası selüloz δD'nin şekerlerdeki hidrojenin% 36'sı ksilem suyu ile değiştiğinde üretilebildiğini ve nem ve yağış mevsimselliği gibi etkilerin selüloz δD vekilini karmaşıklaştırabileceğini göstermektedir.[182] Bu komplikasyonlara rağmen, ağaç halkası δD, son birkaç bin yılın paleoiklim rekonstrüksiyonları için kullanılmıştır. Örneğin, bir ağaç halkası selüloz δD, bölgedeki çam ağaçlarından Beyaz Dağlar California, 6800 yıldan günümüze 50 azalma gösteriyor. Holosen ortasındaki termal maksimumdan bu yana soğuma eğilimi, buz çekirdeği ve polen kayıtları ile tutarlıdır, ancak buna karşılık gelen soğutma büyüklüğü, nem ve toprak suyu bileşimi gibi yerel etkilerden kaynaklanan karmaşık etkiler nedeniyle belirsizdir.[183] Selülozdaki izotopların anlamı ve uygulamaları hala aktif bir çalışma alanıdır.
Bitki yaprak mumları

Karasal bitkiler yapmak yaprak mumlar su kaybını en aza indirmek için yaprak yüzeylerini bir adaptasyon olarak kaplamak. Bu mumlar büyük ölçüde düz zincirli n-alkil lipitler. Çözünmez, uçucu değildir, kimyasal olarak inerttir ve bozunmaya karşı dirençlidir, bu da onları tortul kayıtta kolayca korunmasını sağlar ve bu nedenle, biyobelirteçler.[184]
Karasal bitkiler için ana su kaynağı, büyük ölçüde yağmur suyunun hidrojen izotop bileşimine benzeyen, ancak ortamlar arasında ve zenginleştirme ile değişen toprak suyudur. yağış tarafından tükenme buharlaşma ve atmosferik su buharı ile değiştirin. Kaynak suyun δD değeri ile lipit biyosentezi sahasında yaprak suyunun δD değeri arasında önemli bir sapma olabilir. Kökler tarafından su alımı ile hiçbir fraksiyonlama ilişkilendirilmez, bu işlem, genellikle kılcal gerilim tarafından yönlendirilir. kserofitler aşırı kurak ortamlarda (kabaca 10 tükenme ile) su pompalamak için ATP yakan.[185] Bununla birlikte, yaprak suyu, toprak suyuna göre önemli ölçüde zenginleştirilebilir. terleme sıcaklık, nem ve çevreleyen su buharının bileşiminden etkilenen bir buharlaşma süreci. Yaprak su hidrojen izotop bileşimi, değiştirilmiş bir Craig-Gordon modeli ile tanımlanabilir,[186] nerede ΔDe yaprak suyunun kararlı hal zenginleştirmesidir, εeq sıvı su ve buhar arasındaki sıcaklığa bağlı denge fraksiyonudur, εk yaprak iç hava boşluğu ile atmosfer arasındaki difüzyondan kaynaklanan kinetik izotop etkisidir, ΔDv yaprak / hava dengesizliği, ea atmosferik buhar basıncıdır ve eben iç yaprak buhar basıncıdır.
Péclet Yönlendirme ve difüzyonun karşıt güçlerini tanımlayan etki, modele şu şekilde eklenebilir:
burada E, terleme hızıdır, L, taşınmanın uzunluk ölçeğidir, C, su konsantrasyonudur ve D, difüzyon katsayısıdır.
Yağmursuyu δD'nin lipitlerin nihai δD'si üzerinde temel kontrol olarak rolü iyi belgelenmiş olsa da,[187] yağmur suyundan toprak suyuna ve yaprak suyuna fraksiyonasyon etkilerinin ε üzerindeki önemil / w takdir ediliyor, ancak tam olarak anlaşılamıyor.[176][188]
Organik biyomoleküller genellikle yaprak suyunun δD'sine göre tükenmiştir.[176] Bununla birlikte, organizmalar, biyosentetik yollar ve farklı moleküllerin biyolojik rolleri arasındaki farklılıklar, fraksiyonlamada büyük değişkenliğe yol açabilir; lipit biyobelirteçlerinin çeşitliliği 600 aralığı δD değerlerini kapsar.[189] Lipid biyosentez biyokimyasal olarak karmaşıktır ve izotop fraksiyonlarına yol açabilen birden fazla enzime bağlı aşamaları içerir. Lipid biyosentezinin üç ana yolu vardır. mevalonat yolu, asetojenik yol, ve 1-deoksiD-ksilüloz-5-fosfat / 2-metileritroil-4-fosfat yolu.[190] Asetojenik yol, üretiminden sorumludur. n-alkil lipitleri yaprak mumları gibi ve diğer iki lipit biyosentez yoluna göre kaynak suya göre daha küçük bir AD tükenmesi ile ilişkilidir.[32][191] Yaprak su, yaprak biyomoleküllerinde ana hidrojen kaynağı iken, asetat veya NADPH'den nispeten tükenmiş hidrojen, biyosentez sırasında sıklıkla eklenir ve son molekülün hidrojen bileşimine katkıda bulunur. İkincil hidrojen değişim reaksiyonları, yani birincil biyosentetik yolun dışındaki hidrojenasyon ve dehidrojenasyon reaksiyonları, lipid hidrojen izotop bileşiminin değişkenliğine de önemli ölçüde katkıda bulunur.[192]
Fraksiyonlamadaki biyolojik farklılıkların yalnızca farklı moleküller arasındaki biyokimyasal farklılıklardan değil, aynı zamanda farklı organizmalar arasındaki fizyolojik farklılıklardan da kaynaklandığına dikkat etmek önemlidir. Örneğin, çok yapraklı balmumu moleküllerinin δD değerleri, ağaçlara (medyan ~ -135 ‰) göre çalılar (ortanca ~ -90 ‰) bakımından zenginleştirilmiştir, bunlar her ikisine göre de zenginleştirilmiştir. C3 (medyan ~ -160 ‰) ve C4 otlar (medyan ~ -140 ‰).[176] Bireysel türler arasında, δD değerlerinin önemli farklılıkları belgelenmiştir.[193][194][195][196] Değişken yaprak balmumu δD değerlerine katkıda bulunan diğer fizyolojik faktörler, yaprak gelişiminin mevsimsel zamanlamasını,[197] dış strese veya çevresel değişkenliğe tepki,[198] ve stoma varlığı veya yokluğu[187]
Pek çok fizyolojik adaptasyon doğrudan çevre ile ilişkili olduğunda, fizyolojik faktörler ile çevresel faktörler arasında ayrım yapmak zor olabilir.
Kaynak suyun δD'si üzerindeki çevresel etkilere ek olarak, çeşitli çevresel faktörlerin yaprak balmumu δD değişkenliğine katkıda bulunduğu gösterilmiştir. Nemin, orta nem seviyelerinde lipid levelsD değerlerini etkilediği bilinmektedir, ancak özellikle yüksek (>% 80) veya düşük (<% 40) nem seviyelerinde değildir ve geniş bir zenginleştirilmiş valuesD değerleri eğilimi, daha küçük anlamındadır εl / wkurak bölgelerde görülür.[176][178][193] Coğrafi enlem ile ilişkili olan sıcaklık ve güneş ışığı yoğunluğu, metabolizma ve terleme hızları üzerinde güçlü etkilere sahiptir ve εl / w.[199] Ek olarak, yaprak balmumu moleküllerinin ortalama zincir uzunluğu coğrafi enlem ile değişir ve εl / w artan zincir uzunluğu ile arttığı gösterilmiştir[187]
Biyobelirteçleri antik çevreleri yeniden inşa etmek için bir vekil olarak kullanırken, tortul kayıtların doğasında bulunan önyargıların farkında olmak önemlidir. Çökeltiye katılan yaprak maddesi büyük ölçüde sonbaharda birikir, bu nedenle yaprak mumlarındaki mevsimsel değişiklikler buna göre dikkate alınmalıdır.[187] Ayrıca, çökeltiler, hem uzay hem de zamanda birçok farklı bitki üzerindeki yaprak mumlarını ortalayarak üzerindeki biyolojik kısıtlamaları kalibre etmeyi zorlaştırır.l / w.[176] Son olarak, jeolojik kayıttaki biyomoleküllerin korunması, tüm ekosistemleri tam anlamıyla temsil etmez ve özellikle çökeltiler yüksek sıcaklıklara maruz kalıyorsa, her zaman hidrojen değişimi tehdidi vardır.
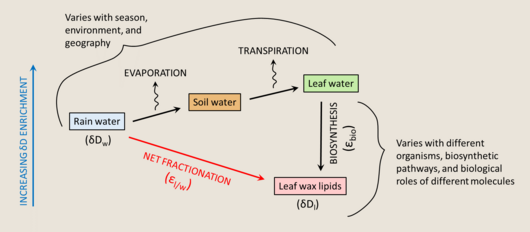
Yaprak mumlarının hidrojen izotop bileşimi, üç ana fraksiyonasyon adımı olan yağmur suyunun δD'si olarak özetlenebilir - toprak suyundan buharlaşma, yaprak suyundan terleme ve net fraksiyonlama olarak birleştirilip ölçülebilen lipit biyosentezi veya εl / w.[176] Tek moleküller için sürekli gelişen ölçüm tekniklerinin uygulanması ve bazı değişkenleri sınırlandırmaya yardımcı olabilecek jeolojik kayıttaki diğer bağımsız temsilcilerle korelasyonla, yaprak mumlarının hidrojen izotop bileşiminin araştırılması son derece verimli olabilir. Yaprak balmumu δD verileri, okyanus sirkülasyonunun ve yüzey sıcaklığının kıtasal yağış üzerinde önemli bir etkiye sahip olduğunu göstererek, karasal hidrolojideki iklim kaynaklı değişiklikleri daha iyi anlamak için başarıyla uygulandı.[200][201] Yaprak balmumu δD değerleri, irtifanın yağmur suyu δD üzerindeki etkisine dayalı olarak eski dağ sıralarındaki yükseklik gradyanlarını yeniden yapılandırmak için paleoaltimetri kayıtları olarak da kullanılmıştır.[202][203]
Alkenonlar

Paleor yapılarda sıklıkla kullanılan bir başka molekül grubu, alkenonlar, uzun zincirli büyük ölçüde doymamış lipidler, yalnızca kokolitoforlar. Kokolitoforlar denizdir haptofit algler ve küresel olarak ikonik türleri içerir Emiliania huxleyi ana olanlardan biri CaCO3 okyanustaki üreticiler. Alkenonların δD değerleri, deniz suyunun δD değerleri ile oldukça ilişkilidir ve bu nedenle deniz suyunun izotopik bileşimini sınırlayan paleo-çevresel özellikleri yeniden yapılandırmak için kullanılabilir. Alkenon δD değerlerinin uygulandığı en kayda değer rekonstrüksiyon, tuzluluk eski okyanusların.

Hem deniz suyunun δD değerleri hem de hiptofit biyokimyası ile ilişkili fraksiyonlar (εbiyo) oldukça iyi anlaşıldığından, alkenonlar tuzluluğun δD üzerindeki ikincil etkisini gözlemlemek için kolayca kullanılabilir.[204] Tuzluluk ve ε arasında iyi kurulmuş pozitif doğrusal bir korelasyon vardır.l / wtuzluluk birimi başına fraksiyonlamada ~ 3 ‰ değişim mertebesinde.[205] Bu etki için varsayılmış mekanizmalar, yüksek tuzlulukta hücre dışı su ile azalmış değişim nedeniyle hücre içi suda D'nin zenginleştirilmesini içerir.[206] Ozmotik basıncı daha yüksek tuzlulukta korumak için artan çözünen üretimine bağlı olarak H'nin hücre içi sudan uzaklaştırılması,[207] ve daha yüksek tuzlulukta daha düşük haptofit büyüme oranları[176]
Alkenon δD değerleri, Akdeniz'deki geçmiş tuzluluk değişikliklerini yeniden yapılandırmak için başarıyla kullanılmıştır.,[208] Kara Deniz,[209][210] Panama Havzası,[211] ve Mozambik Kanalı.[204] Tuzluluğun bir uzantısı olarak, bu veriler aynı zamanda eski tatlı su sel olayları gibi antik çevreler hakkında daha fazla sonuç çıkarmak için de kullanıldı.[208][209] ve çevresel değişikliklere yanıt olarak planktonun evrimi[210]
Kararlı izotop paleoaltimetri
Paleoaltimetriyi yeniden yapılandırmak için su izotop tükenmesi kullanma olasılığı, 1960'ların sonlarında, Caltech jeokimyacı Samuel Epstein tek bir fırtınada farklı yüksekliklerde yağmur suyu toplamaya çalıştı.[212] Δ18O ve δD atlama oranları sırasıyla -1 ila -5 ‰ / km ve -10 ila -40 ‰ / km arasında değişir, ancak konumlara ve mevsimlere göre değişebilir ve rakımla tam olarak doğrusal değildir.[213][214][215] Kararlı izotop paleoaltimetrisindeki ilk çalışmalardan biri, sıvı kapanımlarında -90 ila -139 ‰ arasında bir meteorik su δD imzası göstermiştir. kuvars ve adularia Nevada'da bir epitermal altın-gümüş yatağında ve kararlı izotopların eski topografyanın yeniden inşasında uygulanabilirliğini önerdi. Büyük Havza.[216] Sulu silikat minerallerinin hidrojen ve oksijen izotopları, o zamandan beri, Kuzey Amerika Cordillera, Rocky Dağları, Himalayalar, Avrupa Alpleri ve Yeni Zelanda'daki Güney Alpleri de dahil olmak üzere, dünyanın dört bir yanındaki dağlık alanlardaki topografik geçmişleri yeniden yapılandırmak için kullanıldı.[212] Kil mineralleri ile yapılan laboratuar deneyleri, hidrojen ve oksijen izotop bileşimlerinin, orta sıcaklıkta (<100 ° C) değişime nispeten dirençli olduğunu ve orijinal meteorik su sinyalini koruyabildiğini göstermiştir.[217] Dağ sıralarının sabit yağış izotopları üzerindeki önemli bir etkisi, rüzgar tarafına kıyasla rüzgar altı tarafında yağışta izotopik bir azalmanın meydana geldiği yağmur gölgesi etkisidir. Bir dağın iki tarafındaki izotopik yağış bileşimindeki farklılık, yağmur gölgesi etkisinin büyüklüğünü anlamak için kullanılabilir.[212] Böyle bir çalışmada, simektitin doğu tarafında izotop zenginleşmesi gözlenmiştir. Sierra Nevada California'da ortasındanMiyosen geç Pliyosen, bu dönemde yükseklikte bir düşüş olduğunu düşündürmektedir.[218] Başka bir çalışmada, erken dönemde Kuzey Amerika Cordillera'daki muskovitte -140 ‰ civarında δD değerleri bulundu. Eosen, bu da bugünkünden 1000 m daha yüksek bir rakım olduğunu gösterir.[219] Sulu minerallere ek olarak, paleoaltimetri çalışmaları için yaprak mumları gibi biyobelirteçlerdeki hidrojen izotopları da geliştirilmiştir. The δD lapse rate in leaf waxes (-21‰/km) falls in the range of meteoric water observations.[215][220] As an example study, leaf wax δD data have been used to confirm hydrous mineral paleoaltimetry for the high elevation of the Sierra Nevada during the Eocene.[203]
Fosil yakıtlar
The hydrogen isotope composition of sıvı yağ, gaz ve kömür is an important geochemical tool to study the formation, storage, migration and many other processes. The hydrogen isotopic signal of fossil fuels results from both inheritance of source material and water as well as fractionations during hidrokarbon generation and subsequent alteration by processes such as isotopic exchange or biyolojik bozunma. When interpreting hydrogen isotopic data of sedimentary organic matter one must take all the processes that might have an isotope effect into consideration.
Almost all of the organic hydrogen is exchangeable to some extent. Isotopic exchange of organic hydrogen will reorder the distribution of döteryum and often incorporate external hydrogen. Generally, more mature materials are more substantially exchanged. With effective exchange, aliphatic hydrogen can finally reach isotopic equilibrium at the final stage. Equilibrium fractionation factor varies among different hydrogen sites. For example, aliphatic hydrogen isotope fractionation depends on the carbon atom that the hydrogen atom bonds with. To the first order, alkyl hydrogen isotope composition follows this trend: δDPrimary carbon < δDSecondary carbon < δDTertiary carbon.[221] The fractionation factors between carbon sites also decrease with increasing temperature. This can be potentially used as a thermo-history indicator.[144] The fractionation between whole molecule and water can be estimated by averaging all hydrogen-positions, and this leads to a relatively small variation of equilibrium fractionation between different groups of hydrocarbons ve su. A theoretical prediction estimated this to be −80‰ to −95‰ for steranlar, −90‰ to −95‰ for hopanlar, and −70‰ to −95‰ for typical cycloparaffins between 0 °C to 100 °C.[222] At the temperature of the oil window and gas window, the equilibrium fractionation between different group of organic molecules is relatively small, as compared with large primary signals.
The study of hydrogen isotopes of fossil fuels has been applied as proxies and tools in the following aspects:
- Yeniden yapılanma paleoenvironments of the sources. Because of the high-sensitivity of D content of terrestrial water to hydrological cycles, organic δD can reflect the environment of source formation. To the first order, D/H ratios of coals and n-alkanes from oils have been demonstrated to correlate with solgunluk.
- Source correlation. Marine and göl environments are characterized by distinctly different δD values. Many studies have tried to relate measured δD with source types. For methane, D concentration and clumped isotopes is particularly diagnostic of sources.
- Possible maturity indicators. For example, isoprenoids synthesized by plants are strongly depleted in D(See "Observed variations in isotopic abundance" section), typically ~100‰ to n-alkyl lipids.[223] This gap tends to decrease as rock matures because of the higher D/H exchange rates of isoprenoids. The correlation of δD difference between pristane, phytane and n-alkanes and other maturity indicators has been established across a wide maturity range.[224][225] Another possible maturity indicator based on the "isotope slope" of δD vs. n-alkane chain length was proposed by Tang et al.[226]
- Quantitative apportionment. Dan beri Alkanlar are main components of oil and gas, the isotopic data of n-alkanes have been used to study their migration and mixing. The advantage of hydrogen isotopes over carbon is higher resolution because of larger fractionation. Studying the clumped isotopes of methane provides a new dimension of mixing-constraints. The mixing line in the clumped isotope notation space is a curve rather than a straight line.
- Parmak izi pollutant /oil spills.
Kerojenler ve kömürler
The first stage that sedimentary organic matter (SOM) experiences after ifade dır-dir diagenesis. During diagenesis, biological decomposition can alter the D/H ratio of organics. Several experimental studies have shown that some biodegraded materials become slightly enriched in D(less than 50‰). Most organics become kerojen by the end of diagenesis. Generally, δD of kerojen spans a wide range. Many factors contribute to the kerogen we observe in geological records, including:
- Source water hydrogen isotope patterns: for example, lake systems are more sensitive to hydrological cycles than marine environments.
- Differential fractionation for various organisms and metabolic pathways: differences in organic composition can also reflect in primary signal.
- Isotopic exchange, H loss and H addition: this can involve mixing water-derived D with the primary signal.
- Nesil bitumen, oil and gas: there's a fractionation between the product and kerogen.
Research on the Australian basins showed that δD of lacustrine algal sourced kerogen with terrestrial contributions varies from −105‰ to −200‰, and δD of kerogen from near-coastal depositional environment has a narrower range from −75‰ to −120‰.[227] The smaller span in D/H ratios of coastal kerogen is thought to reflect the relatively stable regional climate. Pedentchouk and his colleagues reported δD values of -70‰ to -120‰ in immature to low mature kerogen from early Cretaceous lacustrine sediments in West Africa.[224]
Coals are from type III kerogen mostly derived from terrestrial plants, which should have a primary D/H signal sensitive to local meteoric water. Reddings et al. analyzed coals from various origins and found them randomly scatter across the range of −90‰ to −170‰.[228] Rigby et al. found D contents decrease from -70‰ to -100‰ with increasing maturity in coal from Bass Basin and attributed this to latter exchange with low D water.[229] Smith et al. studied H isotopes of coal samples from Antarctica and Australia. They found a strong negative correlation between δD and inferred paleolatitude. For coal samples originating from near equatorial regions, δD is around −50‰, while for those originating from polar regions, δD is around −150‰.[230] This δD trend along latitude is consistent meteoric water trend and thus is an evidence that coals can preserve much of the original signals.
There are two types of approach to study the alteration of D/H ratios of kerogen during catagenesis: 1)laboratory incubation of organic matter that enables mechanistic study with controlled experiments. 2)natural sample measurement that provides information of combined effects over geological timescales. The complex composition and chemistry of kerogen complicates the results. Nevertheless, most research on hydrogen isotopes of kerogen show D enrichment with increasing maturity. Type II kerogen(marine derived) from New Albany Shale is reported to have δD rise from −120‰ to −70‰ as vitrinite reflectance increase from 0.3% to 1.5%.[231] Two main mechanisms have been proposed for enrichment. One of them is kinetic fractionation during hydrocarbon generation while the other is isotopic exchange with surrounding water. Anhydrous incubation experiments have shown that the products are generally more depleted in D than their precursors, causing enrichment in residual kerogen. Schimmelmann et al. studied the relationship between terrestrially-derived oil and their source rock kerogens from four Australian Basins. They found that on average the oil is depleted to corresponding kerogen by 23‰.[227] Hydrous incubation experiments suggest that 36–79% of bulk organic hydrogen may come from water at moderate maturity. While still under debate, it appears likely that incorporation of water hydrogen isotopes is the more dominant process for kerogen D- enrichment during catagenesis.[46]
In summary, D content of kerogen and coals are complicated and hard to resolve due to the complex chemistry. Nevertheless, studies have found the possible correlation between coal δD and paleo-latitude.
Doğal gaz
Commonly, hydrogen isotope composition of natural gas from the same well has a trend of δDmetan<δDetan<δDpropane<δDC4+. This is because most natural gas is thought to generated by step-wise termal kırma that is mostly irreversible and thus governed by normal kinetik izotop etkileri that favor light isotopes. The same trend, known as "the normal order",[232] holds for carbon isotopes of natural gas. For example, Angola gas is reported to have a methane δD range of −190‰ to −140‰, an ethane δD of −146‰ to −107‰, a propane δD of −116‰ to −90‰, and a butane δD of −118‰ to −85‰.[233] However, some recent studies show that opposite patterns could also exist, meaning δDmetan>δDetan>δDpropane. This phenomenon is often referred to as 'isotopic reversal' or 'isotopic rollover'. The isotopic order could also be partially reversed, like δDmetan>δDetan<δDpropane or δDmetan<δDetan>δDpropane.[232] Burruss et al. found that in the deepest samples of northern Appalachian basin the hydrogen isotopic order for methane and ethane is reversed.[234] Liu et al., also found partial reversal in oil-related gas from the Tarim Basin.[232] The mechanism causing this reversal is still unknown. Possible explanations include mixing between gases of different maturities and sources, oxidation of methane, etc. Jon Telling et al., synthesized isotopically reversed (in both C and H) low-molecular Alkanlar using gas-phase radical recombination reactions in Elektrik boşalması experiments, providing another possible mechanism.[235]
Metan is a major component of natural gas. Geosphere methane is intriguing for the large input of microbial metanojenez. This process exhibits a strong isotope effect, resulting in greater D-depletion in methane relative to other hydrocarbons. δD ranges from −275‰ to −100‰ in thermogenic methane, and from −400‰ to −150‰ in microbial methane.[98] Also, methane formed by marine methanogens is generally enriched in D relative to methane from freshwater metanojenler. δD of methane has been plotted together with other geochemical tools(like δ13C, gas wetness) to categorize and identify natural gas. A δD-δ13C diagram (sometimes referred to as CD diagram, Whiticar diagram, or Schoell diagram ) is widely used to place methane in one of the three distinct groups: thermogenic methane that is higher in both δ13C and δD; marine microbial methane that is more depleted in 13C and freshwater microbial methane that is more depleted in D. Hydrogenotrophic methanogenesis produces less D-depleted methane relative to acetoclastic methanogenesis. The location where the organism lives and substrate concentration also affect isotopic composition: rumen methanogenesis, which occurs in a more closed system and with higher partial pressures of hydrogen, exhibits a greater fractionation (−300 to −400‰) than wetland methanogenesis (−250 to −170‰).[236][237]
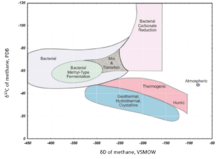
Recent advances in analytical chemistry have enabled high-precision measurements of multiply substituted izotopologlar (or 'clumped isotopologues') like 13CH3D. This emerge as a novel tool for studying methane formation. This proxy is based on the abundance of clumped isotopologues of methane, which should be enriched compared to the stochastic distribution at thermodynamic equilibrium because the reduced zero-point energy for heavy-heavy isotope bonding is more than twice the reduced zero-point energy of heavy-light isotope bonding.[238] The extent of enrichment decreases with increasing temperature, as higher entropi tends to randomize isotope distribution. Stolper et al. established this temperature calibration using laboratory equilibrated methane and field methane from known formation temperature, and applied this to several gas reservoirs to study natural gas formation and mixing.[239] Wang vd. also reported strong non-equilibrium isotope effect in methane clumped isotopes from lab-cultured methanogens and field samples.[240] These methane samples have relatively low abundance of clumped isotopologues, sometimes even lower than the stochastic distribution. This indicates that there are irreversible steps in enzymatic reactions during methanogenesis[240] that fractionation against clumped isotopologues to create the depleted signal. Isotope clumping in methane has proven a robust proxy, and scientists are now moving towards higher-order alkan molecules like ethane for further work.[241]
Sıvı yağ
Oil is generally a product of thermal breakdown of type I and type II kerojen sırasında katajenez. The deuterium content should reflect the source kerogen signal, generation fractionation, isotopic exchange and other maturation effects. The thermal maturation at the oil window can erase much of the primary signals of hydrogen isotopes. The formation of oil involves breaking C-C and C-H bonds, resulting in depletion of 13C and D in the products and enrichment in the residual reactants due to kinetik izotop etkileri. Yongchun Tang and his colleagues modeled this process based on laboratory-calibrated kinetics data and found that the frequency factor ratio for D/H is 1.07.[242] Moreover, oil is also affected by the isotope fractionation from phase-change. However, the behavior of oil gas-liquid fractionation differs from water as the vapor phase of oil is enriched in D.[51] This will deplete residual oil as it gets evaporated. Biological degradation of oil is also expected to fractionate hydrogen isotopes, as enzymatic breaking of C-H bond have a normal kinetic isotope effect. Several degradation experiments show that this fractionation is generally mild, ranging from −11‰ to −79‰.[51] This process should also enrich partially degraded oil. Finally, oil stored in a reservoir often had migrated through subsurface (also known as "geochromatography") from another source region, interacting with water. No data has been published to confirm the fractionation associated with migration, yet theoretical prediction shows that this is likely to be very small.[51]
Many studies of natural samples have shown slight increases in δD with thermal maturity. Amane Waseda reported δD of oil samples in northeast Japan to increase from around −130‰ to around −110‰ with higher maturity.[243] At low termal olgunluk, dos Santos Neto and Hayes reported δD of saturate fraction of oil in Portiguar Basin derived from a lacustrine environment is -90‰, and from a marine-evaporitic environment is -120‰ to −135‰.[46][88]
The bulk analysis of oil, which yields a complicated mixture of organik bileşikler, obscures much of the valuable information. Switching to compound-specific study greatly expanded our understanding of hydrogen isotopes of oil. Analyzing deuterium content at the compound level avoids problems from differences in exchange rates, simplifies sources and products relationships, and draws a much more detailed picture.[51] δD of n-alkanlar are generally thought to be representative of oil as they are the major components. Schimmelmann et al. confirmed that alkane fractions have almost the same D/H ratios as whole oils.[227] Depending on source material type and maturity, δD of n-alkanes can vary from −100‰ to −180‰. A common phenomenon of various oil and matured rock derived n-alkanes is a trend of increasing δD with chain length. For example, Li et al. analyzed oils from the Western Canada Sedimentary Basin and found δD increased between 20‰ and 40‰ from C13 C'ye27.[244] This "isotope slope" is an artifact of kinetic fractionation associated with thermal cracking of carbon chains. This trend has been experimentally reproduced and theoretically modeled by Tang et al.[226]
N-alkanes are also known to preserve detailed information of source material. Li et al. studied oils from the marine-derived Üst Kretase Second White Speckled Şeyl and found strong depleted signal around −180‰ in C12-C18. The low δD of this marine samples was explained by the discharge of a large high latitude nehir.[244] Schimmelmann et al. found that the δD of the oil sampled from coaly facies of the Crayfish group reaches down to −230‰ where as those sampled from algal facies of the same group are around −100‰. Such huge variation is hard to be explained by any other causes than Australia splitting from the Antarctic continent during late Cretaceous.[51] Another special case reported by xiong et al.[245] studied Ordovician carbonates from Bohai Bay Basin. They found big differences between δD of n-alkanes exists, reflecting that the original signal is preserved rather than being homogenized. The result is not obvious as the sample is very mature(inferred vitrinite reflectance R0 up to 2.3). Thus this is a strong evidence that carbonate systems have much lower katalitik verimlilik of hydrogen exchange on hydrocarbons. Strong enrichment(~40‰) in odd carbon numbered Alkanlar to even carbon numbered alkanes is also found in some subset of samples and the reason is unclear at this point. This odd-even effect is also observed in immature clastic sediments.[246]
Ekohidroloji
Alanı ecohydrology is concerned with the interaction between ecosystems and water cycling, from measuring the small scale drainage of water into soil to tracking the broad movements of water evaporating off from trees. Because deuterium acts as a conservative izci, it works well for tracking water movement through plants and ekosistemler. Although water movement in single-process phenomena such as evaporation is relatively simple to track, many systems (e.g. bulut ormanları ) in the environment have multiple sources and tracking water movement becomes more complicated.[247] Isotope spiking can also be done to determine water transport through soil and into plants via injection of deuterated water directly into the ground.[248]
Stable isotope analysis of ksilem water can be used to follow the movement of water from soil into the plants and therefore provide a record of the depth of water acquisition. An advantage to using xylem water is that in theory, the deuterium content should directly reflect the input water without being affected by leaf transpiration. For example, Dawson and Ehleringer used this approach to determine whether trees that grow next to streams are using the surface waters from that stream.[249] Water from the surface would have the same isotopic composition as the stream, while water from farther below in the ground would be from past precipitation inputs. In this case, younger trees had a xylem water isotopic composition very close to the adjacent stream and likely used surface waters to get established. Older trees had depleted xylem water relative to the stream, reflecting that they source their water from deeper underground.[249] Other stable isotope studies have also determined that plants in sekoya ormanları do not just take up water from their roots but acquire a significant proportion of water via stomalı uptake on leaves.[250]
Plant water can be used to characterize other plant physiological processes that affect the hydrologic cycle; for example, leaf waters are widely used for modeling transpiration[251] ve water-use efficiency.[252] In transpiration, the Craig-Gordon model for lake water enrichment through evaporation[253] has been found experimentally to fit well for modelling leaf water enrichment.[254] Transpiration can be measured by direct injection of deuterated water into the base of the tree, trapping all water vapor transpired from the leaves and measuring the subsequent condensate.[255] Water use can also be measured and is calculated from a heavy water injection as follows:
Where WU is the water use in kilograms/day, M is the mass of deuterated water injected in grams, T is the final day of the experiment, Cben is the concentration of deuterium at time interval i in grams/kilogram, and Δtben is the length of time interval i in days. Although the calculated water use via thermal dissipation probing of some tropical plants such as bamboos correlates strongly with measured water use found by tracking D2O movement, the exact values are not the same.[256] In fact, with baklagil ağaç türleri Gliricidia sepium, which produces a heartwood, transpired water did not even correlate strongly with injected D2O concentrations, which would further complicate water use measurements from direct injections. This possibly occurred because heartwoods could accumulate heavy water rather than move the water directly through xylem and to leaves.[256]
Water use efficiency (WUE), which is the ratio of carbon fixation to transpiration, has previously been associated with 13C/12C ratios using the following equation:
Bu denklemde,
, φ is the fraction of fixed carbon that is respired, pCO
2 is the partial pressure of CO
2 in the atmosphere, εcarb is the fractionation of carboxylation, and εfark is the fractionation of diffusion in air. The relation of δD in plant leaf waxes to δ13C has been empirically measured and results in a negative correlation of δD to water use efficiency. This can be explained in part by lower water use efficiency being associated with higher transpiration rates. Transpiration exhibits a normal isotope effect, causing enrichment of deuterium in plant leaf water and therefore enrichment of leaf waxes.
Ekoloji
Göç modelleri
Deuterium abundance can be useful in tracking göç of various animals.[257] Animals with metabolically inert tissue (e.g. feathers or hair) will have synthesized that tissue using hydrogen from source water and food but ideally not incorporate subsequent water over the course of the migration. Because δD tends to vary geographically, the difference between animal tissue δD and post-migration water δD, after accounting for the biological fractionation of assimilation, can provide information regarding animal movement. İçinde monarch butterflies, for example, wing Chitin is metabolically inert after it has been built, so it can reflect the isotopic composition of the environmental water at the time and location of wing growth. This then creates a record of butterfly origin and can be used to determine migration distance.[258] This approach can also be used in bats and birds, using hair and feathers, respectively.[259][260] Since rainwater becomes depleted as elevation is increased, this method can also track altitudinal migration. However, this is technically difficult to do, and the resolution appears to be too poor to track small altitudinal changes.[260] Deuterium is most useful in tracking movement of species between areas with large continental water variation, because species movement can be complicated by the similarity of local water δD values between different geographic regions. For example, source water from Baja California may have the same δD as water from Maine.[261] Further, a proportion of the hydrogen isotope composition within the tissue can exchange with water and complicate the interpretation of measurements. In order to determine this percentage of isotopic exchange, which varies according to local humidity levels, standards of metabolically inert tissue from the species of interest can be constructed and equilibrated to local conditions. This allows measured δD from different geographic regions to be compared against each other.[262]
Trofik etkileşimler
Assimilation of diet into tissue has a tissue-specific fractionation known as the trophic discrimination factor. Diet sources can be tracked through a food web via deuterium isotope profiles, although this is complicated by deuterium having two potential sources – water and food. Food more strongly impacts δD than does exchange with surrounding water, and that signal is seen across trophic levels.[263] However, different organisms derive organic hydrogen in varying ratios of water to food: for example, in quail, 20-30% of organic hydrogen was from water and the remainder from food. The precise percentage of hydrogen from water was dependent on tissue source and metabolic activity.[264] İçinde chironomids, 31-47% of biomass hydrogen derived from water,[263] and in microbes as much as 100% of fatty acid hydrogen can be derived from water depending on substrate.[189] In caterpillars, diet δD from organic matter correlates linearly with tissue δD. The same relationship does not appear to hold consistently for diet δD from water, however – water derived from either the caterpillar or its prey plant is more deuterium enriched than their organic material. Going up trophic levels from prey (plant) to predator (caterpillar) results in an isotopic enrichment.[265] This same trend of enrichment is seen in many other animals - carnivores, omnivores, and herbivores - and appears to follow 15N relative abundances. Carnivores at the same trophic level tend to exhibit the same level of 2H enrichment.[266] Because, as mentioned earlier, the amount of organic hydrogen produced from water varies between species, a model of trophic level related to absolute fractionation is difficult to make if the participating species are not known. Consistency in measuring the same tissues is also important, as different tissues fractionate deuterium differently. In aquatic systems, tracking trophic interactions is valuable for not only understanding the ecology of the system, but also for determining the degree of terrestrial input.[33][267] The patterns of deuterium enrichment consistent within trophic levels is a useful tool for assessing the nature of these interactions in the environment.[33]
Mikrobiyal metabolizma
Biological deuterium fractionation through metabolism is very organism and pathway dependent, resulting in a wide variability in fractionations.[189][268] Despite this, some trends still hold. Hydrogen isotopes tend to fractionate very strongly in ototroflar göre heterotroflar during lipid biosynthesis - chemoautotrophs produce extremely depleted lipids, with the fractionation ranging from roughly −200 to −400‰.[269] This has been observed both in laboratory-grown cultures fed a known quantity of deuterated water and in the environment.[189][270] Proteins, however, do not follow as significant a trend, with both heterotroflar ve ototroflar capable of generating large and variable fractionations.[269] In part, kinetic fractionation of the lighter isotope during formation of reducing equivalents NADH ve NADPH result in lipids and proteins that are isotopically lighter.
Salinity appears to play a role in the degree of deuterium fractionation as well; more saline waters affect growth rate, the rate of hydrogen exchange, and evaporation rate. All of these factors influence lipid δD upon hydrogen being incorporated into biomass. İçinde coccolithophores Emiliania huxleyi ve Gephyrocapsa oceanica, alkenone δD has been found to correlate strongly to organism growth rate divided by salinity.[205] The relationship between deuterium fractionation and salinity could potentially be used in paleoenvironment reconstruction with preserved lipids in the rock record to determine, for example, ocean salinity at the time of organismal growth. However, the degree of fractionation is not necessarily consistent between organisms, complicating the determination of paleosalinity with this method.[205] There also appears to be a negative correlation between growth rate and fractionation in these coccolithophores. Further experiments on unicellular algae Eudorina unicocca ve Volvox aureus show no effect of growth rate (controlled by nitrogen limitation) on fatty acid δD. However, sterols become more D-depleted as growth rate increases,[271] in agreement with alkenone isotopic composition in coccolithophores. Overall, although there are some strong trends with lipid δD, the specific fractionations are compound-specific. As a result, any attempt to create a salinometer through δD measurements will necessarily be specific to a single compound type.
Çevre Kimyası
An important goal of environmental chemistry is tracing the source and degradation of pollutants. Various methods have been employed for fingerprinting pools of environmental pollutants such as the bulk chemical composition of a spill,[272] isotope ratios of the bulk chemical mixture,[273] or isotope ratios of individual constituent compounds. Stable isotopes of carbon and hydrogen can be used as complementary fingerprinting techniques for natural gas.[274] Recently, the D/H ratio of hydrocarbons from the Deepwater Horizon petrol sızıntısı was used to verify that their origin was likely from the Macondo well.[275] Hydrogen isotope ratios have also been used as a measure of the relative amount of biodegradation that has occurred in oil reservoirs in China,[276] and studies on pure cultures of n-alkane degrading organisms have shown a chain-length dependence on the amount of hydrogen isotope fractionation during degradation.[277] Additional studies have also shown hydrogen isotope effects in the degradation of Methyl tert-butyl ether[278] ve Toluen[279][280] that have been suggested to be useful in the evaluation of the level of degradation of these polluting compounds in the environment. In both cases the residual unreacted compounds became enriched in deuterium to a few tens of per mil, with variations exhibited between different organisms and degree of reaction completeness. These observations of heavy residual compounds have been applied to field observations of biodegradation reactions such as the removal of benzene and ethylbenzene,[281] which imparted a D/H fractionation of 27 and 50 per mil, respectively. Additionally analysis of o-xylene in a polluted site showed high residual D/H ratios after biodegradation, consistent with activation of C-H bonds being a rate limiting step in this process[282]
Kaynak ilişkilendirme ve adli tıp
Stable isotope ratios have found uses in various instances where the authenticity or origin of a chemical compound is called into question. Such situations include assessing the authenticity of food, wine and natural flavors; drug screening in sports (see doping ); pharmaceuticals; illicit drugs; and even helping identify human remains. In these cases it is often not sufficient to detect or quantify a certain compound, since the question is the origin of the compound. The strength of hydrogen isotope analysis in answering these questions is that in many cases the D/H ratio of a natural product is related to the natural water D/H values in the area where the product was formed (see: Hidrolojik döngü ). Since D/H ratios vary significantly between different geographic areas, this can serve as a powerful tool in locating the original source of many different substance.
Yiyecek ve lezzet doğrulama
Foods, flavorings and scents are often sold with the guarantee that chemical additives come from natural sources. This claim becomes difficult to evaluate when the chemical compound has a known structure and is readily synthesized in the lab. Authentication of claims regarding the origins of these chemicals has made good use of various stable isotopes, including those of hydrogen. Combined carbon and hydrogen isotope analysis has been used to test the authenticity of (E)-methyl cinnamate,[283] γ-decalactone ve δ-decalactone.[284] Hydrogen and nitrogen isotope ratios have been used for the authentication of alkilpirazinler used as "natural" coffee flavorings.[285]
Doping
The isotope ratio of carbon in the steroids of athletes has been used to determine whether these steroids originated from the body of the athlete or an exogenous source. This test has been used in a number of high-profile anti-doping cases and has various benefits over simply characterizing the concentration of various compounds. Attempts are being made to create similar tests based on stable hydrogen isotopes[286] which could be used to complement the existing testing methods. One concern with this method was that the natural steroids produced by the human body may vary significantly based on the deuterium content of drinking water, leading to false detection of doping based on hydrogen isotope differences. This concern has been addressed in a recent study which concluded that the effect of D/H ratio of drinking water did not pose an insurmountable source of error for this anti-doping testing strategy.[287]
Farmasötik kopyalar
The pharmaceutical industry has revenues in the hundreds of billions of dollars a year globally. With such a large industry sahtecilik and copyright infringement are serious issues, and hydrogen isotope fingerprinting has become a useful tool in verifying the authenticity of various drugs. As described in the preceding sections, the utility of D/H ratios highest when combined with measurements of other isotope ratios as well. In an early study on the stable isotope compositions of tropicamide, hidrokortizon, quinine ve tryptophan, carbon, nitrogen, oxygen and hydrogen stable isotopes were analyzed by EA-IRMS and clear distinctions were able to be made between manufacturers and even batches of the drugs based on their isotope signatures.[288] In this study it was determined that the hydrogen and oxygen isotope ratios were the two best fingerprints for distinguishing between different drug sources. A follow-up study analyzing naproksen from various lots and manufacturers also showed similar ability to distinguish between sources of the drugs.[289] The use of these isotope signatures could not only be used to distinguish between different manufacturers, but also between different synthetic pathways for the same compound.[290] These studies relied on the natural variations that occurred in the synthesis of these drugs, but other studies have used starting ingredients that are intentionally labelled D and 13C, and showed that these labels could be traced into the final pharmaceutical product.[291] D/H ratios can also be determined for specific sites in a drug by 2H NMR, and has been used to distinguish between different synthetic methods for ibuprofen and naproxen in one study,[292] ve prozac ve fluoksetin in another.[293] These studies show that bulk D/H ratio information for EA-IRMS, and site-specific D/H ratios from 2H NMR have great utility for pharmaceutical drug authenticity testing.
Yasadışı ilaçlar
The sources and production mechanisms of yasal olmayan ilaçlar has been another area that has seen successful application of hydrogen isotope characterization. Usually, as with other applications of stable isotope techniques, results are best when combination of multiple stable isotopes are compared with one another. δ2H, δ13C ve δ15N have been used together to analyze tablets of MDA ve MDMA and has successfully identified differences which could be used to differentiate between different sources or production mechanisms.[294] The same combination of stable isotopes with the addition of δ18O was applied to heroin and associated packaging and could successfully distinguish between different samples.[295] Analysis using deuterium NMR was also able to shed light on the origin and processing of both cocaine ve eroin.[296] In the case of heroin this site-specific natural isotopic fraction measured by deuterium NMR (SNIF-NMR) method could be used for determining the geographic origin of the molecule by analyzing so-called natural sites (which were present in the morphine from which heroin is made), as well as gaining information on the synthesis process by analyzing the artificial sites (added during drug processing).
İnsan kalıntılarının kaynağı
The geographical variation in D/H ratio in human içme suyu is recorded in hair. Studies have shown a very strong relation between an individuals' hair and drinking water D/H ratios.[297]
Dan beri musluk suyu D/H ratio has a strong dependence on geography, a persons hair D/H ratio can be used to determine regions in which they were most likely living during hair growth. This idea has been used in criminal investigations to try and constrain the movements of a person prior to their death, in much the same way D/H ratios have been used to track animal migrations. By analyzing sections of hair of varying ages it is possible to determine in what D/H regions a person was living at a specific time prior to their death.[298]
Ayrıca bakınız
Referanslar
- ^ Urey, Harold C. (1932-01-01). "A Hydrogen Isotope of Mass 2". Physical Review. 39 (1): 164–165. Bibcode:1932PhRv...39..164U. doi:10.1103/PhysRev.39.164.
- ^ Chadwick, J. (1933-10-01). "Bakerian Lecture. The Neutron". Londra Kraliyet Cemiyeti Bildirileri: Matematik, Fizik ve Mühendislik Bilimleri. 142 (846): 1–25. Bibcode:1933RSPSA.142....1C. doi:10.1098/rspa.1933.0152.
- ^ "The Nobel Prize in Chemistry 1934". www.nobelprize.org. Alındı 2016-05-13.
- ^ a b "Lawrence and His Laboratory: Episode: A Productive Error". www2.lbl.gov. Alındı 2016-05-13.
- ^ Alvarez, Luis W.; Cornog, Robert (1939-09-15). "Helium and Hydrogen of Mass 3". Physical Review. 56 (6): 613. Bibcode:1939PhRv...56..613A. doi:10.1103/PhysRev.56.613.
- ^ Lucas, L.L.; Unterweger, M.P. (2000-07-01). "Comprehensive review and critical evaluation of the half-life of tritium". Journal of Research of the National Institute of Standards and Technology. 105 (4): 541–9. doi:10.6028/jres.105.043. PMC 4877155. PMID 27551621.
- ^ Wishart, D. S.; Sykes, B. D.; Richards, F. M. (1992-02-01). "The chemical shift index: a fast and simple method for the assignment of protein secondary structure through NMR spectroscopy". Biyokimya. 31 (6): 1647–1651. CiteSeerX 10.1.1.539.2952. doi:10.1021/bi00121a010. PMID 1737021.
- ^ Caligiani, A.; Acquotti, D.; Palla, G.; Bocchi, V. (2007-02-28). "Identification and quantification of the main organic components of vinegars by high resolution 1H NMR spectroscopy". Analytica Chimica Açta. 585 (1): 110–119. doi:10.1016/j.aca.2006.12.016. PMID 17386654.
- ^ Pake, G. E. (1948-04-01). "Nuclear Resonance Absorption in Hydrated Crystals: Fine Structure of the Proton Line". Kimyasal Fizik Dergisi. 16 (4): 327–336. Bibcode:1948JChPh..16..327P. doi:10.1063/1.1746878.
- ^ "Ray-Freeman.org | The Dawn of NMR". www.ray-freeman.org. Alındı 2016-05-13.
- ^ Dufourc, Erick J.; Parish, Edward J.; Chitrakorn, Sarawanee; Smith, Ian C. P. (1984-12-01). "Structural and dynamical details of cholesterol-lipid interaction as revealed by deuterium NMR". Biyokimya. 23 (25): 6062–6071. doi:10.1021/bi00320a025.
- ^ Martin, Gérard J.; Akoka, Serge; Martin, Maryvonne L. (2008-01-01). Webb, Graham A. (ed.). SNIF-NMR—Part 1: Principles. Springer Hollanda. pp. 1651–1658. doi:10.1007/1-4020-3910-7_185. ISBN 9781402038945.
- ^ Allen, Benjamin D.; Cintrat, Jean-Christophe; Faucher, Nicolas; Berthault, Patrick; Rousseau, Bernard; O'Leary, Daniel J. (2005-01-01). "An Isosparteine Derivative for Stereochemical Assignment of Stereogenic (Chiral) Methyl Groups Using Tritium NMR: Theory and Experiment". Journal of the American Chemical Society. 127 (1): 412–420. doi:10.1021/ja045265i. PMID 15631492.
- ^ "Tritium Production - Nuclear Weapons". fas.org. Arşivlenen orijinal 2016-05-03 tarihinde. Alındı 2016-05-13.
- ^ a b "Operation Greenhouse". nükleer silah arşivi.org. Alındı 2016-05-13.
- ^ "Congress to Address Helium-3 Shortage Hurting Scientific Research and Nuclear Security". Popüler Bilim. Alındı 2016-05-13.
- ^ Eveleth, Rose. "Nuclear Bombs Made It Possible to Carbon Date Human Tissue". Smithsonian. Alındı 2016-05-13.
- ^ Laboratory, US Department of Commerce, NOAA, Earth System Research. "ESRL Global Monitoring Division - Education and Outreach". www.esrl.noaa.gov-US. Alındı 2016-05-13.
- ^ England, Matthew H.; Maier-Reimer, Ernst (2001-02-01). "Using chemical tracers to assess ocean models". Jeofizik İncelemeleri. 39 (1): 29–70. Bibcode:2001RvGeo..39...29E. doi:10.1029/1998RG000043. hdl:21.11116 / 0000-0005-0A65-F. S2CID 42081518.
- ^ Craig, Harmon (26 Mayıs 1961). "Meteorik Sulardaki İzotopik Değişimler" (PDF). Bilim. 133 (3465): 1702–1703. Bibcode:1961Sci ... 133.1702C. doi:10.1126 / science.133.3465.1702. PMID 17814749. S2CID 34373069.
- ^ Zborowski, G; Ponticorvo, L; Rittenberg, D (1967-10-01). "Miosen döneminden bu yana yağ asitlerinin biyosentezinde döteryum fraksiyonasyonunun sabitliği hakkında". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 58 (4): 1660–1663. Bibcode:1967PNAS ... 58.1660Z. doi:10.1073 / pnas.58.4.1660. PMC 223976. PMID 5237893.
- ^ Smith, Bruce; Epstein, Samuel (1970). "Tuz bataklık biyotasındaki kararlı hidrojen ve karbon izotoplarının biyojeokimyası". Bitki Fizyolojisi. 46 (5): 738–742. doi:10.1104 / s.46.5.738. PMC 396670. PMID 16657539.
- ^ Schiegl, W. E .; Vogel, J.C. (1970-01-01). "Organik maddenin döteryum içeriği". Dünya ve Gezegen Bilimi Mektupları. 7 (4): 307–313. Bibcode:1970E ve PSL ... 7..307S. doi:10.1016 / 0012-821X (69) 90041-7.
- ^ Estep, Marilyn F .; Hoering, Thomas C. (1980-08-01). "Kararlı hidrojen izotoplarının biyojeokimyası". Geochimica et Cosmochimica Açta. 44 (8): 1197–1206. Bibcode:1980GeCoA..44.1197E. doi:10.1016/0016-7037(80)90073-3.
- ^ a b c Epstein, Samuel; Yapp, Crayton J .; Hall, John H. (1976-05-01). "Sucul ve kara bitkilerinden ekstrakte edilen selülozda değiştirilemeyen hidrojenin D / H oranının belirlenmesi". Dünya ve Gezegen Bilimi Mektupları. 30 (2): 241–251. Bibcode:1976E ve PSL..30..241E. doi:10.1016 / 0012-821X (76) 90251-X.
- ^ Sternberg, Leonel; Deniro, Michael J .; Ajie, Henry (1984-01-01). "Cam, c3 ve c4 bitkilerinden sabunlaşabilir lipitlerin ve selüloz nitratın kararlı hidrojen izotop oranları". Bitki kimyası. 23 (11): 2475–2477. doi:10.1016 / S0031-9422 (00) 84078-9.
- ^ Schoell, Martin (1980-05-01). "Çeşitli kökenlerden doğal gazlardan metanın hidrojen ve karbon izotopik bileşimi". Geochimica et Cosmochimica Açta. 44 (5): 649–661. Bibcode:1980GeCoA..44..649S. doi:10.1016/0016-7037(80)90155-6.
- ^ a b Oturumlar, Alex L. (2016-06-01). "Tortul hidrokarbonların döteryum içeriğini kontrol eden faktörler". Organik Jeokimya. 96: 43–64. doi:10.1016 / j.orggeochem.2016.02.012.
- ^ Wang, David T .; Gruen, Danielle S .; Lollar, Barbara Sherwood; Hinrichs, Kai-Uwe; Stewart, Lucy C .; Holden, James F .; Hristov, Alexander N .; Pohlman, John W .; Morrill, Penny L. (2015/04/24). "Dengesizlik kümelenmiş izotop sinyalleri mikrobiyal metanda". Bilim. 348 (6233): 428–431. Bibcode:2015 Sci ... 348..428W. doi:10.1126 / science.aaa4326. hdl:1721.1/95903. PMID 25745067. S2CID 206634401.
- ^ Eiler, John M. (2007-10-30). ""Kümelenmiş izotop "jeokimya - Doğal olarak oluşan, çoklu ikame edilmiş izotopologların incelenmesi". Dünya ve Gezegen Bilimi Mektupları. 262 (3–4): 309–327. Bibcode:2007E ve PSL.262..309E. doi:10.1016 / j.epsl.2007.08.020.
- ^ Eiler, John M. (2011-12-01). "Karbonat kümelenmiş izotop termometresi kullanılarak paleoiklimin yeniden yapılandırılması". Kuaterner Bilim İncelemeleri. 30 (25–26): 3575–3588. Bibcode:2011QSRv ... 30.3575E. doi:10.1016 / j.quascirev.2011.09.001.
- ^ a b Oturumlar, Alex L .; Burgoyne, Thomas W .; Schimmelmann, Arndt; Hayes, John M. (1999-09-01). "Lipit biyosentezinde hidrojen izotoplarının parçalanması". Organik Jeokimya. 30 (9): 1193–1200. doi:10.1016 / S0146-6380 (99) 00094-7.
- ^ a b c Doucett, Richard R .; İşaretler, Jane C .; Blinn, Dean W .; Caron, Melanie; Hungate, Bruce A. (2007-06-01). "Karasal sübvansiyonları kararlı hidrojen izotopları kullanarak suda yaşayan besin ağlarına ölçme". Ekoloji. 88 (6): 1587–1592. doi:10.1890/06-1184. PMID 17601150.
- ^ Eiler, John M .; Clog, Matthieu; Magyar, Paul; Piasecki, Alison; Oturumlar, Alex; Stolper, Daniel; Deerberg, Michael; Schlueter, Hans-Juergen; Schwieters, Johannes (2013-02-01). "Yüksek çözünürlüklü bir gaz kaynağı izotop oranı kütle spektrometresi". Uluslararası Kütle Spektrometresi Dergisi. 335: 45–56. Bibcode:2013IJMSp.335 ... 45E. doi:10.1016 / j.ijms.2012.10.014.
- ^ Hayes, John M. "İzotopik hesaplamalara giriş." Woods Hole Oşinografi Kurumu, Woods Hole, MA 2543 (2004).
- ^ Rolston, J. H .; Den Hartog, J .; Butler, J.P. (1976). "Hidrojen ve sıvı su arasındaki döteryum izotop ayırma faktörü". Fiziksel Kimya Dergisi. 80 (10): 1064–1067. doi:10.1021 / j100551a008.
- ^ "Elementlerin Kökeni". www2.lbl.gov. Alındı 2016-05-13.
- ^ Borexino İşbirliği (2014-08-28). "Güneş'teki birincil proton-proton füzyon sürecinden gelen nötrinolar". Doğa. 512 (7515): 383–386. Bibcode:2014Natur.512..383B. doi:10.1038 / nature13702. PMID 25164748. S2CID 205240340.
- ^ Dingwall, S .; Mills, C.E .; Phan, N .; Taylor, K .; Boreham, D.R. (2011-02-22). "İnsan Sağlığı ve Trityum'un İçme Suyundaki Biyolojik Etkileri: Bilim Yoluyla İhtiyatlı Politika - ODWAC Yeni Tavsiyesini Ele Alma". Doz-Tepki. 9 (1): 6–31. doi:10.2203 / doz-yanıt.10-048.Boreham. PMC 3057633. PMID 21431084.
- ^ "Parçacıkların spin sınıflandırması". hyperphysics.phy-astr.gsu.edu. Alındı 2016-05-13.
- ^ a b c d e Rozanski, Kazimierz; Araguas-Araguas, Luis; Gonfiantini Roberto (1993). Modern küresel yağışta izotopik modeller. Jeofizik Monograf. Jeofizik Monograf Serisi. 78. s. 1–36. Bibcode:1993GMS .... 78 .... 1R. doi:10.1029 / GM078p0001. ISBN 9781118664025.
- ^ McQuarrie Donald A (2007). Kuantum Kimyası. Üniversite Bilim Kitapları. ISBN 978-1891389504.
- ^ Fisher, Matthew P. A .; Weichman, Peter B .; Grinstein, G .; Fisher, Daniel S. (1989-07-01). "Bozon lokalizasyonu ve süperakışkan-yalıtkan geçişi" (PDF). Fiziksel İnceleme B. 40 (1): 546–570. Bibcode:1989PhRvB..40..546F. doi:10.1103 / PhysRevB.40.546. PMID 9990946.
- ^ Hutchinson, John S .; Iii, Edwin L. Sibert; Hynes, James T. (1984-08-01). "Birleştirilmiş Morse osilatör sistemlerindeki bağlar arasındaki enerji transferinin kuantum dinamikleri". Kimyasal Fizik Dergisi. 81 (3): 1314–1326. Bibcode:1984JChPh..81.1314H. doi:10.1063/1.447763.
- ^ Young, Edward D .; Galy, Albert; Nagahara, Hiroko (2002-03-15). "Doğada kinetik ve denge kütlesine bağlı izotop fraksiyonlama yasaları ve bunların jeokimyasal ve kozmokimyasal önemi". Geochimica et Cosmochimica Açta. 66 (6): 1095–1104. Bibcode:2002GeCoA..66.1095Y. doi:10.1016 / S0016-7037 (01) 00832-8.
- ^ a b c d Schimmelmann, Arndt; Oturumlar, Alex (2006). "Diyajenez ve termal olgunlaşma sırasında organik maddenin hidrojen izotopik (D / H) bileşimi" (PDF). Annu. Rev. Earth Planet. Sci. 34: 501–533. Bibcode:2006AREPS..34..501S. doi:10.1146 / annurev.earth.34.031405.125011.
- ^ Oturumlar, Alex (2004). "Jeolojik zaman ölçeklerinde karbona bağlı hidrojenin izotopik değişimi". GCA. 68 (7): 1545–1559. Bibcode:2004GeCoA..68.1545S. doi:10.1016 / j.gca.2003.06.004.
- ^ O'Neil, James R; Kharaka, Yousif K (1976-02-01). "Kil mineralleri ile su arasındaki hidrojen ve oksijen izotop değişim reaksiyonları". Geochimica et Cosmochimica Açta. 40 (2): 241–246. Bibcode:1976GeCoA..40..241O. doi:10.1016/0016-7037(76)90181-2.
- ^ Klopper, Wim .; Kutzelnigg, Werner. (1990-07-01). "Karbokatyonların bağıl kararlılığı hakkında MP2-R12 hesaplamaları". Fiziksel Kimya Dergisi. 94 (14): 5625–5630. doi:10.1021 / j100377a040.
- ^ "Efsanevi Karbokasyonlar mı?". chemistry.umeche.maine.edu. Alındı 2016-05-13.
- ^ a b c d e f g Oturumlar, Alex (2016). "Tortul hidrokarbonların döteryum içeriğini kontrol eden faktörler". Organik Jeokimya. 96: 43–64. doi:10.1016 / j.orggeochem.2016.02.012.
- ^ Hopfner, A (Ekim 1969). "Buhar Basıncı İzotop Etkileri". Angewandte Chemie. 8 (10): 689–699. doi:10.1002 / anie.196906891.
- ^ [Clog, Matthieu; Aubaud, Cyril; Cartigny, Pierre; Dosso, Laure (2013). "Güney Pasifik MORB'nin hidrojen izotopik bileşimi ve su içeriği: Tükenmiş manto Rezervuarının D / H oranının yeniden değerlendirilmesi". Gezegen Bilimi Mektupları 381: 156-165.] Ve [Englebrecht A. C., Sachs J. P. (2005) Alkenonlarda hidrojen izotopları ve doymamışlık oranları kullanılarak sürüklenme bölgelerindeki tortu kaynağının belirlenmesi. Geochimina ve Cosmochimica Açta, Cilt. 69, No. 17, s. 4253–4265] http://waterisotopes.org
- ^ Clog, Matthieu; Aubaud, Cyril; Cartigny, Pierre; Dosso, Laure (2013). "Güney Pasifik MORB'nin hidrojen izotopik bileşimi ve su içeriği: Tükenmiş manto Rezervuarının D / H oranının yeniden değerlendirilmesi" (PDF). Gezegen Bilimi Mektupları. 381: 156–165. Bibcode:2013E ve PSL.381..156C. doi:10.1016 / j.epsl.2013.08.043.
- ^ Englebrecht A. C., Sachs J. P. (2005) Alkenonlarda hidrojen izotopları ve doymamışlık oranları kullanılarak sürüklenme bölgelerindeki tortu kaynağının belirlenmesi. Geochimina ve Cosmochimica Açta, Cilt. 69, No. 17, s. 4253–4265
- ^ Annu.Rev.Earth Planet.Sci.2010.38: 161–187'den haritaya veri değerleri eklenerek değiştirildi
- ^ a b Lecuyer, C; et al. (1998). "Deniz suyunun Hidrojen izotop bileşimi ve küresel su döngüsü". Kimyasal Jeoloji. 145 (3–4): 249–261. Bibcode:1998ChGeo.145..249L. doi:10.1016 / s0009-2541 (97) 00146-0.
- ^ Masson-Delmotte, V et al. (2008) Antarktika Yüzey Kar İzotopik Kompozisyonunun İncelenmesi: Gözlemler, Atmosferik Dolaşım ve İzotopik Modelleme. Amerikan Meteoroloji Derneği. 3359–3387.
- ^ Bir kağıttan veriler eklenerek değiştirilmiştir [Frankenberg C. et al. (2009) Uzaydan ve Yerden Gözlemlenen Alt Troposferik HDO / H2O Oranlarını Yöneten Dinamik Süreçler. Annu.Rev.Earth Planet.Sci.2010.38: 161–187'den haritada Science 325, 1374–1377.]
- ^ Frankenberg, C .; Yoshimura, K .; Warneke, T .; Aben, I .; Butz, A .; Deutscher, N .; Griffith, D .; Hase, F .; Notholt, J .; Schneider, M .; Schrijver, H .; Röckmann, T. (2009). "Uzaydan ve Yerden Gözlemlenen Alt Troposferik HDO / H2O Oranlarını Yöneten Dinamik Süreçler". Bilim. 325 (5946): 1374–1377. Bibcode:2009Sci ... 325.1374F. doi:10.1126 / science.1173791. PMID 19745148. S2CID 13043951.
- ^ White, J.W.C., Gedzelman, S.D. (1984) Atmosferik su buharının izotopik bileşimi ve eşzamanlı meteorolojik koşullar. JGR: Atmosferler. Cilt 89. Sayı D3. 4937–4939.
- ^ Sacese vd.
- ^ Daha fazla ayrıntı için Bölüm 6. Hidrolojik Döngü'ye bakın.
- ^ Haritaya waterisotopes.org'dan veri eklenerek değiştirildi
- ^ [1]
- ^ http://wateriso.utah.edu/waterisotopes/index.html
- ^ a b Clark, I., Fritz, P. 1954. Hidrojeolojide Çevresel İzotoplar. Lewis Publisher.
- ^ Bölüm 6.1'e bakınız. Daha fazla ayrıntı için hidrolojik döngüde izotopik fraksiyonlama.
- ^ Annu.Rev.Earth Planet.Sci.2010.38: 161–187'den haritada waterisotopes.org'dan veri değerleri eklenerek değiştirildi.
- ^ Sachse, D (2012). "Moleküler Paleohidroloji: Fotosentez Yapan Organizmalardan Lipid Biyobelirteçlerinin Hidrojen-İzotopik Kompozisyonunun Yorumlanması" (PDF). Annu. Rev. Earth Planet. Sci. 40 (1): 221–249. Bibcode:2012AREPS..40..221S. doi:10.1146 / annurev-earth-042711-105535.
- ^ a b Bkz.Bölüm 7.1. Daha fazla ayrıntı için izotop hidrolojisi.
- ^ a b c d Zhang, Z; et al. (2008). "Tatlı su ve deniz yosunlarında hidrojen izotop fraksiyonasyonu: II. Sıcaklık ve azot sınırlı büyüme hızı etkileri". Organik Jeokimya. 40 (3): 428–439. doi:10.1016 / j.orggeochem.2008.11.002.
- ^ Sauer P. E. ve diğerleri, (2000) Çevresel ve iklim koşulları için bir vekil olarak çökeltilerden lipit biyobelirteçlerinin bileşiğe özgü D / H oranları. Geochimica ve Cosmochimica Açta. Cilt 65, No. 2, s. 213–222.
- ^ Sachs J.P. (2014) Fitoplankton Lipidlerinde Hidrojen İzotop İmzaları. Hollanda H.D. ve Turekian K.K. (eds.) Jeokimya Üzerine İnceleme, İkinci Baskı, cilt. 12, sayfa 79–94. Oxford: Elsevier.
- ^ a b c Sessions, A. L. (2002) Metan oksitleyen bakteri Methylococcus capsulatus'un lipidlerinde hidrojen izotop fraksiyonasyonu. Geochimica et Cosmochimica Açta, 66. 22: 3955–3969.
- ^ Bkz.Bölüm 7.5.3. Daha fazla ayrıntı için mikrobiyal metabolizma.
- ^ [Sachse, D et al. (2012) Moleküler Paleohidroloji: Fotosentez Yapan Organizmalardan Lipid Biyobelirteçlerinin Hidrojen-İzotopik Kompozisyonunun Yorumlanması. Annu. Rev. Earth Planet. Sci. 40: 221-49.
- ^ a b Sachse, D; et al. (2012). "Moleküler Paleohidroloji: Fotosentez Yapan Organizmalardan Lipid Biyobelirteçlerinin Hidrojen-İzotopik Kompozisyonunun Yorumlanması" (PDF). Annu. Rev. Earth Planet. Sci. 40 (1): 221–49. Bibcode:2012AREPS..40..221S. doi:10.1146 / annurev-earth-042711-105535.
- ^ Bkz.Bölüm 7.2.2.2. Daha fazla ayrıntı için bitki yaprağı mumları.
- ^ a b c Schmidt, H. L .; Werner, R. A .; Eisenreich, W. (2003). "Doğal bileşiklerdeki D örüntülerinin sistematiği ve biyosentetik yolların aydınlatılmasındaki önemi". Fitokimya İncelemeleri. 2 (1–2): 61–85. doi:10.1023 / b: phyt.0000004185.92648.ae. S2CID 12943614.
- ^ Sessions, A. L. vd. (1999) Lipit biyosentezinde hidrojen izotoplarının parçalanması. Organik Jeokimya. 30. 1193–1200
- ^ Zhang, B. L .; et al. (2002). "Şekerlerin karakterizasyonunda hidrojen izotopik profil. Metabolik yolun etkisi". J Agric gıda Kimya. 50 (6): 1574–80. doi:10.1021 / jf010776z. PMID 11879039.
- ^ Hou vd., 2008
- ^ Sachse vd., 2012
- ^ a b Soto, D.X., Wassenaar, L.I., Hobson, K. A., (2013) Suda yaşayan besin ağlarındaki kararlı hidrojen ve oksijen izotopları, diyet ve menşei izleyicileridir. Fonksiyonel Ekoloji. Cilt 27. Sorun. 2. 535–543.
- ^ Bkz Bölüm 7.3.3. Daha fazla ayrıntı için yağ.
- ^ Waseda Amane (1993). "Olgunluğun Kuzeydoğu Japonya'daki ham petrollerin karbon ve hidrojen izotopları üzerindeki etkisi". Japon Petrol Teknolojisi Derneği Dergisi. 58 (3): 199–208. doi:10.3720 / japt.58.199.
- ^ a b dos Santos Neto, EV; Hayes, JM (1999). "Kuzeydoğu Brezilya'daki Portiguar Havzası'ndan gelen yağları karakterize eden hidrojen ve karbona kararlı izotopların kullanımı". AAPG Bülteni. 83 (3): 496–518. doi:10.1306 / 00aa9be2-1730-11d7-8645000102c1865d.
- ^ Bkz.Bölüm 7.2.2.3. Daha fazla ayrıntı için alkenonlar.
- ^ [Englebrecht, A. C. Sachs. J. P. (2005) Alkenonlarda hidrojen izotopları ve doymamışlık oranları kullanılarak sürüklenme bölgelerindeki tortu kaynağının belirlenmesi. Geochimica ve Cosmochimica Açta. 69. 17: 4253–4265.] Annu.Rev.Earth Planet.Sci.2010.38: 161–187'den haritada.
- ^ Englebrecht, A. C. Sachs. J. P. (2005) Alkenonlarda hidrojen izotopları ve doymamışlık oranları kullanılarak sürüklenme sahalarındaki tortu kaynağının belirlenmesi. Geochimica ve Cosmochimica Açta. 69. 17: 4253–4265.
- ^ Bkz. Bölüm 7.3.1. Daha fazla ayrıntı için Kerojenler ve Kömürler.
- ^ Redding (1980), Rigby ve Smith (1981) ve Smith (1983) tarafından yayınlanan kağıtlardan verilerin Annu.Rev.Earth Planet.Sci.2010.38: 161–187'den haritaya eklenmesiyle değiştirildi.
- ^ Redding, CE (1980). "Kömür ve kerojenlerin hidrojen ve karbon izotopik bileşimi". Dünyanın Fiziği ve Kimyası. 12: 711–723. Bibcode:1980PCE .... 12..711R. doi:10.1016/0079-1946(79)90152-6.
- ^ Rigby, D .; Batts, B.D .; Smith, J.W. (1981). "Olgunlaşmanın fosil yakıtların izotopik bileşimi üzerindeki etkisi". Organik Jeokimya. 3 (1–2): 29–36. doi:10.1016/0146-6380(81)90010-3.
- ^ Smith, J.W. (1983). "Kömürlerin D / H oranı ve çökelmelerinin paleoolatitesi". Doğa. 302 (5906): 322–323. Bibcode:1983Natur.302..322S. doi:10.1038 / 302322a0. S2CID 4317372.
- ^ Bkz Bölüm 7.3.2. Daha fazla ayrıntı için doğal gaz.
- ^ a b Whiticar, Michael (1999). "Bakteri oluşumu ve metanın oksidasyonunun karbon ve hidrojen izotop sistematiği". Kimyasal Jeoloji. 161 (1–3): 291–314. Bibcode:1999ChGeo.161..291W. doi:10.1016 / S0009-2541 (99) 00092-3.
- ^ Hoefs, J. (2009). Kararlı izotop jeokimyası (6. baskı). doi:10.1007/978-3-540-70708-0
- ^ Daha detaylı bir formattaki referanslar ana metinde yer almaktadır.
- ^ Sheppard, S. M. F., Gilg, H. A. (1996) Stable Isotope Geochemistry of Clay Minerals. Kil Mineralleri. 31, 1–24.
- ^ Hoefs, J. (2009). Kararlı izotop jeokimyası (6. baskı). doi:10.1007/978-3-540-70708-0
- ^ Robert, F. 2006. Güneş Sistemi Döteryum / Hidrojen Oranı. Meteorites and the Early Solar System II, D. S. Lauretta ve H. Y. McSween Jr. (editörler), University of Arizona Press, Tucson, 943 pp., S.341-351
- ^ Pinti, Daniele (2011). Döteryum / Hidrojen Oranı, Astrobiyoloji Ansiklopedisi. Berlin Heidelberg: Springer-Verlag.
- ^ "Güneş Sisteminde Döteryum-Hidrojen oranı".
- ^ McKeegan, K. D., Leshin, L.A. (2001) Kararlı İzotop Varyasyonları Dünya dışı Malzemeler. Mineraloji ve Jeokimyada İncelemeler. 43. (1)
- ^ a b Oturumlar, Alex L. (2006-08-01). "Gaz kromatografisi için izotop oranı tespiti". Ayırma Bilimi Dergisi. 29 (12): 1946–1961. doi:10.1002 / jssc.200600002. PMID 16970194.
- ^ Hoefs, Jochen (2009), Kararlı İzotop Jeokimyası (PDF) (6. baskı), Springer-Verlag Berlin Heidelberg, doi:10.1007/978-3-540-70708-0, ISBN 978-3-642-08960-2
- ^ Bigeleisen, Jacob; Perlman, M. L .; Prosser, H.C. (1952-08-01). "İzotopik Analiz İçin Hidrojenik Malzemelerin Hidrojene Dönüştürülmesi". Analitik Kimya. 24 (8): 1356–1357. doi:10.1021 / ac60068a025.
- ^ Godfrey, John D. (1962-12-01). "Doğu-Merkez Sierra Nevada ve Yosemite Ulusal Parkı'ndaki sulu minerallerin döteryum içeriği". Geochimica et Cosmochimica Açta. 26 (12): 1215–1245. Bibcode:1962GeCoA..26.1215G. doi:10.1016/0016-7037(62)90053-4.
- ^ Graff, Jack; Rittenberg, David (1952-05-01). "Organik Bileşiklerde Döteryumun Mikrodeterminasyonu". Analitik Kimya. 24 (5): 878–881. doi:10.1021 / ac60065a032.
- ^ Friedman, Irving (1953-08-01). "Doğal suların ve diğer maddelerin döteryum içeriği". Geochimica et Cosmochimica Açta. 4 (1): 89–103. Bibcode:1953GeCoA ... 4 ... 89F. doi:10.1016/0016-7037(53)90066-0.
- ^ Schimmelmann, Arndt; DeNiro, Michael J. (1993-03-01). "Kararlı izotop analizi için organik ve su hidrojeni hazırlanması: reaksiyon kaplarına ve çinko reaktifine bağlı etkiler". Analitik Kimya. 65 (6): 789–792. doi:10.1021 / ac00054a024.
- ^ Gehre, M .; Hoefling, R .; Kowski, P .; Strauch, G. (1996-01-01). "Krom Metal Kullanarak Kantitatif Hidrojen İzotop Analizi için Numune Hazırlama Cihazı". Analitik Kimya. 68 (24): 4414–4417. doi:10.1021 / ac9606766.
- ^ Yeniden çizilmiş şekil referans olarak http://www.uwyo.edu/sif/instrumentation/tcea.html
- ^ Gehre, Matthias; Yeniden Açılma, Julian; Gilevska, Tetyana; Qi, Haiping; Coplen, Tyler B .; Meijer, Harro A. J .; Brand, Willi A .; Schimmelmann, Arndt (2015-05-19). "Elemental Krom Kullanılarak Organik Numunelerin Çevrimiçi Hidrojen-İzotop Ölçümleri: Yüksek Sıcaklık Elemental Analiz Teknikleri İçin Bir Uzantı". Analitik Kimya. 87 (10): 5198–5205. doi:10.1021 / acs.analchem.5b00085. PMID 25874646.
- ^ Kuder, Tomasz; Philp, Paul (2013-02-05). "Klorlu Etenlerde Hidrojen İzotop Oranlarının Bileşiğe Özgü İzotop Analizinin Gösterilmesi". Çevre Bilimi ve Teknolojisi. 47 (3): 1461–1467. Bibcode:2013EnST ... 47.1461K. doi:10.1021 / es303476v. PMID 23294482.
- ^ Gehre, Matthias; Yeniden Açılma, Julian; Gilevska, Tetyana; Qi, Haiping; Coplen, Tyler B .; Meijer, Harro A. J .; Brand, Willi A .; Schimmelmann, Arndt (2015). "Elemental Krom Kullanılarak Organik Numunelerin Çevrimiçi Hidrojen-İzotop Ölçümleri: Yüksek Sıcaklık Elemental Analiz Teknikleri İçin Bir Uzantı". Analitik Kimya. 87 (10): 5198–5205. doi:10.1021 / acs.analchem.5b00085. PMID 25874646.
- ^ Sauer, Peter E .; Schimmelmann, Arndt; Oturumlar, Alex L .; Topalov, Katarina (2009-04-15). "Katı organik malzemede değiştirilemez hidrojenin D / H tespiti için basitleştirilmiş parti dengelemesi". Kütle Spektrometresinde Hızlı İletişim. 23 (7): 949–956. Bibcode:2009RCMS ... 23..949S. doi:10.1002 / rcm.3954. PMID 19241415.
- ^ Matthews, D. E .; Hayes, J.M. (1978-09-01). "İzotop oranı izleme gaz kromatografisi-kütle spektrometrisi". Analitik Kimya. 50 (11): 1465–1473. doi:10.1021 / ac50033a022.
- ^ a b Begley, Ian S .; Scrimgeour, Charles M. (1997-04-01). "Sürekli Akış Piroliz İzotop Oranı Kütle Spektrometresi ile Su ve Uçucu Organik Bileşikler için Yüksek Hassasiyetli δ2H ve δ18O Ölçümü". Analitik Kimya. 69 (8): 1530–1535. doi:10.1021 / ac960935r.
- ^ a b Hilkert, A. W .; Douthitt, C. B .; Schlüter, H. J .; Brand, W.A. (1999-07-15). "İzotop oranı izleme gaz kromatografisi / Yüksek sıcaklık dönüşüm izotop oranı kütle spektrometresi ile D / H kütle spektrometrisi". Kütle Spektrometresinde Hızlı İletişim. 13 (13): 1226–1230. Bibcode:1999RCMS ... 13.1226H. doi:10.1002 / (sici) 1097-0231 (19990715) 13:13 <1226 :: aid-rcm575> 3.0.co; 2-9.
- ^ Burgoyne, Thomas W .; Hayes, John M. (1998-12-01). "Gaz Kromatografik Atıkların Pirolizi ile Kantitatif H2 Üretimi". Analitik Kimya. 70 (24): 5136–5141. doi:10.1021 / ac980248v.
- ^ Tobias, Herbert J .; Goodman, Keith J .; Blacken, Craig E .; Brenna, J. Thomas. (1995-07-01). "Sürekli Akış İzotop Oranı Kütle Spektrometresi ile Hidrojen Gazından ve Sudan Yüksek Hassasiyetli D / H Ölçümü". Analitik Kimya. 67 (14): 2486–2492. doi:10.1021 / ac00110a025. PMID 8686878.
- ^ Bergamaschi, Peter; Schupp, Michael; Harris, Geoffrey W. (1994-11-20). "Yüksek hassasiyetli doğrudan ölçümler 13CH4/12CH4 ve 12CH3D /12CH4 uzun yollu ayarlanabilir diyot lazer absorpsiyon spektrometresi aracılığıyla atmosferik metan kaynaklarındaki oranlar ". Uygulamalı Optik. 33 (33): 7704–16. Bibcode:1994ApOpt..33.7704B. doi:10.1364 / AO.33.007704. PMID 20962979.
- ^ O'Keefe, Anthony; Deacon, David A. G. (1988-12-01). "Darbeli lazer kaynakları kullanarak absorpsiyon ölçümleri için boşluk halkalı optik spektrometre". Bilimsel Aletlerin İncelenmesi. 59 (12): 2544–2551. Bibcode:1988RScI ... 59.2544O. doi:10.1063/1.1139895.
- ^ Kerstel, E.R. Th .; van Trigt, R .; Reuss, J .; Meijer, H.A. J. (1999-12-01). "Sudaki 2H / 1H, 17O / 16O ve 18O / 16O İzotop Bolluk Oranlarının Lazer Spektrometresi Yoluyla Eşzamanlı Belirlenmesi" (PDF). Analitik Kimya. 71 (23): 5297–5303. doi:10.1021 / ac990621e. hdl:11370 / 7d521457-d577-4369-9d3e-b014903523de. PMID 21662727.
- ^ Brand, Willi A .; Geilmann, Heike; Crosson, Eric R .; Rella, Chris W. (2009-06-30). "Yüksek sıcaklık dönüşüm izotop oranı kütle spektrometresine karşı boşluk halkası aşağı spektroskopisi; saf su örnekleri ve alkol / su karışımlarının δ2H ve δ18O üzerinde bir vaka çalışması". Kütle Spektrometresinde Hızlı İletişim. 23 (12): 1879–1884. doi:10.1002 / rcm.4083. PMID 19449320.
- ^ Martin, Gérard J .; Akoka, Serge; Martin, Maryvonne L. (1 Ocak 2008). SNIF-NMR — Bölüm 1: İlkeler. Modern Manyetik Rezonans. s. 1651–1658. doi:10.1007/1-4020-3910-7_185. ISBN 978-1-4020-3894-5.
- ^ Martin, Gerard J .; Martin, Maryvonne L .; Mabon, Francoise .; Michon, Marie Jo. (Kasım 1982). "Doğal bolluk hidrojen-2 nükleer manyetik rezonans ile doğal alkollerin kökeninin belirlenmesi". Analitik Kimya. 54 (13): 2380–2382. doi:10.1021 / ac00250a057.
- ^ a b c Martin, Maryvonne; Zhang, Benli; Martin, Gérard J. (1 Ocak 2008). SNIF-NMR — Bölüm 2: Kimyasal ve Biyokimyasal Mekanistik Yolların İzleyicileri Olarak İzotop Oranları. Modern Manyetik Rezonans. s. 1659–1667. doi:10.1007/1-4020-3910-7_186. ISBN 978-1-4020-3894-5.
- ^ a b Schmidt, Hanns-Ludwig; Werner, Roland A .; Eisenreich, Wolfgang (Ocak 2003). "Doğal bileşiklerdeki 2H modellerinin sistematiği ve biyosentetik yolların aydınlatılmasında önemi". Fitokimya İncelemeleri. 2 (1–2): 61–85. doi:10.1023 / B: PHYT.0000004185.92648.ae. S2CID 12943614.
- ^ Martin, Gérard J .; Martin, Maryvonne L .; Remaud, Gérald (1 Ocak 2008). SNIF-NMR — Bölüm 3: Mekanik İlişkiden Kaynak Çıkarımına. Modern Manyetik Rezonans. s. 1669–1680. doi:10.1007/1-4020-3910-7_187. ISBN 978-1-4020-3894-5.
- ^ a b Berdagué, Philippe; Lesot, Philippe; Jacob, Jérémy; Terwilliger, Valery J .; Le Milbeau, Claude (15 Ocak 2016). "Sıvı kristallerdeki NAD 2D-NMR'nin miliasindeki metil gruplarının hidrojen izotop profilinin belirlenmesine katkısı" (PDF). Geochimica et Cosmochimica Açta. 173: 337–351. Bibcode:2016GeCoA.173..337B. doi:10.1016 / j.gca.2015.10.004.
- ^ a b Ehlers, Ina; Augusti, Angela; Betson, Tatiana R .; Nilsson, Mats B .; Marshall, John D .; Schleucher, Jürgen (22 Aralık 2015). "İzotopomerler kullanarak uzun vadeli metabolik değişimleri tespit etmek: 20. yüzyılda C3 bitkilerinde fotorespirasyonun CO2 kaynaklı baskılanması". Ulusal Bilimler Akademisi Bildiriler Kitabı. 112 (51): 15585–15590. Bibcode:2015PNAS..11215585E. doi:10.1073 / pnas.1504493112. PMC 4697390. PMID 26644588.
- ^ Lesot, Philippe; Serhan, Zeinab; Billault, Isabelle (25 Kasım 2010). "Anizotropik doğal bolluk 2H NMR spektroskopisi kullanılarak yağ asitleri gibi metabolitlerin bölgeye özgü izotopik fraksiyonasyonunun analizinde son gelişmeler: konjuge linolenik metil esterlere uygulama". Analitik ve Biyoanalitik Kimya. 399 (3): 1187–1200. doi:10.1007 / s00216-010-4394-0. PMID 21107978. S2CID 8646294.
- ^ Zhang, Ben-Li; Yunianta; Vallet, Claude; Martin, Yves-Loı̈c; Martin, Maryvonne L. (Nisan 1997). "Fermentasyon Reaksiyonunda Doğal Bolluk İzotopik Fraksiyonlama: Fermantasyon Ortamının Etkisi". Biyorganik Kimya. 25 (2): 117–129. doi:10.1006 / bioo.1997.1060.
- ^ Duan, Jia-Rong; Billault, Isabelle; Mabon, Françoise; Robins, Richard (2 Ağustos 2002). "Yerfıstığı Tohumu Yağından İzole Edilen Yağ Asitlerinde Doğal Döteryum Dağılımı: Kantitatif 2H NMR Spektroskopisi ile Sahaya Özgü Çalışma". ChemBioChem. 3 (8): 752–9. doi:10.1002 / 1439-7633 (20020802) 3: 8 <752 :: AID-CBIC752> 3.0.CO; 2-G. PMID 12203973.
- ^ Keppler, Frank; Hamilton, John T. G .; McRoberts, W. Colin; Vigano, Ivan; Braß, Marc; Röckmann, Thomas (Haziran 2008). "Atmosferik metanın öncüsü olarak bitki pektininin metoksil grupları: döteryum etiketleme çalışmalarından elde edilen kanıtlar". Yeni Fitolog. 178 (4): 808–814. doi:10.1111 / j.1469-8137.2008.02411.x. PMID 18346110.
- ^ Derwish, G. a. W .; Galli, A .; Giardini-Guidoni, A .; Volpi, G.G (15 Kasım 1964). "İyonun Kütle Spektrometrik Çalışması - Propan içindeki Molekül Reaksiyonları". Kimyasal Fizik Dergisi. 41 (10): 2998–3005. Bibcode:1964JChPh..41.2998D. doi:10.1063/1.1725665.
- ^ "Panorama Nu Instruments Ltd". nu-ins.com.
- ^ Eiler, John M .; Clog, Matthieu; Magyar, Paul; Piasecki, Alison; Oturumlar, Alex; Stolper, Daniel; Deerberg, Michael; Schlueter, Hans-Juergen; Schwieters, Johannes (Şubat 2013). "Yüksek çözünürlüklü bir gaz kaynağı izotop oranı kütle spektrometresi". Uluslararası Kütle Spektrometresi Dergisi. 335: 45–56. Bibcode:2013IJMSp.335 ... 45E. doi:10.1016 / j.ijms.2012.10.014.
- ^ Stolper, D.A .; Oturumlar, A.L .; Ferreira, A.A .; Santos Neto, E.V .; Schimmelmann, A .; Shusta, S.S .; Valentine, D.L .; Eiler, J.M. (Şubat 2014). "Metanda kombine 13C – D ve D – D kümelenmesi: Yöntemler ve ön sonuçlar". Geochimica et Cosmochimica Açta. 126: 169–191. Bibcode:2014GeCoA.126..169S. doi:10.1016 / j.gca.2013.10.045.
- ^ a b Ponton, Camilo. "Propan ve etandaki H izotop değişiminin bloke edici sıcaklıklarını kısıtlayan deneyler".
- ^ a b c d Criss Robert (1999). Kararlı İzotop Dağılımının Prensipleri. New York: Oxford University Press. ISBN 978-0-19-511775-2.
- ^ Craig, Harmon; Gordon, Louis (1965). "Okyanus ve deniz atmosferindeki döteryum ve oksijen 18 varyasyonları". Oşinografik Çalışmalarda ve Paleotem sıcaklıklarında Kararlı İzotoplar.
- ^ Majoube, M. (1971). "Oksijen fraksiyonu 18 ve en deuterium entre l'eau et sa vapeur". J. Chim. Phys. 68: 1423–1436. doi:10.1051 / jcp / 1971681423.
- ^ a b Clark, Ian; Fritz, Peter (1997). Hidrojeolojide Çevresel İzotoplar. Eos İşlemleri. 80. CRC Press LLC. s. 217. Bibcode:1999EOSTr..80..217Z. doi:10.1029 / 99EO00169. ISBN 978-1566702492.
- ^ Rayleigh, Lord (1902). "İkili karışımların damıtılması hakkında". Philos. Mag. Seri 6. 4 (23): 521–537. doi:10.1080/14786440209462876.
- ^ Craig, Harmon (1961). "Meteorik sularda izotopik değişimler". Bilim. 133 (3465): 1702–1703. Bibcode:1961Sci ... 133.1702C. doi:10.1126 / science.133.3465.1702. PMID 17814749. S2CID 34373069.
- ^ a b c d e Dansgaard Willi (1964). "Çökmede kararlı izotoplar". Bize söyle. 16 (4): 436–468. Bibcode:1964 TellA..16..436D. doi:10.1111 / j.2153-3490.1964.tb00181.x.
- ^ Araguas-Araguas, Luis; Froehlich, Klaus; Rozanski, Kazimierz (1998). "Güneydoğu Asya üzerindeki yağışların istikrarlı izotop bileşimi". Jeofizik Araştırmalar Dergisi. 103 (D22): 28, 721–28, 742. Bibcode:1998JGR ... 10328721A. doi:10.1029 / 98jd02582.
- ^ Cobb, Kim M .; Adkins, Jess F .; Partin, Judson W .; Clark, Brian (2007-11-30). "Bölgesel ölçekli iklim, kuzey Borneo'daki yağmur suyu ve mağara damlama suyu oksijen izotoplarının zamansal değişimlerini etkiler". Dünya ve Gezegen Bilimi Mektupları. 263 (3–4): 207–220. Bibcode:2007E ve PSL.263..207C. doi:10.1016 / j.epsl.2007.08.024.
- ^ Partin, Judson W. (2007). "Son Buzul Maksimumundan bu yana batı Pasifik ılık havuz hidrolojisinde bin yıllık eğilimler". Doğa. 449 (7161): 452–456. Bibcode:2007Natur.449..452P. doi:10.1038 / nature06164. PMID 17898765. S2CID 128764777.
- ^ Wang, Y.J. (2001). "Çin, Hulu Mağarası'ndan yüksek çözünürlüklü, kesinlikle tarihli geç Pleistosen muson kaydı". Bilim. 294 (5550): 2345–2348. Bibcode:2001Sci ... 294.2345W. doi:10.1126 / science.1064618. PMID 11743199. S2CID 26237893.
- ^ Tierney, J. E.; Oppo, D. W .; LeGrande, A. N .; Huang, Y .; Rosenthal, Y .; Linsley, B. K. (2012-10-16). "Holosen döneminde Hint Okyanusu atmosferik dolaşımının Sıcak Havuz hidrokliması üzerindeki etkisi". Jeofizik Araştırmalar Dergisi: Atmosferler. 117 (D19): D19108. Bibcode:2012JGRD..11719108T. doi:10.1029 / 2012JD018060. hdl:1912/5587.
- ^ Niedermeyer, Eva M .; Oturumlar, Alex L .; Feakins, Sarah J .; Mohtadi, Mahyar (2014-07-01). "Batı Hint-Pasifik Sıcak Havuzunun son 24.000 yıldaki hidro iklimi". Ulusal Bilimler Akademisi Bildiriler Kitabı. 111 (26): 9402–9406. Bibcode:2014PNAS..111.9402N. doi:10.1073 / pnas.1323585111. PMC 4084490. PMID 24979768.
- ^ GONFIANTINI, ROBERTO (1986/01/01). YAZI TİPLERİ, J. Ch. (ed.). Bölüm 3 - GÖL ÇALIŞMALARINDA ÇEVRESEL İZOTOPLAR A2 - FRITZ, P. Karasal Çevre, B. Çevresel İzotop Jeokimyası El Kitabı. Amsterdam: Elsevier. s. 113–168. doi:10.1016 / b978-0-444-42225-5.50008-5. ISBN 9780444422255.
- ^ a b Criss, R. E .; Davisson, M.L. (1996-04-15). "Yüzey suyu / yeraltı suyu etkileşimlerinin izotopik görüntülemesi, Sacramento Vadisi, Kaliforniya". Hidroloji Dergisi. 178 (1–4): 205–222. Bibcode:1996JHyd..178..205C. doi:10.1016/0022-1694(96)83733-4.
- ^ Barnes, C. J .; Allison, G. B. (1983-01-01). "Döteryum ve 18O'nun kuru topraklarda dağılımı". Hidroloji Dergisi. 60 (1): 141–156. Bibcode:1983JHyd ... 60..141B. doi:10.1016/0022-1694(83)90018-5.
- ^ Meinzer, Frederick (1999). "Mevsimsel olarak kuru tropikal bir ormanda toprak suyunun gölgelik ağaçları arasında bölüştürülmesi". Oekoloji. 121 (3): 293–301. Bibcode:1999Oecol.121..293M. doi:10.1007 / s004420050931. PMID 28308316. S2CID 20985036.
- ^ a b c d Petit, J. R .; Jouzel, J .; Raynaud, D .; Barkov, N. I .; Barnola, J.-M .; Basile, I .; Bender, M .; Chappellaz, J .; Davis, M. (1999). "Antarktika'daki Vostok buz çekirdeğinden geçen 420.000 yılın iklimi ve atmosferik tarihi." Doğa. 399 (6735): 429–436. Bibcode:1999Natur.399..429P. doi:10.1038/20859. S2CID 204993577.
- ^ Epstein, Samuel; Keskin Robert (1963). "Antarktika kar, ateş ve buzdaki oksijen-izotop oranları". Jeoloji Dergisi. 71 (6): 698–720. Bibcode:1963JG ..... 71..698E. doi:10.1086/626950.
- ^ Lorius, C .; Jouzel, J .; Ritz, C .; Merlivat, L .; Barkov, N. I .; Korotkevich, Y. S .; Kotlyakov, V.M. (1985-08-15). "Antarktika buzundan 150.000 yıllık iklim rekoru". Doğa. 316 (6029): 591–596. Bibcode:1985Natur.316..591L. doi:10.1038 / 316591a0. S2CID 4368173.
- ^ Blunier, Thomas; Brook, Edward J. (2001-01-05). "Son Buzul Döneminde Antarktika ve Grönland'da Bin Yıllık Ölçekli İklim Değişikliğinin Zamanlaması". Bilim. 291 (5501): 109–112. Bibcode:2001Sci ... 291..109B. doi:10.1126 / science.291.5501.109. PMID 11141558.
- ^ Dansgaard Willi (1969). "Grönland buz tabakasındaki Camp Century'den bin asırlık iklim rekoru." Bilim. 166 (3903): 366–370. Bibcode:1969Sci ... 166..377D. doi:10.1126 / science.166.3903.377. PMID 17796550. S2CID 9674822.
- ^ Epstein, Samuel; Sharp, R.P .; Gow, A.J. (1970). "Antarktika Buz Tabakası: Byrd İstasyon Çekirdeklerinin Kararlı İzotop Analizleri ve Hemisferik İklim Etkileri". Bilim. 168 (3939): 1570–1572. Bibcode:1970Sci ... 168.1570E. doi:10.1126 / science.168.3939.1570. PMID 17759337. S2CID 32636862.
- ^ Augustin, Laurent; Barbante, Carlo; Barnes, Piers R. F .; Barnola, Jean Marc; Bigler, Matthias; Castellano, Emiliano; Cattani, Olivier; Chappellaz, Jerome; Dahl-Jensen, Dorthe (2004-06-10). "Antarktika buz çekirdeğinden çıkan sekiz buzul döngüsü". Doğa. 429 (6992): 623–628. Bibcode:2004Natur.429..623A. doi:10.1038 / nature02599. PMID 15190344.
- ^ a b Dansgaard, W. (1993). "250 kyr buz çekirdeğinden alınan geçmiş iklimin genel istikrarsızlığının kanıtı". Doğa. 364 (6434): 218–220. Bibcode:1993Natur.364..218D. doi:10.1038 / 364218a0. S2CID 4304321.
- ^ Buizert, Christo; Gkinis, Vasileios; Severinghaus, Jeffrey P .; O, Feng; Lecavalier, Benoit S .; Kindler, Philippe; Leuenberger, Markus; Carlson, Anders E .; Vinther, Bo (2014-09-05). "Grönland sıcaklığının, son dağılma sırasında iklim zorlamasına tepkisi". Bilim. 345 (6201): 1177–1180. Bibcode:2014Sci ... 345.1177B. doi:10.1126 / science.1254961. PMID 25190795. S2CID 206558186.
- ^ Grönland Buz Çekirdeği Projesi (GRIP) Üyeleri (1993-07-15). "GRIP buz çekirdeğinde kaydedilen son buzullararası dönemde iklim dengesizliği". Doğa. 364 (6434): 203–207. Bibcode:1993Natur.364..203G. doi:10.1038 / 364203a0.
- ^ Heinrich, Hartmut (1988). "Son 130.000 yılda Kuzeydoğu Atlantik Okyanusu'nda döngüsel buz raftinginin kökeni ve sonuçları". Kuvaterner Araştırması. 29 (2): 142–152. Bibcode:1988QuRes..29..142H. doi:10.1016/0033-5894(88)90057-9.
- ^ Broecker, Wallace S. (1994-12-01). "Küresel iklim değişikliğini tetikleyen devasa buzdağı deşarj oluyor". Doğa. 372 (6505): 421–424. Bibcode:1994Natur.372..421B. doi:10.1038 / 372421a0. S2CID 4303031.
- ^ Thompson, L. G .; Mosley-Thompson, E .; Davis, M.E .; Lin, P.-N .; Henderson, K. A .; Cole-Dai, J .; Bolzan, J. F .; Liu, K.-b (1995-07-07). "Huascarán, Peru'dan Geç Buzul Aşaması ve Holosen Tropikal Buz Çekirdeği Kayıtları". Bilim. 269 (5220): 46–50. Bibcode:1995Sci ... 269 ... 46T. doi:10.1126 / science.269.5220.46. PMID 17787701. S2CID 25940751.
- ^ Thompson, L.G. (1997). "Tropikal İklim İstikrarsızlık: Qinghai-Tibet Buz Çekirdeğinden Gelen Son Buzul Döngüsü". Bilim. 276 (5320): 1821–1825. doi:10.1126 / science.276.5320.1821.
- ^ a b c d e f g h ben Sachse, Dirk; Billault, Isabelle; Bowen, Gabriel J .; Chikaraishi, Yoshito; Dawson, Todd E .; Feakins, Sarah J .; Freeman, Katherine H .; Magill, Clayton R .; McInerney, Francesca A. (2012-01-01). "Moleküler Paleohidroloji: Fotosentez Yapan Organizmalardan Lipid Biyobelirteçlerinin Hidrojen-İzotopik Kompozisyonunun Yorumlanması" (PDF). Yeryüzü ve Gezegen Bilimleri Yıllık İncelemesi. 40 (1): 221–249. Bibcode:2012AREPS..40..221S. doi:10.1146 / annurev-earth-042711-105535.
- ^ Schimmelmann, Arndt; Oturumlar, Alex L .; Mastalerz, Maria (2006/01/01). "Diyajenez ve Termal Olgunlaşma Sırasında Organik Maddenin Hidrojen İzotopik (d / H) Bileşimi" (PDF). Yeryüzü ve Gezegen Bilimleri Yıllık İncelemesi. 34 (1): 501–533. Bibcode:2006AREPS..34..501S. doi:10.1146 / annurev.earth.34.031405.125011.
- ^ a b Hou, Juzhi; D'Andrea, William J .; Huang, Yongsong (2008-07-15). "Tortul yaprak mumları, kıtasal yağışların D / H oranlarını kaydedebilir mi? Alan, model ve deneysel değerlendirmeler". Geochimica et Cosmochimica Açta. 72 (14): 3503–3517. Bibcode:2008GeCoA..72.3503H. doi:10.1016 / j.gca.2008.04.030.
- ^ Oturumlar, Alex L .; Hayes, John M. (2005-02-01). "Biyojeokimyasal sistemlerde hidrojen izotopik fraksiyonlarının hesaplanması". Geochimica et Cosmochimica Açta. 69 (3): 593–597. Bibcode:2005GeCoA..69..593S. doi:10.1016 / j.gca.2004.08.005.
- ^ Schiegl, W. E. (1974-10-18). "Picea'nın büyüme halkalarında döteryum bolluğunun iklimsel önemi". Doğa. 251 (5476): 582–584. Bibcode:1974Natur.251..582S. doi:10.1038 / 251582a0. S2CID 4179399.
- ^ a b Yapp, Crayton; Epstein, Samuel (1982). "Ağaç selülozundaki hidrojen izotop oranlarının iklimsel önemi". Doğa. 297 (5868): 236–239. Bibcode:1982Natur.297..636Y. doi:10.1038 / 297636a0. S2CID 42877790.
- ^ a b Roden, John; Lin, Guanghui; Ehleringer James (2000). "Ağaç halkalı selülozda hidrojen ve oksijen izotop oranlarının yorumlanması için mekanik bir model". Geochimica et Cosmochimica Açta. 64 (1): 21–35. Bibcode:2000GeCoA..64 ... 21R. doi:10.1016 / s0016-7037 (99) 00195-7.
- ^ Feng, Xiaohong; Epstein, Samuel (1994). "Bristlecone çam ağaçlarından 8000 yıllık bir hidrojen izotop zaman serisinin iklim etkileri". Bilim. 265 (5175): 1079–1081. Bibcode:1994Sci ... 265.1079F. doi:10.1126 / science.265.5175.1079. PMID 17832901. S2CID 15976057.
- ^ Eglinton, Timothy I .; Eglinton, Geoffrey (2008-10-30). "Paleoklimatoloji için moleküler vekiller". Dünya ve Gezegen Bilimi Mektupları. 275 (1–2): 1–16. Bibcode:2008E ve PSL.275 .... 1E. doi:10.1016 / j.epsl.2008.07.012.
- ^ Ellsworth, Patrick Z .; Williams, David G. (2007-01-17). "Odunsu kserofitler tarafından su alımı sırasında hidrojen izotop fraksiyonasyonu". Bitki ve Toprak. 291 (1–2): 93–107. doi:10.1007 / s11104-006-9177-1. S2CID 27533990.
- ^ Farquhar, Graham D .; Cernusak, Lucas A .; Barnes, Belinda (2007-01-01). "Terleme sırasında ağır su fraksiyonasyonu". Bitki Fizyolojisi. 143 (1): 11–18. doi:10.1104 / s.106.093278. PMC 1761995. PMID 17210909.
- ^ a b c d Sachse, Dirk; Radke, Jens; Gleixner, Gerd (2006-04-01). "İklimsel bir eğim boyunca karasal bitkilerden elde edilen tek tek n-alkanların δD değerleri - Tortul biyobelirteç kaydı için çıkarımlar". Organik Jeokimya. 37 (4): 469–483. doi:10.1016 / j.orggeochem.2005.12.003.
- ^ Sauer, Peter E; Eglinton, Timothy I; Hayes, John M; Schimmelmann, Arndt; Oturumlar, Alex L (2001-01-15). "Çevresel ve iklimsel koşullar için bir vekil olarak çökeltilerden lipit biyobelirteçlerinin bileşiğe özgü D / H oranları1". Geochimica et Cosmochimica Açta. 65 (2): 213–222. Bibcode:2001GeCoA..65..213S. doi:10.1016 / S0016-7037 (00) 00520-2.
- ^ a b c d Zhang, Xinning; Gillespie, Aimee L .; Oturumlar, Alex L. (2009-08-04). "Bakteriyel lipidlerdeki büyük D / H varyasyonları, merkezi metabolik yolları yansıtır". Ulusal Bilimler Akademisi Bildiriler Kitabı. 106 (31): 12580–12586. Bibcode:2009PNAS..10612580Z. doi:10.1073 / pnas.0903030106. PMC 2722351. PMID 19617564.
- ^ Chikaraishi, Yoshito; Naraoka, Hiroshi; Poulson, Simon R. (2004-05-01). "Karasal (C3, C4 ve CAM) ve su bitkileri arasında lipit biyosentezinin hidrojen ve karbon izotopik fraksiyonları". Bitki kimyası. 65 (10): 1369–1381. doi:10.1016 / j.phytochem.2004.03.036. PMID 15231410.
- ^ Chikaraishi, Yoshito; Naraoka, Hiroshi (2003-06-01). "Karasal ve su bitkilerinden elde edilen n-alkanların bileşiğe özgü δD – δ13C analizleri". Bitki kimyası. 63 (3): 361–371. doi:10.1016 / S0031-9422 (02) 00749-5. PMID 12737985.
- ^ Behruzyan, B .; Buist, P.H. (2003-02-01). "Yağ asidi desatürasyonunun mekanizması: biyoorganik bir bakış açısı". Prostaglandinler, Lökotrienler ve Esansiyel Yağ Asitleri. 68 (2): 107–112. doi:10.1016 / s0952-3278 (02) 00260-0. PMID 12538074.
- ^ a b Feakins, Sarah J .; Oturumlar, Alex L. (2010-12-01). "Crassulacean asit metabolizması, sulu bitkilerde yaprak mumunun D / H oranını etkiler". Organik Jeokimya. 41 (12): 1269–1276. doi:10.1016 / j.orggeochem.2010.09.007.
- ^ Chikaraishi, Yoshito; Naraoka, Hiroshi (2007-02-01). "Karasal yüksek bitkilerin üç n-alkil bileşik sınıfı (n-alkanoik asit, n-alkan ve n-alkanol) arasındaki δ13C ve δD ilişkileri". Organik Jeokimya. 38 (2): 198–215. doi:10.1016 / j.orggeochem.2006.10.003.
- ^ Hou, Juzhi; D'Andrea, William J .; MacDonald, Dana; Huang, Yongsong (2007-06-01). "Blood Pond, Massachusetts (ABD) çevresindeki karasal ve sucul bitkiler arasında yaprak mumlarında hidrojen izotopik değişkenlik". Organik Jeokimya. 38 (6): 977–984. doi:10.1016 / j.orggeochem.2006.12.009.
- ^ Pedentchouk, Nikolai; Sumner, William; Tipple, Brett; Pagani, Mark (2008/08/01). "Modern anjiyospermlerden ve kozalaklı ağaçlardan elde edilen n-alkanların δ13C ve δD bileşimleri: Merkezi Washington Eyaleti, ABD'de deneysel bir kurulum". Organik Jeokimya. Organik Jeokimyada Gelişmeler 2007 23. Uluslararası Organik Jeokimya Toplantısı Bildirileri. 39 (8): 1066–1071. doi:10.1016 / j.orggeochem.2008.02.005.
- ^ Kahmen, Ansgar; Dawson, Todd E .; Vieth, Andrea; Sachse, Dirk (2011-10-01). "Yaprak balmumu n-alkan δD değerleri, kontrollü çevresel koşullar altında yetiştirildiğinde Populus trichocarpa yapraklarının ontogenisinde erken belirlenir". Bitki, Hücre ve Çevre. 34 (10): 1639–1651. doi:10.1111 / j.1365-3040.2011.02360.x. PMID 21696403.
- ^ Sachse, Dirk; Kahmen, Ansgar; Gleixner, Gerd (2009-06-01). "Yaprak-balmumu lipidlerinin hidrojen izotopik bileşiminde iki yaprak döken ağaç ekosistemi (Fagus sylvativa ve Acerpseudoplatanus) için önemli mevsimsel değişimler". Organik Jeokimya. 40 (6): 732–742. doi:10.1016 / j.orggeochem.2009.02.008.
- ^ Yang, Hong; Pagani, Mark; Briggs, Derek E. G .; Equiza, M. A .; Jagels, Richard; Leng, Qin; LePage, Ben A. (2009-04-08). "Sürekli ışık altında karbon ve hidrojen izotop fraksiyonasyonu: Paleojen ısınma sırasında Yüksek Arktik'in paleo-çevre yorumları için çıkarımlar". Oekoloji. 160 (3): 461–470. Bibcode:2009Oecol.160..461Y. doi:10.1007 / s00442-009-1321-1. PMID 19352720. S2CID 11540486.
- ^ Schefuß, Enno; Schouten, Stefan; Schneider, Ralph R. (2005). "Son 20.000 yılda Orta Afrika hidrolojisinde iklim kontrolleri". Doğa. 437 (7061): 1003–1006. Bibcode:2005Natur.437.1003S. doi:10.1038 / nature03945. PMID 16222296. S2CID 4397896.
- ^ Tierney, Jessica E .; Russell, James M .; Huang, Yongsong; Damsté, Jaap S. Sinninghe; Hopmans, Ellen C .; Cohen, Andrew S. (2008-10-10). "Son 60.000 Yılda Tropikal Güneydoğu Afrika İkliminde Kuzey Yarımküre Kontrolleri". Bilim. 322 (5899): 252–255. Bibcode:2008Sci ... 322..252T. doi:10.1126 / science.1160485. PMID 18787132. S2CID 7364713.
- ^ Polissar, Pratigya J .; Freeman, Katherine H .; Rowley, David B .; McInerney, Francesca A .; Currie, Brian S. (2009-09-30). "Paleoaltimetry of the Tibetan Plateau from D/H ratios of lipid biomarkers". Dünya ve Gezegen Bilimi Mektupları. 287 (1–2): 64–76. Bibcode:2009E&PSL.287...64P. doi:10.1016/j.epsl.2009.07.037.
- ^ a b Hren, M. T.; Pagani, M .; Erwin, D. M.; Brandon, M. (2010). "Biomarker reconstruction of the early Eocene paleotopography and paleoclimate of the northern Sierra Nevada". Jeoloji. 38 (1): 7–10. Bibcode:2010Geo....38....7H. doi:10.1130/g30215.1.
- ^ a b Kasper, Sebastian; van der Meer, Marcel T. J.; Castañeda, Isla S.; Tjallingii, Rik; Brummer, Geert-Jan A.; Sinninghe Damsté, Jaap S .; Schouten, Stefan (2015-01-01). "Testing the alkenone D/H ratio as a paleo indicator of sea surface salinity in a coastal ocean margin (Mozambique Channel)" (PDF). Organik Jeokimya. 78: 62–68. doi:10.1016/j.orggeochem.2014.10.011.
- ^ a b c Schouten, S.; Ossebaar, J.; Schreiber, K.; Kienhuis, M. V. M.; Langer, G.; Benthien, A.; Bijma, J. (2006-03-15). "The effect of temperature, salinity and growth rate on the stable hydrogen isotopic composition of long chain alkenones produced by Emiliania huxleyi and Gephyrocapsa oceanica" (PDF). Biyojeoloji. 3 (1): 113–119. Bibcode:2006BGeo....3..113S. doi:10.5194/bg-3-113-2006.
- ^ Sachse, Dirk; Sachs, Julian P. (2008-02-01). "Inverse relationship between D/H fractionation in cyanobacterial lipids and salinity in Christmas Island saline ponds". Geochimica et Cosmochimica Acta. 72 (3): 793–806. Bibcode:2008GeCoA..72..793S. doi:10.1016/j.gca.2007.11.022.
- ^ Sachs, Julian P.; Schwab, Valérie F. (2011-01-15). "Hydrogen isotopes in dinosterol from the Chesapeake Bay estuary". Geochimica et Cosmochimica Acta. 75 (2): 444–459. Bibcode:2011GeCoA..75..444S. doi:10.1016/j.gca.2010.10.013.
- ^ a b van der Meer, Marcel T. J.; Baas, Marianne; Rijpstra, W. Irene C.; Marino, Gianluca; Rohling, Eelco J.; Sinninghe Damsté, Jaap S .; Schouten, Stefan (2007-10-30). "Hydrogen isotopic compositions of long-chain alkenones record freshwater flooding of the Eastern Mediterranean at the onset of sapropel deposition". Dünya ve Gezegen Bilimi Mektupları. 262 (3–4): 594–600. Bibcode:2007E&PSL.262..594V. doi:10.1016/j.epsl.2007.08.014.
- ^ a b van der Meer, Marcel T. J.; Sangiorgi, Francesca; Baas, Marianne; Brinkhuis, Henk; Sinninghe Damsté, Jaap S .; Schouten, Stefan (2008-03-30). "Molecular isotopic and dinoflagellate evidence for Late Holocene freshening of the Black Sea". Dünya ve Gezegen Bilimi Mektupları. 267 (3–4): 426–434. Bibcode:2008E&PSL.267..426V. doi:10.1016/j.epsl.2007.12.001.
- ^ a b Coolen, Marco J. L.; Orsi, William D.; Balkema, Cherel; Quince, Christopher; Harris, Keith; Sylva, Sean P.; Filipova-Marinova, Mariana; Giosan, Liviu (2013-05-21). "Evolution of the plankton paleome in the Black Sea from the Deglacial to Anthropocene". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 110 (21): 8609–8614. Bibcode:2013PNAS..110.8609C. doi:10.1073/pnas.1219283110. PMC 3666672. PMID 23650351.
- ^ Pahnke, Katharina; Sachs, Julian P.; Keigwin, Lloyd; Timmermann, Axel; Xie, Shang-Ping (2007-12-01). "Eastern tropical Pacific hydrologic changes during the past 27,000 years from D/H ratios in alkenones". Paleo oşinografi. 22 (4): PA4214. Bibcode:2007PalOc..22.4214P. doi:10.1029/2007PA001468. hdl:1912/3454.
- ^ a b c Mulch, Andreas; Chamberlain, C. Page (2007-10-01). "Stable Isotope Paleoaltimetry in Orogenic Belts – The Silicate Record in Surface and Crustal Geological Archives". Mineraloji ve Jeokimya İncelemeleri. 66 (1): 89–118. Bibcode:2007RvMG...66...89M. doi:10.2138/rmg.2007.66.4.
- ^ Gonfiantini, Roberto (2001). "The altitude effect on the isotopic composition of tropical rains". Kimyasal Jeoloji. 181 (1–4): 147–167. Bibcode:2001ChGeo.181..147G. doi:10.1016/s0009-2541(01)00279-0.
- ^ Rowley, David (2001). "A new approach to stable isotope-based paleoaltimetry: implications for paleoaltimetry and paleohypsometry of the high Himalaya since the late Miocene". Dünya ve Gezegen Bilimi Mektupları. 188 (1–2): 253–268. Bibcode:2001E&PSL.188..253R. doi:10.1016/s0012-821x(01)00324-7.
- ^ a b Jia, Guodong (2008). "Soil n-alkane δD vs. altitude gradients along Mount Gongga, China". Geochimica et Cosmochimica Acta. 72 (21): 5165–5174. Bibcode:2008GeCoA..72.5165J. doi:10.1016/j.gca.2008.08.004.
- ^ O'Neil, James R.; Silberman, Miles L. (1974). "Stable isotope relations in epithermal Au-Ag deposits". Economic Geology. 69 (6): 902–909. doi:10.2113/gsecongeo.69.6.902.
- ^ O'Neil, James; Kharaka, Yousif (1976). "Hydrogen and oxygen isotope exchange reactions between clay minerals and water". Geochimica et Cosmochimica Acta. 40 (2): 241–246. Bibcode:1976GeCoA..40..241O. doi:10.1016/0016-7037(76)90181-2.
- ^ Poage, M. A.; Chamberlain, C. P. (2002-08-01). "Stable isotopic evidence for a Pre-Middle Miocene rain shadow in the western Basin and Range: Implications for the paleotopography of the Sierra Nevada". Tectonics. 21 (4): 16–1. Bibcode:2002Tecto..21.1034P. doi:10.1029/2001TC001303.
- ^ Mulch, Andreas; Teyssier, Christian; Cosca, Michael A.; Vanderhaeghe, Olivier; Vennemann, Torsten W. (2004). "Reconstructing paleoelevation in eroded orogens". Jeoloji. 32 (6): 525. Bibcode:2004Geo....32..525M. doi:10.1130/g20394.1.
- ^ Feakins, Sarah J.; Bentley, Lisa Patrick; Salinas, Norma; Shenkin, Alexander; Blonder, Benjamin; Goldsmith, Gregory R.; Ponton, Camilo; Arvin, Lindsay J.; Wu, Mong Sin (2016-06-01). "Plant leaf wax biomarkers capture gradients in hydrogen isotopes of precipitation from the Andes and Amazon". Geochimica et Cosmochimica Acta. 182: 155–172. Bibcode:2016GeCoA.182..155F. doi:10.1016/j.gca.2016.03.018.
- ^ Wang, Ying (2009). "Equilibrium 2H/1H fractionations in organic molecules. II: Linear alkanes, alkenes, ketones, carboxylic acids, esters, alcohols and ethers". GCA. 73 (23): 7076–7086. Bibcode:2009GeCoA..73.7076W. doi:10.1016/j.gca.2009.08.018.
- ^ Wang, Ying (2013). "Equilibrium 2H/1H fractionation in organic molecules: III. Cyclic ketones and hydrocarbons". GCA. 107: 82–95. Bibcode:2013GeCoA.107...82W. doi:10.1016/j.gca.2013.01.001.
- ^ Sessions, Alex (1999). "Lipit biyosentezinde hidrojen izotoplarının parçalanması". Organik Jeokimya. 30 (9): 1193–1200. doi:10.1016 / S0146-6380 (99) 00094-7.
- ^ a b Pedentchouk, Nikolai (2006). "Different response of δD values of n-alkanes, isoprenoids, and kerogen during thermal maturation". GCA. 70 (8): 2063–2072. Bibcode:2006GeCoA..70.2063P. doi:10.1016/j.gca.2006.01.013.
- ^ Dawson, Daniel; Grice, Kliti; Alexander, Robert; Edwards, Dianne (July 2007). "The effect of source and maturity on the stable isotopic compositions of individual hydrocarbons in sediments and crude oils from the Vulcan Sub-basin, Timor Sea, Northern Australia". Organik Jeokimya. 38 (7): 1015–1038. doi:10.1016/j.orggeochem.2007.02.018.
- ^ a b Tang, Yongchun; Huang, Yongsong; Ellis, Geoffrey S.; Wang, Yi; Kralert, Paul G.; Gillaizeau, Bruno; Ma, Qisheng; Hwang, Rong (September 2005). "A kinetic model for thermally induced hydrogen and carbon isotope fractionation of individual n-alkanes in crude oil". Geochimica et Cosmochimica Acta. 69 (18): 4505–4520. Bibcode:2005GeCoA..69.4505T. doi:10.1016/j.gca.2004.12.026.
- ^ a b c Schimmelmann, Arndt (2004). "D/H ratios in terrestrially sourced petroleum systems". Organik Jeokimya. 35 (10): 1169–1195. doi:10.1016/j.orggeochem.2004.05.006.
- ^ Redding, C.E. (1980). "Hydrogen and carbon isotopic composition of coals and kerogens". Physics and Chemistry of the Earth. 12: 711–723. Bibcode:1980PCE....12..711R. doi:10.1016/0079-1946(79)90152-6.
- ^ Rigby, D.; Batts, B.D.; Smith, J.W. (Ocak 1981). "The effect of maturation on the isotopic composition of fossil fuels". Organik Jeokimya. 3 (1–2): 29–36. doi:10.1016/0146-6380(81)90010-3.
- ^ Smith, J.W. (1983). "D/H ratio of coals and palaeolatitude of their deposition". Doğa. 302 (5906): 322–323. Bibcode:1983Natur.302..322S. doi:10.1038/302322a0. S2CID 4317372.
- ^ Lis, Grzegorz (2006). "D/H ratios and hydrogen exchangeability of type-II kerogens with increasing thermal maturity". Organik Jeokimya. 37 (3): 342–353. doi:10.1016/j.orggeochem.2005.10.006.
- ^ a b c Liu, Quanyou (2008). "Hydrogen isotope composition of natural gases from the Tarim Basin and its indication of depositional environments of the source rocks". Science in China Series D: Earth Sciences. 51 (2): 300–311. doi:10.1007/s11430-008-0006-7. S2CID 140549821.
- ^ Prinzhofer, Alain (1995). "Genetic and post-genetic molecular and isotopic fractionations in natural gases". Kimyasal Jeoloji. 126 (3–4): 281–290. Bibcode:1995ChGeo.126..281P. doi:10.1016/0009-2541(95)00123-9.
- ^ Burruss, R.C. (2010). "Carbon and hydrogen isotopic reversals in deep basin gas: Evidence for limits to the stability of hydrocarbons". Organik Jeokimya. 41 (12): 1285–1296. doi:10.1016/j.orggeochem.2010.09.008.
- ^ Telling, Jon (2013). "Carbon and Hydrogen Isotopic Composition of Methane and C2 + Alkanes in Electrical Spark Discharge: Implications for Identifying Sources of Hydrocarbons in Terrestrial and Extraterrestrial Settings". Astrobiology. 13 (5): 483–490. Bibcode:2013AsBio..13..483T. doi:10.1089/ast.2012.0915. PMID 23683048.
- ^ Flanagan, Lawrence B .; Ehleringer, James R .; Pataki, Diane E. (2004-12-15). Stable Isotopes and Biosphere – Atmosphere Interactions: Processes and Biological Controls. Akademik Basın. ISBN 9780080525280.
- ^ Bilek, R. S.; Tyler, S. C.; Kurihara, M .; Yagi, K. (July 2001). "Investigation of cattle methane production and emission over a 24-hour period using measurements of δ13C and δD of emitted CH4 and rumen water". Journal of Geophysical Research. 106 (D14): 2156–2202. Bibcode:2001JGR...10615405B. doi:10.1029/2001JD900177.
- ^ Eiler, John (2007). ""Clumped-isotope" geochemistry—The study of naturally-occurring, multiply-substituted isotopologues". Dünya ve Gezegen Bilimi Mektupları. 262 (3–4): 309–327. Bibcode:2007E&PSL.262..309E. doi:10.1016/j.epsl.2007.08.020.
- ^ Stolper, Daniel (2014). "Formation temperatures of thermogenic and biogenic methane" (PDF). Bilim. 344 (6191): 1500–1503. Bibcode:2014Sci...344.1500S. doi:10.1126/science.1254509. PMID 24970083. S2CID 31569235.
- ^ a b Wang, David (2015). "Nonequilibrium clumped isotope signals in microbial methane". Bilim. 348 (6233): 428–431. Bibcode:2015Sci...348..428W. doi:10.1126 / science.aaa4326. hdl:1721.1/95903. PMID 25745067. S2CID 206634401.
- ^ Clog, M.D. (2014). "Ethane C-C clumping in natural gas : a proxy for cracking processes?". AGÜ Güz Toplantısı Özetleri. 2014: 54A–06. Bibcode:2014AGUFMPP54A..06C.
- ^ Tang, Y.; Perry, J. K.; Jenden, P. D.; Schoell, M. (1 August 2000). "Mathematical modeling of stable carbon isotope ratios in natural gases†". Geochimica et Cosmochimica Acta. 64 (15): 2673–2687. Bibcode:2000GeCoA..64.2673T. doi:10.1016/S0016-7037(00)00377-X.
- ^ Waseda, Amane (1993). "Effect of maturity on carbon and hydrogen isotopes of crude oils in Northeast Japan". Journal of the Japanese Association for Petroleum Technology. 58 (3): 199–208. doi:10.3720/japt.58.199.
- ^ a b Li, Maowen; Huang, Yongsong; Obermajer, Mark; Jiang, Chunqing; Snowdon, Lloyd R; Fowler, Martin G (December 2001). "Hydrogen isotopic compositions of individual alkanes as a new approach to petroleum correlation: case studies from the Western Canada Sedimentary Basin". Organik Jeokimya. 32 (12): 1387–1399. doi:10.1016/S0146-6380(01)00116-4.
- ^ Xiong, Yongqiang (2007). "Compound-specific C- and H-isotope compositions of enclosed organic matter in carbonate rocks: Implications for source identification of sedimentary organic matter and paleoenvironmental reconstruction". Applied Geochemistry. 22 (11): 2553–2565. Bibcode:2007ApGC...22.2553X. doi:10.1016/j.apgeochem.2007.07.009.
- ^ Dawson, Daniel; Grice, Kliti; Wang, Sue X; Alexander, Robert; Radke, Jens (February 2004). "Stable hydrogen isotopic composition of hydrocarbons in torbanites (Late Carboniferous to Late Permian) deposited under various climatic conditions". Organik Jeokimya. 35 (2): 189–197. doi:10.1016/j.orggeochem.2003.09.004.
- ^ Goldsmith, Gregory R.; Muñoz-Villers, Lyssette E.; Holwerda, Friso; McDonnell, Jeffrey J.; Asbjornsen, Heidi; Dawson, Todd E. (2012-11-01). "Stable isotopes reveal linkages among ecohydrological processes in a seasonally dry tropical montane cloud forest". Ekohidroloji. 5 (6): 779–790. doi:10.1002/eco.268.
- ^ Koeniger, Paul; Leibundgut, Christian; Link, Timothy; Marshall, John D. (2010-01-01). "Stable isotopes applied as water tracers in column and field studies". Organik Jeokimya. Stable Isotopes in Biogeosciences (III). 41 (1): 31–40. doi:10.1016/j.orggeochem.2009.07.006.
- ^ a b Dawson, Todd E .; Ehleringer, James R. (1991-03-28). "Streamside trees that do not use stream water". Doğa. 350 (6316): 335–337. Bibcode:1991Natur.350..335D. doi:10.1038/350335a0. S2CID 4367205.
- ^ Limm, Emily Burns; Simonin, Kevin A.; Bothman, Aron G.; Dawson, Todd E. (2009-09-01). "Foliar water uptake: a common water acquisition strategy for plants of the redwood forest". Oekoloji. 161 (3): 449–459. Bibcode:2009Oecol.161..449L. doi:10.1007/s00442-009-1400-3. PMC 2727584. PMID 19585154.
- ^ Farquhar, Graham D.; Cernusak, Lucas A.; Barnes, Belinda (2007-01-01). "Heavy Water Fractionation during Transpiration". Plant Physiology. 143 (1): 11–18. doi:10.1104/pp.106.093278. PMC 1761995. PMID 17210909.
- ^ a b Hou, Juzhi; D'Andrea, William J.; MacDonald, Dana; Huang, Yongsong (2007-08-01). "Evidence for water use efficiency as an important factor in determining the δD values of tree leaf waxes". Organik Jeokimya. 38 (8): 1251–1255. doi:10.1016/j.orggeochem.2007.03.011.
- ^ Craig, Harmon; Gordon, Louis Irwin (1965-01-01). Deuterium and Oxygen 18 Variations in the Ocean and the Marine Atmosphere. Consiglio nazionale delle richerche, Laboratorio de geologia nucleare.
- ^ Roden, John S.; Ehleringer, James R. (1999-08-01). "Observations of Hydrogen and Oxygen Isotopes in Leaf Water Confirm the Craig-Gordon Model under Wide-Ranging Environmental Conditions". Plant Physiology. 120 (4): 1165–1174. doi:10.1104/pp.120.4.1165. PMC 59350. PMID 10444100.
- ^ Calder, Ian R. (1992-01-01). "Deuterium tracing for the estimation of transpiration from trees Part 2. Estimation of transpiration rates and transpiration parameters using a time-averaged deuterium tracing method". Hidroloji Dergisi. 130 (1): 27–35. Bibcode:1992JHyd..130...27C. doi:10.1016/0022-1694(92)90101-Z.
- ^ a b c Schwendenmann, Luitgard; Dierick, Diego; Köhler, Michael; Hölscher, Dirk (2010-07-01). "Can deuterium tracing be used for reliably estimating water use of tropical trees and bamboo?". Tree Physiology. 30 (7): 886–900. doi:10.1093/treephys/tpq045. PMID 20516485.
- ^ Hobson, Keith A. (1999-08-01). "Tracing origins and migration of wildlife using stable isotopes: a review". Oekoloji. 120 (3): 314–326. Bibcode:1999Oecol.120..314H. doi:10.1007/s004420050865. PMID 28308009. S2CID 10231727.
- ^ Flockhart, D. T. Tyler; Wassenaar, Leonard I.; Martin, Tara G.; Hobson, Keith A.; Wunder, Michael B.; Norris, D. Ryan (2013-10-07). "Tracking multi-generational colonization of the breeding grounds by monarch butterflies in eastern North America". Londra B Kraliyet Cemiyeti Bildirileri: Biyolojik Bilimler. 280 (1768): 20131087. doi:10.1098/rspb.2013.1087. PMC 3757963. PMID 23926146.
- ^ Pylant, Cortney L.; Nelson, David M.; Keller, Stephen R. (2014-10-16). "Stable hydrogen isotopes record the summering grounds of eastern red bats (Lasiurus borealis)". PeerJ. 2: e629. doi:10.7717/peerj.629. PMC 4203026. PMID 25337458.
- ^ a b Hardesty, Jessica L.; Fraser, Kevin C. (2010-03-01). "Using deuterium to examine altitudinal migration by Andean birds". Alan Ornitoloji Dergisi. 81 (1): 83–91. doi:10.1111/j.1557-9263.2009.00264.x.
- ^ Fritz, P. (2013-10-22). The Terrestrial Environment, B. Elsevier. ISBN 9781483289830.
- ^ Cryan, Paul M.; Bogan, Michael A.; Rye, Robert O.; Landis, Gary P.; Kester, Cynthia L. (2004-10-20). "Stable Hydrogen Isotope Analysis of Bat Hair as Evidence for Seasonal Molt and Long-Distance Migration". Journal of Mammalogy. 85 (5): 995–1001. doi:10.1644/BRG-202.
- ^ a b Soto, David X.; Wassenaar, Leonard I.; Hobson, Keith A. (2013-04-01). "Stable hydrogen and oxygen isotopes in aquatic food webs are tracers of diet and provenance". Fonksiyonel Ekoloji. 27 (2): 535–543. doi:10.1111/1365-2435.12054.
- ^ Hobson, Keith A.; Atwell, Lisa; Wassenaar, Leonard I. (1999-07-06). "Influence of drinking water and diet on the stable-hydrogen isotope ratios of animal tissues". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 96 (14): 8003–8006. Bibcode:1999PNAS...96.8003H. doi:10.1073/pnas.96.14.8003. PMC 22177. PMID 10393937.
- ^ Peters, Jacob M.; Wolf, Nathan; Stricker, Craig A.; Collier, Timothy R.; Rio, Carlos Martínez del (2012-03-28). "Effects of Trophic Level and Metamorphosis on Discrimination of Hydrogen Isotopes in a Plant-Herbivore System". PLOS ONE. 7 (3): e32744. Bibcode:2012PLoSO...732744P. doi:10.1371/journal.pone.0032744. PMC 3314649. PMID 22470423.
- ^ Birchall, Jennifer; O'connell, Tamsin C.; Heaton, Tim H. E.; Hedges, Robert E. M. (2005-09-01). "Hydrogen isotope ratios in animal body protein reflect trophic level". Hayvan Ekolojisi Dergisi. 74 (5): 877–881. doi:10.1111/j.1365-2656.2005.00979.x.
- ^ Solomon, Christopher T.; Cole, Jonathan J.; Doucett, Richard R.; Pace, Michael L.; Preston, Nicholas D.; Smith, Laura E.; Weidel, Brian C. (2009-08-01). "The influence of environmental water on the hydrogen stable isotope ratio in aquatic consumers". Oekoloji. 161 (2): 313–324. Bibcode:2009Oecol.161..313S. doi:10.1007/s00442-009-1370-5. PMID 19471971. S2CID 12098584.
- ^ Dirghangi, Sitindra S.; Pagani, Mark (2013-10-15). "Hydrogen isotope fractionation during lipid biosynthesis by Haloarcula marismortui". Geochimica et Cosmochimica Acta. 119: 381–390. Bibcode:2013GeCoA.119..381D. doi:10.1016/j.gca.2013.05.023.
- ^ a b Fischer, Curt R.; Bowen, Benjamin P.; Pan, Chongle; Northen, Trent R.; Banfield, Jillian F. (2013-08-16). "Stable-Isotope Probing Reveals That Hydrogen Isotope Fractionation in Proteins and Lipids in a Microbial Community Are Different and Species-Specific". ACS Kimyasal Biyoloji. 8 (8): 1755–1763. doi:10.1021/cb400210q. PMID 23713674.
- ^ Osburn, Magdalena R.; Oturumlar, Alex L .; Pepe-Ranney, Charles; Spear, John R. (2011-09-01). "Hydrogen-isotopic variability in fatty acids from Yellowstone National Park hot spring microbial communities". Geochimica et Cosmochimica Acta. 75 (17): 4830–4845. Bibcode:2011GeCoA..75.4830O. doi:10.1016/j.gca.2011.05.038.
- ^ Zhang, Zhaohui; Sachs, Julian P.; Marchetti, Adrian (2009-03-01). "Hydrogen isotope fractionation in freshwater and marine algae: II. Temperature and nitrogen limited growth rate effects". Organik Jeokimya. 40 (3): 428–439. doi:10.1016/j.orggeochem.2008.11.002.
- ^ Wang, Zhendi; Fingas, Merv F. (2003). "Development of oil hydrocarbon fingerprinting and identification techniques". Deniz Kirliliği Bülteni. 47 (9–12): 423–452. doi:10.1016/S0025-326X(03)00215-7. PMID 12899888.
- ^ Kvenvolden, Keith A.; Hostettler, Frances D.; Rapp, John B.; Carlson, Paul R. (1993). "Hydrocarbons in oil residues on beaches of islands of Prince William Sound, Alaska". Deniz Kirliliği Bülteni. 26 (1): 24–29. doi:10.1016/0025-326X(93)90593-9.
- ^ Kaplan, Isaac R.; Galperin, Yakov; Lu, Shan-Tan; Lee, Ru-Po (1997). "Forensic Environmental Geochemistry: differentiation of fuel-types, their sources and release time". Organik Jeokimya. 27 (5–6): 289–317. doi:10.1016/S0146-6380(97)87941-7.
- ^ Reddy, C. M.; Arey, J. S.; Seewald, J. S.; Sylva, S. P.; Lemkau, K. L.; Nelson, R. K.; Carmichael, C. A.; McIntyre, C. P.; Fenwick, J.; Ventura, G. T.; Van Mooy, B. A. S.; Camilli, R. (2011). "Composition and fate of gas and oil released to the water column during the Deepwater Horizon oil spill". Ulusal Bilimler Akademisi Bildiriler Kitabı. 109 (50): 20229–20234. Bibcode:2012PNAS..10920229R. doi:10.1073/pnas.1101242108. PMC 3528605. PMID 21768331.
- ^ Sun, Yongge; Chen, Zhenyan; Xu, Shiping; Cai, Pingxia (2005). "Stable carbon and hydrogen isotopic fractionation of individual n-alkanes accompanying biodegradation: evidence from a group of progressively biodegraded oils". Organik Jeokimya. 36 (2): 225–238. doi:10.1016/j.orggeochem.2004.09.002.
- ^ Pond, Kristy L.; Huang, Yongsong; Wang, Yi; Kulpa, Charles F. (2002). "Hydrogen Isotopic Composition of Individualn-Alkanes as an Intrinsic Tracer for Bioremediation and Source Identification of Petroleum Contamination". Environmental Science & Technology. 36 (4): 724–728. Bibcode:2002EnST...36..724P. doi:10.1021/es011140r. PMID 11878389.
- ^ Gray, Jennifer R.; Lacrampe-Couloume, Georges; Gandhi, Deepa; Scow, Kate M.; Wilson, Ryan D.; Mackay, Douglas M.; Sherwood Lollar, Barbara (2002). "Carbon and Hydrogen Isotopic Fractionation during Biodegradation of Methyltert-Butyl Ether". Environmental Science & Technology. 36 (9): 1931–1938. Bibcode:2002EnST...36.1931G. doi:10.1021/es011135n. PMID 12026973.
- ^ Morasch, B.; Richnow, H. H.; Schink, B.; Meckenstock, R. U. (2001). "Stable Hydrogen and Carbon Isotope Fractionation during Microbial Toluene Degradation: Mechanistic and Environmental Aspects". Uygulamalı ve Çevresel Mikrobiyoloji. 67 (10): 4842–4849. doi:10.1128/AEM.67.10.4842-4849.2001. PMC 93239. PMID 11571192.
- ^ Ward, Julie A. M.; Ahad, Jason M. E.; Lacrampe-Couloume, Georges; Slater, Greg F.; Edwards, Elizabeth A.; Lollar, Barbara Sherwood (2000). "Hydrogen Isotope Fractionation during Methanogenic Degradation of Toluene: Potential for Direct Verification of Bioremediation". Environmental Science & Technology. 34 (21): 4577–4581. Bibcode:2000EnST...34.4577W. doi:10.1021/es001128j.
- ^ Mancini, Silvia A.; Lacrampe-Couloume, Georges; Jonker, Hendrikus; van Breukelen, Boris M.; Groen, Jacobus; Volkering, Frank; Sherwood Lollar, Barbara (2002-06-01). "Hydrogen Isotopic Enrichment: An Indicator of Biodegradation at a Petroleum Hydrocarbon Contaminated Field Site". Environmental Science & Technology. 36 (11): 2464–2470. Bibcode:2002EnST...36.2464M. doi:10.1021/es011253a. PMID 12075805.
- ^ Steinbach, Alfred; Seifert, Richard; Annweiler, Eva; Michaelis, Walter (2004-01-01). "Hydrogen and Carbon Isotope Fractionation during Anaerobic Biodegradation of Aromatic HydrocarbonsA Field Study". Environmental Science & Technology. 38 (2): 609–616. Bibcode:2004EnST...38..609S. doi:10.1021/es034417r. PMID 14750739.
- ^ Fink, Kathrin; Richling, Elke; Heckel, Frank; Schreier, Peter (2004). "Determination of2H/1H and13C/12C Isotope Ratios of (E)-Methyl Cinnamate from Different Sources Using Isotope Ratio Mass Spectrometry". Tarım ve Gıda Kimyası Dergisi. 52 (10): 3065–3068. doi:10.1021/jf040018j. PMID 15137854.
- ^ Tamura, Hirotoshi; Appel, Markus; Richling, Elke; Schreier, Peter (2005). "Authenticity Assessment of γ- and δ-Decalactone fromPrunusFruits by Gas Chromatography Combustion/Pyrolysis Isotope Ratio Mass Spectrometry (GC-C/P-IRMS)". Tarım ve Gıda Kimyası Dergisi. 53 (13): 5397–5401. doi:10.1021/jf0503964. PMID 15969525.
- ^ Richling, Elke; Preston, Christina; Kavvadias, Dominique; Kahle, Kathrin; Heppel, Christopher; Hummel, Silvia; König, Thorsten; Schreier, Peter (2005). "Determination of the2H/1H and15N/14N Ratios of Alkylpyrazines from Coffee Beans (Coffea arabicaL. andCoffea canephoravar.robusta) by Isotope Ratio Mass Spectrometry". Tarım ve Gıda Kimyası Dergisi. 53 (20): 7925–7930. doi:10.1021/jf0509613. PMID 16190651.
- ^ Piper, Thomas; Thevis, Mario; Flenker, Ulrich; Schänzer, Wilhelm (2009). "Determination of the deuterium/hydrogen ratio of endogenous urinary steroids for doping control purposes". Kütle Spektrometresinde Hızlı İletişim. 23 (13): 1917–1926. doi:10.1002/rcm.4098. PMID 19462405.
- ^ Piper, Thomas; Degenhardt, Karoline; Federherr, Eugen; Thomas, Andreas; Thevis, Mario; Saugy, Martial (2012). "Effect of changes in the deuterium content of drinking water on the hydrogen isotope ratio of urinary steroids in the context of sports drug testing" (PDF). Analitik ve Biyoanalitik Kimya. 405 (9): 2911–2921. doi:10.1007/s00216-012-6504-7. PMID 23128907. S2CID 206911124.
- ^ Jasper, J.P.; Westenberger, B.J.; Spencer, J.A.; Buhse, L.F.; Nasr, M. (2004). "Stable isotopic characterization of active pharmaceutical ingredients". İlaç ve Biyomedikal Analiz Dergisi. 35 (1): 21–30. doi:10.1016/S0731-7085(03)00581-8. PMID 15030876.
- ^ Wokovich, A.M.; Spencer, J.A.; Westenberger, B.J.; Buhse, L.F.; Jasper, J.P. (2005). "Stable isotopic composition of the active pharmaceutical ingredient (API) naproxen". İlaç ve Biyomedikal Analiz Dergisi. 38 (4): 781–784. doi:10.1016/j.jpba.2005.02.033. PMID 15967309.
- ^ Jasper, J.P.; Weaner, L.E.; Duffy, B.J. (2005). "A preliminary multi-stable-isotopic evaluation of three synthetic pathways of Topiramate". İlaç ve Biyomedikal Analiz Dergisi. 39 (1–2): 66–75. doi:10.1016/j.jpba.2005.03.011. PMID 15925470.
- ^ Felton, Linda A.; Shah, Punit P.; Sharp, Zachary; Atudorei, Viorel; Timmins, Graham S. (2010). "Stable isotope-labeled excipients for drug product identification and counterfeit detection". İlaç Geliştirme ve Endüstriyel Eczacılık. 37 (1): 88–92. doi:10.3109/03639045.2010.492397. PMID 20560792. S2CID 25064362.
- ^ Acetti, Daniela; Brenna, Elisabetta; Fronza, Giovanni; Fuganti, Claudio (2008). "Monitoring the synthetic procedures of commercial drugs by 2H NMR spectroscopy: The case of ibuprofen and naproxen". Talanta. 76 (3): 651–655. doi:10.1016/j.talanta.2008.04.009. PMID 18585334.
- ^ Brenna, Elisabetta; Fronza, Giovanni; Fuganti, Claudio (2007). "Traceability of synthetic drugs by position-specific deuterium isotope ratio analysis". Analytica Chimica Açta. 601 (2): 234–239. doi:10.1016/j.aca.2007.08.047. PMID 17920397.
- ^ Carter, James F.; Titterton, Emma L.; Murray, Martin; Sleeman, Richard (2002). "Isotopic characterisation of 3,4-methylenedioxyamphetamine and 3,4-methylenedioxymethylamphetamine (ecstasy)". The Analyst. 127 (6): 830–833. Bibcode:2002Ana...127..830C. doi:10.1039/b201496n. PMID 12146919. S2CID 7161041.
- ^ Idoine, Fay A.; Carter, James F.; Sleeman, Richard (2005). "Bulk and compound-specific isotopic characterisation of illicit heroin and cling film". Kütle Spektrometresinde Hızlı İletişim. 19 (22): 3207–3215. Bibcode:2005RCMS...19.3207I. doi:10.1002/rcm.2153. PMID 16220464.
- ^ Hays, Patrick A.; Remaud, Gérald S.; Jamin, Éric; Martin, Yves-Loïc (2000). "Geographic Origin Determination of Heroin and Cocaine Using Site-Specific Isotopic Ratio Deuterium NMR". Adli Bilimler Dergisi. 45 (3): 14728J. doi:10.1520/JFS14728J.
- ^ Ehleringer, J. R.; Bowen, G. J.; Chesson, L. A.; West, A. G.; Podlesak, D. W.; Cerling, T. E. (2008). "Hydrogen and oxygen isotope ratios in human hair are related to geography". Ulusal Bilimler Akademisi Bildiriler Kitabı. 105 (8): 2788–2793. Bibcode:2008PNAS..105.2788E. doi:10.1073/pnas.0712228105. PMC 2268538. PMID 18299562.
- ^ Chesson, L. A.; Tipple, B. J.; Howa, J. D.; Bowen, G. J.; Barnette, J. E.; Cerling, T. E.; Ehleringer, J. R. (2014-01-01). Turekian, Karl K. (ed.). 14.19 - Stable Isotopes in Forensics Applications A2 - Holland, Heinrich D. Oxford: Elsevier. pp. 285–317. doi:10.1016/b978-0-08-095975-7.01224-9. ISBN 9780080983004.











![{ displaystyle delta _ {hata} = (R_ {std}) [( delta _ {A} - delta _ {B}) / 2] ^ {2}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b9e75bbdba61b6e69549fea3e203581ccaca9704)