Relaps - Relapse
Eczanede, nüksetmek veya tekrar suçlama geçmiş (tipik olarak tıbbi) bir durumun tekrarlamasıdır. Örneğin, multipl Skleroz ve sıtma genellikle en yüksek aktivite ve bazen çok uzun uyku dönemleri sergiler, ardından nüks veya tekrarlama.
Bağlamında uyuşturucu madde kullanım nüksetmek veya uyuşturucu arama davranışının eski haline getirilmesi, bir biçimdir kendiliğinden iyileşme bir süre sonra patolojik ilaç kullanımının tekrarlanmasını içeren kaçınma. Nüks genellikle bir uyuşturucu bağımlılığı veya herhangi bir şekilde Uyuşturucu bağımlısı.
Risk faktörleri
Dopamin D2 reseptör mevcudiyeti
Kullanılabilirliği dopamin reseptörü D2 rol oynar öz yönetim ve güçlendirici etkiler nın-nin kokain ve diğeri uyarıcılar. D2 reseptör mevcudiyeti bir ters ilişki güçlendirme etkilerine karşı savunmasızlığa uyuşturucu madde. Yani, D2 reseptörleri sınırlı hale geldikçe, kullanıcı kokainin güçlendirici etkilerine daha duyarlı hale gelir. Şu anda bilinmeyen bir yatkınlık düşük D2 reseptör kullanılabilirliği mümkündür; ancak çoğu çalışma, D2 reseptör mevcudiyetindeki değişikliklerin bir sonuç yerine öncü kokain kullanımı. Ayrıca, D2 reseptörlerinin uzun süre ilaç maruziyetinden önceki seviyeye geri dönebileceği de kaydedilmiştir. kaçınma nüksetmede etkileri olabilecek bir gerçek tedavi.[1]
Sosyal hiyerarşi
Sosyal etkileşimler oluşumu gibi doğrusal hakimiyet hiyerarşileri uyuşturucu bağımlılığına karşı savunmasızlıkta da rol oynar. Hayvan çalışmaları arasında D2 reseptörü mevcudiyetinde bir fark olduğunu ileri sürmek baskın ve bir içindeki ikincil hayvanlar Sosyal hiyerarşi kokainin işlevindeki farklılığın yanı sıra pekiştirmek bu hayvan gruplarında kendi kendine uygulama. Sosyal olarak baskın hayvanlar, D2 reseptörlerinin daha yüksek bulunabilirliğini sergiler ve kendi kendine uygulamayı sürdürmede başarısız olur.[2]
Tetikleyiciler
Uyuşturucu alma ve nüks, aşağıdakiler de dahil olmak üzere bir dizi faktörden büyük ölçüde etkilenir. farmakokinetik, doz, ve nörokimya uyuşturucunun kendisinin yanı sıra uyuşturucu kullananların çevre ve uyuşturucuya bağlı geçmiş. Bir süre kullanmama veya yoksun bırakma döneminden sonra uyuşturucu kullanımının eski haline döndürülmesi, tipik olarak üç ana tetikleyicinin biri veya bir kombinasyonu ile başlatılır: stres, ilaca veya ilaca yeniden maruz kalma ve çevresel ipuçları. Bu faktörler bir nörokimyasal Uyuşturucu alıcıda ilacı taklit eden ve böylece eski haline döndürmeyi tetikleyen yanıt.[3] Bu ipuçları, uyuşturucuyu kullanmak için güçlü bir istek veya niyete yol açabilir. özlem tarafından Abraham Wikler Aşerme eğilimi, nüksetmeye yönelik üç tetikleyicinin hepsinden büyük ölçüde etkilenmiştir ve şu anda kabul edilen bir ayırt edici özelliktir. Madde bağımlılığı.[4] Stres, uyuşturucu kullanımını eski haline getirmenin en güçlü uyaranlarından biridir çünkü stres ipuçları, aşerme ve uyuşturucu arama davranışını uyarır. kaçınma. Stres kaynaklı aşerme aynı zamanda nüksetme süresinin de tahminidir. Benzer şekilde, bağımlı bireyler daha fazla stres faktörleri bağımlı olmayan kontrollere göre. Eski haline döndürmeye neden olabilecek stresör örnekleri arasında korku, üzüntü veya öfke ayak şoku veya yüksek ses seviyesi gibi fiziksel bir stres veya sosyal bir olay.[5] Uyuşturucuyu hazırlama, uzak duran kullanıcıyı kötüye kullanım ilacına maruz bırakıyor, bu da uyuşturucu arama davranışının eski haline dönmesine ve uyuşturucunun kendi kendine uygulanmasına neden olacak.[6] Belirli bir ilaçla veya o ilacın kullanımıyla önceden var olan bir ilişkisi olan uyaranlar, hem aşermeyi hem de eski haline dönmeyi tetikleyebilir. Bu ipuçları, uyuşturucuyla ilişkili herhangi bir öğeyi, yeri veya kişileri içerir.[7]
Tedavi
Relaps tedavisi biraz yanlış isim çünkü nüksün kendisi bir tedavi başarısızlığıdır; bununla birlikte, uyuşturucunun nüksetme olasılığını azaltmak için halihazırda kullanılan üç ana yaklaşım vardır. Bunlar arasında farmakoterapi, bilişsel davranış teknikleri, ve acil durum yönetimi. Madde bağımlılığını tedavi etmenin ve nüksü önlemenin temel hedefleri, ihtiyaçlar daha önce ilacın kullanımıyla karşılanan ve bu ihtiyaçları alternatif bir şekilde karşılamak için gerekli becerileri geliştirmek.[7]
Farmakoterapi
- İlgili makale: İlaç rehabilitasyonu
Çeşitli ilaçlar bağımlı bir kullanıcıyı stabilize etmek, ilk uyuşturucu kullanımını azaltmak ve ilacın eski haline döndürülmesini önlemek için kullanılır. İlaçlar, ilaçlarda meydana gelen uzun vadeli değişiklikleri normalleştirebilir. beyin ve gergin sistem uzun süreli ilaç kullanımının bir sonucu olarak. Bu terapi yöntemi karmaşık ve çok yönlüdür çünkü ilacı kullanma arzusu için beyin hedefi, ilacın kendisinin neden olduğu hedeften farklı olabilir.[8] Çeşitli mevcudiyet nörotransmiter reseptörleri, benzeri dopamin reseptörü D2 ve içindeki değişiklikler medial prefrontal korteks ilaçla indüklenen, stresle indüklenen ve işaret kaynaklı relaps ile büyük ölçüde bağlantılı olduklarından, nüksü önlemek için farmakoterapi için önemli hedeflerdir. Reseptör kurtarma olabilir yukarı regüle edilmiş yönetimi ile reseptör antagonistleri farmakoterapötik tedaviler ise neruoadaptations medial prefrontal kortekste, bunlar hakkında bilgi eksikliğinden dolayı hala nispeten etkisizdir. uyarlamalar üzerinde moleküler ve hücresel seviyesi.[1][9]
Bilişsel davranış teknikleri
Nüksü tedavi etmeye yönelik çeşitli davranışsal yaklaşımlar, uyuşturucu kullanımı ve eski haline getirmenin öncüllerine ve sonuçlarına odaklanır. Bilişsel davranışçı teknikler (CBT) şunları içerir: Pavlovcu şartlandırma ve edimsel koşullanma, ile karakterize edilen Pozitif takviye ve olumsuz pekiştirme değiştirmek için bilişler, düşünceler, ve duygular uyuşturucu alma davranışıyla ilişkili. BDT'nin ana bir yaklaşımı, maddenin uyuşturucu arama davranışını tetikleme yeteneğini kademeli olarak yitireceği umuduyla, yoksun kullanıcının maddeye maruz kalmadan tekrar tekrar en belirgin tetikleyicilere maruz kaldığı işaret maruziyetidir. Bu yaklaşım, bir nüksün tamamen meydana gelmesini önlemekten çok, muhtemelen bir nüksün şiddetini azaltacaktır. Başka bir yöntem bağımlılara temel öğretir başa çıkma mekanizmaları kullanmaktan kaçınmak için yasadışı uyuşturucu. Herhangi bir eksikliğin giderilmesi önemlidir. başa çıkma becerileri, uyandırması muhtemel ihtiyaçları belirlemek için uyuşturucu arayan ve onlarla tanışmanın başka bir yolunu geliştirmek.[10]
Nüks önleme
Nüks önleme nüksetmeye katkıda bulunan faktörleri iki geniş kategoriye ayırmaya çalışır: anlık belirleyiciler ve gizli öncüller. Anlık belirleyiciler, bir bireyin kontrol duygusunu tehdit eden yüksek riskli durumlar dahil olmak üzere, nüks ile ilişkili çevresel ve duygusal durumlardır. başa çıkma stratejileri, ve sonuç beklentileri. Nüksü etkileyen daha az belirgin faktörler olan gizli öncüller, stres seviyesi ve denge gibi yaşam tarzı faktörlerini ve dürtüleri ve istek. Nüks önleme modeli, bağımlılara çeşitli ani belirleyicileri ve gizli öncülleri tanıyarak ve bunlarla başa çıkarak nüksü tahmin etmeyi öğretir. RP modeli, tedavi ile en büyük başarıyı gösterir. alkolizm ancak diğer tedavi seçeneklerinden üstünlüğü kanıtlanmamıştır.[7][10]
Acil durum yönetimi
Yukarıdaki davranışsal yaklaşımların aksine, acil durum yönetimi öncüllerinin aksine uyuşturucu kullanımının sonuçlarına odaklanmaktadır. Bağımlı davranış takviyeli ödül veya ceza, kalma yeteneğine göre çekingen. Acil durum yönetiminin yaygın bir örneği, jeton veya kupon sistemi, yoksunluğun bireylerin çeşitli perakende ürünler için kullanabilecekleri jetonlar veya kuponlarla ödüllendirildiği.[11]
Hayvan modelleri
Geniş var etik sınırlamalar içinde uyuşturucu bağımlılığı araştırma, çünkü insanların araştırılmak amacıyla ilaçları kendi kendilerine uygulamalarına izin verilemez.[8] Bununla birlikte, laboratuar hayvanlarının incelenmesi ile ilaçlar ve ilaç alımının nörobiyolojisi hakkında çok şey öğrenilebilir.[12] Çoğu çalışma kemirgenler veya insan olmayan primatlar ikincisi, en çok şu ülkelerdeki insanlarla karşılaştırılabilir: farmakokinetik, anatomi of Prefrontal korteks, sosyal davranış, ve ömür.[13] İnsan olmayan primatlarda nüksetmeyi incelemenin diğer avantajları arasında hayvanın eski haline dönme yeteneği yer alır. öz yönetim ilacı elde etmek için karmaşık davranışları öğrenmek.[8] Hayvan çalışmaları, laboratuvar hayvanlarında ilaç alımını sürdürmek için negatif yoksunluk semptomlarında bir azalmanın gerekli olmadığını göstermiştir; bu çalışmaların anahtarı, edimsel şartlandırma ve pekiştirmedir.[3]
Protokoller
Kendi kendine yönetim
İlgili ilacı kendi kendine uygulamak için hayvana bir intravenöz implante edilir. kateter ve bir tepki kolu ile donatılmış bir primat sandalyesine oturdu. Hayvan, havalandırılan bir odaya oturtulur ve kendi kendine ilaç uygulama programına göre eğitilir. Birçok çalışmada kendi kendine yönetim görevi, operant görev tamamlandığında renkleri değiştirebilen veya sönebilen bir uyarıcı ışığın (yanıt panelinin yanında bulunan) sunumuyla başlar. Görsel uyarıdaki değişikliğe, verilen ilacın implante edilen kateterden enjeksiyonu eşlik eder. Bu program, hayvanlar görevi öğrenene kadar sürdürülür.[14]
Yok olma
Yok olma insan olmayan primatlarda bazı sınırlamalarla birlikte insanlarda yoksunluğa benzer. Uyuşturucu arama davranışını söndürmek için ilaç yerine bir tuzlu su çözüm. Hayvan, eğitildiği görevi yerine getirdiğinde, artık ilaç enjeksiyonu ile takviye edilmez. İlaçla ilişkili görsel uyaran ve görevin tamamlanması da kaldırılır. Hayvan, kola basarak uyuşturucu arama davranışını durdurana kadar yok olma seanslarına devam edilir.[15]
Eski durumuna döndürme
Hayvanın uyuşturucu arama davranışı söndürüldükten sonra, aynı uyuşturucu arama davranışının (yani nüksetme) eski haline döndürülmesini teşvik etmek için bir uyarı sunulur. Örneğin, hayvan söz konusu ilacın bir enjeksiyonunu alırsa, muhtemelen daha önce güçlendirilmiş olduğu operant görev üzerinde çalışmaya başlayacaktır.[6] Uyaran, ilacın kendisi, başlangıçta ilaç alımı ile eşleştirilmiş görsel uyaran veya bir stres etkeni olabilir. akustik irkilme veya ayak şoku.[14]
Nöro-görüntüleme
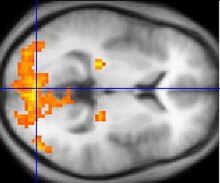
Nöro-görüntüleme kimliğinin belirlenmesine katkıda bulunmuştur sinirsel ilaçların eski haline döndürülmesinde yer alan bileşenler ve ilaç alımını belirleyen faktörler gibi eczokinetik, nörokimya, ve doz ilacın. İnsan olmayan primatlarda kullanılan nörogörüntüleme teknikleri şunları içerir: Pozitron emisyon tomografi (PET) kullanan radyo etiketli ligand nörokimyayı ölçmek için izleyiciler in vivo ve Tek foton emisyonlu bilgisayarlı tomografi (SPECT).[3] Fonksiyonel manyetik rezonans görüntüleme (fMRI) insan deneklerde yaygın olarak kullanılmaktadır çünkü çok daha yüksek çözünürlüğe sahiptir ve radyasyon.[13]
Sınırlamalar
Eski haline getirilmesine rağmen protokoller sıkça kullanılır laboratuar ayarlar için bazı sınırlamalar vardır geçerlilik bir model olarak prosedürlerin özlem ve insanlarda nüks. Birincil sınırlayıcı faktör, insanlarda nüksün nadiren katı yok olma uyuşturucu arama davranışı. Ek olarak, insanların kendi raporları, uyuşturucuyla ilişkili uyaran insanlarda aşermede laboratuvar modellerine göre daha az rol oynar. geçerlilik modelin üç şekilde incelenebilir: resmi denklik, korelasyonel modeller ve fonksiyonel eşdeğerlik. Orta derecede resmi denklik vardır veya yüz geçerliliği Bu, modelin laboratuvar ortamının dışında meydana geldiği için bir şekilde nüksetmeye benzediği anlamına gelir; ancak, bir özlem modeli olarak prosedürler için çok az yüz geçerliliği vardır. tahmini geçerlilik Korelasyon modelleriyle değerlendirilen, prosedürler için henüz belirlenmemiştir. Model için sağlam işlevsel eşdeğerlik vardır, bu da laboratuvardaki nüksün doğadakine makul ölçüde benzer olduğunu düşündürmektedir. İnsan olmayan primatlarda ilaç alımını sınırlayabilecek diğer manipülasyonlar veya takviyeler hakkında daha fazla araştırma yapılması, bu alan için son derece yararlı olacaktır.[16]
Cinsiyetler arasındaki farklar
Daha yüksek bir nüks oranı, daha kısa dönemler vardır. kaçınma ve erkeklere kıyasla kadınlarda uyuşturucuya bağlı ipuçlarına daha yüksek yanıt. Bir çalışma, yumurtalık hormonları, estradiol ve progesteron, kadınlarda değişen düzeylerde bulunan adet döngüsü (veya östrus döngüsü kemirgenlerde), ilaçla tetiklenen nüksetmede önemli bir rol oynar. Sırasında progesteron seviyelerinde belirgin bir artış ve östradiol seviyelerinde bir azalma vardır. luteal faz. Kaygı, sinirlilik ve depresyon, her ikisinin üç belirtisi para çekme ve insan adet döngüsü, en çok luteal fazda şiddetlidir. Açlık gibi döngü ile ilişkili olmayan geri çekilme semptomları da luteal faz sırasında artar, bu da estradiol ve progesteronun doğal olarak oluşan menstrüel seviyenin üzerindeki semptomları arttırmadaki rolünü düşündürür. Aşerme semptomları, insanlarda luteal fazda da artar (bunun tersi sonucun, kokain bağımlılığı olan kadınlarda, döngüsel değişikliklerin farklı kötüye kullanım ilaçlarına özgü olabileceğini düşündürdüğünü belirtmek önemlidir). Ayrıca, luteal faz sırasında ilaca bağlı yanıt azalır, bu da döngüde kullanıma devam etme dürtüsünün azaltılabileceği bir süreyi düşündürür. Bu bulgular, kötüye kullanılan bir uyuşturucuyu bırakmak ve büyütülmüş geri çekilme veya nüksetmeye yatkınlık semptomları için hazırlık yapmak için döngüsel, hormona dayalı bir zamanlamayı içerir.[17][18]
Ayrıca bakınız
Referanslar
- ^ a b Czoty PW, Gage HD, Nader MA (Aralık 2005). "İnsan olmayan primatlarda striatal dopamin D2 reseptörlerinin PET görüntülemesi: kronik racloprid tedavisi ile üretilen bulunabilirlikte artışlar". Sinaps. 58 (4): 215–9. doi:10.1002 / syn.20200. PMID 16206180.
- ^ Czoty PW, Morgan D, Shannon EE, Gage HD, Nader MA (Temmuz 2004). "Sosyal olarak barındırılan sinomolgus maymunlarında kendi kendine kokain veren dopamin D1 ve D2 reseptör fonksiyonunun karakterizasyonu". Psikofarmakoloji. 174 (3): 381–8. doi:10.1007 / s00213-003-1752-z. PMID 14767632.
- ^ a b c Murnane KS, Howell LL (Temmuz 2011). "Primatlarda nörogörüntüleme ve ilaç alımı". Psikofarmakoloji. 216 (2): 153–71. doi:10.1007 / s00213-011-2222-7. PMC 3232674. PMID 21360099.
- ^ Wikler A (Kasım 1948). "Morfin bağımlılığının nörofizyolojik temeli üzerine yapılan araştırmalarda son gelişmeler". Am J Psikiyatri. 105 (5): 329–38. doi:10.1176 / ajp.105.5.329. PMID 18890902.
- ^ Breese GR, Sinha R, Heilig M (Şubat 2011). "Kronik alkol nöroadaptasyonu ve stres, alkol aşermesine ve nüksetmeye yatkınlığa katkıda bulunur". Pharmacol. Orada. 129 (2): 149–71. doi:10.1016 / j.pharmthera.2010.09.007. PMC 3026093. PMID 20951730.
- ^ a b McClung J, Fantegrossi W, Howell LL (Mayıs 2010). "3,4-metilendioksimethamfetamin (MDMA) ve rhesus maymunlarındaki enantiyomerleri ile kendi kendine sönmüş amfetamin uygulamasının eski haline getirilmesi". Psikofarmakoloji. 210 (1): 75–83. doi:10.1007 / s00213-010-1818-7. PMC 2862592. PMID 20309529.
- ^ a b c Larimer ME, Palmer RS, Marlatt GA (1999). "Nüks önleme. Marlatt'ın bilişsel-davranışçı modeline genel bir bakış". Alkol Res Health. 23 (2): 151–60. PMID 10890810.
- ^ a b c Nader MA, Czoty PW (Ağustos 2005). "Kokain kötüye kullanımı maymun modellerinde dopamin D2 reseptörlerinin PET görüntülemesi: çevresel modülasyona karşı genetik yatkınlık". Am J Psikiyatri. 162 (8): 1473–82. doi:10.1176 / appi.ajp.162.8.1473. PMID 16055768.
- ^ Van den Oever MC, Spijker S, Smit AB, De Vries TJ (Kasım 2010). "İlaç arama ve nüksetmede prefrontal korteks plastisite mekanizmaları". Neurosci Biobehav Rev. 35 (2): 276–84. doi:10.1016 / j.neubiorev.2009.11.016. PMID 19932711.
- ^ a b Kadden RM (2002-09-10). "Madde Bağımlılığı İçin Bilişsel Davranış Terapisi: Başa Çıkma Becerileri Eğitimi" (PDF). Davranışsal Sağlık İyileştirme Yönetimi, Chicago Üniversitesi. Arşivlenen orijinal (pdf) 2012-01-05 tarihinde. Alındı 2011-12-03.
- ^ Lussier JP, Heil SH, Mongeon JA, Badger GJ, Higgins ST (Şubat 2006). "Madde kullanım bozuklukları için kupon bazlı pekiştirme tedavisinin bir meta-analizi". Bağımlılık. 101 (2): 192–203. doi:10.1111 / j.1360-0443.2006.01311.x. PMID 16445548.
- ^ Howell LL, Votaw JR, Goodman MM, Lindsey KP (Şubat 2010). "Rhesus maymunlarında kokain kullanımı ve neslinin tükenmesi sırasında kortikal aktivasyon". Psikofarmakoloji. 208 (2): 191–9. doi:10.1007 / s00213-009-1720-3. PMC 2819208. PMID 19924404.
- ^ a b Howell LL, Murnane KS (Mayıs 2011). "Uyuşturucu kullanımı araştırmalarında insan dışı primat pozitron emisyon tomografisi nörogörüntüleme". J. Pharmacol. Tecrübe. Orada. 337 (2): 324–34. doi:10.1124 / jpet.108.136689. PMC 3083112. PMID 21317354.
- ^ a b Kirkland Henry P, Davis M, Howell LL (Ağustos 2009). "Sınırlı ve genişletilmiş erişim koşulları altında kendi kendine kokain uygulama geçmişinin, Rhesus maymunlarında in vivo striatal dopamin nörokimyası ve akustik irkilme üzerindeki etkileri". Psikofarmakoloji. 205 (2): 237–47. doi:10.1007 / s00213-009-1534-3. PMC 2796974. PMID 19365621.
- ^ Andersen ML, Kessler E, Murnane KS, McClung JC, Tufik S, Howell LL (Haziran 2010). "Rhesus maymunlarında modafinilin dopamin taşıyıcı ile ilişkili etkileri". Psikofarmakoloji. 210 (3): 439–48. doi:10.1007 / s00213-010-1839-2. PMC 2874656. PMID 20386883.
- ^ Katz JL, Higgins ST (Temmuz 2003). "Özlem ve uyuşturucu kullanımına yeniden başlamanın eski haline döndürme modelinin geçerliliği". Psikofarmakoloji. 168 (1–2): 21–30. doi:10.1007 / s00213-003-1441-y. PMID 12695875.
- ^ Hudson A, Stamp JA (Ocak 2011). "Yumurtalık hormonları ve ilacın nüksetme eğilimi: bir inceleme". Neurosci Biobehav Rev. 35 (3): 427–36. doi:10.1016 / j.neubiorev.2010.05.001. PMID 20488201.
- ^ Czoty PW, Riddick NV, Gage HD, Sandridge M, Nader SH, Garg S, Bounds M, Garg PK, Nader MA (Şubat 2009). "Adet döngüsü fazının dişi sinomolgus maymunlarında dopamin D2 reseptörü mevcudiyeti üzerindeki etkisi". Nöropsikofarmakoloji. 34 (3): 548–54. doi:10.1038 / npp.2008.3. PMID 18256593.
