Fonksiyonel manyetik rezonans görüntüleme - Functional magnetic resonance imaging
| Fonksiyonel manyetik rezonans görüntüleme | |
|---|---|
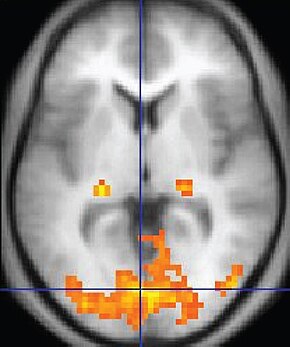 Bir kontrol durumuna kıyasla artan aktivite gösteren sarı alanlara sahip bir fMRI görüntüsü. | |
| Amaç | kan akışına bağlı değişiklikleri tespit ederek beyin aktivitesini ölçer. |
Fonksiyonel manyetik rezonans görüntüleme veya fonksiyonel MR (fMRI) ile ilişkili değişiklikleri tespit ederek beyin aktivitesini ölçer kan akışı.[1][2] Bu teknik, serebral kan akışı ile nöronal aktivasyonun birbirine bağlı olduğu gerçeğine dayanır. Beynin bir bölgesi kullanımdayken o bölgeye kan akışı da artar.[3]
FMRI'nin birincil biçimi, kan oksijen seviyesine bağlı (BOLD) kontrastı,[4] tarafından keşfedildi Seiji Ogawa 1990 yılında. Bu, haritalamak için kullanılan özel bir beyin ve vücut taraması türüdür. sinirsel faaliyet beyin veya omurilik kan akışındaki değişikliği görüntüleyerek insanların veya diğer hayvanlarınhemodinamik yanıt ) beyin hücreleri tarafından enerji kullanımı ile ilgili.[4] 1990'ların başından beri, fMRI egemen hale geldi beyin haritalama araştırma çünkü insanların enjeksiyon veya ameliyat geçirmesini, maddeleri yutmasını veya iyonlaştırıcı radyasyona maruz kalmasını gerektirmiyor.[5] Bu önlem genellikle çeşitli kaynaklardan gelen gürültü nedeniyle bozulur; bu nedenle, altta yatan sinyali çıkarmak için istatistiksel prosedürler kullanılır. Ortaya çıkan beyin aktivasyonu, beyindeki veya çalışılan spesifik bölgedeki aktivasyon gücünün renk kodlamasıyla grafiksel olarak temsil edilebilir. Teknik, aktiviteyi milimetre içinde lokalize edebilir, ancak standart teknikleri kullanarak, birkaç saniyelik bir pencereden daha iyi olamaz.[6] Kontrast elde etmenin diğer yöntemleri şunlardır: arteriyel spin etiketleme[7] ve difüzyon MR. İkinci prosedür BOLD fMRI'ye benzer, ancak beyindeki su moleküllerinin difüzyon büyüklüğüne bağlı olarak kontrast sağlar.
FMRI, görevler / uyaranlar nedeniyle aktiviteden BOLD yanıtları tespit etmenin yanı sıra dinlenme durumu fMRI veya görevsiz fMRI, deneklerin temel BOLD varyansını gösterir. Yaklaşık 1998 yılından bu yana yapılan araştırmalar, bölgenin varlığını ve özelliklerini göstermiştir. varsayılan mod ağı (DMN), diğer adıyla 'Dinlenme Durumu Ağı' (RSN), görünür 'beyin durumlarının' işlevsel olarak bağlı bir sinir ağı.
fMRI, araştırmada ve daha az ölçüde klinik çalışmalarda kullanılır. Diğer beyin fizyolojisi ölçümlerini tamamlayabilir. EEG ve NIRS. Hem uzamsal hem de zaman çözünürlüğünü iyileştiren yeni yöntemler araştırılmaktadır ve bunlar büyük ölçüde BOLD sinyalinden başka biyobelirteçler kullanır. Bazı şirketler, fMRI tekniklerine dayalı yalan dedektörleri gibi ticari ürünler geliştirdiler, ancak araştırmanın yaygın ticarileştirme için yeterince geliştirildiğine inanılmıyor.[8]
Genel Bakış
FMRI kavramı, daha önce MR tarama teknolojisi ve oksijen bakımından zengin kanın özelliklerinin keşfi. MRI beyin taramaları, incelenen beyin bölgesindeki çekirdekleri hizalamak için güçlü, kalıcı, statik bir manyetik alan kullanır. Başka bir manyetik alan, gradyan alanı, daha sonra farklı çekirdekleri uzamsal olarak konumlandırmak için uygulanır. Son olarak, çekirdeği daha yüksek manyetizasyon seviyelerine atmak için bir radyofrekans (RF) darbesi çalınır ve bu etki artık bulundukları yere bağlıdır. RF alanı kaldırıldığında, çekirdekler orijinal hallerine geri döner ve yaydıkları enerji çekirdeklerin konumlarını yeniden oluşturmak için bir bobin ile ölçülür. MRI böylece beyin maddesinin statik yapısal bir görünümünü sağlar. FMRI'nin arkasındaki temel itici güç, nöronal aktivitenin neden olduğu beyindeki fonksiyonel değişiklikleri yakalamak için MRI'yi genişletmekti. Arteriyel (oksijenden zengin) ve venöz (oksijenden fakir) kan arasındaki manyetik özelliklerdeki farklılıklar bu bağlantıyı sağlamıştır.[9]

1890'lardan beri değiştiği bilinmektedir. kan akışı ve kan oksijenasyonu beyin (topluca olarak bilinir hemodinamik ) sinirsel aktivite ile yakından bağlantılıdır.[10] Nöronlar aktif hale geldiğinde, bu beyin bölgelerine yerel kan akışı artar ve oksijenden zengin (oksijenli) kan, yaklaşık 2 saniye sonra oksijeni tükenmiş (oksijensiz) kanın yerini alır. Bu, orijinal düzeye geri dönmeden önce (ve tipik olarak biraz altına düşmeden) 4-6 saniyenin üzerinde zirveye yükselir. Oksijen, hemoglobin molekül Kırmızı kan hücreleri. Oksijenli hemoglobin (dHb) daha manyetiktir (paramanyetik ) manyetizmaya neredeyse dirençli olan oksijenli hemoglobine (Hb) göre (diyamanyetik ). Bu fark, diyamanyetik kan manyetik MR sinyaline daha az müdahale ettiğinden gelişmiş bir MR sinyaline yol açar. Bu gelişme, bir seferde hangi nöronların aktif olduğunu göstermek için haritalanabilir.[11]
Tarih
19. yüzyılın sonlarında, Angelo Mosso yeniden dağıtımını invaziv olmayan bir şekilde ölçebilen 'insan dolaşım dengesini' icat etti. kan duygusal ve entelektüel aktivite sırasında.[12] Bununla birlikte, kısaca bahsedilmesine rağmen William James 1890'da, bu dengenin detayları ve hassas çalışmaları ve deneyler Mosso'nun onunla yaptığı performans, orijinal enstrümanın son keşfine ve Mosso'nun raporlarına kadar büyük ölçüde bilinmiyordu. Stefano Sandrone ve meslektaşlarım.[13] Angelo Mosso, birkaç önemli değişkenler 'gibi modern nörogörüntülemede hala geçerli olansinyal gürültü oranı ', deneysel için uygun seçim paradigma ve aynı anda farklı fizyolojik kayıtlara duyulan ihtiyaç parametreleri.[13] Mosso'nun el yazmaları, dengenin, bilişten kaynaklanan beyin kan akışındaki değişiklikleri gerçekten ölçebildiğine dair doğrudan kanıt sağlamaz.[13] ancak David T Field tarafından gerçekleştirilen modern bir çoğaltma[14] Mosso için mevcut olmayan modern sinyal işleme tekniklerini kullanarak, bu türden bir denge aparatının, bilişle ilgili serebral kan hacmindeki değişiklikleri tespit edebildiğini şimdi göstermiştir.[kaynak belirtilmeli ]
1890'da Charles Roy ve Charles Sherrington ilk olarak beyin fonksiyonunu kan akışına deneysel olarak bağladı. Cambridge Üniversitesi.[15] Beyne giden kan akışının nasıl ölçüleceğini çözmenin bir sonraki adımı Linus Pauling 's ve Charles Coryell'in 1936'da Hb ile oksijen bakımından zengin kanın manyetik alanlar tarafından zayıf bir şekilde itildiğini, dHb'li oksijeni tükenmiş kan ise demir gibi ferromanyetik elementlerden daha az olsa da manyetik alana çekildiğini keşfetti. Seiji Ogawa -de AT&T Bell laboratuvarları bunun beynin sadece statik yapısını inceleyebilecek MRI'yi artırmak için kullanılabileceğini fark etti, çünkü aktive edilmiş beyin bölgelerine kan akışının neden olduğu farklı manyetik özellikler MRI sinyalinde ölçülebilir değişikliklere neden olacaktır. BOLD, 1990 yılında Ogawa tarafından keşfedilen, dHb'nin MRI kontrastıdır. Thulborn ve arkadaşlarının daha önceki çalışmalarına dayanan bir çığır açan 1990 çalışmasında, Ogawa ve meslektaşları kemirgenleri güçlü bir manyetik alanda (7.0T MRI. Kandaki oksijen seviyesini manipüle etmek için hayvanların soluduğu oksijen oranını değiştirdiler. Bu oran düştükçe, MRG'de beyindeki kan akışının bir haritası görüldü. Bunu, oksijenli veya oksijeni alınmış kan içeren test tüpleri yerleştirerek ve ayrı görüntüler oluşturarak doğruladılar. Ayrıca, gradyan-eko görüntülerinin T denilen bir manyetizasyon kaybına bağlı olduğunu da gösterdiler.2* çürüme, en iyi görüntüleri üretti. Bu kan akışı değişikliklerinin fonksiyonel beyin aktivitesiyle ilgili olduğunu göstermek için fareler tarafından solunan havanın bileşimini değiştirdiler ve EEG ile beyin aktivitesini izlerken taradılar.[16] MRI kullanarak bölgesel beyin aktivitesini tespit etmeye yönelik ilk girişim Belliveau ve meslektaşları tarafından gerçekleştirildi.[17] -de Harvard Üniversitesi intravenöz enjeksiyondan sonra kan dolaşımında kalan ferromanyetik bir madde olan kontrast madde Magnevist kullanılarak. Bununla birlikte, bu yöntem, kontrast madde enjeksiyonunun uygunsuzluğundan ve maddenin kanda sadece kısa bir süre kaldığından dolayı insan fMRI'sinde popüler değildir.[18]
İnsanlarda BOLD kontrastını kullanan ilk araştırma 1992'deki üç çalışma oldu. Kenneth Kwong ve meslektaşları, hem gradyan-eko hem de ters çevirme kurtarma kullanarak yankı düzlemsel görüntüleme İnsanın açık bir şekilde aktivasyonunu gösteren yayınlanmış çalışmalar 1.5 T manyetik alan kuvvetinde (EPI) dizisi görsel korteks.[19] Harvard ekibi böylece hem kan akışının hem de kan hacminin aktivite nöral dokusunda lokal olarak arttığını gösterdi. Ogawa ve diğerleri daha yüksek bir alan (4.0 T) kullanarak benzer bir çalışma yürüttüler ve BOLD sinyalinin T2 * manyetizasyon kaybına bağlı olduğunu gösterdi. T2 * bozunması, manyetik tutarlılığı (enine manyetizasyon) kaybeden uzay hacmindeki manyetize çekirdeklerden ve konumlar arasında uygulanan manyetik alan gücündeki kasıtlı farklılıklardan (uzaysal gradyan alan homojenliği) kaynaklanır. Bandettini ve meslektaşları, istemli hareketleri kontrol eden devrenin son aşamasında bir beyin bölgesi olan birincil motor kortekste aktivasyonu göstermek için 1.5 T'de EPI'yi kullandılar. Bu erken çalışmalar tarafından kullanılan manyetik alanlar, darbe dizileri ve prosedürler ve teknikler, günümüz fMRI çalışmalarında hala kullanılmaktadır. Ancak günümüzde araştırmacılar genellikle daha fazla dilimden (daha güçlü manyetik gradyanlar kullanarak) veri toplar ve istatistiksel teknikler kullanarak verileri önceden işler ve analiz eder.[20]
Fizyoloji
Beyin, birincil enerji kaynağı olan glikozu depolamaz. Nöronlar aktif hale geldiğinde, onları orijinal polarizasyon durumuna geri döndürmek, iyonların nöronal hücre zarları boyunca her iki yönde aktif olarak pompalanmasını gerektirir. Onlar için enerji iyon pompaları esas olarak glikozdan üretilir. Daha fazla glikoz taşımak için daha fazla kan akar ve ayrıca kırmızı kan hücrelerinde oksijenli hemoglobin molekülleri şeklinde daha fazla oksijen getirir. Bu, hem daha yüksek bir kan akışı hızından hem de kan damarlarının genişlemesinden kaynaklanmaktadır. Kan akışı değişikliği, nöral aktivitenin olduğu yerin 2 veya 3 mm'si içinde lokalizedir. Genellikle getirilen oksijen, yanan glikozda tüketilen oksijenden daha fazladır (glikoz tüketiminin çoğunun oksidatif olup olmadığı henüz belirlenmemiştir) ve bu, beyin bölgesindeki kan damarlarındaki oksijensiz hemoglobinde (dHb) net bir azalmaya neden olur. Bu, kanın manyetik özelliğini değiştirerek, manyetizasyona ve MRI işleminin neden olduğu nihai bozulmaya daha az müdahale etmesini sağlar.[21]
Serebral kan akışı (CBF), farklı beyin bölgelerinde tüketilen glikoza farklı şekilde karşılık gelir. İlk sonuçlar, glukoz tüketiminden daha fazla giriş olduğunu göstermektedir. amigdala, Bazal ganglion, talamus ve singulat korteks, bunların tümü hızlı yanıtlar için işe alınır. Yanal bölge gibi daha düşünceli olan bölgelerde önden ve yanal parietal loblar, gelen akışın tüketimden daha az olduğu görülüyor. Bu, BOLD hassasiyetini etkiler.[22]
Hemoglobin, bağlı bir oksijen molekülüne sahip olup olmadığına bağlı olarak manyetik alanlara nasıl tepki verdiğine göre farklılık gösterir. DHb molekülü manyetik alanlara daha çok çekilir. Bu nedenle, bir MRI tarayıcısı tarafından indüklenen çevreleyen manyetik alanı bozarak, buradaki çekirdeklerin T yoluyla mıknatıslanmayı daha hızlı kaybetmesine neden olur.2* çürüme. Böylece T'ye duyarlı MR darbe dizileri2* Kanın yüksek oranda oksijenli olduğu yerlerde daha fazla MR sinyali ve olmadığı yerlerde daha az gösterir. Bu etki, manyetik alanın kuvvetinin karesi ile artar. Dolayısıyla fMRI sinyali hem güçlü bir manyetik alana (1.5 T veya daha yüksek) hem de EPI gibi T'ye duyarlı bir darbe dizisine ihtiyaç duyar.2* kontrast.[23]
Fizyolojik kan akışı yanıtı büyük ölçüde zamansal duyarlılığa karar verir, yani BOLD fMRI'de nöronlar aktif olduğunda ne kadar doğru ölçebiliriz. Temel zaman çözünürlük parametresi (örnekleme zamanı) TR olarak belirtilir; TR, belirli bir beyin diliminin ne sıklıkla heyecanlandığını ve manyetizasyonunu kaybetmesine izin verildiğini belirtir. TR'ler çok kısadan (500 ms) çok uzuna (3 sn) kadar değişebilir. Özellikle fMRI için, hemodinamik yanıt 10 saniyenin üzerinde sürer, çarpılarak yükselir (yani, mevcut değerin bir oranı olarak), 4 ila 6 saniyede zirveye ulaşır ve ardından çarparak düşer. Kan akış sistemindeki, yani vasküler sistemdeki değişiklikler, zamanla nöronal aktiviteye verilen yanıtları bütünleştirir. Bu yanıt sorunsuz ve sürekli bir işlev olduğu için, her zamankinden daha hızlı TR'lerle örnekleme yardımcı olmuyor; zaten basit doğrusal enterpolasyonla elde edilebilen yanıt eğrisi üzerinde daha fazla nokta verir. Çeşitli denemelerde bir uyarıcı sunulduğunda şaşırtma gibi deneysel paradigmalar zamansal çözünürlüğü iyileştirebilir, ancak elde edilen etkili veri noktalarının sayısını azaltır.[24]
BOLD hemodinamik yanıt

MR sinyalindeki nöronal aktiviteden kaynaklanan değişikliğe hemodinamik yanıt (HDR) denir. Vasküler sistemin beynin glikoz ihtiyacına yanıt vermesi biraz zaman aldığından, onu tetikleyen nöronal olayları birkaç saniye geciktirir. Bu noktadan itibaren tipik olarak uyarandan yaklaşık 5 saniye sonra zirveye yükselir. Nöronlar, örneğin sürekli bir uyarandan ateşlenmeye devam ederse, nöronlar aktif kalırken tepe düz bir platoya yayılır. Aktivite durduktan sonra, BOLD sinyali orijinal seviyenin, taban çizgisinin altına düşer, bu fenomen altta kalma olarak adlandırılır. Zamanla sinyal taban çizgisine geri döner. Bir beyin bölgesindeki sürekli metabolik gereksinimlerin hedefin altında kalmaya katkıda bulunduğuna dair bazı kanıtlar vardır.[25]
Nöral sistemin, daha fazla glikoz ihtiyacına dair vasküler sisteme geri bildirim sağladığı mekanizma, kısmen salgılanmasıdır. glutamat nöron ateşlemesinin bir parçası olarak. Bu glutamat yakındaki destekleyici hücreleri etkiler, astrositler, bir değişikliğe neden olmak kalsiyum iyon konsantrasyonu. Bu da bültenler nitrik oksit astrositlerin ve orta büyüklükteki kan damarlarının temas noktasında, küçük atardamarlar. Nitrik oksit bir vazodilatör arteriyollerin genişlemesine ve daha fazla kan çekmesine neden olur.[26]
Bir tek voksel zaman içindeki yanıt sinyaline zaman süreci denir. Tipik olarak, tarayıcıdan gelen gürültü adı verilen istenmeyen sinyal, rastgele beyin aktivitesi ve benzer öğeler, sinyalin kendisi kadar büyüktür. Bunları ortadan kaldırmak için, fMRI çalışmaları bir uyaran sunumunu birçok kez tekrarlar.[27]
Uzamsal çözünürlük
Bir fMRI çalışmasının mekansal çözünürlüğü, yakın yerler arasında ne kadar iyi ayrım yaptığını ifade eder. MRI'da olduğu gibi voksellerin boyutuyla ölçülür. Bir voksel, boyutları dilim kalınlığına, bir dilimin alanına ve dilime tarama işlemi tarafından uygulanan ızgaraya göre belirlenen üç boyutlu dikdörtgen bir küboiddir. Tam beyin çalışmaları daha büyük vokseller kullanırken, belirli ilgi alanlarına odaklananlar genellikle daha küçük boyutlar kullanır. Boyutlar 4 ila 5 mm arasında değişir veya laminer çözünürlük fMRI (lfMRI), milimetre altı.[28] Daha küçük vokseller ortalama olarak daha az nöron içerir, daha az kan akışı içerir ve dolayısıyla daha büyük voksellerden daha az sinyale sahiptir. Daha küçük vokseller, daha uzun tarama süreleri anlamına gelir, çünkü tarama süresi, dilim başına voksel sayısı ve dilim sayısı ile doğrudan yükselir. Bu, hem tarayıcının içindeki özne için rahatsızlığa hem de mıknatıslanma sinyalinin kaybına neden olabilir. Bir voksel tipik olarak birkaç milyon nöron ve on milyarlarca sinapslar, gerçek sayı voksel boyutuna ve görüntülenen beynin alanına bağlıdır.[29]
Vasküler arter sistemi, beyin yüzeyine ve beyin içi bölgelere girerken daha küçük damarlara taze kan dalları besleyerek, bağlantılı bir şekilde sonuçlanır. kılcal damar beyin içindeki yatak. Drenaj sistemi de benzer şekilde gittikçe büyüyor damarlar oksijeni tükenmiş kanı taşıdığı için. FMRI sinyaline dHb katkısı, hem aktivite alanına yakın kılcal damarlardan hem de daha uzakta olabilecek daha büyük drenaj damarlarından gelir. İyi bir uzaysal çözünürlük için, büyük damarlardan gelen sinyalin bastırılması gerekir, çünkü sinirsel aktivitenin olduğu alana karşılık gelmez. Bu, güçlü statik manyetik alanlar kullanılarak veya spin-eko darbe dizileri kullanılarak elde edilebilir.[30] Bunlarla fMRI, milimetreden santimetreye kadar uzamsal bir aralığı inceleyebilir ve dolayısıyla Brodmann alanları (santim), subkortikal çekirdekler, örneğin kuyruklu, Putamen ve talamus ve kombine hipokampal alt alanlar dentat girus /CA3, CA1, ve alt okul.[31]
Zamansal çözünürlük
Temporal çözünürlük, fMRI ile güvenilir bir şekilde ayrılan en küçük nöral aktivite dönemidir. Buna karar veren unsurlardan biri örnekleme zamanı, TR'dir. Bununla birlikte, 1 veya 2 saniyelik bir TR'nin altında, tarama, çok fazla ek bilgi eklemeden yalnızca daha keskin HDR eğrileri oluşturur (örneğin, daha düşük bir TR'de eğri boşluklarının matematiksel olarak enterpolasyonuyla elde edilenin ötesinde). Geçici çözünürlük, denemeler boyunca uyaran sunumunu kademelendirerek iyileştirilebilir. Veri denemelerinin üçte biri normal olarak örneklenirse, üçte biri 1 sn, 4 sn, 7 sn vb. Ve son üçte biri 2 sn, 5 sn ve 8 sn'de örnekleniyorsa, birleştirilmiş veriler 1 sn'lik bir çözünürlük sağlar ancak toplam olayların yalnızca üçte biri kadar.
Gereken zaman çözünürlüğü, çeşitli olaylar için beyin işleme süresine bağlıdır. Buradaki geniş aralığın bir örneği görsel işleme sistemi tarafından verilmektedir. Gözün gördükleri, bir milisaniye içinde retinanın fotoreseptörlerine kaydedilir. Bu sinyaller talamus yoluyla onlarca milisaniye içinde birincil görsel kortekse ulaşır. Görme eylemiyle ilgili nöronal aktivite 100 ms'den fazla sürer. Araba kazasından kaçınmak için yoldan çıkmak gibi hızlı bir tepki yaklaşık 200 ms sürer. Yaklaşık yarım saniyede, olayın farkındalığı ve yansıması devreye girer. Benzer bir olayı hatırlamak birkaç saniye sürebilir ve korku uyarılması gibi duygusal veya fizyolojik değişiklikler dakikalar veya saatler sürebilir. Yüzleri veya sahneleri tanımak gibi öğrenilen değişiklikler günler, aylar veya yıllar sürebilir. Çoğu fMRI deneyinde, birkaç saniye süren beyin süreçleri incelenir ve çalışma birkaç on dakika sürer. Denekler bu süre içinde başlarını hareket ettirebilirler ve bu baş hareketinin düzeltilmesi gerekir. Temel sinyalde zamanla kayma da olur. Can sıkıntısı ve öğrenme, hem özne davranışını hem de bilişsel süreçleri değiştirebilir.[32]
Çoklu aktivasyondan doğrusal ekleme
Bir kişi iki görevi aynı anda veya örtüşen şekilde gerçekleştirdiğinde, BOLD yanıtının doğrusal olarak artması beklenir. Bu, sürekli türevlenebilir sistemlerin, pertürbasyonlar küçük olduğunda doğrusal davranmasının beklenebileceği ilkesine dayanan birçok fMRI çalışmasının temel bir varsayımıdır; birinci sıraya doğrusaldırlar. Doğrusal toplama, tek tek yanıtlar birleştirilmeden (birbirine eklenmeden) önce izin verilen tek işlemin her birinin ayrı bir ölçeklendirmesi olduğu anlamına gelir. Ölçeklendirme sadece sabit bir sayı ile çarpma olduğu için, bu, örneğin diğerine göre iki kat nöral tepkiyi çağrıştıran bir olayın, aynı anda iki kez sunulan ilk olay olarak modellenebileceği anlamına gelir. İkiye katlanan etkinliğin HDR'si, tek etkinliğin yalnızca iki katıdır.
Davranışın doğrusal olduğu ölçüde, rastgele bir uyarana BOLD yanıtının zaman süreci, bu uyaranın BOLD tepkisi dürtüyle evrişimi ile modellenebilir. BOLD yanıt büyüklüğünü tahmin etmede doğru zaman süreci modellemesi önemlidir.[33][34]
Bu güçlü varsayım ilk olarak 1996 yılında Boynton ve meslektaşları tarafından, saniyede 8 kez titreyen desenlerin birincil görsel korteksi üzerindeki etkilerini kontrol eden ve 3 ila 24 saniye sunan meslektaşları tarafından incelenmiştir. Elde ettikleri sonuçlar, görüntünün görsel kontrastı artırıldığında, HDR şeklinin aynı kaldığını, ancak genliğinin orantılı olarak arttığını gösterdi. Bazı istisnalar dışında, daha uzun uyaranlara verilen yanıtlar, aynı daha uzun süreyi özetleyen birden çok daha kısa uyarıcıya yönelik yanıtların bir araya getirilmesiyle de çıkarılabilir. 1997'de Dale ve Buckner, belirli süreli bloklar yerine tek tek olayların da aynı şekilde toplanıp özetlenmediğini test ettiler ve yaptıklarını buldular. Ancak 2 saniyeden daha kısa zaman aralıklarında doğrusal modelden sapmalar da buldular.
FMRI yanıtındaki bir doğrusal olmama kaynağı, sunulan bir uyarıcıdan gelen beyin aktivitesinin sonraki, benzer bir uyarıcı üzerindeki diğer aktiviteyi bastırdığı refrakter dönemdendir. Uyaranlar kısaldıkça refrakter dönem daha belirgin hale gelir. Refrakter dönem yaşla değişmez ve HDR'lerin genlikleri değişmez.[kaynak belirtilmeli ]. Dönem, beyin bölgelerine göre farklılık gösterir. İkisinde de birincil motor korteks ve görsel korteks, HDR genliği, bir uyaran veya yanıt süresi ile doğrusal olarak ölçeklenir. Karşılık gelen ikincil bölgelerde, tamamlayıcı motor korteks, motor davranışın ve harekete duyarlı V5 bölgesinin planlanmasında yer alan güçlü bir refrakter dönem görülür ve HDR genliği, çeşitli uyaran veya yanıt süreleri boyunca sabit kalır. Refrakter etkisi benzer bir şekilde kullanılabilir alışma Bir kişinin bir uyarıcının hangi özelliklerini yeni olarak ayırt ettiğini görmek için.[35] Doygunluk nedeniyle doğrusallığın başka sınırları vardır: büyük uyarma seviyelerinde maksimum BOLD tepkisine ulaşılır.
Sinirsel aktiviteyi BOLD sinyaliyle eşleştirme
Araştırmacılar, BOLD sinyalini hem implante edilmiş elektrotlardan (çoğunlukla maymunlarda) gelen sinyallere hem de alan potansiyellerinin sinyallerine (yani kafatasının dışında ölçülen beyin aktivitesinden gelen elektrik veya manyetik alan) karşı kontrol ettiler. EEG ve MEG. Hem post-nöron-sinaptik aktiviteyi hem de dahili nöron işlemeyi içeren yerel alan potansiyeli, BOLD sinyalini daha iyi tahmin eder.[36] Dolayısıyla, BOLD kontrastı esas olarak bir nörona girdileri ve nöronun vücudundaki bütünleyici işlemeyi yansıtır ve nöronların çıkış ateşlemesini daha az yansıtır. İnsanlarda elektrotlar yalnızca tedavi olarak ameliyata ihtiyaç duyan hastalara implante edilebilir, ancak kanıtlar en azından benzer bir ilişki olduğunu göstermektedir. Işitsel korteks ve birincil görsel korteks. BOLD fMRI tarafından kortikal alanlarda (beyin yüzey bölgeleri) tespit edilen aktivasyon konumlarının, CBF tabanlı fonksiyonel haritalarla hesaplandığı bilinmektedir. PET taramaları. Sadece birkaç milimetre boyutunda olan bazı bölgeler, örneğin yanal genikülat çekirdek Görsel girdileri retinadan görsel kortekse aktaran talamusun (LGN), görsel girdiyle sunulduğunda doğru BOLD sinyali ürettiği gösterilmiştir. Gibi yakın bölgeler pulvinar çekirdek en azından talamik çekirdeklerde BOLD yanıtının uzamsal boyutu için milimetre çözünürlüğünü gösteren bu görev için uyarılmamışlardır. Sıçan beyninde, tek bıyık dokunuşunun BOLD sinyallerini ortaya çıkardığı gösterilmiştir. somatosensoriyel korteks.[37]
Ancak, BOLD sinyali bir bölgedeki geri besleme ve ileri beslemeli aktif ağları ayıramaz; vasküler tepkinin yavaşlığı, son sinyalin tüm bölgenin ağının özetlenmiş versiyonu olduğu anlamına gelir; işlem ilerledikçe kan akışı kesintili değildir. Ayrıca, diğer nöronlardan bir nörona hem inhibe edici hem de uyarıcı girdi toplamı ve BOLD sinyaline katkıda bulunur. Bir nöronun içinde bu iki giriş birbirini götürür.[38] BOLD yanıtı ayrıca hastalık, sedasyon, anksiyete, kan damarlarını genişleten ilaçlar gibi çeşitli faktörlerden etkilenebilir.[39] ve dikkat (nöromodülasyon)[40].
BOLD sinyalinin genliği, şeklini mutlaka etkilemez. Daha güçlü nöral aktivite için daha yüksek genlikli bir sinyal görülebilir, ancak daha zayıf bir sinyalle aynı yerde zirve yapar. Ayrıca, genlik mutlaka davranışsal performansı yansıtmaz. Karmaşık bir bilişsel görev, başlangıçta iyi performansla ilişkili yüksek genlikli sinyalleri tetikleyebilir, ancak özne bunda daha iyi hale geldikçe, performans aynı kaldıkça genlik azalabilir. Bunun, görevin yerine getirilmesindeki artan verimlilikten kaynaklanması bekleniyor.[41] Beyin bölgelerindeki BOLD tepkisi, aynı görev için bile doğrudan karşılaştırılamaz, çünkü nöronların yoğunluğu ve kan tedarik özellikleri beyinde sabit değildir. Bununla birlikte, BOLD yanıtı genellikle aynı beyin bölgesi ve aynı görev için denekler arasında karşılaştırılabilir.[42]
BOLD sinyalinin daha yeni karakterizasyonu, yüksek alan mıknatısları (bazen "optofMRI" olarak adlandırılan bir teknik) kullanarak BOLD yanıtını eşzamanlı olarak izlerken nöronal ateşlemeyi hassas bir şekilde kontrol etmek için kemirgenlerde optogenetik teknikler kullanmıştır.[43][44] Bu teknikler, nöronal ateşlemenin, yakın aralıklı nöronal ateşleme patlamaları üzerinden BOLD sinyalinin yaklaşık olarak doğrusal toplamı dahil olmak üzere ölçülen BOLD sinyali ile iyi korelasyon gösterdiğini ileri sürmektedir.[45] Doğrusal toplama, yaygın olarak kullanılan olayla ilgili fMRI tasarımlarının bir varsayımıdır.[46]
Tıbbi kullanım

Doktorlar, beyin ameliyatı veya benzeri invaziv tedavinin bir hasta için ne kadar riskli olduğunu değerlendirmek ve normal, hastalıklı veya yaralı bir beynin nasıl çalıştığını öğrenmek için fMRI kullanır. Konuşma, hareket etme, algılama veya planlama gibi kritik işlevlerle bağlantılı bölgeleri belirlemek için beyni fMRI ile haritalandırırlar. Bu, beynin ameliyat ve radyasyon tedavisi için plan yapmak için faydalıdır. Klinisyenler ayrıca beyni anatomik olarak haritalamak ve tümörlerin, felç, kafa ve beyin hasarının veya aşağıdaki gibi hastalıkların etkilerini tespit etmek için fMRI kullanır. Alzheimer ve gelişimsel engeller gibi Otizm vb..[47][48]
FMRI'nin klinik kullanımı hala araştırma kullanımının gerisinde kalmaktadır.[49] Beyin patolojileri olan hastaların fMRI ile taranması, tipik araştırma deneği popülasyonu olan sağlıklı genç gönüllülere göre daha zordur. Tümörler ve lezyonlar, sinirsel HDR'yi maskeleyerek sinirsel aktiviteyle ilgili olmayan şekillerde kan akışını değiştirebilir. Gibi ilaçlar antihistaminikler ve hatta kafein HDR'yi etkileyebilir.[50] Bazı hastalar, bazı çalışmaları imkansız kılan kompülsif yalan söyleme gibi bozukluklardan muzdarip olabilir.[51] Klinik sorunları olanların uzun süre hareketsiz kalması daha zordur. Koltuk başlıkları veya ısırma çubukları kullanmak, tarayıcının içinde nöbet geçiren epilepsi hastalarına zarar verebilir; ısırık çubukları diş protezi olanları da rahatsız edebilir.[52]
Bu zorluklara rağmen, fMRI klinik olarak fonksiyonel alanları haritalamak, dil ve hafıza bölgelerinde sol-sağ hemisferik asimetriyi kontrol etmek, bir nöbetin sinirsel ilişkilerini kontrol etmek, beynin felçten nasıl kısmen iyileştiğini incelemek, bir ilacın veya davranışsal terapi çalışır, Alzheimer'ın başlangıcını tespit eder ve depresyon gibi bozuklukların varlığına dikkat edin. Fonksiyonel alanların haritalanması ve dil ve hafızanın lateralizasyonunun anlaşılması, cerrahların beyin dokusunu çalıştırmaları ve çıkarmaları gerektiğinde kritik beyin bölgelerini kaldırmamasına yardımcı olur. Bu, tümörlerin çıkarılmasında ve inatçı olmayan hastalarda özellikle önemlidir. Temporal lob epilepsi. Lezyon oluşturan tümörler, işlevsel olarak yararlı dokunun gereksiz yere çıkarılmamasını sağlamak için ameliyat öncesi planlama gerektirir. İyileşen depresif hastalar, serebellumda değişmiş fMRI aktivitesi göstermiştir ve bu, nüksetme eğilimini gösterebilir. İlaçlar uygulandıktan sonra beyin aktivitesini analiz eden farmakolojik fMRI, bir ilacın ilaçlara ne kadar nüfuz ettiğini kontrol etmek için kullanılabilir. Kan beyin bariyeri ve ilacın doz ve etki bilgileri.[53]
Hayvan araştırması
Araştırma öncelikle insan dışı primatlarda yapılır. rhesus makak. Bu çalışmalar hem insan sonuçlarını kontrol etmek veya tahmin etmek hem de fMRI tekniğinin kendisini doğrulamak için kullanılabilir. Ancak çalışmalar zordur çünkü bir hayvanı hareketsiz kalmaya motive etmek zordur ve meyve suyu gibi tipik teşvikler, hayvan onu yutarken kafa hareketini tetikler. Makak gibi daha büyük hayvanlardan oluşan bir koloninin sürdürülmesi de pahalıdır.[54]
Verilerin analizi
FMRI veri analizinin amacı, beyin aktivasyonu ile deneğin tarama sırasında gerçekleştirdiği bir görev arasındaki korelasyonları tespit etmektir. Ayrıca, öznede indüklenen hafıza ve tanıma gibi belirli bilişsel durumlarla korelasyonları keşfetmeyi amaçlamaktadır.[55] BOLD aktivasyon imzası nispeten zayıftır, bu nedenle elde edilen verilerdeki diğer gürültü kaynakları dikkatlice kontrol edilmelidir. Bu, görevle ilgili etkinleştirme için gerçek istatistiksel aramanın başlayabilmesi için önce alınan görüntüler üzerinde bir dizi işlem adımının gerçekleştirilmesi gerektiği anlamına gelir.[56] Bununla birlikte, örneğin, bir kişinin yaşadığı duyguları yalnızca fMRI'larından yüksek derecede doğrulukla tahmin etmek mümkündür.[57]
Gürültü kaynakları
Gürültü, çalışmanın ilgisini çekmeyen unsurlardan MR sinyalinde istenmeyen değişikliklerdir. FMRI'deki beş ana gürültü kaynağı, termal gürültü, sistem gürültüsü, fizyolojik gürültü, rastgele sinirsel aktivite ve hem insanlar arasında hem de bir kişi içindeki görevler arasında hem zihinsel stratejilerdeki hem de davranışlardaki farklılıklardır. Termal gürültü, statik alan gücüne paralel olarak çoğalır, ancak fizyolojik gürültü, alan gücünün karesi olarak çoğalır. Sinyal aynı zamanda alan gücünün karesi olarak çoğaldığından ve fizyolojik gürültü toplam gürültünün büyük bir oranı olduğundan, 3 T'nin üzerindeki daha yüksek alan güçleri her zaman orantılı olarak daha iyi görüntüler üretmez.
Isı, elektronların fMRI dedektöründe hareket etmesine ve akımı bozmasına neden olarak termal gürültü üretir. Sıcaklıkla birlikte termal gürültü artar. Ayrıca alıcı bobin tarafından tespit edilen frekans aralığına ve elektrik direncine de bağlıdır. Anatomiden bağımsız olarak tüm vokselleri benzer şekilde etkiler.[58]
Sistem gürültüsü görüntüleme donanımından geliyor. Bir biçim, süper iletken mıknatıs alanının zamanla sürüklenmesinin neden olduğu tarayıcı kaymasıdır. Diğer bir biçim, beynin kendi akım veya voltaj dağılımındaki değişikliklerdir ve alıcı bobinde değişikliklere neden olur ve duyarlılığını azaltır. Bu endüktans etkisini atlamak için empedans eşleştirme adı verilen bir prosedür kullanılır. Manyetik alandan tek tip olmayan gürültü de olabilir. Bu, genellikle manyetik alanı yamamak için, örneğin deneğin ağzına fiziksel olarak yerleştirilmiş küçük mıknatıslar olan şimşirici bobinler kullanılarak ayarlanır. Düzensizlikler genellikle kulak gibi beyin sinüslerine yakındır ve boşluğu uzun süre tıkamak rahatsız edici olabilir. Tarama işlemi MR sinyalini, üst üste binen uzamsal frekansların (yani numunenin hacminde tekrarlanan kenarlar) her birinin çizgilerle temsil edildiği k-uzayında elde eder. Bunu voksellere dönüştürmek, bazı kayıplar ve bozulmalara neden olur.[59]
Fizyolojik gürültü, tarayıcıda nefes alma, kalp atışları veya deneğin kıpır kıpır kıpır kıpır kıpır kıpır kıpır kıpır kıpır kıpır eden veya düğme basma gibi fiziksel tepkiler veren baş ve beyin hareketinden kaynaklanır. Baş hareketleri, tarama devam ederken voksel-nöron eşlemesinin değişmesine neden olur. FMRI dilimler halinde elde edildiğinden, hareketten sonra, bir voksel uzayda aynı mutlak konumu ifade etmeye devam ederken, altındaki nöronlar değişecektir. Diğer bir fizyolojik gürültü kaynağı, zaman içinde kan akışı, kan hacmi ve oksijen kullanım oranındaki değişikliktir. Bu son bileşen fizyolojik gürültünün üçte ikisine katkıda bulunur ve bu da toplam gürültüye ana katkı sağlar.[60]
En iyi deneysel tasarımla bile, bir özneye çarpan diğer tüm arka plan uyaranlarını kontrol etmek ve sınırlamak mümkün değildir - tarayıcı gürültüsü, rastgele düşünceler, fiziksel duyumlar ve benzeri. Bunlar deneysel manipülasyondan bağımsız olarak sinirsel aktivite üretir. Bunlar matematiksel modellemeye uygun değildir ve çalışma tasarımı tarafından kontrol edilmelidir.
Bir kişinin bir uyarana yanıt verme veya tepki verme ve sorunları çözme stratejileri genellikle zamanla ve görevler üzerinden değişir. Bu, bir denek içinde denemeden denemeye nöral aktivitede varyasyonlar oluşturur. İnsanlar arasında çok fazla sinirsel aktivite benzer nedenlerden dolayı farklılık gösterir. Araştırmacılar, katılımcıların söz konusu görev için tipik olarak nasıl performans gösterdiğini görmek için genellikle pilot çalışmalar yürütür. Ayrıca, taramadan önce bir deneme eğitim oturumunda deneklere nasıl yanıt verileceği veya tepki verileceği konusunda eğitim verirler.[61]
Ön işleme
Tarayıcı platformu, her TR'de deneğin kafasının 3 D hacmini oluşturur. Bu, taramadaki voksel başına bir değer olmak üzere bir dizi voksel yoğunluğu değerinden oluşur. Vokseller, üç boyutlu yapıyı tek bir çizgi halinde açarak birbiri ardına düzenlenir. Bir seanstan alınan bu tür birkaç cilt, deneğin kafa konumunu ayarlamadan tarayıcıda kaldığı süre boyunca bir çalışmaya karşılık gelen 4 D hacim oluşturmak üzere birleştirilir. Bu 4 D cilt, analiz için başlangıç noktasıdır. Bu analizin ilk kısmı ön işlemedir.
Ön işlemenin ilk adımı, geleneksel olarak dilim zamanlama düzeltmesidir. The MR scanner acquires different slices within a single brain volume at different times, and hence the slices represent brain activity at different timepoints. Since this complicates later analysis, a timing correction is applied to bring all slices to the same timepoint reference. This is done by assuming the timecourse of a voxel is smooth when plotted as a dotted line. Hence the voxel's intensity value at other times not in the sampled frames can be calculated by filling in the dots to create a continuous curve.
Head motion correction is another common preprocessing step. When the head moves, the neurons under a voxel move and hence its timecourse now represents largely that of some other voxel in the past. Hence the timecourse curve is effectively cut and pasted from one voxel to another. Motion correction tries different ways of undoing this to see which undoing of the cut-and-paste produces the smoothest timecourse for all voxels. The undoing is by applying a rigid-body transform to the volume, by shifting and rotating the whole volume data to account for motion. The transformed volume is compared statistically to the volume at the first timepoint to see how well they match, using a cost function such as ilişki veya karşılıklı bilgi. The transformation that gives the minimal cost function is chosen as the model for head motion. Since the head can move in a vastly varied number of ways, it is not possible to search for all possible candidates; nor is there right now an algorithm that provides a globally optimal solution independent of the first transformations we try in a chain.
Distortion corrections account for field nonuniformities of the scanner. One method, as described before, is to use shimming coils. Another is to recreate a field map of the main field by acquiring two images with differing echo times. If the field were uniform, the differences between the two images also would be uniform. Note these are not true preprocessing techniques since they are independent of the study itself. Bias field estimation is a real preprocessing technique using mathematical models of the noise from distortion, such as Markov rasgele alanları ve beklenti maksimizasyonu algorithms, to correct for distortion.
In general, fMRI studies acquire both many functional images with fMRI and a structural image with MRI. The structural image is usually of a higher resolution and depends on a different signal, the T1 magnetic field decay after excitation. To demarcate regions of interest in the functional image, one needs to align it with the structural one. Even when whole-brain analysis is done, to interpret the final results, that is to figure out which regions the active voxels fall in, one has to align the functional image to the structural one. This is done with a coregistration algorithm that works similar to the motion-correction one, except that here the resolutions are different, and the intensity values cannot be directly compared since the generating signal is different.
Typical MRI studies scan a few different subjects. To integrate the results across subjects, one possibility is to use a common brain atlas, and adjust all the brains to align to the atlas, and then analyze them as a single group. The atlases commonly used are the Talairach one, a single brain of an elderly woman created by Jean Talairach, ve Montreal Nöroloji Enstitüsü (MNI) one. The second is a probabilistic map created by combining scans from over a hundred individuals. This normalization to a standard template is done by mathematically checking which combination of stretching, squeezing, and warping reduces the differences between the target and the reference. While this is conceptually similar to motion correction, the changes required are more complex than just translation and rotation, and hence optimization even more likely to depend on the first transformations in the chain that is checked.
Temporal filtering is the removal of frequencies of no interest from the signal. A voxel's intensity change over time can be represented as the sum of a number of different repeating waves with differing periods and heights. A plot with these periods on the x-axis and the heights on the y-axis is called a güç spektrumu, and this plot is created with the Fourier dönüşümü tekniği. Temporal filtering amounts to removing the periodic waves not of interest to us from the power spectrum, and then summing the waves back again, using the ters Fourier dönüşümü to create a new timecourse for the voxel. A high-pass filter removes the lower frequencies, and the lowest frequency that can be identified with this technique is the reciprocal of twice the TR. A low-pass filter removes the higher frequencies, while a band-pass filter removes all frequencies except the particular range of interest.
Smoothing, or spatial filtering, is the idea of averaging the intensities of nearby voxels to produce a smooth spatial map of intensity change across the brain or region of interest. The averaging is often done by kıvrım Birlikte Gauss filtresi, which, at every spatial point, weights neighboring voxels by their distance, with the weights falling exponentially following the Çan eğrisi. If the true spatial extent of activation, that is the spread of the cluster of voxels simultaneously active, matches the width of the filter used, this process improves the sinyal gürültü oranı. It also makes the total noise for each voxel follow a bell-curve distribution, since adding together a large number of independent, identical distributions of any kind produces the bell curve as the limit case. But if the presumed spatial extent of activation does not match the filter, signal is reduced.[62]
istatistiksel analiz
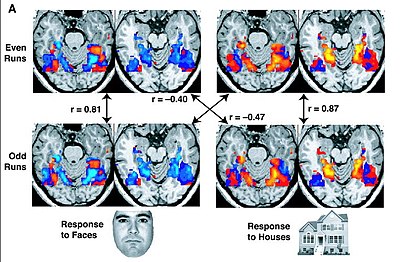
One common approach to analysing fMRI data is to consider each voxel separately within the framework of the general linear model. The model assumes, at every time point, that the HDR is equal to the scaled and summed version of the events active at that point. A researcher creates a design matrix specifying which events are active at any timepoint. One common way is to create a matrix with one column per overlapping event, and one row per time point, and to mark it if a particular event, say a stimulus, is active at that time point. One then assumes a specific shape for the HDR, leaving only its amplitude changeable in active voxels. The design matrix and this shape are used to generate a prediction of the exact HDR response of the voxel at every timepoint, using the mathematical procedure of kıvrım. This prediction does not include the scaling required for every event before summing them.
The basic model assumes the observed HDR is the predicted HDR scaled by the weights for each event and then added, with noise mixed in. This generates a set of linear equations with more equations than unknowns. A linear equation has an exact solution, under most conditions, when equations and unknowns match. Hence one could choose any subset of the equations, with the number equal to the number of variables, and solve them. But, when these solutions are plugged into the left-out equations, there will be a mismatch between the right and left sides, the error. The GLM model attempts to find the scaling weights that minimize the sum of the squares of the error. This method is provably optimal if the error were distributed as a bell curve, and if the scaling-and-summing model were accurate. For a more mathematical description of the GLM model, see genelleştirilmiş doğrusal modeller.
The GLM model does not take into account the contribution of relationships between multiple voxels. Whereas GLM analysis methods assess whether a voxel or region's signal amplitude is higher or lower for one condition than another, newer statistical models such as multi-voxel pattern analysis (MVPA), utilize the unique contributions of multiple voxels within a voxel-population. In a typical implementation, a classifier or more basic algorithm is trained to distinguish trials for different conditions within a subset of the data. The trained model is then tested by predicting the conditions of the remaining (independent) data. This approach is most typically achieved by training and testing on different scanner sessions or runs. If the classifier is linear, then the training model is a set of weights used to scale the value in each voxel before summing them to generate a single number that determines the condition for each testing set trial. More information on training and testing classifiers is at istatistiksel sınıflandırma.[63]
Combining with other methods
It is common to combine fMRI signal acquisition with tracking of participants' responses and reaction times. Physiological measures such as heart rate, breathing, skin conductance (rate of sweating), and eye movements are sometimes captured simultaneously with fMRI.[kaynak belirtilmeli ] The method can also be combined with other brain-imaging techniques such as transcranial stimulation, direct cortical stimulation ve özellikle, EEG.[64] The fMRI procedure can also be combined with near-infrared spectroscopy (NIRS) to have supplementary information about both oxyhemoglobin and deoxyhemoglobin.
The fMRI technique can complement or supplement other techniques because of its unique strengths and gaps. It can noninvasively record brain signals without risks of ionising radiation inherent in other scanning methods, such as CT veya EVCİL HAYVAN scans.[65] It can also record signal from all regions of the brain, unlike EEG/MEG, which are biased toward the cortical surface.[66] But fMRI temporal resolution is poorer than that of EEG since the HDR takes tens of seconds to climb to its peak. Combining EEG with fMRI is hence potentially powerful because the two have complementary strengths—EEG has high temporal resolution, and fMRI high spatial resolution. But simultaneous acquisition needs to account for the EEG signal from varying blood flow triggered by the fMRI gradient field, and the EEG signal from the static field.[67] Ayrıntılar için bkz. EEG vs fMRI.
While fMRI stands out due to its potential to capture neural processes associated with health and disease, brain stimulation techniques such as transcranial magnetic stimulation (TMS) have the power to alter these neural processes. Therefore, a combination of both is needed to investigate the mechanisms of action of TMS treatment and on the other hand introduce causality into otherwise pure correlational observations. The current state-of-the-art setup for these concurrent TMS/fMRI experiments comprises a large-volume head coil, usually a birdcage coil, with the MR-compatible TMS coil being mounted inside that birdcage coil. It was applied in a multitude of experiments studying local and network interactions. However, classic setups with the TMS coil placed inside MR birdcage-type head coil are characterised by poor signal to noise ratios compared to multi-channel receive arrays used in clinical neuroimaging today. Moreover, the presence of the TMS coil inside the MR birdcage coil causes artefacts beneath the TMS coil, i.e. at the stimulation target. For these reasons new MR coil arrays were currently developed [68] dedicated to concurrent TMS/fMRI experiments.[69]
Issues in fMRI
Tasarım
If the baseline condition is too close to maximum activation, certain processes may not be represented appropriately.[70] Another limitation on experimental design is head motion, which can lead to artificial intensity changes of the fMRI signal.[70]
In a block design, two or more conditions are alternated by blocks. Each block will have a duration of a certain number of fMRI scans and within each block only one condition is presented. By making the conditions differ in only the cognitive process of interest, the fMRI signal that differentiates the conditions should represent this cognitive process of interest. This is known as the subtraction paradigm.[71]The increase in fMRI signal in response to a stimulus is additive. This means that the amplitude of the hemodynamic response (HDR) increases when multiple stimuli are presented in rapid succession. When each block is alternated with a rest condition in which the HDR has enough time to return to baseline, a maximum amount of variability is introduced in the signal. As such, we conclude that block designs offer considerable statistical power.[72][73] There are however severe drawbacks to this method, as the signal is very sensitive to signal drift, such as head motion, especially when only a few blocks are used. Another limiting factor is a poor choice of baseline, as it may prevent meaningful conclusions from being drawn. There are also problems with many tasks lacking the ability to be repeated. Since within each block only one condition is presented, rastgeleleştirme of stimulus types is not possible within a block. This makes the type of stimulus within each block very predictable. As a consequence, participants may become aware of the order of the events.[72][73]
Event-related designs allow more real world testing, however, the statistical power of event related designs is inherently low, because the signal change in the BOLD fMRI signal following a single stimulus presentation is small.[74][75]
Both block and event-related designs are based on the subtraction paradigma, which assumes that specific cognitive processes can be added selectively in different conditions. Any difference in blood flow (the BOLD signal) between these two conditions is then assumed to reflect the differing cognitive process. In addition, this model assumes that a cognitive process can be selectively added to a set of active cognitive processes without affecting them.[71][açıklama gerekli ]
Baseline versus activity conditions
The brain is never completely at rest. It never stops functioning and firing neuronal signals, as well as using oxygen as long as the person in question is alive. In fact, in Stark and Squire's, 2001 study[76] When zero is not zero: The problem of ambiguous baseline conditions in fMRI, activity in the medial temporal lobe (as well as in other brain regions) was substantially higher during rest than during several alternative baseline conditions. The effect of this elevated activity during rest was to reduce, eliminate, or even reverse the sign of the activity during task conditions relevant to memory functions. These results demonstrate that periods of rest are associated with significant cognitive activity and are therefore not an optimal baseline for cognition tasks. In order to discern baseline and activation conditions it is necessary to interpret a lot of information. This includes situations as simple as breathing. Periodic blocks may result in identical data of other variance in the data if the person breathes at a regular rate of 1 breath/5sec, and the blocks occur every 10s, thus impairing the data.
Reverse inference
Neuroimaging methods such as fMRI and MRI offer a measure of the activation of certain brain areas in response to cognitive tasks engaged in during the scanning process. Data obtained during this time allow cognitive neuroscientists to gain information regarding the role of particular brain regions in cognitive function.[77] However, an issue arises when certain brain regions are alleged by researchers to identify the activation of previously labeled cognitive processes.[78] Poldrack[79] clearly describes this issue:
- The usual kind of inference that is drawn from neuroimaging data is of the form ‘if cognitive process X is engaged, then brain area Z is active.’ Perusal of the discussion sections of a few fMRI articles will quickly reveal, however, an epidemic of reasoning taking the following form:
- (1) In the present study, when task comparison A was presented, brain area Z was active.
- (2) In other studies, when cognitive process X was putatively engaged, then brain area Z was active.
- (3) Thus, the activity of area Z in the present study demonstrates engagement of cognitive process X by task comparison A.
- This is a ‘reverse inference’, in that it reasons backwards from the presence of brain activation to the engagement of a particular cognitive function.
Reverse inference demonstrates the logical fallacy of affirming what you just found, although this logic could be supported by instances where a certain outcome is generated solely by a specific occurrence. With regard to the brain and brain function it is seldom that a particular brain region is activated solely by one cognitive process.[79] Some suggestions to improve the legitimacy of reverse inference have included both increasing the selectivity of response in the brain region of interest and increasing the önceki olasılık of the cognitive process in question.[79] However, Poldrack[77] suggests that reverse inference should be used merely as a guide to direct further inquiry rather than a direct means to interpret results.
Forward inference
Forward inference is a data driven method that uses patterns of brain activation to distinguish between competing cognitive theories. It shares characteristics with cognitive psychology's dissociation logic and philosophy's ileri zincirleme. For example, Henson[80] discusses forward inference's contribution to the "single process theory vs. dual process theory " debate with regard to tanıma hafızası. Forward inference supports the dual process theory by demonstrating that there are two qualitatively different brain activation patterns when distinguishing between "remember vs. know judgments ". The main issue with forward inference is that it is a correlational method. Therefore, one cannot be completely confident that brain regions activated during cognitive process are completely necessary for that execution of those processes.[77] In fact, there are many known cases that demonstrate just that. For example, the hippocampus has been shown to be activated during klasik koşullanma,[81] however lesion studies have demonstrated that classical conditioning can occur without the hippocampus.[82]
Riskler
The most common risk to participants in an fMRI study is klostrofobi[83] and there are reported risks for pregnant women to go through the scanning process.[84] Scanning sessions also subject participants to loud high-pitched noises from Lorentz kuvvetleri induced in the gradient coils by the rapidly switching current in the powerful static field. The gradient switching can also induce currents in the body causing nerve tingling. Implanted medical devices such as kalp pilleri could malfunction because of these currents. The radio-frequency field of the excitation coil may heat up the body, and this has to be monitored more carefully in those running a fever, the diabetic, and those with circulatory problems. Local burning from metal necklaces and other jewellery is also a risk.[85]
The strong static magnetic field can cause damage by pulling in nearby heavy metal objects converting them to projectiles.[86]
There is no proven risk of biological harm from even very powerful static magnetic fields.[87][88] Ancak, genotoksik (i.e., potentially carcinogenic) effects of MRI scanning have been demonstrated in vivo and in vitro,[89][90][91][92] leading a recent review to recommend "a need for further studies and prudent use in order to avoid unnecessary examinations, according to the ihtiyat ilkesi ".[88] In a comparison of genotoxic effects of MRI compared with those of CT scans, Knuuti et al. reported that even though the DNA damage detected after MRI was at a level comparable to that produced by scans using ionizing radiation (low-dose coronary CT angiography, nuclear imaging, and X-ray angiography), differences in the mechanism by which this damage takes place suggests that the cancer risk of MRI, if any, is unknown.[93]
Gelişmiş yöntemler
The first fMRI studies validated the technique against brain activity known, from other techniques, to be correlated to tasks. By the early 2000s, fMRI studies began to discover novel correlations. Still their technical disadvantages have spurred researchers to try more advanced ways to increase the power of both clinical and research studies.
Better spatial resolution
MRI, in general, has better spatial resolution than EEG and MEG, but not as good a resolution as invasive procedures such as single-unit electrodes. While typical resolutions are in the millimeter range, ultra-high-resolution MRI or MR spectroscopy works at a resolution of tens of micrometers. It uses 7 T fields, small-bore scanners that can fit small animals such as rats, and external contrast agents such as fine iron oxide. Fitting a human requires larger-bore scanners, which make higher fields strengths harder to achieve, especially if the field has to be uniform; it also requires either internal contrast such as BOLD or a non-toxic external contrast agent unlike iron oxide.
Parallel imaging is another technique to improve spatial resolution. This uses multiple coils for excitation and reception. Spatial resolution improves as the square root of the number of coils used. This can be done either with a phased array where the coils are combined in parallel and often sample overlapping areas with gaps in the sampling or with massive coil arrays, which are a much denser set of receivers separate from the excitation coils. These, however, pick up signals better from the brain surface, and less well from deeper structures such as the hipokamp.[kaynak belirtilmeli ]
Better temporal resolution
Temporal resolution of fMRI is limited by: (1) the feedback mechanism that raises the blood flow operating slowly; (2) having to wait till net magnetization recovers before sampling a slice again; and (3) having to acquire multiple slices to cover the whole brain or region of interest. Advanced techniques to improve temporal resolution address these issues. Using multiple coils speeds up acquisition time in exact proportion to the coils used. Another technique is to decide which parts of the signal matter less and drop those. This could be either those sections of the image that repeat often in a spatial map (that is small clusters dotting the image periodically) or those sections repeating infrequently (larger clusters). The first, a high-pass filter in k-space, has been proposed by Gary H. Glover ve şuradaki meslektaşlarım Stanford. These mechanisms assume the researcher has an idea of the expected shape of the activation image.
Typical gradient-echo EPI uses two gradient coils within a slice, and turns on first one coil and then the other, tracing a set of lines in k-space. Turning on both gradient coils can generate angled lines, which cover the same grid space faster. Both gradient coils can also be turned on in a specific sequence to trace a spiral shape in k-space. This spiral imaging sequence acquires images faster than gradient-echo sequences, but needs more math transformations (and consequent assumptions) since converting back to voxel space requires the data be in grid form (a set of equally spaced points in both horizontal and vertical directions).
New contrast mechanisms
BOLD contrast depends on blood flow, which is both slowly changing and subject to noisy influences. Other biomarkers now looked at to provide better contrast include temperature, acidity/alkalinity (pH), calcium-sensitive agents, neuronal magnetic field, and the Lorentz effect. Temperature contrast depends on changes in brain temperature from its activity. The initial burning of glucose raises the temperature, and the subsequent inflow of fresh, cold blood lowers it. These changes alter the magnetic properties of tissue. Since the internal contrast is too difficult to measure, external agents such tülyum compounds are used to enhance the effect. Contrast based on pH depends on changes in the acid/alkaline balance of brain cells when they go active. This too often uses an external agent. Calcium-sensitive agents make MRI more sensitive to calcium concentrations, with calcium ions often being the messengers for hücresel sinyalleşme pathways in active neurons. Neuronal magnetic field contrast measures the magnetic and electric changes from neuronal firing directly. Lorentz-effect imaging tries to measure the physical displacement of active neurons carrying an electric current within the strong static field.[94]
Ticari kullanım
Some experiments have shown the neural correlates of peoples' brand preferences. Samuel M. McClure used fMRI to show the dorsolateral prefrontal korteks, hippocampus and orta beyin were more active when people knowingly drank Coca-Cola as opposed to when they drank unlabeled Coke.[95] Other studies have shown the brain activity that characterizes men's preference for sports cars, and even differences between Democrats and Republicans in their reaction to campaign commercials with images of the 9/11 attacks. Nöropazarlama companies have seized on these studies as a better tool to poll user preferences than the conventional survey technique. One such company was BrightHouse,[96] now shut down[97]. Another is Oxford, UK-based Neurosense,[98] which advises clients how they could potentially use fMRI as part of their marketing business activity.[99] A third is Sales Brain in California.[100]
At least two companies have been set up to use fMRI in yalan tespiti: No Lie MRI and the Cephos Corporation [101]. No Lie MRI charges close to $5000 for its services. These companies depend on evidence such as that from a study by Joshua Greene at Harvard Üniversitesi önermek Prefrontal korteks is more active in those contemplating lying.[102]
However, there is still a fair amount of controversy over whether these techniques are reliable enough to be used in a legal setting [103]. Some studies indicate that while there is an overall positive correlation, there is a great deal of variation between findings and in some cases considerable difficulty in replicating the findings.[104] A federal magistrate judge in Tennessee prohibited fMRI evidence to back up a defendant's claim of telling the truth, on the grounds that such scans do not measure up to the legal standard of scientific evidence.[105]. Most researchers agree that the ability of fMRI to detect deception in a real life setting has not been established.[8][106]
Use of the fMRI has been left out of legal debates throughout its history. Use of this technology has not been allowed due to holes in the evidence supporting fMRI. First, most evidence supporting fMRIs accuracy was done in a lab under controlled circumstances with solid facts. This type of testing does not pertain to real life. Real-life scenarios can be much more complicated with many other affecting factors.[107] It has been shown that many other factors affect BOLD other than a typical lie. There have been tests done showing that drug use alters blood flow in the brain, which drastically affects the outcome of BOLD testing. Furthermore, individuals with diseases or disorders such as schizophrenia or compulsive lying can lead to abnormal results as well. Lastly, there is an ethical question relating to fMRI scanning. This testing of BOLD has led to controversy over if fMRIs are an invasion of privacy. Being able to scan and interpret what people are thinking may be thought of as immoral and the controversy still continues.[108]
Because of these factors and more, fMRI evidence has been excluded from any form of legal system. The testing is too uncontrolled and unpredictable. Therefore, it has been stated that fMRI has much more testing to do before it can be considered viable in the eyes the legal system.[109]
Eleştiri
Some scholars have criticized fMRI studies for problematic statistical analyses, often based on low-güç, small-sample studies.[110][111] Other fMRI researchers have defended their work as valid.[112] In 2018, Turner and colleagues have suggested that the small sizes affect the replicability of task-based fMRI studies and claimed that even datasets with at least 100 participants the results may not be well replicated,[113] although there are debates on it.[114][115]
In one real but satirical fMRI study, a dead salmon was shown pictures of humans in different emotional states. The authors provided evidence, according to two different commonly used statistical tests, of areas in the salmon's brain suggesting meaningful activity. The study was used to highlight the need for more careful statistical analyses in fMRI research, given the large number of voxels in a typical fMRI scan and the çoklu karşılaştırma problemi.[116][117] Before the controversies were publicized in 2010, between 25-40% of studies on fMRI being published were not using the corrected comparisons. But by 2012, that number had dropped to 10%.[118] Dr. Sally Satel, writing in Time, cautioned that while brain scans have scientific value, individual brain areas often serve multiple purposes and "reverse inferences" as commonly used in press reports carry a significant chance of drawing invalid conclusions.[119]In 2015, it was discovered that a statistical bug was found in the fMRI computations which likely invalidated at least 40,000 fMRI studies preceding 2015, and researchers suggest that results prior to the bug fix cannot be relied upon.[120][121] Furthermore, it was later shown that how one sets the parameters in the software determines the false positive rate. In other words, study outcome can be determined by changing software parameters.[122]
In 2020 professor Ahmad Hariri, (Duke University) one of the first researchers to use fMRI, performed a largescale experiment that sought to test the reliability of fMRI on individual people.In the study, he copied protocols from 56 published papers in psychology that used fMRI. The results suggest that fMRI has poor reliability when it comes to individual cases, but good reliability when it comes to general human thought patterns[123][124][125]
Ayrıca bakınız
- Beyin fonksiyonu
- Beyin haritalama
- Olayla ilgili fMRI
- Fonksiyonel nörogörüntüleme
- Functional ultrasound imaging
- Nörobilim veritabanları listesi
- Signal enhancement by extravascular water protons (SEEP fMRI)
Notlar
Alıntılar
- ^ "Magnetic Resonance, a critical peer-reviewed introduction; functional MRI". Avrupa Manyetik Rezonans Forumu. Alındı 17 Kasım 2014.
- ^ Huettel, Song & McCarthy (2009)
- ^ Logothetis, N. K.; Pauls, Jon; Auguth, M.; Trinath, T.; Oeltermann, A. (July 2001). "A neurophysiological investigation of the basis of the BOLD signal in fMRI". Doğa. 412 (6843): 150–157. Bibcode:2001Natur.412..150L. doi:10.1038/35084005. PMID 11449264. S2CID 969175.
Our results show unequivocally that a spatially localized increase in the BOLD contrast directly and monotonically reflects an increase in neural activity.
- ^ a b Huettel, Song & McCarthy (2009, s. 26)
- ^ Huettel, Song & McCarthy (2009, s. 4)
- ^ Thomas, Roger K (1 January 1993). "INTRODUCTION: A Biopsychology Festschrift in Honor of Lelon J. Peacock". Genel Psikoloji Dergisi. 120 (1): 5.
- ^ Detre, John A.; Rao, Hengyi; Wang, Danny J.J.; Chen, Yu Fen; Wang, Ze (May 2012). "Applications of arterial spin labeled MRI in the brain". Manyetik Rezonans Görüntüleme Dergisi. 35 (5): 1026–1037. doi:10.1002/jmri.23581. PMC 3326188. PMID 22246782.
- ^ a b Langleben, D. D.; Moriarty, J. C. (2013). "Using Brain Imaging for Lie Detection: Where Science, Law and Research Policy Collide". Psychol Public Policy Law. 19 (2): 222–234. doi:10.1037/a0028841. PMC 3680134. PMID 23772173.CS1 Maint: yazar parametresini kullanır (bağlantı)
- ^ Huettel, Song & McCarthy (2009, pp. 198–200, 208–211)
- ^ Huettel, Song & McCarthy (2009, s. 168); Roy & Sherrington (1890)
- ^ Huettel, Song & McCarthy (2009, pp. 198–200, 208–211)
- ^ Sandrone, Stefano; Bacigaluppi, Marco; Galloni, Marco R .; Martino, Gianvito (November 2012). "Angelo Mosso (1846–1910)". Nöroloji Dergisi. 259 (11): 2513–2514. doi:10.1007/s00415-012-6632-1. PMID 23010944. S2CID 13365830.
- ^ a b c Sandrone, Stefano; Bacigaluppi, Marco; Galloni, Marco R .; Cappa, Stefano F .; Moro, Andrea; Catani, Marco; Filippi, Massimo; Monti, Martin M.; Perani, Daniela; Martino, Gianvito (February 2014). "Beyin aktivitesini dengeyle tartmak: Angelo Mosso'nun orijinal el yazmaları gün ışığına çıktı". Beyin. 137 (2): 621–633. doi:10.1093 / beyin / awt091. PMID 23687118.
- ^ Field, David T.; Inman, Laura A. (February 2014). "Weighing brain activity with the balance: a contemporary replication of Angelo Mosso's historical experiment". Beyin. 137 (2): 634–639. doi:10.1093/brain/awt352. PMID 24408614.
- ^ Raichle (2000, s. 39)
- ^ Logothetis (2008, s. S3); Ogawa et al. (1990)
- ^ Belliveau, J.; Kennedy, D .; McKinstry, R.; Buchbinder, B.; Weisskoff, R.; Cohen, M .; Vevea, J.; Brady, T.; Rosen, B. (1 November 1991). "Manyetik rezonans görüntüleme ile insan görsel korteksinin fonksiyonel haritalaması". Bilim. 254 (5032): 716–719. Bibcode:1991Sci...254..716B. doi:10.1126 / science.1948051. PMID 1948051.
- ^ Huettel, Song & McCarthy (2009, pp. 204–5)
- ^ Kwong, K K; Belliveau, J W; Chesler, D A; Goldberg, I E; Weisskoff, R M; Poncelet, B P; Kennedy, D N; Hoppel, B E; Cohen, M S; Turner, R (15 June 1992). "Dynamic magnetic resonance imaging of human brain activity during primary sensory stimulation". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 89 (12): 5675–5679. Bibcode:1992PNAS...89.5675K. doi:10.1073 / pnas.89.12.5675. PMC 49355. PMID 1608978.
- ^ Huettel, Song & McCarthy (2009, pp. 205–208)
- ^ Huettel, Song & McCarthy (2009, s. 6–7)
- ^ Huettel, Song & McCarthy (2009, s. 199)
- ^ Huettel, Song & McCarthy (2009, s. 194)
- ^ Huettel, Song & McCarthy (2009, pp. 220–229)
- ^ Huettel, Song & McCarthy (2009, s. 208–214)
- ^ Ogawa & Sung (2007)
- ^ Huettel, Song & McCarthy (2009, pp. 243–45)
- ^ Sharoh, Daniel; van Mourik, Tim; Bains, Lauren J.; Segaert, Katrien; Weber, Kirsten; Hagoort, Peter; Norris, David G. (15 October 2019). "Laminar specific fMRI reveals directed interactions in distributed networks during language processing". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 116 (42): 21185–21190. doi:10.1073/pnas.1907858116. PMC 6800353. PMID 31570628.
- ^ Huettel, Song & McCarthy (2009, pp. 214–220)
- ^ Logothetis (2008, pp. S4–S6)
- ^ Carr, Rissman & Wagner (2010)
- ^ Huettel, Song & McCarthy (2009, pp. 220–29)
- ^ Cohen, Mark S. (August 1997). "Parametric Analysis of fMRI Data Using Linear Systems Methods". NeuroImage. 6 (2): 93–103. doi:10.1006/nimg.1997.0278. PMID 9299383. S2CID 7708045.
- ^ Boynton, Geoffrey M.; Engel, Stephen A.; Glover, Gary H.; Heeger, David J. (1 July 1996). "Linear Systems Analysis of Functional Magnetic Resonance Imaging in Human V1". Nörobilim Dergisi. 16 (13): 4207–4221. doi:10.1523/JNEUROSCI.16-13-04207.1996. PMC 6579007. PMID 8753882.
- ^ Huettel, Song & McCarthy (2009, pp. 229–37)
- ^ Logothetis, Nikos K.; Pauls, Jon; Augath, Mark; Trinath, Torsten; Oeltermann, Axel (July 2001). "Neurophysiological investigation of the basis of the fMRI signal". Doğa. 412 (6843): 150–157. Bibcode:2001Natur.412..150L. doi:10.1038/35084005. PMID 11449264. S2CID 969175.
- ^ Kim vd. (2000, pp. 109–110)
- ^ Huettel, Song & McCarthy (2009, pp. 209–210)
- ^ Bulte (2006, s. 48)
- ^ Logothetis (2008, s. S7–S8)
- ^ Huettel, Song & McCarthy (2009, pp. 209–210)
- ^ Kim vd. (2000, pp. 107–109)
- ^ Desai, M .; Kahn, I.; Knoblich, U.; Bernstein, J .; Atallah, H.; Yang, A .; Kopell, N.; Buckner, R. L .; Graybiel, A. M.; Moore, C. I.; Boyden, E. S. (2011). "Mapping brain networks in awake mice using combined optical neural control and fMRI". Nörofizyoloji Dergisi. 105 (3): 1393–1405. doi:10.1152/jn.00828.2010. PMC 3074423. PMID 21160013.
- ^ Lee, Jin Hyung; Durand, Remy; Gradinaru, Viviana; Zhang, Feng; Goshen, Inbal; Kim, Dae-Shik; Fenno, Lief E.; Ramakrishnan, Charu; Deisseroth, Karl (June 2010). "Tip ve kablolamaya göre optogenetik olarak tanımlanan nöronlar tarafından yönlendirilen global ve yerel fMRI sinyalleri". Doğa. 465 (7299): 788–792. Bibcode:2010Natur.465..788L. doi:10.1038 / nature09108. PMC 3177305. PMID 20473285.
- ^ Kahn, I.; Desai, M .; Knoblich, U.; Bernstein, J .; Henninger, M.; Graybiel, A. M.; Boyden, E. S.; Buckner, R. L .; Moore, C. I. (19 October 2011). "Characterization of the Functional MRI Response Temporal Linearity via Optical Control of Neocortical Pyramidal Neurons". Nörobilim Dergisi. 31 (42): 15086–15091. doi:10.1523/JNEUROSCI.0007-11.2011. PMC 3225054. PMID 22016542.
- ^ Dale, Anders M.; Buckner, Randy L. (1997). "Selective averaging of rapidly presented individual trials using fMRI". İnsan Beyin Haritalama. 5 (5): 329–340. doi:10.1002/(SICI)1097-0193(1997)5:5<329::AID-HBM1>3.0.CO;2-5. PMID 20408237.
- ^ (Functional MR Imaging (fMRI) - Brain 2011 )
- ^ Subbaraju, Vigneshwaran; Sundaram, Suresh; Narasimhan, Sundararajan (March 2018). "Identification of lateralized compensatory neural activities within the social brain due to autism spectrum disorder in adolescent males". Avrupa Nörobilim Dergisi. 47 (6): 631–642. doi:10.1111/ejn.13634. PMID 28661076. S2CID 4306986.
- ^ Rombouts, Barkhof & Sheltens (2007, s. 1)
- ^ Rombouts, Barkhof & Sheltens (2007, s. 4–5)
- ^ Rombouts, Barkhof & Sheltens (2007, s. 10)
- ^ Rombouts, Barkhof & Sheltens (2007, s. 14)
- ^ Rombouts, Barkhof & Sheltens (2007, pp. 18–26)
- ^ Huettel, Song & McCarthy (2009, pp. 476–80)
- ^ Logothetis (2008)
- ^ Huettel, Song & McCarthy (2009, sayfa 243–244)
- ^ Görmek bu gelen makale Şimdi Felsefe magazine, which states that computers could predict emotional states purely from fMRI data in between 70% and 84% of cases.
- ^ Huettel, Song & McCarthy (2009, pp. 256–8)
- ^ Huettel, Song & McCarthy (2009, pp. 258–9)
- ^ Huettel, Song & McCarthy (2009, pp. 259–62)
- ^ Huettel, Song & McCarthy (2009, pp. 262–7); Lindquist (2008)
- ^ Preprocessing is summarized from Huettel, Song & McCarthy (2009, pp. 267–289), modified by the newer review by Lindquist (2008, pp. 11–13).
- ^ For the basic GLM model, see the description by Huettel, Song & McCarthy (2009, pp. 343–256). MVPA and multivoxel pattern classification are covered in the same text in pp. 408–415.
- ^ Huettel, Song & McCarthy (2009, s. 449)
- ^ Huettel, Song & McCarthy (2009, s. 4); Logothetis (2008)
- ^ Ilmoniemi & Aronen (2000, s. 454)
- ^ Huettel, Song & McCarthy (2009, s. 449)
- ^ "Concurrent TMS/fMRI » fmri.at | neuroimaging & stimulation".
- ^ Navarro de Lara, Lucia I.; Tik, Martin; Woletz, Michael; Frass-Kriegl, Roberta; Moser, Ewald; Laistler, Elmar; Windischberger, Christian (April 2017). "High-sensitivity TMS/fMRI of the Human Motor Cortex Using a Dedicated Multichannel MR Coil". NeuroImage. 150: 262–269. doi:10.1016/j.neuroimage.2017.02.062. PMID 28254457. S2CID 3676325.
- ^ a b Haller S.; Bartsch A. (2009). "Pitfalls in fMRI". Avrupa Radyolojisi. 19 (11): 2689–2706. doi:10.1007/s00330-009-1456-9. PMID 19504107. S2CID 26759374.
- ^ a b Grabowski, T.J.; Damasio, A.R. (2000). "Investigating Language with Functional Neuroimaging". Brain Mapping: The Systems. s. 425–461. doi:10.1016/B978-012692545-6/50016-7. ISBN 978-0-12-692545-6.
- ^ a b Aguirre, G.K.; D'Esposito, M. (1999). "Experimental design for brain fMRI". In Bandettini, P.A.; Moonen, C. (eds.). Fonksiyonel MR. Berlin: Springer-Verlag. s. 369–380.
- ^ a b Donaldson, D.; Bucknar, R. (2001). "Effective paradigm design". In Jezzard, P.; Matthews, P. M.; Smith, S. M. (eds.). Functional MRI: An introduction to methods. New York: Oxford University Press. s. 177–195.
- ^ Rosen, Bruce R.; Buckner, Randy L .; Dale, Anders M. (3 February 1998). "Event-related functional MRI: Past, present, and future". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 95 (3): 773–780. Bibcode:1998PNAS...95..773R. doi:10.1073/pnas.95.3.773. PMC 33797. PMID 9448240.
- ^ D'Esposito, Mark; Zarahn, Eric; Aguirre, Geoffrey K. (1999). "Event-related functional MRI: Implications for cognitive psychology". Psikolojik Bülten. 125 (1): 155–164. doi:10.1037/0033-2909.125.1.155. PMID 9990848.
- ^ Stark, Craig E. L.; Squire, Larry R. (23 October 2001). "When zero is not zero: The problem of ambiguous baseline conditions in fMRI". Amerika Birleşik Devletleri Ulusal Bilimler Akademisi Bildirileri. 98 (22): 12760–12766. Bibcode:2001PNAS...9812760S. doi:10.1073/pnas.221462998. PMC 60127. PMID 11592989.
- ^ a b c Poldrack RA (2008). "The role of fMRI in cognitive neuroscience: where do we stand?". Curr. Opin. Nörobiyol. 18 (2): 223–7. doi:10.1016/j.conb.2008.07.006. PMID 18678252. S2CID 14983903.
- ^ Harrison, Glenn W. (November 2008). "Neuroeconomics: A Rejoiner". Ekonomi ve Felsefe. 24 (3): 533–544. doi:10.1017/s0266267108002149. S2CID 154376751.
- ^ a b c Poldrack, R (February 2006). "Can cognitive processes be inferred from neuroimaging data?" (PDF). Bilişsel Bilimlerdeki Eğilimler. 10 (2): 59–63. doi:10.1016/j.tics.2005.12.004. PMID 16406760. S2CID 13498984.
- ^ Henson R (2006). "Forward inference using functional neuroimaging: dissociations versus associations". Trends Cogn. Sci. (Düzenleyici Ed.). 10 (2): 64–9. doi:10.1016/j.tics.2005.12.005. PMID 16406759. S2CID 27185.
- ^ Knight, David C.; Smith, Christine N.; Cheng, Dominic T.; Stein, Elliot A.; Helmstetter, Fred J. (September 2004). "Amygdala and hippocampal activity during acquisition and extinction of human fear conditioning". Bilişsel, Duyuşsal ve Davranışsal Sinirbilim. 4 (3): 317–325. doi:10.3758/cabn.4.3.317. PMID 15535167.
- ^ Gabrieli, John D. E.; McGlinchey-Berroth, Regina; Carrillo, Maria C.; Gluck, Mark A .; Cermak, Laird S.; Disterhoft, John F. (1995). "Intact delay-eyeblink classical conditioning in amnesia". Davranışsal Sinirbilim. 109 (5): 819–827. doi:10.1037//0735-7044.109.5.819. PMID 8554707.
- ^ Huettel, Song & McCarthy (2009, s. 53)
- ^ Sahito & Slany (2012, s. 60)
- ^ Huettel, Song & McCarthy (2009, pp. 50–52)
- ^ Huettel, Song & McCarthy (2009, s. 44)
- ^ Formica, Domenico; Silvestri, Sergio (22 April 2004). "Biological effects of exposure to magnetic resonance imaging: an overview". BioMedical Engineering OnLine. 3: 11. doi:10.1186/1475-925X-3-11. PMC 419710. PMID 15104797.
- ^ a b Hartwig, Valentina; Giovannetti, Giulio; Vanello, Nicola; Lombardi, Massimo; Landini, Luigi; Simi, Silvana (2009). "Biological Effects and Safety in Magnetic Resonance Imaging: A Review". Uluslararası Çevre Araştırmaları ve Halk Sağlığı Dergisi. 6 (6): 1778–1798. doi:10.3390/ijerph6061778. PMC 2705217. PMID 19578460.
- ^ Fiechter, Michael; Stehli, Julia; Fuchs, Tobias A.; Dougoud, Svetlana; Gaemperli, Oliver; Kaufmann, Philipp A. (7 August 2013). "Impact of cardiac magnetic resonance imaging on human lymphocyte DNA integrity". Avrupa Kalp Dergisi. 34 (30): 2340–2345. doi:10.1093/eurheartj/eht184. PMC 3736059. PMID 23793096.
- ^ Lee, Joong Won; Kim, Myeong Seong; Kim, Yang Jee; Choi, Young Joo; Lee, Younghyun; Chung, Hai Won (October 2011). "Genotoxic effects of 3 T magnetic resonance imaging in cultured human lymphocytes". Biyoelektromanyetik. 32 (7): 535–542. doi:10.1002/bem.20664. PMID 21412810.
- ^ Simi, Silvana; Ballardin, Michela; Casella, Marta; De Marchi, Daniele; Hartwig, Valentina; Giovannetti, Giulio; Vanello, Nicola; Gabbriellini, Sabrina; Landini, Luigi; Lombardi, Massimo (October 2008). "Is the genotoxic effect of magnetic resonance negligible? Low persistence of micronucleus frequency in lymphocytes of individuals after cardiac scan". Mutasyon Araştırması / Mutagenezin Temel ve Moleküler Mekanizmaları. 645 (1–2): 39–43. doi:10.1016 / j.mrfmmm.2008.08.011. PMID 18804118.
- ^ Suzuki, Y .; Ikehata, M; Nakamura, K; Nishioka, M; Asanuma, K; Koana, T; Shimizu, H (1 Kasım 2001). "Statik manyetik alanlara maruz kalan farelerde mikronüklei indüksiyonu". Mutagenez. 16 (6): 499–501. doi:10.1093 / mutage / 16.6.499. PMID 11682641.
- ^ Knuuti, J .; Saraste, A .; Kallio, M .; Minn, H. (2 Ağustos 2013). "Kardiyak manyetik rezonans görüntüleme DNA hasarına neden oluyor mu?". Avrupa Kalp Dergisi. 34 (30): 2337–2339. doi:10.1093 / eurheartj / eht214. PMID 23821403.
- ^ Huettel, Şarkı ve McCarthy (2009, s. 420–40).
- ^ Lowenberg (2008); (Beyin dolandırıcılığı mı? 2004 ); McClure vd. (2004)
- ^ (Beyin dolandırıcılığı mı? 2004 )
- ^ Lowenberg (2008)
- ^ Devlin (2012)
- ^ (Beyin dolandırıcılığı mı? 2004 )
- ^ Brammer (2004)
- ^ Sahito ve Slany (2012, s. 57)
- ^ Narayan (2009)
- ^ Sahito ve Slany (2012, s. 41)
- ^ Narayan (2009)
- ^ Miller (2010)
- ^ Narayan (2009)
- ^ Mobbs, Dean; Lau, Hakwan C; Jones, Owen D; Frith, Christopher D (17 Nisan 2007). "Hukuk, Sorumluluk ve Beyin". PLOS Biyolojisi. 5 (4): e103. doi:10.1371 / journal.pbio.0050103. PMC 1852146. PMID 17439297. S2CID 7519294.
- ^ Simpson, JR (2008). "Fonksiyonel MRI yalan tespiti: gerçek olamayacak kadar iyi mi?". Amerikan Psikiyatri Akademisi ve Hukuk Dergisi. 36 (4): 491–8. PMID 19092066.
- ^ Gaudet Lyn M. (2011). "Beyin parmak izi, bilimsel kanıt ve Daubert: Hindistan'dan bir uyarı dersi". Jurimetrics. 51 (3): 293–318. JSTOR 41307131.
- ^ Vul, Edward; Harris, Christine; Winkielman, Piotr; Pashler Harold (Mayıs 2009). "FMRI Duygu, Kişilik ve Sosyal Biliş Çalışmalarında Şaşırtıcı Derecede Yüksek Korelasyonlar". Psikolojik Bilimler Üzerine Perspektifler. 4 (3): 274–290. doi:10.1111 / j.1745-6924.2009.01125.x. PMID 26158964. S2CID 242553.
- ^ Rinck PA (2005). "Rinckside - İşlevsel görüntüleme, 'satın alma' tetikleyicisinin aranmasına yol açar". Rinckside.
- ^ Lieberman, Matthew D .; Berkman, Elliot T .; Wager, Tor D. (Mayıs 2009). "Sosyal Sinirbilimdeki İlişkiler Voodoo Değildir: Vul ve diğerleri (2009) Üzerine Yorum". Psikolojik Bilimler Üzerine Perspektifler. 4 (3): 299–307. doi:10.1111 / j.1745-6924.2009.01128.x. PMC 5017149. PMID 26158967.
- ^ Turner, Benjamin O .; Paul, Erick J .; Miller, Michael B .; Barbey, Aron K. (Aralık 2018). "Küçük örnek boyutları, görev tabanlı fMRI çalışmalarının tekrarlanabilirliğini azaltır". İletişim Biyolojisi. 1 (1): 62. doi:10.1038 / s42003-018-0073-z. PMC 6123695. PMID 30271944.
- ^ Nee, Derek Evan (Aralık 2019). "fMRI tekrarlanabilirliği, yeterli bireysel düzeydeki verilere bağlıdır". İletişim Biyolojisi. 2 (1): 130. doi:10.1038 / s42003-019-0378-6. PMC 6461660. PMID 30993214.
- ^ Turner, Benjamin O .; Santander, Tyler; Paul, Erick J .; Barbey, Aron K .; Miller, Michael B. (Aralık 2019). "Yanıt: fMRI tekrarlanabilirliği, yeterli bireysel düzeydeki verilere bağlıdır". İletişim Biyolojisi. 2 (1): 129. doi:10.1038 / s42003-019-0379-5. PMC 6461603. PMID 30993213.
- ^ Margulies Daniel S. (2011). "Şüphe Somonu". Kritik Sinirbilim. s. 273–285. doi:10.1002 / 9781444343359.ch13. ISBN 978-1-4443-4335-9.
- ^ Bennett, Cm; Miller, Mb; Wolford, Gl (Temmuz 2009). "Post-mortem Atlantic Salmon'da türler arası bakış açısının sinirsel bağlantıları: çoklu karşılaştırmaların düzeltilmesi için bir argüman". NeuroImage. 47: S125. CiteSeerX 10.1.1.161.8384. doi:10.1016 / S1053-8119 (09) 71202-9. S2CID 220973284.
- ^ "Nörobilimde IgNobel Ödülü: Ölü somon çalışması". Scicurious Brain, Scientific American Blog Ağı. 2012-09-25. Alındı 2014-11-28.
- ^ Satel, Sally (30 Mayıs 2013). "Beyin Taramalarını Çok Fazla Okumayın". Zaman. Alındı 15 Eylül 2020.
- ^ Eklund, Anders; Nichols, Thomas E .; Knutsson, Hans (2016). "Küme başarısızlığı: Neden uzamsal kapsam için fMRI çıkarımları yanlış pozitif oranları artırdı?". Ulusal Bilimler Akademisi Bildiriler Kitabı. 113 (28): 7900–7905. doi:10.1073 / pnas.1602413113. PMC 4948312. PMID 27357684.
- ^ "FMRI Yazılımındaki Bir Hata, 15 Yıllık Beyin Araştırmalarını Geçersiz Kılabilir".
- ^ Mueller, Karsten; Lepsien, Jöran; Möller, Harald E .; Lohmann, Gabriele (28 Haziran 2017). "Yorum: Küme hatası: Uzamsal kapsam için fMRI çıkarımları neden yanlış pozitif oranları artırdı?". İnsan Nörobiliminde Sınırlar. 11: 345. doi:10.3389 / fnhum.2017.00345. PMC 5487467. PMID 28701944.
- ^ Taylor, Michelle (4 Haziran 2020). "fMRI Pioneer 15 Yıllık Kendi Çalışmasıyla Teknolojiden Şüphe Ediyor". LaboratoryEquipment.com. Alındı 15 Eylül 2020.
- ^ Ouellette, Jennifer (8 Temmuz 2020). "Duke bilim adamı, yeni çalışma hatası fMRI ile kendi araştırmasını sorguluyor". Ars Technica. Alındı 15 Eylül 2020.
- ^ Cohen, Arianne (25 Haziran 2020). "Duke Üniversitesi araştırmacıları okuduğunuz her beyin aktivitesi çalışmasının yanlış olduğunu söylüyor". Hızlı Şirket. Alındı 15 Eylül 2020.
Referanslar
- "Beyin dolandırıcılığı", Doğa Sinirbilim, 7 (7): 683, 2004, doi:10.1038 / nn0704-683, PMID 15220922
- Brammer, M. (2004), "Yazışma: Beyin dolandırıcılığı?", Doğa Sinirbilim, 7 (10): 1015, doi:10.1038 / nn1004-1015, PMID 15452565, S2CID 5158938
- Bulte, D. (2006), BOLD Fizyoloji (Ders slaytları) (PDF), Centre for FMRI of the Brain, University of Oxford, arşivlenen orijinal (PDF) 24 Mayıs 2012, alındı Aralık 31, 2011
- Carr, Valerie A .; Rissman, Jesse; Wagner, Anthony D. (Şubat 2010). "İnsan Medial Temporal Lobunun Yüksek Çözünürlüklü fMRI ile Görüntülenmesi". Nöron. 65 (3): 298–308. doi:10.1016 / j.neuron.2009.12.022. PMC 2844113. PMID 20159444.
- Devlin, H. (2012), FMRI'ye giriş: Klinik ve ticari kullanım, The Oxford Centre for Functional MRI of the Brain, University of Oxford, UK, orijinal 7 Aralık 2011 tarihinde, alındı 1 Ocak, 2012
- Fonksiyonel MR Görüntüleme (fMRI) - Beyin, Amerikan Radyoloji Koleji ve Kuzey Amerika Radyoloji Derneği, 24 Mayıs 2011, alındı 30 Aralık 2011
- Huettel, S. A .; Song, A. W .; McCarthy, G. (2009), Fonksiyonel Manyetik Rezonans Görüntüleme (2. baskı), Massachusetts: Sinauer, ISBN 978-0-87893-286-3
- Ilmoniemi, R. J .; Aronen, H. J. (2000), Moonen, C. T. W .; Bandettini, P.A. (editörler), Tıbbi Radyoloji: Tanısal görüntüleme, Fonksiyonel MRI: fMRI, MEG, EEG ve TMS'de yansıtılan kortikal uyarılabilirlik ve bağlanabilirlik, Tıbbi Radyoloji, Berlin: Springer, s. 453–463, doi:10.1007/978-3-642-58716-0_37, ISBN 978-3-540-67215-9
- Kim, S. G .; Lee, S. P .; Goodyear, B .; Silva, A.C. (2000), Moonen, C. T. W .; Bandettini, P.A. (editörler), Tıbbi Radyoloji: Tanısal görüntüleme, Fonksiyonel MRI: BOLD ve diğer fMRI tekniklerinin mekansal çözünürlüğü, Tıbbi Radyoloji, Berlin: Springer, s. 195–203, doi:10.1007/978-3-642-58716-0_18, ISBN 978-3-540-67215-9
- Lindquist, M. A. (2008), "fMRI verilerinin istatistiksel analizi", İstatistik Bilimi, 23 (4): 439–64, arXiv:0906.3662, doi:10.1214 / 09-STS282, S2CID 14221210
- Logothetis, N. K. (12 Haziran 2008), "fMRI ile neler yapabiliriz ve ne yapamayız", Doğa, 453 (7197): 869–78, Bibcode:2008Natur.453..869L, doi:10.1038 / nature06976, PMID 18548064, S2CID 4403097
- Lowenberg, K. (7 Ekim 2008), Neuro-Cola: Nörobilimin tüketici tercihini ölçme yeteneği, Stanford Hukuk Merkezi ve Biyolojik Bilimler Blogu, alındı 1 Ocak, 2012
- McClure, S .; Li, J .; Tomlin, D .; Cypert, K. S .; Montague, L. M .; Montague, P. R. (2004), "Kültürel Olarak Tanıdık İçecekler için Davranışsal Tercihin Sinirsel İlişkileri", Nöron, 44 (2): 379–387, doi:10.1016 / j.neuron.2004.09.019, PMID 15473974, S2CID 15015392
- Miller, G. (2010), "fMRI yalan tespiti yasal bir testte başarısız oluyor", Bilim, 328 (5984): 1336–1337, Bibcode:2010Sci ... 328.1336M, doi:10.1126 / science.328.5984.1336-a, PMID 20538919
- Narayan, A. (20 Temmuz 2009), "FMRI beyin taraması: Daha iyi bir yalan makinesi mi?", Zaman, alındı 1 Ocak, 2012
- Ogawa, S .; Lee, T. M .; Nayak, A. S .; Glynn, P. (1990), "Yüksek manyetik alanlarda kemirgen beyninin manyetik rezonans görüntüsünde oksijenasyona duyarlı kontrast", Tıpta Manyetik Rezonans, 14 (1): 68–78, doi:10.1002 / mrm.1910140108, PMID 2161986, S2CID 12379024
- Ogawa, S .; Sung, Y. (2007), "Fonksiyonel Manyetik Rezonans Görüntüleme", Scholarpedia, 2 (10): 3105, Bibcode:2007SchpJ ... 2.3105O, doi:10.4249 / alimpedia.3105
- Raichle, M. E. (2000), Toga, A. W .; Mazziotta, J. C. (editörler), Beyin haritalama: sistemler, Londra: Academic Press, ISBN 978-0-12-692545-6, dan arşivlendi orijinal 2012-01-13 tarihinde
- Rombouts, S.A.R.B .; Barkhof, F .; Sheltens, P. (2007), Fonksiyonel beyin MRG'nin klinik uygulamaları, İngiltere: Oxford University Press, ISBN 978-0-19-856629-8
- Roy, C. S .; Sherrington, C. S. (1890), "Beynin kan beslemesinin düzenlenmesi hakkında", Journal of Physiology, 11 (1–2): 85–158, doi:10.1113 / jphysiol.1890.sp000321, PMC 1514242, PMID 16991945
- Sahito, F .; Slany, W. (2012), "İşlevsel Manyetik Rezonans Görüntüleme ve İnsan Güvenliğini Devlet Güvenliğiyle Dengelemenin Zorluğu", İnsan Güvenliği Perspektifleri 1, 2012 (1): 38–66, arXiv:1204.3543, Bibcode:2012arXiv1204.3543S
Ders kitapları
- EMRF / TRTF (editör Peter A. Rinck), Manyetik Rezonans: Hakemli, eleştirel bir giriş (Ücretsiz erişim çevrimiçi ders kitabı )
- Joseph P. Hornak, MRG'nin temelleri (internet üzerinden )
- Richard B. Buxton, Fonksiyonel manyetik rezonans görüntülemeye giriş: İlkeler ve teknikler, Cambridge University Press, 2002, ISBN 0-521-58113-3
- Roberto Cabeza ve Alan Kingstone, Editörler, Bilişin İşlevsel Nörogörüntülemesi El Kitabı, İkinci Baskı, MIT Press, 2006, ISBN 0-262-03344-5
- Huettel, S. A .; Song, A. W .; McCarthy, G., Fonksiyonel Manyetik Rezonans Görüntüleme İkinci BaskıMassachusetts, 2009: Sinauer, ISBN 978-0-87893-286-3
daha fazla okuma
- Langleben, D.D .; Schroeder, L .; Maldjian, J.A .; Gür, R.C .; McDonald, S .; Ragland, J.D .; O'Brien, C.P .; Childress, A.R. (Mart 2002). "Simüle Aldatma Sırasında Beyin Aktivitesi: Olayla İlişkili Fonksiyonel Manyetik Rezonans Çalışması". NeuroImage. 15 (3): 727–732. doi:10.1006 / nimg.2001.1003. PMID 11848716. S2CID 14676750.
- Mehagnoul-Schipper, D. Jannet; van der Kallen, Bas F.W .; Colier, Willy N.J.M .; van der Sluijs, Marco C .; van Erning, Leon J.Th.O .; Thijssen, Henk O.M .; Oeseburg, Berend; Hoefnagels, Willibrord H.L .; Jansen, René W.M.M. (Mayıs 2002). "Yakın kızılötesi spektroskopi ve sağlıklı genç ve yaşlı deneklerde fonksiyonel manyetik rezonans görüntüleme ile beyin aktivasyonu sırasında serebral oksijenasyon değişikliklerinin eşzamanlı ölçümleri". İnsan Beyin Haritalama. 16 (1): 14–23. doi:10.1002 / hbm.10026. PMC 6871837. PMID 11870923.
- Sally Satel; Scott O. Lilienfeld (2015). Beyni Yıkanmış: Akılsız Sinirbilimin Baştan Çıkarıcı Çekiciliği. Temel Kitaplar. ISBN 978-0465062911.
Dış bağlantılar
- www.mri-tutorial.com MRI-TUTORIAL.COM - Nörogörüntüleme hakkında ücretsiz bir öğrenme havuzu
- BrainMapping.ORG projesi - Bilgi Beyin Haritalama ve yöntemleri için Topluluk web sitesi
- RadiologyTube.com'da fMRI Videoları - Bir fMRI videoları koleksiyonu
- Columbia Üniversitesi Görüntüleme ve Bilişsel Bilimler Programı: fMRI
