Alüminyum hidroksit - Aluminium hydroxide
 | |
 | |
| İsimler | |
|---|---|
| Tercih edilen IUPAC adı Alüminyum hidroksit | |
| Sistematik IUPAC adı Alüminyum (3+) trioksidanid | |
| Diğer isimler Alüminik asit Alüminik hidroksit | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA Bilgi Kartı | 100.040.433 |
| KEGG | |
PubChem Müşteri Kimliği | |
| RTECS numarası |
|
| UNII | |
CompTox Kontrol Paneli (EPA) | |
| |
| Özellikleri[1][2] | |
| Al (OH)3 | |
| Molar kütle | 78.00 g / mol |
| Görünüm | Beyaz amorf pudra |
| Yoğunluk | 2,42 g / cm3, sağlam |
| Erime noktası | 300 ° C (572 ° F; 573 K) |
| 0.0001 g / 100 mL | |
Çözünürlük ürünü (Ksp) | 3×10−34 |
| Çözünürlük | içinde çözünür asitler ve alkaliler |
| Asitlik (pKa) | >7 |
| İzoelektrik noktası | 7.7 |
| Termokimya[3] | |
Std entalpisi oluşum (ΔfH⦵298) | −1277 kJ · mol−1 |
| Farmakoloji[4] | |
| A02AB01 (DSÖ) | |
| |
| Tehlikeler | |
| Güvenlik Bilgi Formu | Harici MSDS |
| GHS piktogramları |  |
| H319, H335 | |
| P264, P261, P280, P271, P312, P304 + 340, P305 + 351 + 338, P337 + 313 | |
| NFPA 704 (ateş elması) | |
| Alevlenme noktası | Yanıcı değil |
| Ölümcül doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz ) | > 5000 mg / kg (sıçan, ağızdan) |
| Bağıntılı bileşikler | |
Diğer anyonlar | Yok |
Bağıntılı bileşikler | Sodyum oksit, alüminyum oksit hidroksit |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
Alüminyum hidroksitAl (OH)3, doğada mineral olarak bulunur gibsit (hydrargillite olarak da bilinir) ve üçü daha nadirdir polimorflar: bayerit, doyleit ve nordstrandit. Alüminyum hidroksit amfoterik doğada, yani her ikisine de sahiptir temel ve asidik özellikleri. Yakından ilişkilidir alüminyum oksit hidroksit, AlO (OH) ve alüminyum oksit veya alümina (Al2Ö3), ikincisi de amfoteriktir. Bu bileşikler birlikte alüminyumun ana bileşenleridir cevher boksit.
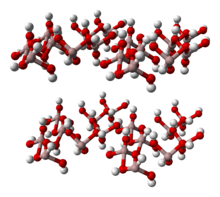
Yapısı
Al (OH)3 iki katman arasındaki oktahedral deliklerin üçte ikisini kaplayan alüminyum iyonları ile çift hidroksil gruplarından oluşur.[5][6] Dört polimorflar tanınmış.[7] Tüm özellik katmanları sekiz yüzlü alüminyum hidroksit üniteleri, hidrojen bağları katmanlar arasında. Polimorflar, katmanların istiflenmesi açısından farklılık gösterir. Tüm Al (OH) formları3 kristaller altıgen[tartışmalı ]:
- gibsit γ-Al (OH) olarak da bilinir3 [8] veya α-Al (OH)3[kaynak belirtilmeli ]
- bayerit α-Al (OH) olarak da bilinir3 [8] veya β-alümina trihidrat [kaynak belirtilmeli]
- Nordstrandit Al (OH) olarak da bilinir3[8]
- doyleit
Hidrargilitbir zamanlar alüminyum hidroksit olduğu düşünülürse, bir alüminyum fosfat. Bununla birlikte, ikisi de gibsit ve hidrargilit alüminyum hidroksitin aynı polimorfizmine atıfta bulunun gibsit Amerika Birleşik Devletleri'nde en yaygın olarak kullanılır ve hidrargilit Avrupa'da daha sık kullanılır. Hydrargillite adını Yunan su için kelimeler (hidra) ve kil (Argylles).
Özellikleri
Alüminyum hidroksit amfoterik. İçinde asit, bir Brønsted – Lowry tabanı. Asidi nötralize ederek bir tuz oluşturur:[9]
- 3 HCl + Al (OH)3 → AlCl3 + 3 H2Ö
Bazlarda, bir Lewis asidi hidroksit iyonlarını bağlayarak:[9]
- Al (OH)3 + OH− → Al (OH)4−
Üretim

Ticari olarak kullanılan hemen hemen tüm alüminyum hidroksit, Bayer süreci[10] çözülmeyi içeren boksit 270 ° C'ye (518 ° F) kadar sodyum hidroksit içinde. Atık katı, boksit atıkları, uzaklaştırılır ve kalan çözeltiden alüminyum hidroksit çökeltilir. sodyum alüminat. Bu alüminyum hidroksit, alüminyum oksit veya alümina tarafından kalsinasyon.
Kalıntı veya boksit atıkları Çoğunlukla demir oksit olan, artık sodyum hidroksit nedeniyle oldukça kostiktir. Tarihsel olarak lagünlerde saklandı; bu yol açtı Ajka alümina fabrikası kazası 2010 yılında, bir baraj patlamasının dokuz kişinin boğulmasına yol açtığı Macaristan'da. Kimyasal yanıklar için ek 122 aranan tedavi. Çamur, 40 kilometrekarelik (15 sq mi) araziyi kirletti ve Tuna. Düşük seviyelerde ağır metaller nedeniyle çamurun toksik olmadığı düşünülürken, ilişkili bulamacın pH'si 13'tür.[11]
Kullanımlar
Yangın geciktirici dolgu
Alüminyum hidroksit ayrıca polimer uygulamaları için alev geciktirici bir dolgu maddesi olarak kullanım alanı bulur. Bu uygulamalar için seçilmiştir çünkü renksizdir (çoğu polimer gibi), ucuzdur ve iyi alev geciktirici özelliklere sahiptir.[12] Magnezyum hidroksit ve karışımları Huntit ve hidromanyezit benzer şekilde kullanılır[13][14][15][16][17] Yaklaşık 180 ° C'de (356 ° F) ayrışır, işlem sırasında önemli miktarda ısı emer ve su buharı verir. Alev geciktirici olarak davranmasının yanı sıra, özellikle polyester, akrilik, etilen vinil asetat, epoksiler, PVC ve kauçuk başta olmak üzere çok çeşitli polimerlerde duman bastırıcı olarak çok etkilidir.[18]
Al bileşiklerinin öncüsü
Alüminyum hidroksit bir hammadde diğer alüminyum bileşiklerin üretimi için: uzmanlık kalsine alüminalar, alüminyum sülfat polialuminyum klorür, alüminyum klorür, zeolitler, sodyum alüminat, aktifleştirilmiş alümina ve alüminyum nitrat.[6]
Yeni çöktürülmüş alüminyum hidroksit formları jeller alüminyum tuzlarının uygulanmasının temeli olan topaklaştırıcılar su arıtmada. Bu jel zamanla kristalleşir. Alüminyum hidroksit jelleri dehidre edilebilir (ör. Suyla karışabilen susuz çözücüler kullanılarak etanol ) asitlerde kolaylıkla çözünebilen amorf bir alüminyum hidroksit tozu oluşturmak için. Isıtma, onu aşağıdaki gibi kullanılan aktifleştirilmiş alüminalara dönüştürür. kurutucular, adsorban gaz arıtmada ve katalizör destekleri.[12]
Eczacılığa ait
"Algeldrat" jenerik adı altında, alüminyum hidroksit, bir antiasit insanlarda ve hayvanlarda (esas olarak kediler ve köpekler). Gibi diğer alternatiflere göre tercih edilir. sodyum bikarbonat çünkü Al (OH)3çözünmez olduğundan mide pH'ını 7'nin üzerine çıkarmaz ve dolayısıyla mide tarafından fazla asit salgılanmasını tetiklemez. Marka isimleri arasında Alu-Cap, Aludrox, Gaviscon veya Pepsamar bulunur. Midede bulunan fazla asit ile reaksiyona girerek mide içeriğinin asitliğini azaltır,[19][20] semptomları hafifletebilir ülserler, göğüste ağrılı yanma hissi veya dispepsi. Bu tür ürünler neden olabilir kabızlık alüminyum iyonları kasılmaları engellediği için düz kas gastrointestinal sistemdeki hücreler, yavaşlama peristalsis dışkı geçmesi için gereken sürenin uzatılması kolon.[21] Bu tür bazı ürünler, eşit konsantrasyonlarda dahil edilerek bu tür etkileri en aza indirecek şekilde formüle edilmiştir. magnezyum hidroksit veya magnezyum karbonat dengeleyici müshil Etkileri.[22]
Bu bileşik ayrıca kontrol etmek için kullanılır. hiperfosfatemi (yükseltilmiş fosfat veya böbrek yetmezliği olan insanlarda ve hayvanlarda kandaki fosfor seviyeleri). Normalde böbrekler kandaki fazla fosfatı filtreler, ancak böbrek yetmezliği fosfatın birikmesine neden olabilir. Alüminyum tuzu, yutulduğunda fosfata bağlanır. bağırsaklar ve emilebilecek fosfor miktarını azaltın.[23][24]
Çökelmiş alüminyum hidroksit, bir yardımcı bazılarında aşılar (Örneğin. şarbon aşısı ). Alüminyum hidroksit yardımcı maddesinin iyi bilinen markalarından biri, Brenntag Biosector tarafından yapılan Alhydrogel'dir.[25][tam alıntı gerekli ] Proteini iyi emdiği için, aşıdaki proteinlerin depolama sırasında çökelmesini veya kabın duvarlarına yapışmasını önleyerek aşıları stabilize etme işlevi de görür. Alüminyum hidroksit bazen "şap ", genellikle birkaç sülfattan biri için ayrılmış bir terim.[kaynak belirtilmeli ]
Alüminyum hidroksit içeren aşı formülasyonları, bağışıklık sistemi salıverilmesine neden olarak ürik asit, immünolojik Tehlike sinyal. Bu, belirli türlerini kuvvetle çeker monositler farklılaşan dentritik hücreler. Dendritik hücreler antijeni alır, Lenf düğümleri ve teşvik etmek T hücreleri ve B hücreleri.[26] Bir malın indüksiyonuna katkıda bulunuyor gibi görünüyor. Th2 yanıt, bu nedenle antikorlar tarafından bloke edilen patojenlere karşı immünizasyon için faydalıdır. Bununla birlikte, birçok patojene karşı koruma için önemli olan hücresel (Th1) bağışıklık tepkilerini uyarma kapasitesi azdır.[27] ne de antijen olduğunda yararlı değildir peptid tabanlı.[28]
Emniyet
1960'larda ve 1970'lerde alüminyumun çeşitli nörolojik bozukluklar, dahil olmak üzere Alzheimer hastalığı.[29][30] O zamandan beri birden fazla epidemiyolojik Çalışmalar, çevresel veya yutulmuş alüminyuma maruz kalma ile nörolojik bozukluklar arasında bir bağlantı bulamamıştır, ancak bu çalışmalarda enjekte edilen alüminyuma bakılmamıştır.[31][32][33]
Referanslar
- ^ Çözünürlük ürünü için: "Arşivlenmiş kopya". Arşivlenen orijinal 15 Haziran 2012'de. Alındı 17 Mayıs 2012.CS1 Maint: başlık olarak arşivlenmiş kopya (bağlantı)
- ^ İzoelektrik nokta için: Gayer, K. H .; Thompson, L.C .; Zajicek, O. T. (Eylül 1958). "Alüminyum hidroksitin asidik ve bazik ortamda 25? C'de çözünürlüğü". Kanada Kimya Dergisi. 36 (9): 1268–1271. doi:10.1139 / v58-184. ISSN 0008-4042.
- ^ Zumdahl Steven S. (2009). Kimyasal Prensipler (6. baskı). Houghton Mifflin Şirketi. ISBN 978-0-618-94690-7.
- ^ Siyah, Ronald A .; Hill, D. Ashley (15 Haziran 2003). "Gebelikte Reçetesiz Satılan İlaçlar". Amerikan Aile Hekimi. 67 (12): 2517–2524. ISSN 0002-838X. PMID 12825840. Alındı 1 Temmuz 2017.
- ^ Wells, A.F. (1975), Yapısal İnorganik Kimya (4. baskı), Oxford: Clarendon Press
- ^ a b Evans, K.A. (1993). "Alüminyum oksitlerin ve alüminyum hidroksitlerin özellikleri ve kullanımları". A. J. Downs (ed.). Alüminyum, galyum, indiyum ve talyum kimyası (1. baskı). Londra; New York: Blackie Akademik ve Profesyonel. ISBN 9780751401035.
- ^ Karamalidis, A. K .; Dzombak D.A. (2010). Yüzey Kompleksasyon Modellemesi: Gibbsite. John Wiley & Sons. s. 15–17. ISBN 978-0-470-58768-3.
- ^ a b c Wefers, Karl; Misra, Chanakya (1987). Alüminyum oksitleri ve hidroksitleri. Alcoa Araştırma Laboratuvarları. s. 2. OCLC 894928306.
- ^ a b Sınırsız (26 Temmuz 2016). "Bazik ve Amfoterik Hidroksitler". Sınırsız Kimya. Arşivlenen orijinal 22 Ağustos 2017. Alındı 2 Temmuz 2017.
- ^ Hind, AR; Bhargava SK; Grocott SC (1999). "Bayer Proses Katılarının Yüzey Kimyası: Bir Gözden Geçirme". Kolloidler Surf Physiochem Eng Yönleri. 146 (1–3): 359–74. doi:10.1016 / S0927-7757 (98) 00798-5.
- ^ "Macaristan, Zehirli Çamur Torrentiyle Mücadele Ediyor". BBC Haber Web Sitesi. 5 Ekim 2010.
- ^ a b Hudson, L. Keith; Misra, Chanakya; Perrotta, Anthony J .; Wefers, Karl; Williams, F. S. (2000). "Aluminyum oksit". Ullmann'ın Endüstriyel Kimya Ansiklopedisi. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a01_557.
- ^ Hollingbery, LA; Hull TR (2010). "Huntit ve Hidromagnezitin Yangın Geciktirici Davranışı - Bir İnceleme" (PDF). Polimer Bozulması ve Kararlılığı. 95 (12): 2213–2225. doi:10.1016 / j.polymdegradstab.2010.08.019.
- ^ Hollingbery, LA; Hull TR (2010). "Huntit ve Hidromagnezitin Termal Ayrışması - Bir İnceleme" (PDF). Thermochimica Açta. 509 (1–2): 1–11. doi:10.1016 / j.tca.2010.06.012.
- ^ Hollingbery, LA; Hull TR (2012). "Hidromagnezitli Doğal Karışımlarda Huntitin Yanmayı Geciktirici Etkileri" (PDF). Polimer Bozulması ve Kararlılığı. 97 (4): 504–512. doi:10.1016 / j.polymdegradstab.2012.01.024.
- ^ Hollingbery, LA; Hull TR (2012). "Huntit ve Hidromagnezitin Doğal Karışımlarının Termal Ayrışması" (PDF). Thermochimica Açta. 528: 45–52. doi:10.1016 / j.tca.2011.11.002.
- ^ Hull, TR; Witkowski A; Hollingbery LA (2011). "Mineral Dolgu Maddelerinin Yangın Geciktirici Etkisi" (PDF). Polimer Bozulması ve Kararlılığı. 96 (8): 1462–1469. doi:10.1016 / j.polymdegradstab.2011.05.006.
- ^ Huber Tasarlanmış Malzemeler. "Huber Halojen Olmayan Alev Geciktirici Katkı Maddeleri" (PDF). Alındı 3 Temmuz 2017.
- ^ Galbraith, A; Bullock, S; Mani, E; Hunt, B; Richards, A (1999). Farmakolojinin temelleri: hemşireler ve sağlık uzmanları için bir metin. Harlow: Pearson. s. 482.
- ^ Papich, Mark G. (2007). "Alüminyum Hidroksit ve Alüminyum Karbonat". Saunders Veteriner İlaçları El Kitabı (2. baskı). St. Louis, Mo: Saunders / Elsevier. s. 15–16. ISBN 9781416028888.
- ^ Washington, Neena (2 Ağustos 1991). Antasitler ve Anti Reflü Ajanlar. Boca Raton, FL: CRC Press. s. 10. ISBN 978-0-8493-5444-1.
- ^ Bill, Robert L. (1 Eylül 2016). Veteriner Teknisyenleri için Klinik Farmakoloji ve Terapötikler - E-Kitap. Elsevier Sağlık Bilimleri. s. 105. ISBN 9780323444026.
- ^ Çekül, Donald C. (2011). "Alüminyum Hidroksit". Plumb's Veteriner İlaçları El Kitabı (7. baskı). Stockholm, Wisconsin; Ames, Iowa: Wiley. sayfa 36–37. ISBN 9780470959640.
- ^ Lifelearn Inc. (1 Kasım 2010). "Alüminyum Hidroksit". Evcil Hayvanınızı Tanıyın. Alındı 30 Haziran 2017.
- ^ "Brenntag Biosector - Brenntag Hakkında". brenntag.com. Alındı 19 Nisan 2018.
- ^ Kool, M; Soullié T; van Nimwegen M; Willart MA; Muskens F; Jung S; Hoogsteden HC; Hammad H; Lambrecht BN (24 Mart 2008). "Alum adjuvanı, ürik asidi indükleyerek ve inflamatuar dendritik hücreleri aktive ederek adaptif bağışıklığı artırır". J Exp Med. 205 (4): 869–82. doi:10.1084 / jem.20071087. PMC 2807488. PMID 18362170.
- ^ Petrovsky N, Aguilar JC (2004). "Aşı adjuvanları: mevcut durum ve gelecekteki eğilimler". İmmünol Hücre Biol. 82 (5): 488–96. doi:10.1111 / j.0818-9641.2004.01272.x. PMID 15479434. S2CID 154670.
- ^ Cranage, MP; Robinson A (2003). Robinson A; Hudson MJ; Cranage MP (editörler). Aşı Protokolleri - Moleküler Tıp Biyomedikal Protokollerinde Yöntemlerin Cilt 87'si (2. baskı). Springer. s. 176. ISBN 978-1-59259-399-6.
- ^ "Alzheimer Efsanesi". Alzheimer Derneği. Alındı 29 Temmuz 2012.
- ^ Khan, A (1 Eylül 2008). "Alüminyum ve Alzheimer hastalığı". Alzheimer Derneği. Arşivlenen orijinal 11 Mart 2012 tarihinde. Alındı 8 Mart 2012.
- ^ Rondeau V (2002). "Alzheimer hastalığı ve ilişkili bozukluklarla ilişkili olarak alüminyum ve silika üzerine epidemiyolojik çalışmaların bir incelemesi". Rev Çevre Sağlığı. 17 (2): 107–21. doi:10.1515 / REVEH.2002.17.2.107. PMC 4764671. PMID 12222737.
- ^ Martyn CN, Coggon DN, Inskip H, Lacey RF, Young WF (Mayıs 1997). "İçme suyundaki alüminyum konsantrasyonları ve Alzheimer hastalığı riski". Epidemiyoloji. 8 (3): 281–6. doi:10.1097/00001648-199705000-00009. JSTOR 3702254. PMID 9115023. S2CID 32190038.
- ^ Graves AB, Rosner D, Echeverria D, Mortimer JA, Larson EB (Eylül 1998). "Çözücülere ve alüminyuma mesleki maruziyet ve tahmini Alzheimer hastalığı riski". Occup Environ Med. 55 (9): 627–33. doi:10.1136 / oem.55.9.627. PMC 1757634. PMID 9861186.
Dış bağlantılar
- Uluslararası Kimyasal Güvenlik Kartı 0373
- "Kil varlığında çöken alüminyum hidroksitin bazı özellikleri", Toprak Araştırma Enstitüsü, R C Turner, Tarım Bakanlığı, Ottawa
- Yaşlanmanın polinükleer hidroksialuminyum katyonlarının özelliklerine etkisi
- İkinci bir polinükleer hidroksialüminyum katyon türü, oluşumu ve bazı özellikleri


