Klor dioksit - Chlorine dioxide
| |||
 | |||
| İsimler | |||
|---|---|---|---|
| IUPAC adı Klor dioksit | |||
| Diğer isimler Klor (IV) oksit | |||
| Tanımlayıcılar | |||
3 boyutlu model (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| ECHA Bilgi Kartı | 100.030.135 | ||
| EC Numarası |
| ||
| E numarası | E926 (cam ajanları, ...) | ||
| 1265 | |||
| MeSH | Klor + dioksit | ||
PubChem Müşteri Kimliği | |||
| RTECS numarası |
| ||
| UNII | |||
| BM numarası | 9191 | ||
CompTox Kontrol Paneli (EPA) | |||
| |||
| |||
| Özellikleri | |||
| ClÖ2 | |||
| Molar kütle | 67.45 g · mol−1 | ||
| Görünüm | Sarı ila kırmızımsı gaz | ||
| Koku | Buruk | ||
| Yoğunluk | 2,757 g dm−3[1] | ||
| Erime noktası | -59 ° C (-74 ° F; 214 K) | ||
| Kaynama noktası | 11 ° C (52 ° F; 284 K) | ||
| 8 g / L (20 ° C'de) | |||
| Çözünürlük | alkali içinde çözünür ve sülfürik asit çözümler | ||
| Buhar basıncı | > 1 atm[2] | ||
Henry yasası sabit (kH) | 4.01×10−2 atm m3 mol−1 | ||
| Asitlik (pKa) | 3.0(5) | ||
| Termokimya | |||
Standart azı dişi entropi (S | 257.22 J K−1 mol−1 | ||
Std entalpisi oluşum (ΔfH⦵298) | 104,60 kJ / mol | ||
| Tehlikeler | |||
| Ana tehlikeler | Akut toksisite | ||
| Güvenlik Bilgi Formu | Güvenlik Bilgi Formu Arşiv. | ||
| GHS piktogramları |    | ||
| GHS Sinyal kelimesi | Tehlike | ||
| H271, H314, H330 | |||
| P210, P220, P280, P283, P260, P264, P271, P284, P301, P330, P331, P311, P306, P360, P304, P340, P305, P351, P338, P371 + 380 + 375, P405, P403 + 233, P501 | |||
| NFPA 704 (ateş elması) | |||
| Ölümcül doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz ) | 94 mg / kg (oral, sıçan)[3] | ||
LCLo (en düşük yayınlanan ) | 260 ppm (sıçan, 2 saat)[4] | ||
| NIOSH (ABD sağlık maruziyet sınırları): | |||
PEL (İzin verilebilir) | TWA 0.1 ppm (0.3 mg / m23)[2] | ||
REL (Önerilen) | TWA 0.1 ppm (0.3 mg / m23) ST 0.3 ppm (0.9 mg / m23)[2] | ||
IDLH (Ani tehlike) | 5 ppm[2] | ||
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |||
| Bilgi kutusu referansları | |||
Klor dioksit bir kimyasal bileşik ClO formülüyle2 sarımsı yeşil olarak var olan gaz 11 ° C'nin üzerinde, 11 ° C ile -59 ° C arasında kırmızımsı kahverengi bir sıvı ve -59 ° C'nin altında parlak turuncu kristaller olarak. O bir oksitleyici ajan, oksidasyon-indirgeme yoluyla bir veya daha fazla elektron kazanırken oksijeni çeşitli substratlara aktarabilir (redoks ). O değil hidrolize etmek suya girdiğinde ve genellikle suda çözelti içinde çözünmüş bir gaz olarak ele alınır. Klor dioksit ile ilgili olası tehlikeler arasında sağlık sorunları, patlayıcılık ve yangın tutuşması bulunur.[5] Yaygın olarak bir çamaşır suyu.
Klor dioksit 1811'de keşfedildi ve kağıt endüstrisinde ağartma amacıyla ve içme suyunun arıtılmasında yaygın olarak kullanıldı. Daha yeni gelişmeler, uygulamasını gıda işleme, bina ve araçların dezenfeksiyonu, küf eradikasyonu, hava dezenfeksiyonu ve koku kontrolü, yüzme havuzlarının tedavisi, dişçilik uygulamaları ve yara temizliği alanlarında genişletmiştir.
Bileşik, çocukluk otizmi de dahil olmak üzere çok çeşitli hastalıklar için yenilebilir bir tedavi olarak sahtekarlıkla pazarlanmıştır.[6] ve COVID-19.[7][8][9] Verilen çocuklar lavman Çocukluk otizmi için sözde bir tedavi olarak klor dioksitin yaşamı tehdit eden rahatsızlıklara maruz kaldı.[6] ABD Gıda ve İlaç İdaresi (FDA), klor dioksitin yutulmasının veya diğer dahili kullanımının (belki diş hekimi gözetiminde ağızdan durulama dışında) sağlık açısından hiçbir faydası olmadığını ve herhangi bir nedenle dahili olarak kullanılmaması gerektiğini belirtmiştir.[10][11]
Yapı ve bağ
Klor dioksit nötr bir klor bileşiği. Hem kimyasal yapısında hem de davranışında elementel klordan çok farklıdır.[12] Klor dioksitin en önemli özelliklerinden biri, özellikle soğuk suda yüksek suda çözünürlüğüdür. Klor dioksit yapmaz hidrolize etmek suya girdiğinde; çözelti içinde çözünmüş bir gaz olarak kalır. Klor dioksit, suda klordan yaklaşık 10 kat daha fazla çözünür.[12]
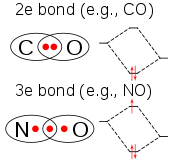
Molekül ClO2 tek sayıda değerlik elektronları ve bu nedenle, bir paramanyetik radikal. Elektronik yapısı uzun zamandır şaşkın kimyagerlere sahip çünkü Lewis yapıları çok tatmin edici. 1933'te L. O. Brockway, bir üç elektronlu bağ.[13] Eczacı Linus Pauling bu fikri daha da geliştirdi ve ikiye ulaştı rezonans yapıları bir tarafta çift bağ ve diğer tarafta tek bir bağ artı üç elektron bağı içerir.[14] Pauling'in görüşüne göre, ikinci kombinasyon, çok az bir bağı temsil etmelidir. zayıf çift bağdan. İçinde moleküler yörünge teorisi Üçüncü elektron bağlanma önleyici bir yörüngeye yerleştirilirse bu fikir yaygındır. Daha sonra yapılan çalışmalar, en yüksek işgal edilen moleküler yörünge aslında eksik doldurulmuş bir antibonding yörüngesidir.[15]
Hazırlık
Klor dioksit, seyreltici maddelerden ayrıldığında son derece şiddetli bir şekilde ayrışabilen bir bileşiktir. Sonuç olarak, bir gaz fazı aşamasından geçmeden bunun çözeltilerinin üretilmesini içeren hazırlama yöntemleri sıklıkla tercih edilir. Kullanımın güvenli bir şekilde düzenlenmesi önemlidir.
Kloritin oksidasyonu
Laboratuvarda, ClO2 oksidasyon ile hazırlanabilir Sodyum klorit klor ile:[16]
- 2 NaClO2 + Cl2 → 2 ClO2 + 2 NaCl
Geleneksel olarak klor dioksit dezenfeksiyon sodyumdan uygulamalar yapılmıştır klorit veya sodyum klorit -hipoklorit yöntem:
- 2 NaClO2 + 2 HCl + NaOCl → 2 ClO2 + 3 NaCl + H2Ö
veya sodyum klorit -hidroklorik asit yöntem:
- 5 NaClO2 + 4 HCl → 5 NaCl + 4 ClO2 + 2 H2Ö
veya klorit–sülfürik asit yöntem:
- 4 ClO−
2 + 2 H2YANİ4 → 2 ClO2 + HClO3 + 2 YANİ2−
4 + H2O + HCl
Her üç yöntem de yüksek klorit dönüşüm verimine sahip klor dioksit üretebilir. Diğer işlemlerden farklı olarak, klorit-sülfürik asit yöntemi, eşdeğer miktarda klor dioksit üretmek için% 25 daha fazla klorit gerekmesine rağmen, tamamen klorsuz klor dioksit üretir. Alternatif olarak, hidrojen peroksit küçük ölçekli uygulamalarda verimli bir şekilde kullanılabilir.[12]
Kloratın azaltılması
Laboratuvarda klor dioksit de reaksiyona sokularak hazırlanabilir. potasyum klorat ile oksalik asit:
- 2 KClO3 + 2 H2C2Ö4 → K2C2Ö4 + 2 ClO2 + 2 CO2 + 2 H2Ö
- 2 KClO3 + H2C2Ö4 + 2 H2YANİ4 → 2 KHSO4 + 2 ClO2 + 2 CO2 + 2 H2Ö
Bugün dünyada üretilen klor dioksitin% 95'inden fazlası, Sodyum klorat, kullanmak için hamur ağartma. Güçlü bir asit çözeltisinde, uygun bir indirgen madde gibi metanol, hidrojen peroksit, hidroklorik asit veya kükürt dioksit.[12] Modern teknolojiler metanol veya hidrojen peroksite dayanır, çünkü bu kimyasallar en iyi ekonomiyi sağlar ve elementel kloru birlikte üretmez. Genel tepki şu şekilde yazılabilir:[17]
- klorat + asit + indirgeme ajanı → klor dioksit + yan ürünleri
Tipik bir örnek olarak, Sodyum klorat ile hidroklorik asit tek bir reaktörde aşağıdaki yoldan ilerlediğine inanılmaktadır:
- ClO−
3 + Cl−
+ H+
→ ClO−
2 + HOCl - ClO−
3 + ClO−
2 + 2 H+
→ 2 ClO
2 + H
2Ö - HOCI + Cl−
+ H+
→ Cl
2 + H
2Ö
genel reaksiyonu veren
- 2 ClO−
3 + 2 Cl−
+ 4 H+
→ 2 ClO
2 + Cl
2 + 2 H
2Ö.
Ticari olarak daha önemli üretim rotası kullanır metanol indirgeyici ajan olarak ve sülfürik asit asitlik için. Klorür bazlı prosesleri kullanmamanın iki avantajı, elementel klor oluşumunun olmaması ve sodyum sülfat selüloz değirmeni için değerli bir kimyasal olan bir yan üründür. Bu metanol bazlı işlemler, yüksek verimlilik sağlar ve çok güvenli hale getirilebilir.[12]
Klorat, hidrojen peroksit ve sülfürik asit kullanan değişken süreç, 1999'dan beri su arıtımı ve diğer küçük ölçekli dezenfeksiyon yüksek verimlilikte klorsuz ürün ürettiği için uygulamalar.
Diğer işlemler
Çok saf klor dioksit, bir klorit çözeltisinin elektroliziyle de üretilebilir:[18]
- 2 NaClO2 + 2 H2O → 2 ClO2 + 2 NaOH + H2
Seyreltik klor gazını katı sodyum klorit ile reaksiyona sokan gaz-katı yöntemiyle yüksek saflıkta klor dioksit gazı (havada veya nitrojende% 7,7) üretilebilir:[18]
- 2 NaClO2 + Cl2 → 2 ClO2 + 2 NaCl
İşleme özellikleri
10 kPa'nın üzerindeki kısmi basınçlarda[12] (veya havadaki hacimce% 10'dan fazla gaz fazı konsantrasyonları STP ), ClO2 patlayarak ayrışabilir klor ve oksijen. Ayrışma ışık, sıcak noktalar, kimyasal reaksiyon veya basınç şoku ile başlatılabilir. Bu nedenle, klor dioksit gazı asla konsantre formda işlenmez, ancak hemen hemen her zaman litre başına 0.5 ila 10 gramlık bir konsantrasyon aralığında suda çözünmüş bir gaz olarak kullanılır. Çözünürlüğü daha düşük sıcaklıklarda artar, bu nedenle litre başına 3 gramın üzerindeki konsantrasyonlarda saklanırken soğutulmuş su (5 ° C) kullanılması yaygındır. Amerika Birleşik Devletleri gibi birçok ülkede, klor dioksit gazı herhangi bir konsantrasyonda taşınmayabilir ve hemen hemen her zaman bir klor dioksit jeneratörü kullanılarak uygulama yerinde üretilir.[12] Bazı ülkelerde,[hangi? ] Konsantrasyon olarak litre başına 3 gramın altındaki klor dioksit çözeltileri kara yoluyla taşınabilir, ancak bunlar nispeten kararsızdır ve hızla bozulur.
Kullanımlar
Klor dioksit, odun hamurunun ağartılması ve için dezenfeksiyon (aranan klorlama ) belediye içme suyu.[19][20]:4–1[21] Bir dezenfektan olarak, benzersiz nitelikleri nedeniyle düşük konsantrasyonlarda bile etkilidir.[12][20]
Ağartma
Klor dioksit bazen odun hamurunun ağartılması klor ile kombinasyon halinde, ancak ECF (elementel klorsuz) ağartma dizilerinde tek başına kullanılır. Orta derecede asidik olarak kullanılır pH (3,5 ila 6). Klor dioksit kullanımı miktarı en aza indirir. organoklor bileşikler üretildi.[22] Klor dioksit (ECF teknolojisi) şu anda dünya çapında en önemli ağartma yöntemidir. Tüm ağartılmışların yaklaşık% 95'i kraft hamuru ECF ağartma dizilerinde klor dioksit kullanılarak yapılır.[23]
Klor dioksit, çamaşır suyu un.[24]
Su arıtma
Niagara Şelalesi, New York, su arıtma tesisi ilk olarak klor dioksit kullandı içme suyu 1944'te tat ve koku üretimini yok etmek için tedavi fenolik bileşikler ".[20]:4–17[21] Klor dioksit, içme suyu dezenfektanı olarak 1956'da büyük ölçekte tanıtıldı. Brüksel, Belçika, klordan klor dioksite değişti.[21] Su arıtmada en yaygın kullanımı, önoksidan aksi takdirde üretebilecek doğal su kirliliklerini yok etmek için içme suyunun klorlanmasından önce trihalometanlar serbest klora maruz kalma üzerine.[25][26][27] Trihalometanlar kanserojen dezenfeksiyondan şüphelenilen yan ürünlerdir[28] ham suda doğal olarak oluşan organiklerin klorlanması ile ilişkilidir.[27] Klor dioksit de yukarıda çalışırken klordan üstündür. pH 7,[20]:4–33 amonyak ve aminlerin varlığında[kaynak belirtilmeli ] ve su dağıtım sistemlerindeki biyofilmlerin kontrolü için.[27] Klor dioksit, birçok endüstriyel su arıtma uygulamalarında bir biyosit dahil olmak üzere soğutma kuleleri, proses suyu ve gıda işleme.[29]
Klor dioksit, klordan daha az aşındırıcıdır ve kontrol için üstündür. Lejyonella bakteri.[21][30]Klor dioksit diğer bazı ikincil su dezenfeksiyon yöntemlerinden daha üstündür, çünkü klor dioksit bir EPA Kayıtlı biyosit, pH'dan olumsuz etkilenmez, zamanla etkinliğini kaybetmez (bakteri buna dirençli büyümez) ve bundan olumsuz etkilenmez. silika ve fosfatlar yaygın olarak kullanılan içme suyu korozyon önleyicileridir.
Su kaynaklı patojenik ajanlara karşı çoğu durumda dezenfektan olarak klordan daha etkilidir. virüsler,[31] bakteri ve protozoa - I dahil ederek kistler nın-nin Giardia ve ookistler nın-nin Cryptosporidium.[20]:4–20–4–21
Su arıtmada klor dioksit kullanımı, ABD'de şu anda içme suyunda milyonda maksimum 1 kısım ile sınırlı olan yan ürün klorit oluşumuna yol açmaktadır.[20]:4–33 Bu EPA standardı, ABD'de klor dioksit kullanımını nispeten yüksek kaliteli suyla sınırlar çünkü bu, klorit konsantrasyonunu veya demir bazlı pıhtılaştırıcılarla işlenecek suyu en aza indirir (demir, kloriti klorüre indirgeyebilir).[kaynak belirtilmeli ]
Kamuya açık krizlerde kullanın
Klor dioksit, oksitleyici veya dezenfektan olarak birçok uygulamaya sahiptir.[12] Klor dioksit hava dezenfeksiyonu için kullanılabilir[32] ve Amerika Birleşik Devletleri'ndeki binaların dekontaminasyonunda kullanılan ana ajan oldu. 2001 şarbon saldırıları.[33] Felaketten sonra Katrina Kasırgası içinde New Orleans, Louisiana ve çevredeki Körfez Kıyısı, tehlikeli bölgeleri yok etmek için klor dioksit kullanıldı. kalıp sel suları altında kalan evlerden.[34]
COVID-19 salgınını ele alırken, ABD Çevre Koruma Ajansı birçoklarının listesini yayınladı dezenfektanlar nedene karşı çevresel önlemlerde kullanım kriterlerini karşılayan koronavirüs.[35][36] Bazıları dayanmaktadır Sodyum klorit her üründe farklı formülasyonlar kullanılmasına rağmen, klor dioksite aktive edilir. EPA listesindeki diğer birçok ürün şunları içerir: sodyum hipoklorit adı benzer olan ancak sodyum klorit ile karıştırılmaması gereken, çünkü çok farklı kimyasal etki modlarına sahiptirler.
Diğer dezenfeksiyon kullanımları
Klor dioksit, küf ve maya geliştiren yaban mersini, ahududu ve çilek gibi meyveleri "sterilize etmek" için bir fümigant işlemi olarak kullanılabilir.[37]
Klor dioksit, kesimden sonra püskürterek veya suya daldırarak kümes hayvanlarını dezenfekte etmek için kullanılabilir.[38]
Klor dioksit dezenfeksiyon için kullanılabilir. endoskoplar Tristel ticari adı altında olduğu gibi.[39] Ayrıca bir önceki ön temizlemeden oluşan üçlü olarak da mevcuttur. sürfaktan ve bir sonraki durulama deiyonize su ve düşük seviyeli bir antioksidan.[40]
Klor dioksit, kontrol için kullanılabilir. zebra ve Quagga midyeleri su girişlerinde.[20]:4–34
Klor dioksitin etkili olduğu gösterilmiştir. tahta kurusu yok etme.[41]
Sözde tıp
Klor dioksit, beyin kanserinden AIDS'e kadar bir dizi hastalık için hileli bir şekilde sihirli bir tedavi olarak pazarlanmaktadır. Lavman klor dioksitin çocukluk çağı için sözde bir çaresi otizm şikayetlerle sonuçlanan FDA hayatı tehdit eden reaksiyonları bildirme,[42] ve hatta ölüm.[43]Klor dioksit, MMS, Mucize Mineral Çözeltisi ve CD protokolü dahil ancak bunlarla sınırlı olmamak üzere çeşitli marka adlarıyla yeniden etiketlenmiştir.[44] Klor dioksitin tıbbi özelliklerinin bilimsel bir temeli yoktur ve FDA, kullanımına karşı uyarıda bulunmuştur.[45][46]
Diğer kullanımlar
Klor dioksit, yok etmek için oksidan olarak kullanılır. fenoller içinde atık su akarsular ve hayvansal yan ürün (işleme) bitkilerinin hava temizleyicilerinde koku kontrolü için.[20]:4–34 Ayrıca su ile aktive olan ve gece boyunca teknede veya arabada bırakılan klor dioksit üreten paketlerde, arabalar ve tekneler için deodorant olarak kullanılabilir.
Su ve takviyelerdeki güvenlik sorunları
Klor dioksit toksiktir, bu nedenle güvenli kullanımını sağlamak için maruziyet sınırlarına ihtiyaç vardır. Birleşik Devletler Çevre Koruma Ajansı içme suyunda klor dioksit için maksimum seviyesi 0,8 mg / L ayarlamıştır.[47] iş güvenliği ve sağlığı idaresi (OSHA), bir ajans Amerika Birleşik Devletleri Çalışma Bakanlığı, 8 saatlik bir izin verilen maruz kalma sınırı havada 0.1 ppm (0.3 mg /m3 ) klor dioksit ile çalışan kişiler için.[48]
30 Temmuz 2010'da ve 1 Ekim 2010'da, Amerika Birleşik Devletleri Gıda ve İlaç Dairesi ürünün kullanımına karşı uyardı "Mucize Mineral Takviyesi Talimatlara göre yapıldığında klor dioksit üreten "veya" MMS ". MMS, HIV, kanser dahil olmak üzere çeşitli rahatsızlıkların tedavisi olarak pazarlanmaktadır. otizm ve sivilce. FDA uyarıları tüketicileri, MMS'in sağlığa ciddi zarar verebileceği konusunda bilgilendirdi ve dehidrasyonun neden olduğu çok sayıda mide bulantısı, ishal, şiddetli kusma ve hayatı tehdit eden düşük tansiyon raporu aldığını belirtti.[49][50] Bu uyarı, 12 Ağustos 2019'da üçüncü kez, 8 Nisan 2020'de ise dördüncü kez tekrarlandı ve MMS tüketmenin çamaşır suyu içmekle aynı şey olduğunu belirterek ve tüketicileri herhangi bir nedenle bunları kullanmamaya veya bu ürünleri çocuklarına vermemeye çağırdı. .[46]
Referanslar
- ^ Haynes, William M. (2010). Kimya ve Fizik El Kitabı (91 ed.). Boca Raton, Florida, ABD: CRC Basın. s. 4–58. ISBN 978-1-43982077-3.
- ^ a b c d Kimyasal Tehlikeler için NIOSH Cep Rehberi. "#0116". Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü (NIOSH).
- ^ Dobson, Stuart; Cary, Richard; Kimyasal Güvenlik Uluslararası Programı (2002). Klor dioksit (gaz). Dünya Sağlık Örgütü. s. 4. Alındı 17 Ağustos 2020.
- ^ "Klor dioksit". Yaşam ve Sağlık için Hemen Tehlikeli Konsantrasyonlar (IDLH). Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü (NIOSH).
- ^ "Klor Dioksit ve Klorit için Toksikolojik Profil" (PDF). Toksik Maddeler ve Hastalık Sicili Ajansı, ABD HHS. Arşivlenen orijinal (PDF) 2019-06-14 tarihinde.
- ^ a b "Ebeveynler otizmi 'iyileştirmek' için çocuklarını çamaşır suyu ile zehirliyor. Bu anneler onu durdurmaya çalışıyor.". NBC Haberleri. Alındı 2019-05-21.
- ^ "Sahte haber: Klor dioksit koronavirüsü durdurmayacak". Detroit Haberleri. Alındı 2020-04-03.
- ^ Friedman, Lisa (2020-04-03). "E.P.A., Sahte Koronavirüs Temizleyicileri Satıcılarına Karşı Yasal İşlemi Tehdit Ediyor". New York Times. ISSN 0362-4331. Alındı 2020-04-03.
- ^ Spencer, Sarnac Hale. "Duyduğunuz koronavirüs 'tedavileri'? Sahte. Klor dioksit içme.". BUGÜN AMERİKA. Alındı 2020-04-03.
- ^ FDA, "Çamaşır suyu içmek kanseri veya otizmi iyileştirmez,". NBC Haberleri. Alındı 2019-08-13.
- ^ Gıda ve İlaç İdaresi (2019-08-12). "FDA, tüketicileri Mucize Mineral Çözeltinin tehlikeli ve potansiyel olarak yaşamı tehdit eden yan etkileri konusunda uyarıyor". fda.gov. Arşivlenen orijinal 2019-08-14 tarihinde. Alındı 2019-08-16.
- ^ a b c d e f g h ben Vogt, H .; Balej, J .; Bennett, J. E .; Wintzer, P .; Sheikh, S. A .; Gallone, P .; Vasudevan, S .; Pelin, K. "Klor Oksitler ve Klor Oksijen Asitleri". Ullmann'ın Endüstriyel Kimya Ansiklopedisi. Weinheim: Wiley-VCH.
- ^ Brockway, L. O. (Mart 1933). "Klor Dioksitteki Üç Elektron Bağı" (PDF). Ulusal Bilimler Akademisi Bildiriler Kitabı. 19 (3): 303–307. Bibcode:1933PNAS ... 19..303B. doi:10.1073 / pnas.19.3.303. PMC 1085967. PMID 16577512.
- ^ Pauling, Linus (1988). Genel Kimya. Mineola, NY: Dover Yayınları. ISBN 0-486-65622-5.
- ^ Flesch, R .; Plenge, J .; Rühl, E. (2006). "Klor dioksitin çekirdek seviyesinde uyarılması ve parçalanması". Uluslararası Kütle Spektrometresi Dergisi. 249-250: 68–76. Bibcode:2006IJMSp.249 ... 68F. doi:10.1016 / j.ijms.2005.12.046.
- ^ Derby, R. I .; Hutchinson, W. S. (1953). Klor (IV) Oksit. İnorganik Sentezler. 4. s. 152–158. doi:10.1002 / 9780470132357.ch51. ISBN 978-0-470-13235-7.
- ^ Ni, Y .; Wang, X. (1996). "Metanol Esaslı ClO2 Üretimi Sürecinin Mekanizması". Uluslararası Selüloz Ağartma Konferansı. TAPPI. s. 454–462.[kalıcı ölü bağlantı ]
- ^ a b Beyaz, George W .; Beyaz, Geo Clifford (1999). Klorlama ve alternatif dezenfektanlar el kitabı (4. baskı). New York: John Wiley. ISBN 0-471-29207-9.
- ^ Kundak, Thomas Wilson (1997). İnorganik Kimya: Endüstriyel ve Çevresel Bir Perspektif. Akademik Basın. pp.198 –199. ISBN 0-12-678550-3.
- ^ a b c d e f g h Alternatif Dezenfektanlar ve Oksidanlar Kılavuzu, bölüm 4: Klor Dioksit (PDF), US Environmental Protection Agency: Office of Water, Nisan 1999, 2015-09-05 tarihinde orjinalinden arşivlenmiştir., alındı 2009-11-27CS1 bakımlı: uygun olmayan url (bağlantı)
- ^ a b c d Blok, Seymour Stanton (2001). Dezenfeksiyon, Sterilizasyon ve Koruma (5. baskı). Lippincott, Williams & Wilkins. s. 215. ISBN 0-683-30740-1.
- ^ Sjöström, E. (1993). Ahşap Kimyası: Temeller ve Uygulamalar. Akademik Basın. ISBN 0-12-647480-X. OCLC 58509724.
- ^ "AET - Raporlar - Bilim - Dünya Ağartılmış Kimyasal Selüloz Üretimindeki Eğilimler: 1990–2005". Arşivlenen orijinal 2017-07-30 tarihinde. Alındı 2016-02-26.
- ^ Harrel, C.G. (1952). "Un Üretiminde Olgunlaştırma ve Ağartma Maddeleri". Endüstri ve Mühendislik Kimyası. 44 (1): 95–100. doi:10.1021 / ie50505a030.
- ^ Sorlini, S .; Collivignarelli, C. (2005). "On İtalyan doğal suyunun klor, klor dioksit ve ozon ile kimyasal oksidasyonu sırasında trihalometan oluşumu". Tuzdan arındırma. 176 (1–3): 103–111. doi:10.1016 / j.desal.2004.10.022.
- ^ Li, J .; Yu, Z .; Gao, M. (1996). "Klor dioksit ile arıtılmış suda trihalometan oluşumu üzerine bir pilot çalışma". Zhonghua Yufang Yixue Zazhi (Çin Önleyici Tıp Dergisi) (Çin'de). 30 (1): 10–13. PMID 8758861.
- ^ a b c Volk, C. J .; Hofmann, R .; Chauret, C .; Gagnon, G. A .; Ranger, G .; Andrews, R.C. (2002). "Klor dioksit dezenfeksiyonunun uygulanması: Arıtma değişikliğinin tam ölçekli bir dağıtım sisteminde içme suyu kalitesi üzerindeki etkileri". Çevre Mühendisliği ve Bilimi Dergisi. 1 (5): 323–330. doi:10.1139 / s02-026.
- ^ Pereira, M. A .; Lin, L. H .; Lippitt, J. M .; Herren, S.L. (1982). "Karsinojenezin başlatıcıları ve destekleyicileri olarak trihalometanlar". Çevre Sağlığı Perspektifleri. 46: 151–156. doi:10.2307/3429432. JSTOR 3429432. PMC 1569022. PMID 7151756.
- ^ Andrews, L .; Anahtar, A .; Martin, R .; Grodner, R .; Park, D. (2002). "Karides ve kerevitin klor dioksitle yıkanması sulu klora bir alternatiftir". Gıda Mikrobiyolojisi. 19 (4): 261–267. doi:10.1006 / fmic.2002.0493.
- ^ Zhang, Zhe; McCann, Carole; Stout, Janet E .; Piesczynski, Steve; Hawks, Robert; Vidic, Radisav; Yu, Victor L. (2007). "Klor Dioksitin Güvenliği ve Etkinliği Lejyonella Hastane Su Sisteminde kontrol " (PDF). Enfeksiyon Kontrolü ve Hastane Epidemiyolojisi. 28 (8): 1009–1012. doi:10.1086/518847. PMID 17620253. Alındı 2009-11-27.
- ^ Ogata, N .; Shibata, T. (Ocak 2008). "Düşük konsantrasyonlu klor dioksit gazının influenza A virüsü enfeksiyonuna karşı koruyucu etkisi". Genel Viroloji Dergisi. 89 (pt 1): 60–67. doi:10.1099 / vir.0.83393-0. PMID 18089729.
- ^ Zhang, Y.-L .; Zheng, S.-Y .; Zhi, Q. (2007). "Sabunlarda Klor Dioksit ile Hava Dezenfeksiyonu". Çevre ve Sağlık Dergisi. 24 (4): 245–246.
- ^ "Klor dioksit kullanarak şarbon sporu dekontaminasyonu". Birleşik Devletler Çevre Koruma Ajansı. 2007. Alındı 2009-11-27.
- ^ Sy, Kaye V .; McWatters, Kay H .; Beuchat Larry R. (2005). "Gazlı Klor Dioksitin Yaban Mersini, Çilek ve Ahududu Üzerindeki Salmonella, Mayalar ve Küfleri Öldürmede Dezenfektan Olarak Etkisi". Gıda Koruma Dergisi. Uluslararası Gıda Koruma Derneği. 68 (6): 1165–1175. doi:10.4315 / 0362-028x-68.6.1165. PMID 15954703.
- ^ "Dezenfektanların COVID-19 koronavirüsü öldürmesi gerektiğini nereden biliyoruz". Kimya ve Mühendislik Haberleri. Alındı 2020-03-28.
- ^ ABD EPA, OCSPP (2020-03-13). "Liste N: SARS-CoV-2'ye Karşı Kullanım için Dezenfektanlar". ABD EPA. Alındı 2020-03-28.
- ^ O'Brian, D. (2017). "Klor Dioksit Torbaları Üretimi Daha Güvenli Hale Getirebilir ve Bozulmayı Azaltabilir". AgResearch Dergisi. USDA Tarımsal Araştırma Servisi (Temmuz). Alındı 2018-06-21.
- ^ "Klorlu tavuk paniğinin ardındaki gerçek". Büyük olay. 2019-05-29. Alındı 2020-02-05.
- ^ Coates, D. (2001). "Esnek endoskopların dekontaminasyonu için bir klor dioksit üreteci ile donatılmış bir otomatik yıkayıcı / dezenfektörde (Medivator) klor dioksit (Tristel One-Shot) kullanımının bir değerlendirmesi". Journal of Hospital Infection. 48 (1): 55–65. doi:10.1053 / jhin.2001.0956. PMID 11358471.
- ^ "Tristel Wipes Sistemi Ürün Bilgileri" (PDF). Etik Ajanlar. Arşivlenen orijinal (PDF) 2016-04-15 tarihinde. Alındı 2012-11-01.
- ^ Gibbs, S. G .; Lowe, J. J .; Smith, P. W .; Hewlett, A. L. (2012). "Tahtakuru kontrolüne alternatif olarak gaz halindeki klor dioksit". Enfeksiyon Kontrolü ve Hastane Epidemiyolojisi. 33 (5): 495–9. doi:10.1086/665320. PMID 22476276. S2CID 14105046.
- ^ Bartley, Lisa (2016-10-29). "SoCal ebeveynlerinden oluşan bir grup, otizmli çocukları çamaşır suyu kullanarak gizlice tedavi etmeye çalışıyor". ABC 7 Haberleri. ABC. Alındı 2019-03-24.
- ^ Ryan, Frances (2016-07-13). "Otizm için ölümcül olabilen sahte tedaviler". Gardiyan. Guardian Media Group. Alındı 2019-03-24.
- ^ "Çocuklarına Otizmi 'İyileştirmek' İçin Lavman Veren Ebeveynler". vice.com. 2015-03-12. Alındı 2018-04-05.
- ^ "FDA, Tüketicileri Mucize Mineral Çözeltisi (MMS) İçmekten Ciddi Zarara Karşı Uyardı". 2011-02-03. Arşivlenen orijinal 2011-02-03 tarihinde. Alındı 2018-04-05.
- ^ a b Gıda ve İlaç İdaresi (2019-08-12). "FDA, tüketicileri Mucize Mineral Çözeltinin tehlikeli ve potansiyel olarak yaşamı tehdit eden yan etkileri konusunda uyarıyor". fda.gov. Arşivlenen orijinal 2019-08-14 tarihinde. Alındı 2019-08-16.
- ^ "ATSDR: Klor Dioksit ve Klorit için ToxFAQs ™".
- ^ "Klor Dioksit için İş Sağlığı ve Güvenliği Rehberi". Arşivlenen orijinal 2012-12-04 tarihinde. Alındı 2012-12-08.
- ^ "Basın Duyuruları - FDA, Tüketicileri Mucize Mineral Çözeltisi (MMS) İçmekten Ciddi Zarara Karşı Uyardı". Arşivlenen orijinal 2017-01-12 tarihinde.
- ^ "'Mucize 'Tedavisi Güçlü Ağartıcıya Dönüşüyor ". ABD Gıda ve İlaç İdaresi. 2015-11-20. Arşivlendi 2017-11-01 tarihinde orjinalinden. Alındı 2017-12-06.
Dış bağlantılar
 İle ilgili medya Klor dioksit Wikimedia Commons'ta
İle ilgili medya Klor dioksit Wikimedia Commons'ta



