Radyocerrahi - Radiosurgery
| Radyocerrahi | |
|---|---|
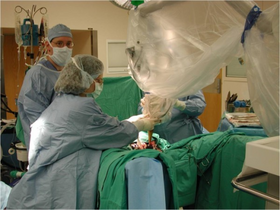 Yerleştirilen bir radyocerrahi sistemini gösteren intraoperatif fotoğraf. Fotoğraftaki hasta rektum kanseri tedavisi görüyor. | |
| Uzmanlık | Onkoloji |
| MedlinePlus | 007577 |
| eTıp | 1423298 |
Radyocerrahi dır-dir ameliyat kullanma radyasyon,[1] yani, tam olarak seçilmiş alanların yok edilmesi doku kullanma iyonlaştırıcı radyasyon bıçakla eksizyon yerine. Diğer formlar gibi radyasyon tedavisi (radyoterapi olarak da adlandırılır), genellikle tedavi etmek için kullanılır kanser. Radyocerrahi başlangıçta İsveçli beyin cerrahı tarafından tanımlandı Lars Leksell "ilgi konusu intrakraniyal bölgeye stereotaktik olarak yönlendirilmiş tek bir yüksek doz radyasyon fraksiyonu" olarak.[2]
İçinde stereotaktik radyocerrahi (SRS), kelime "stereotaktik "üç boyutlu bir koordinat sistemi Bu, hastanın tanısal görüntülerinde görülen sanal bir hedefin hastadaki gerçek hedef konumla doğru korelasyonunu sağlar. Stereotaktik radyocerrahi de çağrılabilir stereotaktik vücut radyasyon tedavisi (SBRT) veya stereotaktik ablatif radyoterapi (SABR) dışında kullanıldığında Merkezi sinir sistemi (CNS).[3]
Tarih
Stereotaktik radyocerrahi ilk olarak 1949'da İsveçli beyin cerrahı Lars Leksell tarafından beyindeki geleneksel cerrahiye uygun olmayan küçük hedefleri tedavi etmek için geliştirildi. Tasarladığı ilk stereotaktik alet, problar ve elektrotlar kullanıyordu.[4] Elektrotları radyasyonla değiştirmeye yönelik ilk girişim ellili yılların başlarında yapıldı. röntgen.[5] Bu aletin prensibi, çok yönlerden gelen dar radyasyon ışınları ile kafa içi hedefi vurmaktı. Işın yolları, hedef hacimde birleşir ve orada ölümcül bir kümülatif radyasyon dozu verirken, dozu bitişik sağlıklı doku ile sınırlar. On yıl sonra, fizikçiler Kurt Liden ve Börje Larsson'un katkılarıyla önemli ölçüde önemli ilerleme kaydedildi.[6] Şu anda stereotaktik proton ışınlar röntgenlerin yerini almıştı.[7] Ağır parçacık ışını, cerrahi bıçak için mükemmel bir yedek olarak sunuldu, ancak senkrosiklotron çok sakardı. Leksell, cerrahın kendisi tarafından idare edilebilecek pratik, kompakt, hassas ve basit bir araç geliştirmeye devam etti. 1968'de bu, makineye kurulan Gamma Knife ile sonuçlandı. Karolinska Enstitüsü ve birkaçından oluşuyordu kobalt-60 radyoaktif gama ışınları ile ışınlama için merkezi kanallara sahip bir tür kaska yerleştirilmiş kaynaklar.[8] Bu prototip, ağrıyı, hareket bozukluklarını veya geleneksel tedaviye yanıt vermeyen davranış bozukluklarını tedavi etmek için fonksiyonel beyin cerrahisi prosedürleri için yarık benzeri radyasyon lezyonları üretmek üzere tasarlandı. Bu ilk ünitenin başarısı, 179 kobalt-60 kaynağı içeren ikinci bir cihazın yapımına yol açtı. Bu ikinci Gamma Knife ünitesi, beyin tümörlerini ve intrakraniyalleri tedavi etmek için küresel lezyonlar üretmek üzere tasarlanmıştır. arteriyovenöz malformasyonlar (AVM'ler).[9] 1980'lerde tamamı 201 kobalt-60 kaynağıyla ek üniteler kuruldu.[10]
Bu gelişmelere paralel olarak, benzer bir yaklaşım, doğrusal parçacık hızlandırıcı veya Linac. İlk 4'ün kurulumuMeV klinik lineer hızlandırıcı, Haziran 1952'de Tıbbi Araştırma Konseyi (MRC) Radyoterapötik Araştırma Biriminde başladı. Hammersmith Hastanesi, Londra.[11] Sistem, 1953 Şubat'ında fizik ve diğer testler için devredildi ve o yıl 7 Eylül'de hastaları tedavi etmeye başladı. Bu arada, Stanford Mikrodalga Laboratuvarı'ndaki çalışma, 1956'da Kaliforniya'daki Stanford Üniversite Hastanesi'ne kurulan bir 6-MV hızlandırıcının geliştirilmesine yol açtı.[12] Linac birimleri hızlı bir şekilde geleneksel fraksiyonlu cihazlar için tercih edilen cihazlar haline geldi radyoterapi ancak özel Linac radyocerrahisinin gerçeğe dönüşmesinden önce 1980'lere kadar sürdü. 1982'de İspanyol beyin cerrahı J. Barcia-Salorio, AVM'lerin tedavisinde kobalt kaynaklı ve ardından Linac tabanlı foton radyocerrahisinin rolünü değerlendirmeye başladı ve epilepsi.[13] 1984'te Betti ve Derechinsky, Linac tabanlı bir radyocerrahi sistemi tanımladılar.[14] Winston ve Lutz, iyileştirilmiş bir stereotaktik konumlandırma cihazı ve çeşitli bileşenlerin doğruluğunu ölçmek için bir yöntem ekleyerek Linac tabanlı radyocerrahi prototip teknolojilerini daha da geliştirdi.[15] Değiştirilmiş bir Linac kullanarak, Amerika Birleşik Devletleri'ndeki ilk hasta Boston'da tedavi edildi. Brigham ve Kadın Hastanesi Şubat 1986'da.
21'inci yüzyıl
Tıbbi görüntüleme ve hesaplamadaki teknolojik gelişmeler, stereotaktik radyocerrahinin klinik olarak daha fazla benimsenmesine yol açtı ve 21. yüzyılda kapsamını genişletti.[16][17] "Stereotaktik" kelimesinin içerdiği lokalizasyon doğruluğu ve kesinliği, radyocerrahi müdahaleler için son derece önemlidir ve önemli ölçüde iyileştirilmiştir. görüntü rehberliği gibi teknolojiler N-localizer[18] ve Sturm-Pastyr yerelleştiricisi[19] başlangıçta için geliştirilmiş olan stereotaktik cerrahi.
21. yüzyılda orijinal radyocerrahi kavramı, beş adede kadar tedaviyi içerecek şekilde genişledi. kesirler ve stereotaktik radyocerrahi, farklı olarak yeniden tanımlandı beyin cerrahisi harici olarak oluşturulan kullanan disiplin iyonlaştırıcı radyasyon cerrahi bir kesiğe gerek kalmadan, tipik olarak baş veya omurgada tanımlanmış hedefleri etkisiz hale getirmek veya ortadan kaldırmak için.[20] Stereotaktik radyocerrahi ve fraksiyone radyoterapi kavramları arasındaki benzerliklerden bağımsız olarak, tedaviye ulaşma mekanizması ince bir şekilde farklıdır, ancak her iki tedavi yönteminin de belirli endikasyonlar için aynı sonuçlara sahip olduğu bildirilmiştir.[21] Stereotaktik radyocerrahinin, bitişik normal dokuyu korurken hedef dokuyu yok etmek için küçük alanlara hassas, yüksek dozlar vermeye daha fazla vurgu vardır. Aynı prensip geleneksel radyoterapide de izlenir, ancak daha geniş alanlara yayılan daha düşük doz oranlarının kullanılması daha olasıdır (örneğin, VMAT tedaviler). Fraksiyone radyoterapi daha çok farklı yöntemlere dayanır. radyosensitivite hedefin ve çevresindeki normal dokunun toplam birikmiş radyasyon dozu.[20] Tarihsel olarak, fraksiyone radyoterapi alanı, orijinal stereotaktik radyocerrahi konseptinden, ilkelerin keşfini takiben gelişti. radyobiyoloji: onarım, yeniden sınıflandırma, yeniden doldurma ve yeniden oksijenleme.[22] Günümüzde, fraksiyone radyoterapiye dirençli olabilen tümörler radyocerrahiye iyi yanıt verebildiğinden ve güvenli radyocerrahi için kritik organlara çok büyük veya çok yakın olan tümörler fraksiyonlu radyoterapi için uygun adaylar olabileceğinden, her iki tedavi tekniği de tamamlayıcıdır.[21]
Bugün hem Gamma Knife hem de Linac radyocerrahi programları dünya çapında ticari olarak mevcuttur. Gamma Knife radyocerrahiye adanırken, birçok Linac geleneksel fraksiyone radyoterapi için üretilmiştir ve özel radyocerrahi araçları haline gelmek için ek teknoloji ve uzmanlık gerektirir. Bu farklı yaklaşımlar arasında etkinlik açısından net bir fark yoktur.[23][24] Büyük üreticiler, Varian ve Elekta Özel radyocerrahi Linacs yanı sıra radyocerrahi yetenekleri ile geleneksel tedavi için tasarlanmış makineler sunar. Geleneksel Linac'leri ışın şekillendirme teknolojisi, tedavi planlaması ve görüntü kılavuzluk araçlarıyla tamamlamak üzere tasarlanmış sistemler sağlamak için.[25] Özel bir radyocerrahi Linac örneği, CyberKnife, hastanın etrafında hareket eden ve tümörü geniş bir sabit pozisyon setinden ışınlayan ve böylece Gamma Knife konseptini taklit eden robotik bir kol üzerine monte edilmiş kompakt bir Linac.
Klinik uygulamalar
CNS dışında kullanıldığında stereotaktik vücut radyasyon tedavisi (SBRT) veya stereotaktik ablatif radyoterapi (SABR) olarak adlandırılabilir.[3]
Merkezi sinir sistemi
Radyocerrahi, multidisipliner bir ekip tarafından gerçekleştirilir. beyin cerrahları, radyasyon onkologları ve tıbbi fizikçiler tıbbi lineer hızlandırıcılar, Gamma Knife ünitesi ve Cyberknife ünitesi dahil olmak üzere son derece sofistike, son derece hassas ve karmaşık cihazları çalıştırmak ve sürdürmek. Beyin ve omurgadaki hedeflerin son derece hassas şekilde ışınlanması, şu yolla elde edilen tıbbi görüntülerden elde edilen bilgiler kullanılarak planlanır. bilgisayarlı tomografi, manyetik rezonans görüntüleme, ve anjiyografi.
Radyocerrahi, öncelikle tümörlerin, vasküler lezyonların ve fonksiyonel bozuklukların tedavisi için endikedir. Bu teknikle önemli klinik yargı kullanılmalı ve değerlendirmeler lezyon tipi, varsa patolojisi, boyutu, yeri ve yaşı ile hastanın genel sağlığını içermelidir. Radyocerrahinin genel kontrendikasyonları arasında, hedef lezyonun aşırı büyük boyutu veya pratik tedavi için çok sayıda lezyon yer alır. Hastalar bir ila beş gün içinde şu şekilde tedavi edilebilir: ayakta tedavi gören hastalar. Karşılaştırıldığında, ortalama hastanede kalış süresi kraniyotomi (kafatasının açılmasını gerektiren geleneksel beyin cerrahisi) yaklaşık 15 gündür. Radyocerrahinin sonucu, tedaviden sonraki aylara kadar belli olmayabilir. Radyocerrahi tümörü ortadan kaldırmadığı, biyolojik olarak inaktive ettiği için, lezyonun büyümesinin olmaması normalde tedavi başarısı olarak kabul edilir. Radyocerrahi için genel endikasyonlar, birçok beyin tümörünü içerir. akustik nöromalar, Germinomlar, meningiomlar, metastazlar diğerleri arasında trigeminal nevralji, arteriyovenöz malformasyonlar ve kafa tabanı tümörleri. Stereotaktik radyoterapinin ekstrakraniyal lezyonlara genişlemesi artıyor ve metastaz, karaciğer kanseri, akciğer kanseri, pankreas kanseri vb.
Hareket mekanizması

Radyocerrahinin temel ilkesi, seçici iyonlaşma yüksek enerjili radyasyon ışınları aracılığıyla dokunun. İyonlaşma üretimidir iyonlar ve serbest radikaller zarar veren hücreler. Hücredeki sudan veya biyolojik materyallerden oluşabilen bu iyonlar ve radikaller, DNA, proteinler ve lipidlere onarılamaz hasar vererek hücrenin ölümüne neden olabilir. Böylelikle, tedavi edilecek doku hacminde kesin bir yıkıcı etki ile biyolojik inaktivasyon gerçekleştirilir. Radyasyon dozu genellikle şu şekilde ölçülür: griler (bir gri (Gy), birinin emilimidir joule kilogram kütle başına enerji). Hem ışınlanan farklı organları hem de radyasyon türünü dikkate almaya çalışan bir birim, Sievert, hem yatırılan enerji miktarını hem de biyolojik etkinliği tanımlayan bir birim.
Riskler
New York Times Aralık 2010'da, radyocerrahinin lineer hızlandırıcı yöntemiyle radyasyon aşırı dozlarının meydana geldiğini, bunun büyük ölçüde stereotaktik radyocerrahi için güçlendirilen ekipmandaki yetersiz korumalardan kaynaklandığını bildirdi.[26] ABD'de Gıda ve İlaç İdaresi (FDA) bu cihazları düzenlerken, Gamma Knife, Nükleer Düzenleme Komisyonu. NYT odaklanmış makale Varian ekipman ve ilgili yazılım, ancak sorun muhtemelen bu üreticiyle sınırlı olmayacak.[kaynak belirtilmeli ]
Bu kanıttır ki immünoterapi stereotaktik radyoterapiyi takiben radyasyon nekrozunun tedavisi için faydalı olabilir.[27]
Radyasyon kaynağı türleri
Uygun radyasyon ve cihaz türünün seçimi, kritik yapılarla ilişkili olarak lezyon tipi, boyutu ve konumu gibi birçok faktöre bağlıdır. Veriler, çeşitli tekniklerin tümü ile benzer klinik sonuçların mümkün olduğunu göstermektedir. Kullanılan cihazdan daha önemli olan tedavi endikasyonları, verilen toplam doz, fraksiyonasyon programı ve tedavi planının uygunluğudur.
Gama Bıçağı
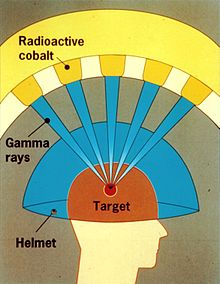
Gama bıçağı, özellikle beyindeki tümör hücrelerini tedavi etmek için Gama radyasyonu kullanan Gama Bıçağı (Leksell Gama Bıçağı olarak da bilinir), Elekta AB kamuya açık bir İsveç şirketi, tedavi etmek için kullanılır BEYİn tümörü radyasyonu küçük bir hacim üzerinde yoğunlaştıracak şekilde yüksek yoğunluklu gama radyasyon tedavisi uygulayarak. Cihaz, 1967'de Karolinska Enstitüsü'nde icat edildi. Stockholm, İsveç, Lars Leksell, Romanya doğumlu beyin cerrahı Ladislau Steiner ve radyobiyolog Dan Börje Larsson Uppsala Üniversitesi, İsveç. İlk Gamma Knife, ABD'li beyin cerrahı arasında yapılan bir anlaşmayla Amerika Birleşik Devletleri'ne getirildi. Robert Wheeler Rand ve Leksell ve Kaliforniya Üniversitesi, Los Angeles'a (UCLA) 1979'da verildi.
Bir Gama Bıçağı tipik olarak 201 içerir kobalt-60 yaklaşık 30 kaynakCuries her biri (1.1TBq ), ağır bir şekilde hemisferik bir diziye yerleştirilmiş korumalı montaj. Cihazın amacı gama radyasyonu hastanın beynindeki bir hedef noktadan. Hasta, beyin tümörünün gama ışınlarının hedef noktasında sabit kalması için kafatasına cerrahi olarak sabitlenmiş özel bir kask takar. Bir ablatif radyasyon dozu böylelikle tümör yoluyla bir tedavi seansında gönderilirken, çevreleyen beyin dokuları nispeten korunur.
Gamma Knife tedavisi, tüm radyocerrahi gibi, kanser hücrelerini öldürmek ve tümörleri küçültmek için radyasyon dozlarını kullanır ve sağlıklı beyin dokusuna zarar vermekten kaçınmak için hassas bir şekilde verilir. Gamma Knife radyocerrahisi, birçok gama radyasyonu ışınını bir veya daha fazla tümöre doğru şekilde odaklayabilir. Her bir ışın nispeten düşük yoğunluktadır, bu nedenle radyasyonun müdahale eden beyin dokusu üzerinde çok az etkisi vardır ve yalnızca tümörün kendisinde yoğunlaşır.
Gamma Knife radyocerrahisinin, boyutu 4 cm'ye (1,6 inç) kadar olan iyi huylu veya kötü huylu beyin tümörleri olan hastalarda etkili olduğu kanıtlanmıştır. vasküler gibi malformasyonlar arteriyovenöz malformasyon (AVM), ağrı ve diğer işlevsel sorunlar.[28][29][30][31] Trigeminal nevraljinin tedavisi için prosedür hastalar üzerinde tekrar tekrar kullanılabilir.
Gamma Knife radyocerrahisini takiben akut komplikasyonlar nadirdir,[32] ve komplikasyonlar tedavi edilen durumla ilgilidir.[33][34]
Doğrusal hızlandırıcı tabanlı tedaviler
Doğrusal bir hızlandırıcı (linac), yüksek hızda çarpan hızlandırılmış elektronların etkisiyle x-ışınları üretir. z hedef (genellikle tungsten). Bu nedenle bir Linac, genellikle 6 MV foton kullanılmasına rağmen, herhangi bir enerjinin x-ışınlarını üretebilir. Bir Linac ile portal, dağıtım açısını değiştirmek için uzayda hareket eder. Doğrusal hızlandırıcı ekipman ayrıca, teslim noktasını değiştirmek için hastayı tedavi yatağında yatarak hareket ettirebilir. Bu tedaviler, hastanın hareketini kısıtlamak için stereotaktik bir çerçeve kullanmayı içerir. Brainlab'ın Novalis Shaped Beam Radyocerrahi sistemi ve Tx Radyocerrahi platformu, hem hasta için rahat hem de doğru olduğu kanıtlanmış X-ray görüntüleme ile çerçevesiz, invaziv olmayan bir teknik uygular. Varian'dan Üçleme veya Accuray'den CyberKnife, bir tedavi sırasında herhangi bir hasta hareketini tespit etmek için gerçek zamanlı görüntülemeyle birleştirilmiş non-invaziv immobilizasyon cihazlarıyla da kullanılabilir.
Doğrusal hızlandırıcılar yüksek enerjili X-ışınları yayar; işlem genellikle "X ışını tedavisi" veya "foton tedavisi" olarak adlandırılır. "Gama ışını" terimi genellikle kobalt-60 gibi bir radyoizotoptan yayılan fotonlar için ayrılmıştır (aşağıya bakınız). Bu tür radyasyon, yüksek voltaj hızlandırıcıların yaydığı radyasyondan önemli ölçüde farklı değildir. Doğrusal hızlandırıcı terapide, emisyon başlığı ("portal ") mekanik olarak tam veya kısmi bir daire içinde hasta etrafında döndürülür. Hastanın yattığı masa," kanepe "de küçük doğrusal veya açısal adımlarla hareket ettirilebilir. Portal ve ayakların hareketlerinin kombinasyonu Kanepe, ışınlanacak doku hacminin bilgisayarlı planlanmasını mümkün kılar.6 MeV yüksek enerjiye sahip cihazlar, hedefin derinliği nedeniyle beyin tedavisi için en uygun olanlardır. Emisyon başlığından çıkan enerji ışını ile lezyonun boyutuna göre ayarlanabilir kolimatörler. Bunlar, farklı çaplarda, tipik olarak 5 mm adımlarla 5 ila 40 mm arasında değişen, değiştirilebilir menfezler veya radyasyon ışınını uyacak şekilde şekillendirmek için tedavi sırasında dinamik olarak hareket ettirilebilen bir dizi metal yaprakçıktan oluşan çok kanatlı kolimatörler olabilirler. kesilecek kütle. 2017 itibariyle[Güncelleme] Linac'lar, 0,15 ila 0,3 mm gibi son derece dar kiriş geometrileri elde edebilir. Bu nedenle, trigeminal nevralji, vb. Gibi, şimdiye kadar açık veya endoskopik cerrahi ile gerçekleştirilmiş birkaç çeşit ameliyat için kullanılabilirler. Trigeminal nevralji için etkinliğinin tam mekanizması bilinmemektedir; ancak bu amaçla kullanımı çok yaygın hale gelmiştir. Uzun vadeli takip verileri, radyofrekans ablasyon kadar etkili olduğunu, ancak ağrının tekrarını önlemede cerrahiden daha düşük olduğunu göstermiştir.
X-ışınlarını floroskopide görülebilen çok küçük bir alana göndermek için hareketli bir kol üzerine monte edilmiş küçük bir hızlandırıcı kullanan bir tür doğrusal hızlandırıcı terapisine Cyberknife tedavisi denir. 1990'daki ilk başlangıcından beri çerçevesiz robotik Cyberknife sisteminin birkaç nesli geliştirilmiştir. John R. Adler, bir Stanford Üniversitesi nöroşirürji ve radyasyon onkolojisi profesörü ve Russell ve Peter Schonberg, Schonberg Research'te yer alan Accuray şirketi tarafından satılmaktadır. Sunnyvale, Kaliforniya, ABD. Bu tür CyberKnife sistemlerinin çoğu dünya çapında mevcuttur.
Cyberknife, Gamma Knife tedavisi ile karşılaştırılabilir (yukarıya bakın), ancak radyoizotoplar tarafından yayılan gama ışınlarını kullanmaz. Ayrıca, bir bilgisayar tedavi sırasında hastanın konumunu izlediği için hastayı tutmak için bir çerçeve kullanmaz. floroskopi. Cyberknife radyocerrahisinin robotik konsepti, hastayı stereotaksik bir çerçeve ile sabitlemek yerine tümörün izlenmesini sağlar. Herhangi bir çerçeve gerekmediği için bazı radyocerrahi konseptleri ekstrakraniyal tümörleri tedavi etmek için genişletilebilir. Bu durumda, Cyberknife robotik kolu tümör hareketini (yani solunum hareketini) izler.[35] Stereo röntgen görüntüleme ve kızılötesi izleme sensörlerinin bir kombinasyonu, tümör konumunu gerçek zamanlı olarak belirler.
Proton ışın tedavisi
Protonlar ayrıca radyocerrahide adı verilen bir prosedürde kullanılabilir. Proton Işın Terapisi (PBT) veya proton tedavisi. Protonlar, bir tıbbi tarafından proton donör materyallerinden çıkarılır. senkrotron veya siklotron ve bir insan vücudunu geçmek için gereken enerjiye, genellikle yaklaşık 200 MeV'ye ulaşana kadar, güçlü mıknatıslar kullanarak, dairesel, boşaltılmış bir kanal veya boşluk boyunca birbirini takip eden geçişlerde hızlandırılır. Daha sonra ışınlama hedefi olan hastanın vücudunda tedavi edilecek bölgeye doğru salınırlar. Yalnızca belirli bir enerjinin protonlarını ileten bazı makinelerde, uygun penetrasyon derecesini sağlamak için ışın enerjisini ayarlamak için ışın kaynağı ile hasta arasına plastikten yapılmış özel bir maske yerleştirilir. Fenomeni Bragg zirvesi Proton enerjisinin çoğu sınırlı bir mesafede biriktiği için, bu aralığın dışındaki doku (ve bir dereceye kadar bu aralığın içindeki doku da) radyasyonun etkilerinden korunduğundan, diğer radyasyon türlerine göre proton terapisi avantajları sağlar. Protonların bu özelliği, "derinlik yükü etkisi "denizaltı karşıtı savaşta kullanılan patlayıcı silahlara benzetilerek, çok düzensiz şekilli hedeflerin etrafında bile uyumlu doz dağılımlarının oluşturulmasına ve radyasyona duyarlı yapılar tarafından çevrelenmiş veya geri durdurulmuş hedeflere daha yüksek dozlar için izin verir. optik kiazma veya beyin sapı. "Yoğunluk modülasyonlu" tekniklerin geliştirilmesi, doğrusal hızlandırıcı radyocerrahi kullanılarak benzer uyumların elde edilmesine izin verdi.
2013 itibarıyla[Güncelleme] "Bir avuç nadir pediatrik kanser" dışında, çoğu durumda proton tedavisinin diğer tedavi türlerinden daha iyi olduğuna dair hiçbir kanıt yoktu. Giderek artan sayıda çok pahalı PBT kurulumuna yanıt veren eleştirmenler, "tıbbi silâhlanma yarışı "ve" çılgın tıp ve sürdürülemez kamu politikası ".[36]
Referanslar
- ^ Elsevier, Dorland'ın Resimli Tıp Sözlüğü, Elsevier.
- ^ Leksell, Lars (Aralık 1951). "Beynin stereotaksik yöntemi ve radyocerrahi". Acta Chirurgica Scandinavica. 102 (4): 316–9. PMID 14914373.
- ^ a b Stereotaktik vücut radyoterapisi (SBRT)
- ^ Leksell, Lars (1949). "İntraserebral cerrahi için stereotaksik bir aparat". Acta Chirurgica Scandinavica. 99: 229.
- ^ Leksell, Lars (Aralık 1951). "Beynin stereotaksik yöntemi ve radyocerrahi". Acta Chirurgica Scandinavica. 102 (4): 316–9. PMID 14914373.
- ^ Larsson, Borje (1958). "Bir beyin cerrahisi aracı olarak yüksek enerjili proton ışını". Doğa. 182 (4644): 1222–3. Bibcode:1958Natur.182.1222L. doi:10.1038 / 1821222a0. PMID 13590280. S2CID 4163683.
- ^ Leksell, Lars (Ekim 1960). "Yüksek enerjili proton demetinin ürettiği beynin derinliklerinde lezyonlar". Acta Radiologica. 54 (4): 251–64. doi:10.3109/00016926009172547. PMID 13760648.
- ^ Leksell, Lars (Eylül 1983). "Stereotaktik Radyocerrahi". Nöroloji, Nöroşirürji ve Psikiyatri Dergisi. 46 (9): 797–803. doi:10.1136 / jnnp.46.9.797. PMC 1027560. PMID 6352865.
- ^ Wu, Andrew (Nisan 1990). "Gamma Knife fiziği stereotaktik radyocerrahide yakınsak ışınlara yaklaşımı". Uluslararası Radyasyon Onkolojisi Dergisi, Biyoloji, Fizik. 18 (4): 941–949. doi:10.1016 / 0360-3016 (90) 90421-f. PMID 2182583.
- ^ Walton, L (1987). "Sheffield stereotaktik radyocerrahi birimi: fiziksel özellikler ve çalışma ilkeleri". İngiliz Radyoloji Dergisi. 60 (717): 897–906. doi:10.1259/0007-1285-60-717-897. PMID 3311273.
- ^ Fry, D.W. (1948). "4 MeV elektron için hareketli dalga doğrusal hızlandırıcı". Doğa. 162 (4126): 859–61. Bibcode:1948Natur.162..859F. doi:10.1038 / 162859a0. PMID 18103121. S2CID 4075004.
- ^ Bernier, J (2004). "Radyasyon onkolojisi: başarılarla dolu bir yüzyıl". Doğa Yorumları. Kanser. 4 (9): 737–47. doi:10.1038 / nrc1451. PMID 15343280. S2CID 12382751.
- ^ Barcia-Salorio, J.L. (1982). "Karotis-kavernöz fistülün radyocerrahi tedavisi". Uygulamalı Nörofizyoloji. 45 (4–5): 520–522. doi:10.1159/000101675. PMID 7036892.
- ^ Betti, O.O. (1984). "Doğrusal Hızlandırıcı ile Hiperselektif Ensefalik Işınlama". Doğrusal hızlandırıcı ile hiperselektif ensefalik ışınlama. Acta Neurochirurgica Ek. 33. s. 385–390. doi:10.1007/978-3-7091-8726-5_60. ISBN 978-3-211-81773-5.
- ^ Winston, K.R. (1988). "Stereotaktik radyocerrahi için beyin cerrahisi aracı olarak doğrusal hızlandırıcı". Nöroşirürji. 22 (3): 454–464. doi:10.1227/00006123-198803000-00002. PMID 3129667.
- ^ De Salles, A (2008). "Beyinden omurgaya radyocerrahi: 20 yıllık deneyim". Rekonstrüktif Nöroşirurji. Açta Neurochirurgica. Ek. Açta Neurochirurgica Supplementum. 101. s. 163–168. doi:10.1007/978-3-211-78205-7_28. ISBN 978-3-211-78204-0. PMID 18642653.
- ^ Timmerman, Robert (2006). "Tıbbi olarak inoperabl erken evre akciğer kanseri için stereotaktik vücut radyasyon terapisinin bir faz II çalışmasında merkezi tümörleri tedavi ederken aşırı toksisite". Klinik Onkoloji Dergisi. 24 (30): 4833–9. doi:10.1200 / JCO.2006.07.5937. PMID 17050868.
- ^ Galloway, RL Jr. (2015). "Görüntü Güdümlü Cerrahiye Giriş ve Tarihsel Perspektifler". Golby, AJ (ed.). Görüntü Rehberli Nöroşirurji. Amsterdam: Elsevier. s. 2–4. doi:10.1016 / B978-0-12-800870-6.00001-7. ISBN 978-0-12-800870-6.
- ^ Sturm V, Pastyr O, Schlegel W, Scharfenberg H, Zabel HJ, Netzeband G, Schabbert S, Berberich W (1983). "Entegre stereotaktik nöroradyolojik araştırmalar için temel olarak değiştirilmiş bir Riechert-Mundinger cihazıyla stereotaktik bilgisayar tomografisi". Açta Neurochirurgica. 68 (1–2): 11–17. doi:10.1007 / BF01406197. PMID 6344559. S2CID 38864553.
- ^ a b Barnett, Gene H. (2007). "Stereotaktik radyocerrahi - organize bir nöroşirürji onaylı tanım". Nöroşirurji Dergisi. 106 (1): 1–5. doi:10.3171 / jns.2007.106.1.1. PMID 17240553. S2CID 1007105.
- ^ a b Taraklar, Stephanie (2010). "LINAC tabanlı tek doz radyocerrahiden sonra, vestibüler schwannomalı hastalar için fraksiyone stereotaktik radyoterapiden sonra klinik sonuçlardaki farklılıklar". Uluslararası Radyasyon Onkolojisi Dergisi, Biyoloji, Fizik. 76 (1): 193–200. doi:10.1016 / j.ijrobp.2009.01.064. PMID 19604653.
- ^ Bernier Jacques (2004). "Radyasyon onkolojisi: başarılarla dolu bir yüzyıl". Doğa Yorumları. Kanser. 4 (9): 737–747. doi:10.1038 / nrc1451. PMID 15343280. S2CID 12382751.
- ^ Mathis, S; Eisner, W (6 Ekim 2010). Gamma Knife ile uyarlanmış lineer hızlandırıcılar: İki radyocerrahi uygulamasının karşılaştırması (Bildiri). HTA-Projektbericht 47. eISSN 1993-0496. ISSN 1993-0488.
- ^ McDermott, M.W. (2010). Radyocerrahi. Karger Tıp ve Bilimsel Yayıncılar. s. 196. ISBN 9783805593656.
- ^ Schoelles, Karen M .; Uhl, Stacey; Launders, Jason; Inamdar, Rohit; Bruening, Wendy; Sullivan, Nancy; Tipton, Kelley N. (2011). "Şu anda SBRT için Pazarlanan Cihazlar". Stereotaktik Vücut Radyasyon Tedavisi. Sağlık Araştırmaları ve Kalite Ajansı (ABD). PMID 21735562.
- ^ "Nokta Tespit Işını Görünmez Şekilde Gezinerek İyileşmek Yerine Zarar Veriyor". New York Times. 2010-12-28.
- ^ Kaidar-Person O, Zagar TM, Deal A, Moschos SJ, Ewend MG, Sasaki-Adams D, Lee CB, Collichio FA, Fried D, Marks LB, Chera BS (Temmuz 2017). "Melanom beyin metastazları için stereotaktik radyoterapiyi takiben radyasyon nekrozu insidansı: immünoterapinin potansiyel etkisi". Antikanser İlaçlar. 28 (6): 669–675. doi:10.1097 / CAD.0000000000000497. PMID 28368903. S2CID 3560210.
- ^ Régis J, Bartolomei F, Hayashi M, Chauvel P (2002). "Mezial temporal lob epilepsisinde radyocerrahinin rolü". Zentralbl. Neurochir. 63 (3): 101–5. doi:10.1055 / s-2002-35824. PMID 12457334.
- ^ Kwon Y, Whang CJ (1995). "Stereotaktik Gamma Knife radyocerrahi distoni tedavisi için". Stereotact Funct Neurosurg. 64 Özel Sayı 1: 222–7. doi:10.1159/000098782. PMID 8584831.
- ^ Donnet A, Valade D, Régis J (Şubat 2005). "Dirençli küme baş ağrısı için gama bıçağı tedavisi: ileriye dönük açık çalışma". J. Neurol. Neurosurg. Psikiyatri. 76 (2): 218–21. doi:10.1136 / jnnp.2004.041202. PMC 1739520. PMID 15654036.
- ^ Herman JM, Petit JH, Amin P, Kwok Y, Dutta PR, Chin LS (Mayıs 2004). "Dirençli veya tekrarlayan trigeminal nevralji için gama bıçak radyocerrahisini tekrarlayın: tedavi sonuçları ve yaşam kalitesi değerlendirmesi". Int. J. Radiat. Oncol. Biol. Phys. 59 (1): 112–6. doi:10.1016 / j.ijrobp.2003.10.041. PMID 15093906.
- ^ Chin LS, Lazio BE, Biggins T, Amin P (Mayıs 2000). "Gamma knife radyocerrahisini takiben akut komplikasyonlar nadirdir". Surg Neurol. 53 (5): 498–502, tartışma 502. doi:10.1016 / S0090-3019 (00) 00219-6. PMID 10874151.
- ^ Stafford SL, Pollock BE, Foote RL ve diğerleri. (Kasım 2001). "Meningioma radyocerrahi: tümör kontrolü, sonuçları ve 190 ardışık hasta arasında komplikasyonlar". Nöroşirürji. 49 (5): 1029–37, tartışma 1037–8. doi:10.1097/00006123-200111000-00001. PMID 11846894. S2CID 13646182.
- ^ Cho DY, Tsao M, Lee WY, Chang CS (Mayıs 2006). "İyi huylu kafa tabanı tümörleri için açık cerrahi ve gama bıçaklı radyocerrahinin sosyoekonomik maliyetleri". Nöroşirürji. 58 (5): 866–73, tartışma 866–73. doi:10.1227 / 01.NEU.0000209892.42585.9B. PMID 16639320. S2CID 38660074.
- ^ Schweikard Achim; Shiomi Hiroya; Adler John (2004). "Radyocerrahide solunum takibi". Tıp fiziği. 31 (10): 2738–2741. Bibcode:2004MedPh..31.2738S. doi:10.1118/1.1774132. PMID 15543778. S2CID 22656004.
- ^ Roxanne Nelson (30 Ocak 2013). "Proton-Işın Radyoterapi Kalanlarının Belirsizliği". Medscape. Alındı 22 Mart 2017.
Dış bağlantılar
- Solunumla Hareket Eden Tümörleri Tedavi Etmek Radyocerrahiden hareketli hedeflere kitap (Temmuz 2007)
- Şekilli Işın Radyocerrahisi Çok kanatlı kolimasyon kullanarak LINAC tabanlı radyocerrahi hakkında rezervasyon yapın (Mart 2011)
