Enfeksiyon - Infection - Wikipedia
| Enfeksiyon | |
|---|---|
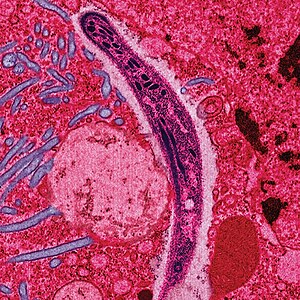 | |
| Yanlış renkli elektron mikrografı gösteren sıtma sporozoit içinden geçmek midgut epitel bir sıçan | |
| Uzmanlık | Bulaşıcı hastalık |
| Nedenleri | bakteriyel, viral, parazit, mantar |
Bir enfeksiyon bir organizmanın vücudunun istilasıdır Dokular tarafından hastalığa neden olan ajanlar, bunların çarpımı ve tepkisi ev sahibi bulaşıcı ajanlara dokular ve toksinler Üretirler.[1][2] Bir bulaşıcı hastalıkolarak da bilinir bulaşıcı hastalık veya Bulaşıcı hastalık, bir hastalık enfeksiyondan kaynaklanan.
Enfeksiyonlara bulaşıcı ajanlar neden olur (patojenler ) dahil olmak üzere:
- Virüsler ve gibi ilgili ajanlar viroidler (HIV, Rinovirüs, Lyssavirüsler gibi Kuduz virüsü, Ebolavirüs ve Şiddetli akut solunum sendromu koronavirüs 2 )
- Bakteri (Tüberküloz, Staphylococcus aureus, Escherichia coli, Clostridium botulinum, ve Salmonella spp.)
- Mantarlar, ayrıca şu şekilde alt sınıflandırılır:
- Ascomycota gibi mayalar dahil Candida filamentli mantarlar, örneğin Aspergillus, Pnömosist türler ve dermatofitler, insanlarda deri ve diğer yüzeysel yapıların enfeksiyonuna neden olan bir grup organizma.[3]
- Basidiomycota insan patojenik cins dahil Cryptococcus.[4]
- Prionlar (toksin salgılamasalar da)
- Parazitler, genellikle aşağıdakilere ayrılır:[5]
- Tek hücreli organizmalar (ör. sıtma, Toksoplazma, Babesia )
- Makroparazitler[6] (solucanlar veya helmintler ) dahil olmak üzere nematodlar gibi parazit yuvarlak kurtlar ve kıl kurtları, tenyalar (sestodlar) ve flukes (trematodlar, örneğin şistozomiyaz )
- Eklembacaklılar gibi keneler, akarlar, pireler, ve bit, kavramsal olarak enfeksiyonlara benzeyen insan hastalığına da neden olabilir, ancak bu makroparazitler tarafından bir insan veya hayvan vücudunun istilasına genellikle istila. (Neden olduğu hastalıklar helmintler Aynı zamanda makroparazitler olan, bazen istila olarak da adlandırılır, ancak bazen enfeksiyon olarak adlandırılır.)
Ev sahipleri enfeksiyonlarla savaşabilir. bağışıklık sistemi. Memeli ev sahipleri enfeksiyonlara bir doğuştan yanıt, genellikle içeren iltihap ve ardından bir uyarlanabilir tepki.[7]
Özel ilaçlar enfeksiyonları tedavi etmek için kullanılanlar arasında antibiyotikler, antiviraller, antifungaller, antiprotozoaller, ve antihelminthics. Bulaşıcı hastalıklar 2013 yılında 9,2 milyon ölümle sonuçlandı (tüm ölümlerin yaklaşık% 17'si).[8] Şubesi ilaç enfeksiyonlara odaklanan, bulaşıcı hastalık.[9]
Sınıflandırma
Subklinik ve klinik (gizli ve görünür)
Semptomatik enfeksiyonlar bariz ve klinikaktif olan ancak belirgin semptomlar üretmeyen bir enfeksiyona görünmeyen sessiz, belirti göstermemiş veya gizli. Aktif olmayan veya uykuda olan bir enfeksiyona gizli enfeksiyon.[10] Gizli bir bakteriyel enfeksiyon örneği gizli tüberküloz. Bazı viral enfeksiyonlar da gizli olabilir. gizli viral enfeksiyonlar bunlardan herhangi biri Herpesviridae aile.[11]
Kelime enfeksiyon Yapabilmek belirtmek belirli bir patojenin varlığı (ne kadar az olursa olsun) ama aynı zamanda sıklıkla duyu ima etmek klinik olarak belirgin enfeksiyon (başka bir deyişle, bulaşıcı hastalık vakası).[12] Bu gerçek bazen bazılarını yaratır belirsizlik veya bazılarını sorar kullanım tartışma; bunun üstesinden gelmek için yaygındır sağlık profesyonelleri hakkında konuşmak kolonizasyon (ziyade enfeksiyon) bazı patojenlerin mevcut olduğunu, ancak klinik olarak belirgin enfeksiyon (hastalık yok) olmadığını kastettiklerinde.
Enfeksiyonları tanımlamak için farklı terimler kullanılır. İlki akut bir enfeksiyondur. Akut enfeksiyon, semptomların hızla geliştiği enfeksiyondur; seyri hızlı veya uzun olabilir.[13] Sonraki kronik bir enfeksiyondur. Kronik bir enfeksiyon, semptomların yavaş yavaş, haftalarca veya aylarca geliştiği ve yavaş çözüldüğü zamandır.[14] Subakut enfeksiyon, semptomların gelişmesinin akut enfeksiyondan daha uzun sürdüğü ancak kronik bir enfeksiyondan daha hızlı ortaya çıktığı bir enfeksiyondur. Gizli enfeksiyon, akut bir ataktan sonra ortaya çıkabilen bir enfeksiyon türüdür; organizma mevcuttur ancak semptomlar yoktur; zaman sonra hastalık yeniden ortaya çıkabilir. Fokal enfeksiyon, organizmaların kan dolaşımı yoluyla vücudun başka bir bölgesine gittiği ilk enfeksiyon bölgesi olarak tanımlanır.[15]
Birincil ve fırsatçı
Birçok çeşit arasında mikroorganizmalar sağlıklı bireylerde nispeten az sayıda hastalık neden olur.[16] Bulaşıcı hastalık, bu birkaç kişi arasındaki etkileşimden kaynaklanır. patojenler ve bulaştıkları konakçıların savunmaları. Herhangi bir patojenden kaynaklanan hastalığın görünümü ve ciddiyeti, bu patojenin konakçıya zarar verme kabiliyetinin yanı sıra konağın patojene direnme kabiliyetine bağlıdır. Bununla birlikte, bir konağın bağışıklık sistemi, enfeksiyonu kontrol etme girişiminde konakçının kendisine de zarar verebilir. Bu nedenle klinisyenler, bulaşıcı mikroorganizmaları veya mikropları konak savunmalarının durumuna göre sınıflandırır - birincil patojenler veya olarak fırsatçı patojenler:
Birincil patojenler
Birincil patojenler, normal, sağlıklı konukçu içinde varlıklarının veya faaliyetlerinin bir sonucu olarak hastalığa neden olurlar. şiddet (neden oldukları hastalığın ciddiyeti) kısmen, üreme ve yayılma ihtiyaçlarının gerekli bir sonucudur. İnsanların en yaygın birincil patojenlerinin birçoğu yalnızca insanları enfekte eder, ancak birçok ciddi hastalığa çevreden edinilen veya insan olmayan konakçıları enfekte eden organizmalar neden olur.
Fırsatçı patojenler
Fırsatçı patojenler, dirençli bir konakçıda bulaşıcı bir hastalığa neden olabilir (immün yetmezlik ) veya vücudun içine alışılmadık erişimleri varsa (örneğin, travma ). Fırsatçı enfeksiyon ev sahibi ile normalde temas halinde olan mikroplardan kaynaklanabilir, örneğin patojenik bakteri veya içindeki mantarlar gastrointestinal ya da üst solunum yolları ve diğer konakçılardan elde edilen (aksi takdirde zararsız) mikroplardan da kaynaklanabilirler (örn. Clostridium difficile kolit ) veya bir sonucu olarak çevreden travmatik giriş (olduğu gibi cerrahi yara enfeksiyonları veya bileşik kırıklar ). Fırsatçı bir hastalık, konağın savunmasının bozulmasını gerektirir ve bu, genetik kusurlar (gibi Kronik granülomatöz hastalık ), maruz kalmak antimikrobiyal uyuşturucu veya bağışıklığı baskılayıcı kimyasallar (aşağıdaki gibi meydana gelebilir) zehirlenme veya kanser kemoterapi ), maruz kalmak iyonlaştırıcı radyasyon veya immünosupresif aktiviteye sahip bulaşıcı bir hastalığın sonucu olarak (örn. kızamık, sıtma veya HIV hastalığı ). Birincil patojenler ayrıca, bağışıklık yetersizliği olan bir konakçıda normalde meydana gelenden daha düşük dirençli bir konakçıda daha ciddi hastalığa neden olabilir.[17]
İkincil enfeksiyon
Birincil enfeksiyon pratik olarak şu şekilde görülebilir: ana neden bir bireyin mevcut sağlık problemi için ikincil bir enfeksiyon, sekel veya karışıklık bu kök nedenden. Örneğin, akciğer tüberkülozu genellikle birincil enfeksiyondur, ancak yalnızca yanmak veya penetran travma (temel neden) derin dokulara alışılmadık erişime izin verilen ikincil bir enfeksiyondur. Birincil patojenler genellikle birincil enfeksiyona neden olur ve ayrıca sıklıkla ikincil enfeksiyona neden olur. Fırsatçı enfeksiyonlar genellikle ikincil enfeksiyonlar olarak görülür (çünkü bağışıklık yetersizliği veya yaralanma predispozan faktördü).
Diğer enfeksiyon türleri
Diğer enfeksiyon türleri karışık, iyatrojenik, nozokomiyal ve toplum kaynaklı enfeksiyondan oluşur. Karışık enfeksiyon, iki veya daha fazla patojenin neden olduğu bir enfeksiyondur. Bunun bir örneği, Bacteroides fragilis ve Escherichia coli'nin neden olduğu Apandisittir. İkincisi, iyatrojenik bir enfeksiyondur. Bu tür enfeksiyon, bir sağlık çalışanından hastaya bulaşan enfeksiyondur. Bir nozokomiyal enfeksiyon, bir sağlık bakımı ortamında da ortaya çıkan bir enfeksiyondur. Hastane enfeksiyonları, hastanede kalış sırasında ortaya çıkan enfeksiyonlardır. Son olarak, toplum tarafından edinilen bir enfeksiyon, enfeksiyonun bütün bir topluluktan elde edildiği bir enfeksiyondur.[15]
Bulaşıcı ya da değil
Belirli bir hastalığın bulaşıcı olduğunu kanıtlamanın bir yolu, Koch'un postülatları (ilk öneren Robert Koch ), ilk olarak bunu gerektiren bulaşıcı etken sadece hastalığı olan ve sağlıklı kontrollerde olmayan hastalarda tanımlanabilir olması ve ikincisi, enfeksiyon etkenine yakalanan hastalarda da hastalığı geliştirmesi. Bu postülatlar ilk olarak keşifte kullanılmıştır. Mikobakteriler türler neden olur tüberküloz.
Bununla birlikte, Koch'un önermeleri genellikle modern uygulamada etik nedenlerle test edilemez. Bunları kanıtlamak için sağlıklı bir bireyin deneysel enfeksiyonu patojen saf bir kültür olarak üretilmiştir. Tersine, açık bir şekilde bulaşıcı hastalıklar bile her zaman bulaşıcı kriterleri karşılamamaktadır; Örneğin, Treponema pallidum nedensel spiroket nın-nin frengi, olamaz kültürlü laboratuvar ortamında - bununla birlikte organizma tavşanda kültürlenebilir testisler. Saf bir kültürün, plaka kültüründen türetilen mikroplardan türetildiği zamana kıyasla, konakçı olarak hizmet veren bir hayvan kaynağından geldiği daha az açıktır.
Epidemiyoloji veya hastalığın kim, neden ve nerede ortaya çıktığı ve çeşitli popülasyonların bir hastalığa sahip olup olmadığını neyin belirlediğinin incelenmesi ve analizi, bulaşıcı hastalıkları anlamak için kullanılan diğer önemli bir araçtır. Epidemiyologlar, belirli yaş gruplarının daha fazla veya daha az enfeksiyon oranına sahip olup olmadığı gibi bir popülasyon içindeki gruplar arasındaki farklılıkları belirleyebilir; farklı mahallelerde yaşayan grupların enfekte olma olasılığının daha yüksek olup olmadığı; ve cinsiyet ve ırk gibi diğer faktörlere göre. Araştırmacılar ayrıca bir hastalık olup olmadığını değerlendirebilir salgın sporadik veya ara sıra meydana gelen bir olay; endemik, bir bölgede meydana gelen düzenli vakaların sabit düzeyde olduğu; epidemi hızlı bir şekilde ortaya çıkan ve bir bölgede alışılmadık derecede yüksek sayıda vaka ile; veya pandemi, küresel bir salgın olan. Bulaşıcı hastalığın nedeni bilinmiyorsa, epidemiyoloji enfeksiyon kaynaklarının izlenmesine yardımcı olmak için kullanılabilir.
Bulaşıcılık
Bulaşıcı hastalıklar, hasta bir kişiyle veya salgılarıyla temas yoluyla kolayca bulaştıklarında bazen bulaşıcı hastalıklar olarak adlandırılır (örn. grip ). Bu nedenle, bulaşıcı bir hastalık, özellikle bulaşıcı olan veya kolayca bulaşan bulaşıcı hastalığın bir alt kümesidir. Vektör bulaşması veya cinsel yolla bulaşma gibi daha özel enfeksiyon yollarına sahip diğer bulaşıcı, bulaşıcı veya bulaşıcı hastalık türleri genellikle "bulaşıcı" olarak kabul edilmez ve genellikle tıbbi izolasyon gerektirmez (bazen genel olarak karantina ) kurbanların. Bununla birlikte, "bulaşıcı" ve "bulaşıcı hastalık" (kolay bulaşıcı hastalık) kelimesinin bu özel çağrışımına her zaman popüler kullanımda saygı duyulmamaktadır. Bulaşıcı hastalıklar genellikle doğrudan temas yoluyla insandan insana bulaşır. Temas türleri kişiden kişiye ve damlacık yayılır. Hava yoluyla bulaşma, kontamine nesneler, yiyecek ve içme suyu, hayvan teması, hayvan rezervuarları, böcek ısırıkları ve çevresel rezervuarlar gibi dolaylı temas, bulaşıcı hastalıkların bulaşmasının başka bir yoludur.[18]
Anatomik konuma göre
Enfeksiyonlar anatomik konuma göre sınıflandırılabilir veya organ sistemi dahil olmak üzere enfekte:
- İdrar yolu enfeksiyonu
- Deri enfeksiyonu
- Solunum yolu enfeksiyonu
- Odontojenik enfeksiyon (bir enfeksiyondan kaynaklanan bir enfeksiyon diş veya yakın çevredeki dokularda)
- Vajinal enfeksiyonlar
- İntraamniyotik enfeksiyon
Ek olarak, iltihap enfeksiyonun en yaygın neden olduğu yer Zatürre, menenjit ve salpenjit.
Belirti ve bulgular
Bir enfeksiyonun semptomları, hastalığın türüne bağlıdır. Bazı enfeksiyon belirtileri genel olarak tüm vücudu etkiler, örneğin yorgunluk iştahsızlık, kilo kaybı ateşler, gece terlemeleri, titreme, ağrı ve sızılar. Diğerleri cilt gibi bireysel vücut kısımlarına özeldir. döküntüler, öksürme veya a burun akması.
Bazı durumlarda bulaşıcı hastalıklar olabilir asemptomatik belirli bir ev sahibi içindeki kurslarının çoğu veya tamamı için. İkinci durumda, hastalık yalnızca asemptomatik bir taşıyıcıyla temastan sonra ikincil olarak hastalanan konakçılarda bir "hastalık" (tanım gereği bir hastalık anlamına gelir) olarak tanımlanabilir. Bazı enfeksiyonlar konakçıda hastalığa neden olmadığından, enfeksiyon bulaşıcı bir hastalıkla eşanlamlı değildir.[17]
Bakteriyel veya viral
Bakteriyel ve viral enfeksiyonların her ikisi de aynı tür semptomlara neden olabileceğinden, belirli bir enfeksiyonun nedeninin hangisi olduğunu ayırt etmek zor olabilir.[19] İkisini ayırt etmek önemlidir, çünkü viral enfeksiyonlar tedavi edilemez. antibiyotikler oysa bakteriyel enfeksiyonlar olabilir.[20]
| Karakteristik | Viral enfeksiyon | Bakteriyel enfeksiyon |
|---|---|---|
| Tipik semptomlar | Genelde viral enfeksiyonlar sistemiktir. Bu, vücudun birçok farklı bölümünü veya aynı anda birden fazla vücut sistemini içerdikleri anlamına gelir; örn. burun akıntısı, sinüs tıkanıklığı, öksürük, vücut ağrıları vb. Bazen viral olduğu gibi lokal olabilirler. konjunktivit veya "pembe göz" ve uçuk. Herpes gibi sadece birkaç viral enfeksiyon ağrılıdır. Viral enfeksiyonların ağrısı genellikle kaşıntılı veya yanma olarak tanımlanır.[19] | Bakteriyel enfeksiyonun klasik semptomları lokalize kızarıklık, ısı, şişme ve ağrıdır. Bakteriyel bir enfeksiyonun ayırt edici özelliklerinden biri, vücudun belirli bir bölümünde bulunan lokal ağrıdır. Örneğin, bir kesik oluşursa ve bakteri ile enfekte olursa, enfeksiyon bölgesinde ağrı oluşur. Bakteriyel boğaz ağrısı genellikle boğazın bir tarafında daha fazla ağrı ile karakterizedir. Bir kulak enfeksiyonu Ağrı sadece bir kulakta meydana gelirse bakteriyel olarak teşhis edilme olasılığı daha yüksektir.[19] İrin ve süt rengi sıvı üreten bir kesik büyük olasılıkla enfekte.[açıklama gerekli ][21] |
| Sebep olmak | Patojenik virüsler | Patojenik bakteri |
Patofizyoloji
Enfeksiyonlar için geçerli olan genel bir olaylar zinciri vardır.[22] Olaylar zinciri, bulaşıcı ajan, rezervuar, duyarlı bir konağa girme, çıkış ve yeni konaklara aktarımı içeren birkaç adım içerir. Bir enfeksiyonun gelişmesi için bağlantıların her biri kronolojik bir sırayla mevcut olmalıdır. Bu adımları anlamak, sağlık çalışanlarının enfeksiyonu hedeflemesine ve ilk etapta ortaya çıkmasını önlemesine yardımcı olur.[23]
Kolonizasyon

Enfeksiyon, bir organizma vücuda başarıyla girdiğinde, büyüdüğünde ve çoğaldığında başlar. Buna kolonizasyon denir. Çoğu insan kolayca enfekte olmaz. Bağışıklık sistemi zayıflamış veya zayıflamış olanlar, kronik veya kalıcı enfeksiyonlara karşı artan bir duyarlılığa sahiptir. Bastırılmış bireyler bağışıklık sistemi özellikle duyarlı fırsatçı enfeksiyonlar. Ev sahibine giriş konak-patojen arayüzü, genellikle mukoza gibi deliklerde ağız boşluğu açık yaralardan burun, gözler, cinsel organ, anüs veya mikrop girebilir. İlk giriş yerinde birkaç organizma büyüyebilirken, çoğu göç eder ve farklı organlarda sistemik enfeksiyona neden olur. Bazı patojenler konakçı hücrelerde (hücre içi) büyürken diğerleri vücut sıvılarında serbestçe büyür.
Yara kolonizasyon, enfekte yaralarda replike edici organizmalar varken doku yaralandığında yara içindeki replike olmayan mikroorganizmaları ifade eder.[24] Herşey Çok hücreli organizmalar bir dereceye kadar dış organizmalar tarafından kolonize edilir ve bunların büyük çoğunluğu, karşılıklı veya ortak ev sahibi ile ilişki. İlkine bir örnek, anaerobik bakteri kolonileşen türler memeli kolon ve ikincisinin bir örneği, çeşitli türlerdir. stafilokok var olan Insan derisi. Bu kolonizasyonların hiçbiri enfeksiyon olarak kabul edilmez. Bir enfeksiyon ile kolonizasyon arasındaki fark genellikle sadece bir durumdur. Patojenik olmayan organizmalar, belirli koşullar altında ve hatta en çok öldürücü organizmanın tehlikeli bir enfeksiyona neden olması için belirli koşullar gerektirir. Bazı kolonize bakteriler, örneğin Corynebacteria sp. ve viridans streptococci, patojenik bakterilerin yapışmasını ve kolonizasyonunu önler ve böylece konakçı ile simbiyotik bir ilişki kurar, enfeksiyonu ve hızlanmayı önler yara iyileşmesi.
Bir konakçının bir patojen tarafından aşılanmasının sonucuna dahil olan değişkenler ve nihai sonuç şunları içerir:
- giriş yolu patojen ve kazandığı ana bölgelere erişim
- içsel şiddet belirli organizmanın
- ilk aşılayıcının miktarı veya yükü
- bağışıklık kolonize edilen konağın durumu
Örnek olarak, birkaç stafilokok türler ciltte zararsız kalır, ancak normal olarak mevcut olduklarında steril bir kapsül gibi boşluk bağlantı ya da periton direnç göstermeden çoğalın ve zarar verin.
İlginç bir gerçek gaz kromatografisi - kütle spektrometrisi, 16S ribozomal RNA analiz Omics ve diğer ileri teknolojiler son on yıllarda insanlara daha belirgin hale getirdi, mikrobiyal kolonizasyon, insanların neredeyse olduğunu düşündüğü ortamlarda bile çok yaygın. steril. Bakteriyel kolonizasyon olması normal olduğundan, hangi kronik yaraların enfekte olarak sınıflandırılabileceğini ve ne kadar ilerleme riski olduğunu bilmek zordur. Klinik uygulamada görülen çok sayıda yara olmasına rağmen, değerlendirilen semptomlar ve belirtiler için sınırlı kalitede veri vardır. Journal of the American Medical Association'ın "Rasyonel Klinik Muayene Serisi" nde kronik yaraların gözden geçirilmesi, enfeksiyonun bir göstergesi olarak artan ağrının önemini ölçtü.[28] İnceleme, en yararlı bulgunun ağrı düzeyindeki bir artış olduğunu [olasılık oranı (LR) aralığı, 11-20], enfeksiyonu çok daha olası hale getirdiğini, ancak ağrı yokluğunun (negatif olasılık oranı aralığı, 0.64-0.88) olduğunu gösterdi. enfeksiyonu dışlamaz (özet LR 0.64-0.88).
Hastalık
Hastalık konakçının koruyucu bağışıklık mekanizmaları tehlikeye atılırsa ve organizma konakçıya zarar verirse ortaya çıkabilir. Mikroorganizmalar çeşitli toksinler veya yıkıcı enzimler salgılayarak doku hasarına neden olabilir. Örneğin, Klostridium tetani kasları felç eden bir toksin salgılar ve stafilokok şok ve sepsis üreten toksinleri serbest bırakır. Tüm bulaşıcı ajanlar tüm konakçılarda hastalığa neden olmaz. Örneğin, enfeksiyon kapmış kişilerin% 5'inden azı çocuk felci hastalık geliştirmek.[29] Öte yandan, bazı bulaşıcı ajanlar oldukça öldürücüdür. Prion neden olan Deli dana hastalığı ve Creutzfeldt-Jakob hastalığı her zaman enfeksiyon kapmış tüm hayvanları ve insanları öldürür.
Kalıcı enfeksiyonlar, vücut ilk enfeksiyondan sonra organizmayı temizleyemediği için ortaya çıkar. Kalıcı enfeksiyonlar, bulaşıcı organizmanın sürekli mevcudiyeti ile karakterize edilir, genellikle aktif enfeksiyonun ara sıra tekrarlayan nüksleri ile gizli enfeksiyon gibi. Vücudun farklı hücrelerine bulaşarak kalıcı bir enfeksiyonu sürdürebilen bazı virüsler vardır. Bir kez edinilen bazı virüsler asla bedeni terk etmez. Tipik bir örnek, sinirlerde saklanma ve belirli koşullar ortaya çıktığında yeniden aktive olma eğiliminde olan herpes virüsüdür.
Kalıcı enfeksiyonlar her yıl dünya çapında milyonlarca ölüme neden oluyor.[30] Parazitlerin neden olduğu kronik enfeksiyonlar, pek çok az gelişmiş ülkede yüksek morbidite ve mortaliteden sorumludur.
Aktarma

Enfekte eden organizmaların hayatta kalması ve enfeksiyon döngüsünü diğer konakçılarda tekrar etmesi için, onlar (veya soyları) mevcut bir rezervuarı terk etmeli ve başka bir yerde enfeksiyona neden olmalıdır. Enfeksiyon bulaşması birçok potansiyel yolla gerçekleşebilir:
- Damlacık temasıolarak da bilinir solunum yoluve ortaya çıkan enfeksiyon olarak adlandırılabilir hava kaynaklı hastalık. Enfekte bir kişi başka bir kişiye öksürür veya hapşırırsa, ılık, nemli damlacıklar içinde asılı duran mikroorganizmalar, burun, ağız veya göz yüzeylerinden vücuda girebilir.
- Fekal-oral geçiş, burada gıda maddeleri veya su kontamine olur (insanlar yemek hazırlamadan önce ellerini yıkamazlar veya arıtılmamış lağım içme suyu kaynağına bırakılırsa) ve bunları yiyip içen insanlar enfekte olur. Fekal-oral yoldan bulaşan yaygın patojenler şunları içerir: Vibrio cholerae, Giardia Türler, rotavirüsler, Entameba histolytica, Escherichia coli, ve bant kurtları.[31] Bu patojenlerin çoğu neden olur gastroenterit.
- Cinsel yolla bulaşmaortaya çıkan hastalık çağrılırken cinsel yolla bulaşan hastalık
- Oral iletimÖncelikle oral yollarla bulaşan hastalıklar, doğrudan sözlü temas yoluyla yakalanabilir. öpüşmek veya bir bardak veya sigara paylaşmak gibi dolaylı temas yoluyla.
- Doğrudan temasla iletimDoğrudan temasla bulaşan bazı hastalıklar şunlardır: atlet ayağı, impetigo ve siğiller
- Araç şanzımanı, cansız bir rezervuarla bulaşma (yiyecek, su, toprak).[32]
- Dikey iletimdoğrudan anneden embriyo, cenin ya da bebek sırasında gebelik veya doğum. Bir sonucu olarak ortaya çıkabilir önceden var olan enfeksiyon veya hamilelik sırasında edinilen biri.
- İyatrojenik aktarmatıbbi prosedürler nedeniyle enjeksiyon veya transplantasyon enfekte malzeme.
- Vektör kaynaklı iletimtarafından iletildi vektör, hangisi bir organizma bu sebep olmaz hastalık kendisi ancak enfeksiyonu ileterek iletir patojenler birinden ev sahibi başka bir.[33]
Aralarındaki ilişki virülans ve bulaşıcılık karmaşıktır; bir hastalık hızla ölümcül olursa, konakçı, mikrop başka bir konağa geçmeden önce ölebilir.
Teşhis
Bu bölüm için ek alıntılara ihtiyaç var doğrulama. (Aralık 2019) (Bu şablon mesajını nasıl ve ne zaman kaldıracağınızı öğrenin) |
Enfeksiyöz hastalığın teşhisi bazen bir enfeksiyöz ajanın doğrudan veya dolaylı olarak tanımlanmasını içerir.[34] Uygulamada, çoğu küçük bulaşıcı hastalık, örneğin siğiller, kutanöz apseler, solunum sistemi enfeksiyonlar ve ishalli hastalıklar klinik sunumlarıyla teşhis edilir ve spesifik nedensel ajan bilgisi olmadan tedavi edilir. Hastalığın nedeni ile ilgili sonuçlar, bir hastanın belirli bir ajanla temasa geçme olasılığına, bir toplulukta bir mikrop varlığına ve diğer epidemiyolojik hususlara dayanmaktadır. Yeterli çaba gösterildiğinde, bilinen tüm bulaşıcı ajanlar spesifik olarak tanımlanabilir. Bununla birlikte, tanımlamanın faydaları, genellikle belirli bir tedavi olmadığından, nedeni açık olduğundan veya bir enfeksiyonun sonucu olduğundan, genellikle maliyetten büyük ölçüde ağır basmaktadır. iyi huylu.
Bulaşıcı hastalık teşhisi neredeyse her zaman tıbbi geçmiş ve fiziksel muayene. Daha ayrıntılı tanımlama teknikleri, bir hastadan izole edilen enfeksiyöz ajanların kültürünü içerir. Kültür, mikroskobik özelliklerini inceleyerek, patojenler tarafından üretilen maddelerin varlığını tespit ederek ve bir organizmayı genotipiyle doğrudan tanımlayarak bulaşıcı organizmaların tanımlanmasına izin verir. Diğer teknikler (örneğin X ışınları, CAT taramaları, PET taramaları veya NMR ) bulaşıcı bir ajanın büyümesinden kaynaklanan dahili anormalliklerin görüntülerini üretmek için kullanılır. Görüntüler, örneğin bir kemiğin tespit edilmesinde faydalıdır. apse veya a süngerimsi ensefalopati tarafından üretildi Prion.
Semptomatik teşhis
Teşhis, bulaşıcı bir hastalığı olan herhangi bir kişide semptomların ortaya çıkmasıyla desteklenir, ancak şüpheyi doğrulamak için genellikle ek teşhis tekniklerine ihtiyaç duyar. Bazı belirtiler spesifik olarak karakteristiktir ve bir hastalığın göstergesidir ve patognomonik işaretler; ama bunlar nadirdir. Tüm enfeksiyonlar semptomatik değildir.[35]
Çocuklarda varlığı siyanoz hızlı nefes alma, zayıf periferik perfüzyon veya peteşiyal döküntü 5 kattan fazla ciddi enfeksiyon riskini artırır.[36] Diğer önemli göstergeler arasında ebeveyn endişesi, klinik içgüdü ve 40 ° C'den yüksek sıcaklık bulunur.[36]
Mikrobiyal kültür

Mikrobiyolojik kültür bulaşıcı hastalıkları teşhis etmek için kullanılan temel bir araçtır. Mikrobiyal bir kültürde büyüme ortamı belirli bir aracı için sağlanır. Potansiyel olarak hastalıklı doku veya sıvıdan alınan bir numune daha sonra bu ortam içinde büyüyebilen bir enfeksiyöz ajanın varlığı açısından test edilir. Çoğu patojenik bakteri, besinlerle kolayca büyür agar, büyümesi için gerekli karbonhidratları ve proteinleri sağlayan bir katı ortam formu bakteri bol miktarda su ile birlikte. Tek bir bakteri, plakanın yüzeyinde a denilen görünür bir höyüğe dönüşecektir. koloni, diğer kolonilerden ayrılabilen veya bir "çim" halinde birlikte eritilebilen. Bir koloninin boyutu, rengi, şekli ve şekli bakteri türünün karakteristiğidir, spesifik genetik yapısı ( Gerginlik ) ve büyümesini destekleyen çevre. Tanımlamaya yardımcı olmak için genellikle diğer bileşenler plakaya eklenir. Plakalar, bazı bakterilerin büyümesine izin verirken diğerlerinin büyümesine izin veren veya bazı bakterilere yanıt olarak renk değiştiren ve diğerlerine yanıt vermeyen maddeler içerebilir. Bunlar gibi bakteriyolojik plakalar, bulaşıcı bakterinin klinik tanımlanmasında yaygın olarak kullanılmaktadır. Mikrobiyal kültür ayrıca virüsler: ortam, bu durumda, virüsün enfekte edebileceği ve sonra değiştirebileceği veya öldürebileceği kültürde yetiştirilen hücrelerdir. Viral tanımlama durumunda, ölü hücrelerin bir bölgesi viral büyümeden kaynaklanır ve "plak" olarak adlandırılır. Ökaryotik parazitler belirli bir ajanı tanımlamanın bir yolu olarak kültürde de büyütülebilir.
Uygun plaka kültür tekniklerinin yokluğunda, bazı mikroplar canlı hayvanlarda kültür gerektirir. Bakteriler, örneğin Mycobacterium leprae ve Treponema pallidum Hayvanlarda yetiştirilebilir, ancak serolojik ve mikroskobik teknikler canlı hayvanların kullanımını gereksiz kılar. Virüsler ayrıca genellikle kültür veya hayvanlarda büyümeye alternatifler kullanılarak tanımlanır. Bazı virüsler içinde büyümüş olabilir embriyonlu yumurtalar. Başka bir yararlı tanımlama yöntemi, Xenodiagnosis veya bulaşıcı bir ajanın büyümesini desteklemek için bir vektörün kullanılmasıdır. Chagas hastalığı en önemli örnektir, çünkü nedensel ajanın varlığını doğrudan göstermek zordur, Trypanosoma cruzi bir hastada, bu nedenle kesin olarak tanı koymayı zorlaştırır. Bu durumda, ksenodiyagnoz, vektör Chagas ajanı T. cruzi, enfekte olmamış tritomin Enfekte olduğundan şüphelenilen bir kişiden kan yemeğini alan böcek. Hata daha sonra büyümesi için incelenir T. cruzi bağırsakları içinde.
Mikroskopi
Bulaşıcı hastalık tanısında bir diğer temel araç da mikroskopi. Yukarıda tartışılan hemen hemen tüm kültür teknikleri, bir noktada, bulaşıcı ajanın kesin tanımlanması için mikroskobik incelemeye dayanır. Mikroskopi, bileşik gibi basit aletlerle yapılabilir. ışık mikroskobu veya çok karmaşık araçlarla elektron mikroskobu. Hastalardan alınan örnekler doğrudan ışık mikroskobu altında görüntülenebilir ve çoğu zaman hızlı bir şekilde tanımlamaya yol açabilir. Mikroskopi genellikle aşağıdakilerle birlikte kullanılır: biyokimyasal boyama teknikler ve birlikte kullanıldığında son derece spesifik hale getirilebilir antikor temelli teknikler. Örneğin, kullanımı antikorlar yapay olarak yapıldı floresan (floresan etiketli antikorlar), belirli bir bölgeye bağlanmak ve bunu tanımlamak için yönlendirilebilir. antijenler bir patojen üzerinde mevcut. Bir floresan mikroskobu daha sonra klinik numuneler veya kültürlenmiş hücreler içinde içselleştirilmiş antijenlere bağlanan floresan etiketli antikorları saptamak için kullanılır. Bu teknik, ışık mikroskobunun bir virüsü doğrudan tanımlayamadığı viral hastalıkların teşhisinde özellikle yararlıdır.
Diğer mikroskobik prosedürler de bulaşıcı ajanların tanımlanmasına yardımcı olabilir. Hemen hemen tüm hücreler bir dizi temel maddeyle kolayca boyanır boyalar nedeniyle elektrostatik negatif yüklü hücresel moleküller ile boya üzerindeki pozitif yük arasındaki çekim. Bir hücre normalde mikroskop altında şeffaftır ve bir leke kullanmak hücrenin arka planıyla kontrastını artırır. Bir hücreyi bir boya ile boyama Giemsa leke veya kristal Menekşe bir mikroskobun boyutunu, şeklini, iç ve dış bileşenlerini ve diğer hücrelerle olan ilişkilerini açıklamasına izin verir. Bakterilerin farklı boyama prosedürlerine verdiği yanıt, taksonomik sınıflandırma mikropların da. İki yöntem, Gram boyama ve aside dirençli leke, bakterileri sınıflandırmak ve hastalık teşhisi için kullanılan standart yaklaşımlardır. Gram boyası bakteri gruplarını tanımlar Firmicutes ve Aktinobakteriler her ikisi de birçok önemli insan patojeni içerir. Aside dirençli boyama prosedürü, Aktinobakteriyel cinsleri tanımlar Mikobakteri ve Nocardia.
Biyokimyasal testler
Enfeksiyöz ajanların tanımlanmasında kullanılan biyokimyasal testler; metabolik veya enzimatik belirli bir bulaşıcı ajanın özelliği olan ürünler. Bakteri fermente olduğundan karbonhidratlar onların karakteristik kalıplarında cins ve Türler tespiti mayalanma ürünler genellikle bakteri tanımlamasında kullanılır. Asitler, alkoller ve gazlar genellikle bu testlerde bakteri büyüdüğünde tespit edilir seçici sıvı veya katı ortam.
İzolasyonu enzimler Enfekte dokudan elde edilmesi, bulaşıcı bir hastalığın biyokimyasal teşhisinin temelini de sağlayabilir. Örneğin, insanlar ikisini de yapamaz RNA kopyaları ne de ters transkriptaz ve bu enzimlerin varlığı, spesifik viral enfeksiyon tiplerinin karakteristik özelliğidir. Viral proteinin yeteneği hemaglutinin bağlamak Kırmızı kan hücreleri birlikte tespit edilebilir bir matris haline getirilmesi, viral enfeksiyon için bir biyokimyasal test olarak da karakterize edilebilir, ancak hemaglutinin kesinlikle bir enzim ve metabolik işlevi yoktur.
Serolojik yöntemler mikroorganizmaları tanımlamak için kullanılan son derece hassas, spesifik ve genellikle son derece hızlı testlerdir. Bu testler, bir antikorun spesifik olarak bir antijene bağlanma yeteneğine dayanmaktadır. Antijen, genellikle bulaşıcı bir ajan tarafından yapılan bir protein veya karbonhidrat, antikor tarafından bağlanır. Bu bağlanma daha sonra, teste bağlı olarak çeşitli şekillerde gözle görülür şekilde açık olabilen bir olaylar zincirini başlatır. Örneğin, "Strep boğaz "genellikle dakikalar içinde teşhis edilir ve nedensel ajan tarafından yapılan antijenlerin görünümüne dayanır, S. pyogenes pamuklu çubukla hastanın boğazından alınır. Varsa serolojik testler genellikle tercih edilen tanımlama yoludur, ancak testlerin geliştirilmesi maliyetlidir ve testte kullanılan reaktifler genellikle soğutma. Bazı serolojik yöntemler son derece maliyetlidir, ancak "strep testi" gibi yaygın olarak kullanıldıklarında ucuz olabilirler.[17]
Karmaşık serolojik teknikler, Immunoassayler. İmmünolojik testler, bir tür enstrümantasyonla tespit edilebilen bir elektromanyetik veya partikül radyasyon sinyali üretmek için temel olarak temel antikor - antijen bağlanmasını kullanabilir. Bilinmeyenlerin sinyali, hedef antijenin miktarının belirlenmesine izin veren standartlarla karşılaştırılabilir. Enfeksiyöz hastalıkların teşhisine yardımcı olmak için, immünolojik testler, enfeksiyonlu ajanlardan veya yabancı bir ajana yanıt olarak enfekte bir organizma tarafından üretilen proteinlerden antijenleri tespit edebilir veya ölçebilir. Örneğin immünolojik test A, bir virüs partikülünden bir yüzey proteininin varlığını tespit edebilir. Öte yandan immünolojik test B, bir organizmanın bağışıklık sistemi tarafından üretilen ve virüsü nötralize etmek ve yok etmesine izin vermek için yapılan antikorları tespit edebilir veya ölçebilir.
Enstrümantasyon, antikor - antijen bağlanmasına bağlı ikincil reaksiyonlar tarafından oluşturulan son derece küçük sinyalleri okumak için kullanılabilir. Enstrümantasyon, bulaşıcı hastalığın teşhisi için uygun maliyetli otomatik bir süreç sağlamak için örnekleme, reaktif kullanımı, reaksiyon süreleri, sinyal algılama, sonuçların hesaplanması ve veri yönetimini kontrol edebilir.
PCR tabanlı teşhis
Dayalı teknolojiler polimeraz zincirleme reaksiyonu (PCR) yöntemi, çeşitli nedenlerle, yakın gelecekte neredeyse her yerde bulunan altın teşhis standartları haline gelecektir. Birincisi, bulaşıcı ajanların kataloğu, insan popülasyonunun neredeyse tüm önemli bulaşıcı ajanlarının tanımlandığı noktaya kadar büyümüştür. İkincisi, hastalığa neden olmak için insan vücudunda bulaşıcı bir ajan büyümelidir; esasen bir hastalığa neden olması için kendi nükleik asitlerini çoğaltması gerekir. Enfekte dokudaki nükleik asidin bu amplifikasyonu, enfeksiyöz ajanı PCR kullanarak tespit etme fırsatı sunar. Üçüncüsü, PCR'yi yönetmek için gerekli araçlar, primerler, türetilmiştir genomlar bulaşıcı etkenler ve zamanla bu genomlar biliniyorlarsa.
Bu nedenle, herhangi bir bulaşıcı ajanı hızla ve spesifik olarak tespit etmek için teknolojik yetenek şu anda mevcuttur. PCR'nin standart bir tanı aracı olarak kullanımına yönelik geriye kalan tek engel, maliyeti ve uygulamasıdır ve bunların hiçbiri aşılmaz değildir. Bazı hastalıkların teşhisi, PCR yöntemlerinin geliştirilmesinden fayda sağlamayacaktır. klostridial hastalıklar (tetanos ve botulizm ). Bu hastalıklar, temelde, son derece güçlü bakteriler üreten nispeten az sayıdaki bulaşıcı bakteri tarafından gerçekleştirilen biyolojik zehirlenmelerdir. nörotoksinler. Enfeksiyöz ajanda önemli bir proliferasyon meydana gelmez, bu PCR'nin herhangi bir bakteri varlığını tespit etme kabiliyetini sınırlar.
Metagenomik sıralama
Zayıflatıcı ve yaşamı tehdit eden hastalığa neden olan çok çeşitli bakteri, virüs ve diğer patojenler göz önüne alındığında, enfeksiyonun nedenini hızlı bir şekilde belirleme yeteneği önemli ancak çoğu zaman zordur. Örneğin, vakaların yarısından fazlası ensefalit, beyni etkileyen ciddi bir hastalık, son teknoloji klinik laboratuar yöntemleri kullanılarak yapılan kapsamlı testlere rağmen teşhis edilemiyor. Metagenomik şu anda klinik kullanım için araştırılıyor ve her şeyi kapsayan tek bir test kullanarak enfeksiyonu teşhis etmenin hassas ve hızlı bir yolu olarak umut vaat ediyor. Bu test, mevcut PCR testlerine benzer; ancak, genetik materyalin amplifikasyonu kullanmaktan ziyade tarafsızdır primerler belirli bir bulaşıcı ajan için. Bu amplifikasyon adımının ardından yeni nesil dizileme ve hizalama karşılaştırmaları binlerce organizma ve viral genomun büyük veri tabanlarını kullanarak.
Metagenomik dizileme, özellikle hasta olduğunda tanı için yararlı olabilir. bağışıklığı bozulmuş. Her zamankinden daha geniş bir enfeksiyon ajanı dizisi, bağışıklık sistemi baskılanması olan bireylere ciddi zarar verebilir, bu nedenle klinik taramanın genellikle daha geniş olması gerekir. Ek olarak, semptomların ifadesi genellikle atipiktir ve sunuma dayalı klinik teşhisi zorlaştırır. Thirdly, diagnostic methods that rely on the detection of antibodies are more likely to fail. A broad, sensitive test for pathogens that detects the presence of infectious material rather than antibodies is therefore highly desirable.
Indication of tests
Genellikle bir gösterge for a specific identification of an infectious agent only when such identification can aid in the treatment or prevention of the disease, or to advance knowledge of the course of an illness prior to the development of effective therapeutic or preventative measures. For example, in the early 1980s, prior to the appearance of AZT tedavisi için AIDS, the course of the disease was closely followed by monitoring the composition of patient blood samples, even though the outcome would not offer the patient any further treatment options. In part, these studies on the appearance of HIV in specific communities permitted the advancement of hipotezler as to the route of transmission of the virus. By understanding how the disease was transmitted, resources could be targeted to the communities at greatest risk in campaigns aimed at reducing the number of new infections. Spesifik serolojik diagnostic identification, and later genotipik or molecular identification, of HIV also enabled the development of hypotheses as to the geçici ve coğrafi origins of the virus, as well as a myriad of other hypothesis.[17] The development of molecular diagnostic tools have enabled physicians and researchers to monitor the efficacy of treatment with anti-retroviral drugs. Molecular diagnostics are now commonly used to identify HIV in healthy people long before the onset of illness and have been used to demonstrate the existence of people who are genetically resistant to HIV infection. Thus, while there still is no cure for AIDS, there is great therapeutic and predictive benefit to identifying the virus and monitoring the virus levels within the blood of infected individuals, both for the patient and for the community at large.
Önleme
Techniques like hand washing, wearing gowns, and wearing face masks can help prevent infections from being passed from one person to another. Aseptic technique was introduced in medicine and surgery in the late 19th century and greatly reduced the incidence of infections caused by surgery. Sık el yıkama remains the most important defense against the spread of unwanted organisms.[38] There are other forms of prevention such as avoiding the use of illicit drugs, using a condom, wearing gloves, and having a healthy lifestyle with a balanced diet and regular exercise. Cooking foods well and avoiding foods that have been left outside for a long time is also important.
Antimicrobial substances used to prevent transmission of infections include:
- antiseptics, which are applied to living doku /cilt
- dezenfektanlar, which destroy microorganisms found on non-living objects.
- antibiyotikler, aranan profilaktik when given as prevention rather as treatment of infection. However, long term use of antibiotics leads to resistance of bacteria. While humans do not become immune to antibiotics, the bacteria does. Thus, avoiding using antibiotics longer than necessary helps preventing bacteria from forming mutations that aide in antibiotic resistance.
One of the ways to prevent or slow down the transmission of infectious diseases is to recognize the different characteristics of various diseases.[39] Some critical disease characteristics that should be evaluated include şiddet, distance traveled by victims, and level of contagiousness. The human strains of Ebola virus, for example, incapacitate their victims extremely quickly and kill them soon after. As a result, the victims of this disease do not have the opportunity to travel very far from the initial infection zone.[40] Also, this virus must spread through skin lesions or permeable membranes such as the eye. Thus, the initial stage of Ebola is not very contagious since its victims experience only internal hemorrhaging. As a result of the above features, the spread of Ebola is very rapid and usually stays within a relatively confined geographical area. In contrast, the İnsan bağışıklık eksikliği virüsü (HIV ) kills its victims very slowly by attacking their immune system.[17] As a result, many of its victims transmit the virus to other individuals before even realizing that they are carrying the disease. Also, the relatively low virulence allows its victims to travel long distances, increasing the likelihood of an epidemi.
Another effective way to decrease the transmission rate of infectious diseases is to recognize the effects of küçük dünya ağları.[39] In epidemics, there are often extensive interactions within hubs or groups of infected individuals and other interactions within discrete hubs of susceptible individuals. Despite the low interaction between discrete hubs, the disease can jump to and spread in a susceptible hub via a single or few interactions with an infected hub. Thus, infection rates in small-world networks can be reduced somewhat if interactions between individuals within infected hubs are eliminated (Figure 1). However, infection rates can be drastically reduced if the main focus is on the prevention of transmission jumps between hubs. The use of needle exchange programs in areas with a high density of drug users with HIV is an example of the successful implementation of this treatment method. [6][tam alıntı gerekli ] Another example is the use of ring culling or vaccination of potentially susceptible livestock in adjacent farms to prevent the spread of the ayak ve ağız virus in 2001.[41]
A general method to prevent transmission of vektör -borne pathogens is pest control.
In cases where infection is merely suspected, individuals may be quarantined until the incubation period has passed and the disease manifests itself or the person remains healthy. Groups may undergo quarantine, or in the case of communities, a kordon sanitaire may be imposed to prevent infection from spreading beyond the community, or in the case of protective sequestration, into a community. Public health authorities may implement other forms of sosyal mesafe, such as school closings, to control an epidemic.
Bağışıklık

Infection with most pathogens does not result in death of the host and the offending organism is ultimately cleared after the symptoms of the disease have waned.[16] This process requires immune mechanisms to kill or inactivate the aşı of the pathogen. Specific acquired dokunulmazlık against infectious diseases may be mediated by antikorlar ve / veya T lenfositleri. Immunity mediated by these two factors may be manifested by:
- a direct effect upon a pathogen, such as antibody-initiated Tamamlayıcı -dependent bacteriolysis, opsonoization, phagocytosis and killing, as occurs for some bacteria,
- neutralization of viruses so that these organisms cannot enter cells,
- or by T lymphocytes, which will kill a cell parasitized by a microorganism.
The immune system response to a microorganism often causes symptoms such as a high ateş ve iltihap, and has the potential to be more devastating than direct damage caused by a microbe.[17]
Resistance to infection (dokunulmazlık ) may be acquired following a disease, by asymptomatic carriage of the pathogen, by harboring an organism with a similar structure (crossreacting), or by aşılama. Knowledge of the protective antigens and specific acquired host immune factors is more complete for primary pathogens than for fırsatçı patojenler.There is also the phenomenon of sürü bağışıklığı which offers a measure of protection to those otherwise vulnerable people when a large enough proportion of the population has acquired immunity from certain infections.
Immune resistance to an infectious disease requires a critical level of either antigen-specific antibodies and/or T cells when the host encounters the pathogen. Some individuals develop natural serum antibodies to the surface polysaccharides of some agents although they have had little or no contact with the agent, these natural antibodies confer specific protection to adults and are passively transmitted to newborns.
Host genetic factors
The organism that is the target of an infecting action of a specific infectious agent is called the host. The host harbouring an agent that is in a mature or sexually active stage phase is called the definitive host. The intermediate host comes in contact during the larvae stage. A host can be anything living and can attain to asexual and sexual reproduction.[42]The clearance of the pathogens, either treatment-induced or spontaneous, it can be influenced by the genetic variants carried by the individual patients. For instance, for genotype 1 hepatitis C treated with Pegylated interferon-alpha-2a veya Pegylated interferon-alpha-2b (brand names Pegasys or PEG-Intron) combined with ribavirin, it has been shown that genetic polymorphisms near the human IL28B gene, encoding interferon lambda 3, are associated with significant differences in the treatment-induced clearance of the virus. This finding, originally reported in Nature,[43] showed that genotype 1 hepatitis C patients carrying certain genetic variant alleles near the IL28B gene are more possibly to achieve sustained virological response after the treatment than others. Later report from Nature[44] demonstrated that the same genetic variants are also associated with the natural clearance of the genotype 1 hepatitis C virus.
Tedaviler
When infection attacks the body, anti-enfektif drugs can suppress the infection. Several broad types of anti-infective drugs exist, depending on the type of organism targeted; they include antibacterial (antibiyotik; dahil olmak üzere antitubercular ), antiviral, mantar önleyici ve antiparazitik (dahil olmak üzere antiprotozoal ve antihelminthic ) agents. Depending on the severity and the type of infection, the antibiotic may be given by mouth or by injection, or may be applied topikal olarak. Severe infections of the beyin are usually treated with intravenöz antibiyotikler. Sometimes, multiple antibiotics are used in case there is resistance to one antibiotic. Antibiotics only work for bacteria and do not affect viruses. Antibiotics work by slowing down the multiplication of bacteria or killing the bacteria. The most common classes of antibiotics used in medicine include penisilin, sefalosporinler, aminoglikozitler, makrolidler, kinolonlar ve tetrasiklinler.[45][46]
Not all infections require treatment, and for many self-limiting infections the treatment may cause more side-effects than benefits. Antimicrobial stewardship is the concept that healthcare providers should treat an infection with an antimicrobial that specifically works well for the target pathogen for the shortest amount of time and to only treat when there is a known or highly suspected pathogen that will respond to the medication.[47]
Epidemiyoloji


In 2010, about 10 million people died of infectious diseases.[49]
Dünya Sağlık Örgütü collects information on global deaths by International Classification of Disease (ICD) code categories. The following table lists the top infectious disease by number of deaths in 2002. 1993 data is included for comparison.
| Sıra | Ölüm nedeni | Deaths 2002 (milyon olarak) | Yüzdesi all deaths | Deaths 1993 (milyon olarak) | 1993 Rank |
|---|---|---|---|---|---|
| Yok | All infectious diseases | 14.7 | 25.9% | 16.4 | 32.2% |
| 1 | Alt solunum yolu enfeksiyonları[52] | 3.9 | 6.9% | 4.1 | 1 |
| 2 | HIV /AIDS | 2.8 | 4.9% | 0.7 | 7 |
| 3 | İshalli hastalıklar[53] | 1.8 | 3.2% | 3.0 | 2 |
| 4 | Tüberküloz (TB) | 1.6 | 2.7% | 2.7 | 3 |
| 5 | Sıtma | 1.3 | 2.2% | 2.0 | 4 |
| 6 | Kızamık | 0.6 | 1.1% | 1.1 | 5 |
| 7 | Boğmaca | 0.29 | 0.5% | 0.36 | 7 |
| 8 | Tetanos | 0.21 | 0.4% | 0.15 | 12 |
| 9 | Menenjit | 0.17 | 0.3% | 0.25 | 8 |
| 10 | Frengi | 0.16 | 0.3% | 0.19 | 11 |
| 11 | Hepatit B | 0.10 | 0.2% | 0.93 | 6 |
| 12–17 | Tropikal Hastalıklar (6)[54] | 0.13 | 0.2% | 0.53 | 9, 10, 16–18 |
| Note: Other causes of death include maternal and perinatal conditions (5.2%), nutritional deficiencies (0.9%), noncommunicable conditions (58.8%), and injuries (9.1%). | |||||
The top three single agent/disease killers are HIV /AIDS, TB ve sıtma. While the number of deaths due to nearly every disease have decreased, deaths due to HIV/AIDS have increased fourfold. Childhood diseases include boğmaca, çocuk felci, difteri, kızamık ve tetanos. Children also make up a large percentage of lower respiratory and diarrheal deaths. In 2012, approximately 3.1 million people have died due to lower respiratory infections, making it the number 4 leading cause of death in the world.[55]
Historic pandemics
With their potential for unpredictable and explosive impacts, infectious diseases have been major actors in human Tarih.[56] Bir pandemi (or global epidemi ) is a disease that affects people over an extensive geographical area. Örneğin:
- Justinianus Vebası, from 541 to 542, killed between 50% and 60% of Europe's population.[57]
- Kara Ölüm of 1347 to 1352 killed 25 million in Europe over 5 years. The plague reduced the old world population from an estimated 450 million to between 350 and 375 million in the 14th century.
- Tanımı Çiçek hastalığı, measles, and tifüs to the areas of Central and South America by European explorers during the 15th and 16th centuries caused pandemics among the native inhabitants. Between 1518 and 1568 disease pandemics are said to have caused the population of Meksika to fall from 20 million to 3 million.[58]
- The first European grip epidemic occurred between 1556 and 1560, with an estimated mortality rate of 20%.[58]
- Çiçek hastalığı killed an estimated 60 million Europeans during the 18th century[59] (approximately 400,000 per year).[60] Up to 30% of those infected, including 80% of the children under 5 years of age, died from the disease, and one-third of the survivors went blind.[61]
- In the 19th century, tüberküloz killed an estimated one-quarter of the adult population of Europe;[62] by 1918 one in six deaths in France were still caused by TB.
- The Influenza Pandemic of 1918 (or the İspanyol gribi ) killed 25–50 million people (about 2% of world population of 1.7 billion).[63] Bugün Grip kills about 250,000 to 500,000 worldwide each year.
Emerging diseases
In most cases, microorganisms live in harmony with their hosts via mutual veya ortak etkileşimler. Diseases can emerge when existing parasites become pathogenic or when new pathogenic parasites enter a new host.
- Birlikte evrim arasında parazit ve ev sahibi can lead to hosts becoming dayanıklı to the parasites or the parasites may evolve greater şiddet, giden immunopathological disease.
- Human activity is involved with many emerging infectious diseases, gibi çevresel değişim enabling a parasite to occupy new nişler. When that happens, a patojen that had been confined to a remote habitat has a wider distribution and possibly a new ev sahibi organizma. Parasites jumping from nonhuman to human hosts are known as zoonozlar. Under disease invasion, when a parasite invades a new host species, it may become pathogenic in the new host.[64]
Several human activities have led to the emergence of zoonotic human pathogens, including viruses, bacteria, protozoa, and rickettsia,[65] ve yayılması vektör kaynaklı hastalıklar,[64] Ayrıca bakınız globalization and disease ve wildlife disease:
- Encroachment on wildlife habitatlar. The construction of new villages and housing developments in rural areas force animals to live in dense populations, creating opportunities for microbes to mutate and emerge.[66]
- Değişiklikler tarım. The introduction of new crops attracts new crop pests and the microbes they carry to farming communities, exposing people to unfamiliar diseases.
- Yıkımı rain forests. As countries make use of their rain forests, by building roads through forests and clearing areas for settlement or commercial ventures, people encounter insects and other animals harboring previously unknown microorganisms.
- Kontrolsüz kentleşme. The rapid growth of cities in many developing countries tends to concentrate large numbers of people into crowded areas with poor sanitation. These conditions foster transmission of contagious diseases.
- Modern Ulaşım. Ships and other cargo carriers often harbor unintended "passengers", that can spread diseases to faraway destinations. While with international jet-airplane travel, people infected with a disease can carry it to distant lands, or home to their families, before their first symptoms appear.
Germ hastalık teorisi

İçinde Antik dönem, Yunan tarihçi Tukididler (c. 460 – c. 400 BCE) was the first person to write, in his account of the plague of Athens, bu hastalıklar enfekte bir kişiden başkalarına yayılabilir.[67][68] Onun içinde Farklı Ateş Türleri Hakkında (c. AD 175), the Greco-Roman physician Galen speculated that plagues were spread by "certain seeds of plague", which were present in the air.[69] İçinde Sushruta Samhita, eski Hint doktoru Sushruta kuramsal: "Cüzzam, ateş, tüketim, göz hastalıkları ve bir kişiden diğerine cinsel birliktelik, fiziksel temas, birlikte yemek yeme, birlikte uyumak, birlikte oturmak ve aynı kıyafetleri, çelenkleri ve macunları kullanmak yoluyla bulaşan diğer bulaşıcı hastalıklar . "[70][71] This book has been dated to about the sixth century BC.[72]
A basic form of contagion theory was proposed by Farsça doktor İbn Sina (Avrupa'da Avicenna olarak bilinir) The Canon of Medicine (1025), daha sonra 16. yüzyıla kadar Avrupa'da en yetkili tıp ders kitabı oldu. IV.Kitapta Canon, İbn Sina tartıştı salgın hastalıklar, klasik miasma teorisi ve bunu kendi erken bulaşma teorisiyle harmanlamaya çalışıyor. He mentioned that people can transmit disease to others by breath, noted contagion with tüberküloz, and discussed the transmission of disease through water and dirt.[73] Görünmez bulaşma kavramı daha sonra birkaç kişi tarafından tartışıldı. Islamic scholars içinde Eyyubi Sultanlığı onlara kim dedi najasat ("impure substances"). fıkıh akademisyen İbnü'l-Hac el-Abdari (c. 1250–1336), while discussing Islamic diet ve hijyen, bulaşmanın su, yiyecek ve giysileri nasıl kirletebileceği ve su kaynağı yoluyla yayılabileceği konusunda uyarılar verdi ve bulaşmanın görünmeyen parçacıklar olduğunu ima etmiş olabilir.[74]
Ne zaman Kara Ölüm hıyarcıklı veba ulaştı Endülüs 14. yüzyılda Arap hekimler İbn Hatime (c. 1369) ve İbnü'l-Hatib (1313-1374) bulaşıcı hastalıklara "küçük bedenler" neden olduğunu varsaydı ve bunların giysiler, kaplar ve küpeler yoluyla nasıl bulaşabileceklerini açıkladı.[75] Ideas of contagion became more popular in Europe during the Rönesans, particularly through the writing of the Italian physician Girolamo Fracastoro.[76] Anton van Leeuwenhoek (1632–1723) advanced the science of mikroskopi by being the first to observe microorganisms, allowing for easy visualization of bacteria.
In the mid-19th century John Snow ve William Budd did important work demonstrating the contagiousness of typhoid and cholera through contaminated water. Both are credited with decreasing epidemics of cholera in their towns by implementing measures to prevent contamination of water.[77] Louis Pasteur proved beyond doubt that certain diseases are caused by infectious agents, and developed a vaccine for kuduz. Robert Koch, provided the study of infectious diseases with a scientific basis known as Koch'un postülatları. Edward Jenner, Jonas Salk ve Albert Sabin developed effective vaccines for Çiçek hastalığı ve çocuk felci, which would later result in the yok etme and near-eradication of these diseases, respectively. Alexander Fleming discovered the world's first antibiyotik, Penisilin, which Florey and Chain then developed. Gerhard Domagk gelişmiş sulphonamides, the first broad spectrum sentetik antibacterial drugs.
Medical specialists
tıbbi tedavi of infectious diseases falls into the medical field nın-nin Bulaşıcı hastalık and in some cases the study of propagation pertains to the field of Epidemiyoloji. Generally, infections are initially diagnosed by Birincil bakım physicians or Dahiliye uzmanlar. For example, an "uncomplicated" Zatürre will generally be treated by the internist ya da göğüs hastalıkları uzmanı (lung physician). The work of the infectious diseases specialist therefore entails working with both patients and general practitioners, as well as laboratuvar bilim adamları, immunologists, bacteriologists and other specialists.
An infectious disease team may be alerted when:
- The disease has not been definitively diagnosed after an initial workup
- The patient is bağışıklığı bozulmuş (for example, in AIDS yada sonra kemoterapi );
- bulaşıcı etken is of an uncommon nature (e.g. tropikal Hastalıklar );
- The disease has not responded to first line antibiyotikler;
- The disease might be dangerous to other patients, and the patient might have to be isolated
Toplum ve kültür
A number of studies have reported associations between pathogen load in an area and human behavior. Higher pathogen load is associated with decreased size of ethnic and religious groups in an area. This may be due high pathogen load favoring avoidance of other groups, which may reduce pathogen transmission, or a high pathogen load preventing the creation of large settlements and armies that enforce a common culture. Higher pathogen load is also associated with more restricted sexual behavior, which may reduce pathogen transmission. It also associated with higher preferences for health and attractiveness in mates. Daha yüksek doğurganlık oranı and shorter or less parental care per child is another association that may be a compensation for the higher mortality rate. There is also an association with çok eşlilik which may be due to higher pathogen load, making selecting males with a high genetic resistance increasingly important. Higher pathogen load is also associated with more collectivism and less individualism, which may limit contacts with outside groups and infections. There are alternative explanations for at least some of the associations although some of these explanations may in turn ultimately be due to pathogen load. Thus, polygyny may also be due to a lower male:female ratio in these areas but this may ultimately be due to male infants having increased mortality from infectious diseases. Another example is that poor socioeconomic factors may ultimately in part be due to high pathogen load preventing economic development.[78]
Fosil kaydı

Evidence of infection in fossil remains is a subject of interest for paleopathologists, scientists who study occurrences of injuries and illness in extinct life forms. Signs of infection have been discovered in the bones of carnivorous dinosaurs. When present, however, these infections seem to tend to be confined to only small regions of the body. A skull attributed to the early carnivorous dinosaur Herrerasaurus ischigualastensis exhibits pit-like wounds surrounded by swollen and porous bone. The unusual texture of the bone around the wounds suggests they were afflicted by a short-lived, non-lethal infection. Scientists who studied the skull speculated that the bite marks were received in a fight with another Herrerasaurus. Other carnivorous dinosaurs with documented evidence of infection include Akrokantosaurus, Allosaurus, Tyrannosaurus and a tyrannosaur from the Kirtland Formasyonu. The infections from both tyrannosaurs were received by being bitten during a fight, like the Herrerasaurus örnek.[79]
Uzay
A 2006 Space Shuttle experiment found that Salmonella typhimurium, a bacterium that can cause Gıda zehirlenmesi, became more virulent when cultivated in space.[80] On April 29, 2013, scientists in Rensselaer Polytechnic Institute, funded by NASA, reported that, during uzay uçuşu üzerinde Uluslararası Uzay istasyonu, mikroplar seem to adapt to the uzay ortamı in ways "not observed on Earth" and in ways that "can lead to increases in growth and şiddet ".[81] More recently, in 2017, bakteri were found to be more resistant to antibiyotikler and to thrive in the near-weightlessness of space.[82] Mikroorganizmalar have been observed to survive the vakum of outer space.[83][84]
Ayrıca bakınız
- Bioinformatics Resource Centers for Infectious Diseases
- Biyolojik tehlike
- Kanla bulaşan hastalık
- Koenfeksiyon
- Kopenhag Mutabakatı
- Cordon sanitaire
- Disease diffusion mapping
- Epidemiyolojik geçiş
- Gıda kaynaklı hastalık
- Gen tedavisi
- Tıp tarihi
- Hastane kaynaklı enfeksiyon
- Bulaşıcı hastalıkların ortadan kaldırılması
- Human Microbiome Project
- Enfeksiyon kontrolü
- İzolasyon (sağlık bakımı)
- Bakteriyel vajinoz mikrobiyotasının listesi
- Orana göre ölüm nedenleri listesi
- List of diseases caused by insects
- Salgın listesi
- Bulaşıcı hastalıkların listesi
- Bulaşıcı hastalıkların matematiksel modellemesi
- Membran vezikül ticareti
- Multiplicity of infection
- İhmal edilen tropikal hastalıklar
- Sentinel gözetimi
- Sosyal mesafe
- Spatiotemporal Epidemiological Modeler (STEM)
- Yayılma enfeksiyonu
- Threshold host density
- İletim (tıp)
- Ubi pus, ibi evacua (Latin: "where there is irin, there evacuate it")
- Aşıyla önlenebilir hastalıklar
- Su kaynaklı hastalıklar
Referanslar
- ^ Definition of "infection" from several medical dictionaries – Retrieved on 2012-04-03
- ^ "Utilizing antibiotics agents effectively will preserve present day medication". Haber Gana. 21 Kasım 2015. Alındı 21 Kasım 2015.
- ^ "Mantar Hastalıkları Türleri". www.cdc.gov. 2019-06-27. Alındı 2019-12-09.
- ^ Mada, Pradeep Kumar; Jamil, Radia T.; Alam, Mohammed U. (2019), "Cryptococcus (Cryptococcosis)", StatPearlsStatPearls Yayıncılık, PMID 28613714, alındı 2019-12-09
- ^ "About Parasites". www.cdc.gov. 2019-02-25. Alındı 2019-12-09.
- ^ Brown, Peter J. (1987). "Microparasites and Macroparasites". Kültürel antropoloji. 2 (1): 155–71. doi:10.1525/can.1987.2.1.02a00120. JSTOR 656401.
- ^ Alberto Signore (2013). "About inflammation and infection" (PDF). EJNMMI Research. 8 (3).
- ^ GBD 2013 Mortality and Why of Death, Collaborators (17 Aralık 2014). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study". Lancet. 385 (9963): 117–71. doi:10.1016 / S0140-6736 (14) 61682-2. PMC 4340604. PMID 25530442.
- ^ "Infectious Disease, Internal Medicine". Association of American Medical Colleges. Arşivlenen orijinal on 2015-02-06. Alındı 2015-08-20.
Infectious disease is the subspecialty of internal medicine dealing with the diagnosis and treatment of communicable diseases of all types, in all organs, and in all ages of patients.
- ^ Kayser, Fritz H; Kurt A Bienz; Johannes Eckert; Rolf M Zinkernagel (2005). Tıbbi mikrobiyoloji. Stuttgart: Georg Thieme Verlag. s. 398. ISBN 978-3-13-131991-3.
- ^ Grinde, Bjørn (2013-10-25). "Herpesviruses: latency and reactivation – viral strategies and host response". Journal of Oral Microbiology. 5: 22766. doi:10.3402/jom.v5i0.22766. ISSN 0901-8328. PMC 3809354. PMID 24167660.
- ^ Elsevier, Dorland'ın Resimli Tıp Sözlüğü, Elsevier.
- ^ "Acute infections (MPKB)". mpkb.org. Alındı 2019-12-09.
- ^ Boldogh, Istvan; Albrecht, Thomas; Porter, David D. (1996), Baron, Samuel (ed.), "Persistent Viral Infections", Tıbbi Mikrobiyoloji (4th ed.), University of Texas Medical Branch at Galveston, ISBN 978-0-9631172-1-2, PMID 21413348, alındı 2020-01-23
- ^ a b Foster, John (2018). Mikrobiyoloji. New York: Norton. s. 39. ISBN 978-0-393-60257-9.
- ^ a b This section incorporates kamu malı materials included in the text: Tıbbi Mikrobiyoloji Fourth Edition: Bölüm 8 (1996). Baron, Samuel MD. The University of Texas Medical Branch at Galveston. Tıbbi Mikrobiyoloji. University of Texas Medical Branch at Galveston. 1996. ISBN 9780963117212. Archived from the original on June 29, 2009. Alındı 2013-11-27.CS1 bakimi: BOT: orijinal url durumu bilinmiyor (bağlantı)
- ^ a b c d e f Ryan KJ, Ray CG, eds. (2004). Sherris Tıbbi Mikrobiyoloji (4. baskı). McGraw Hill. ISBN 978-0-8385-8529-0.
- ^ Higurea & Pietrangelo 2016[sayfa gerekli ]
- ^ a b c "Bacterial vs. Viral Infections – Do You Know the Difference?" National Information Program on Antibiotics
- ^ Robert N. Golden; Fred Peterson (2009). The Truth About Illness and Disease. Bilgi Bankası Yayıncılık. s. 181. ISBN 978-1438126371.
- ^ "Enfeksiyon". Rencare. Arşivlenen orijinal on March 5, 2012. Alındı 4 Temmuz 2013.
- ^ Infection Cycle – Retrieved on 2010-01-21 Arşivlendi 17 Mayıs 2014, Wayback Makinesi
- ^ Understanding Infectious Diseases Arşivlendi 2009-09-24 at the Wayback Makinesi Science.Education.Nih.Gov article – Retrieved on 2010-01-21
- ^ Negut, Irina; Grumezescu, Valentina; Grumezescu, Alexandru Mihai (2018-09-18). "Treatment Strategies for Infected Wounds". Moleküller. 23 (9): 2392. doi:10.3390/molecules23092392. ISSN 1420-3049. PMC 6225154. PMID 30231567.
- ^ Duerkop, Breck A; Hooper, Lora V (2013-07-01). "Resident viruses and their interactions with the immune system". Doğa İmmünolojisi. 14 (7): 654–59. doi:10.1038/ni.2614. PMC 3760236. PMID 23778792.
- ^ "Bacterial Pathogenesis at Washington University". StudyBlue. Aziz Louis. Alındı 2016-12-02.
- ^ "Print Friendly". www.lifeextension.com. Arşivlenen orijinal on 2016-12-02. Alındı 2016-12-02.
- ^ Reddy M, Gill SS, Wu W, et al. (Feb 2012). "Does this patient have an infection of a chronic wound?". JAMA. 307 (6): 605–11. doi:10.1001/jama.2012.98. PMID 22318282.
- ^ http://www.immunize.org/catg.d/p4215.pdf
- ^ Chronic Infection Information Retrieved on 2010-01-14 Arşivlendi 22 Temmuz 2015, Wayback Makinesi
- ^ Intestinal Parasites and Infection Arşivlendi 2010-10-28 de Wayback Makinesi fungusfocus.com – Retrieved on 2010-01-21
- ^ "Clinical Infectious Disease – Introduction". www.microbiologybook.org. Alındı 2017-04-19.
- ^ Pathogens and vectors. MetaPathogen.com.
- ^ Seventer JM, Hochberg NS (October 2016). "Principles of Infectious Diseases: Transmission, Diagnosis, Prevention, and Control". International Encyclopedia of Public Health: 22–39. doi:10.1016/B978-0-12-803678-5.00516-6. ISBN 9780128037089. PMC 7150340.
- ^ Ljubin-Sternak, Suncanica; Mestrovic, Tomislav (2014). "Review: Chlamydia trachonmatis and Genital Mycoplasmias: Pathogens with an Impact on Human Reproductive Health". Journal of Pathogens. 2014 (183167): 3. doi:10.1155/2014/183167. PMC 4295611. PMID 25614838.
- ^ a b Van den Bruel A, Haj-Hassan T, Thompson M, Buntinx F, Mant D (March 2010). "Diagnostic value of clinical features at presentation to identify serious infection in children in developed countries: a systematic review". Lancet. 375 (9717): 834–45. doi:10.1016/S0140-6736(09)62000-6. PMID 20132979. S2CID 28014329.
- ^ Bloomfield SF, Aiello AE, Cookson B, O'Boyle C, Larson EL (2007). "The effectiveness of hand hygiene procedures including hand-washing and alcohol-based hand sanitizers in reducing the risks of infections in home and community settings". Amerikan Enfeksiyon Kontrolü Dergisi. 35 (10): S27–S64. doi:10.1016/j.ajic.2007.07.001. PMC 7115270.
- ^ ""Generalized Infectious Cycle" Diagram Illustration". science.education.nih.gov. Arşivlenen orijinal 2009-09-24 tarihinde. Alındı 2010-01-21.
- ^ a b Watt Duncan (2003). Six degrees: the science of a connected age. Londra: William Heinemann. ISBN 978-0-393-04142-2.
- ^ Preston, Richard (1995). The hot zone. Garden City, N.Y.: Anchor Books. ISBN 978-0-385-49522-6.
- ^ Ferguson NM, Donnelly CA, Anderson RM (May 2001). "The foot-and-mouth epidemic in Great Britain: pattern of spread and impact of interventions". Bilim. 292 (5519): 1155–60. Bibcode:2001Sci...292.1155F. doi:10.1126/science.1061020. PMID 11303090. S2CID 16914744.
- ^ Barreto ML, Teixeira MG, Carmo EH (2006). "Infectious diseases epidemiology". Epidemiyoloji ve Toplum Sağlığı Dergisi. 60 (3): 192–95. doi:10.1136/jech.2003.011593. PMC 2465549. PMID 16476746.
- ^ Ge D, Fellay J, Thompson AJ, Simon JS, Shianna KV, Urban TJ, Heinzen EL, Qiu P, Bertelsen AH, Muir AJ, Sulkowski M, McHutchison JG, Goldstein DB (2009). "Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance". Doğa. 461 (7262): 399–401. Bibcode:2009Natur.461..399G. doi:10.1038/nature08309. PMID 19684573. S2CID 1707096.
- ^ Thomas DL, Thio CL, Martin MP, Qi Y, Ge D, O'Huigin C, Kidd J, Kidd K, Khakoo SI, Alexander G, Goedert JJ, Kirk GD, Donfield SM, Rosen HR, Tobler LH, Busch MP, McHutchison JG, Goldstein DB, Carrington M (2009). "Genetic variation in IL28B and spontaneous clearance of hepatitis C virus". Doğa. 461 (7265): 798–801. Bibcode:2009Natur.461..798T. doi:10.1038/nature08463. PMC 3172006. PMID 19759533.
- ^ Fair RJ, Tor Y (2014). "Antibiotics and Bacterial Resistance in the 21st Century". Perspectives in Medicinal Chemistry. 6: 25–64. doi:10.4137/PMC.S14459. PMC 4159373. PMID 25232278. Alındı 13 Mayıs 2020.
- ^ "Antibiotics: List of Common Antibiotics & Types". Drugs.com. Alındı 2020-11-10.
- ^ O'Brien, Deirdre J.; Gould, Ian M. (August 2013). "Maximizing the impact of antimicrobial stewardship". Bulaşıcı Hastalıklarda Güncel Görüş. 26 (4): 352–58. doi:10.1097/QCO.0b013e3283631046. PMID 23806898. S2CID 5487584.
- ^ Dünya Sağlık Örgütü (February 2009). "Age-standardized DALYs per 100,000 by cause, and Member State, 2004".
- ^ "Could Ebola rank among the deadliest communicable diseases?". CBC Haberleri. 20 October 2014.
- ^ "The World Health Report (Annex Table 2)" (PDF). 2004.
- ^ "Tablo 5" (PDF). 1995.
- ^ Lower respiratory infections include various pneumonias, influenzas ve acute bronchitis.
- ^ Diarrheal diseases are caused by many different organisms, including kolera, botulizm, ve E. coli birkaç isim. See also: Intestinal infectious diseases
- ^ Tropical diseases include Chagas hastalığı, dengue fever, lenfatik filaryaz, leishmaniasis, onkoserkiyazis, schistosomiasis ve tripanozomiyaz.
- ^ "WHO | The top 10 causes of death". DSÖ. Alındı 2015-09-24.
- ^ Fauci AS, Morens DM (2012). "The perpetual challenge of infectious diseases". New England Tıp Dergisi. 366 (5): 454–61. doi:10.1056/NEJMra1108296. PMID 22296079.
- ^ "Infectious and Epidemic Disease in History" Arşivlendi July 12, 2012, at Archive.today
- ^ a b Dobson AP, Carter ER (1996). "Infectious Diseases and Human Population History" (PDF). BioScience. 46 (2): 115–26. doi:10.2307/1312814. JSTOR 1312814.
- ^ "Smallpox". North Carolina Digital History.
- ^ Smallpox and Vaccinia. Ulusal Biyoteknoloji Bilgi Merkezi. Arşivlendi 1 Haziran 2009, Wayback Makinesi
- ^ Barquet, Nicolau (15 October 1997). "Smallpox: The Triumph over the Most Terrible of the Ministers of Death". İç Hastalıkları Yıllıkları. 127 (8_Part_1): 635–42. doi:10.7326/0003-4819-127-8_Part_1-199710150-00010. PMID 9341063. S2CID 20357515.
- ^ Multidrug-Resistant "Tuberculosis". Hastalık Kontrol ve Önleme Merkezleri. Arşivlendi 9 Mart 2010, Wayback Makinesi
- ^ "Influenza of 1918 (Spanish Flu) and the US Navy". 20 February 2006. Archived from orijinal on 20 February 2006.
- ^ a b Krauss H; Weber A; Appel M (2003). Zoonoses: Infectious Diseases Transmissible from Animals to Humans (3. baskı). Washington, D.C .: ASM Press. ISBN 978-1-55581-236-2.
- ^ Potter P (July 2013). "Summer buzz". Emerg Infect Dis. 19 (3): 1184. doi:10.3201/eid1907.AC1907. PMC 3903457.
- ^ Peter Daszak; Andrew A. Cunningham; Alex D. Hyatt (27 January 2000). "Emerging Infectious Diseases of Wildlife – Threats to Biodiversity and Human Health". Bilim. 287 (5452): 443–49. Bibcode:2000Sci...287..443D. doi:10.1126/science.287.5452.443. PMID 10642539.
- ^ Singer, Charles ve Dorothea (1917) "Girolamo Fracastoro'nun [1478? –1553] enfeksiyon teorisinin kaynağı, karakteri ve etkisine özel referansla bilimsel konumu" Tıp Tarihi Yıllıkları, 1 : 1–34; bkz. s. 14.
- ^ Thukydides ve Richard Crawley, çev., Peloponnesos Savaşı Tarihi (London: J.M. Dent & Sons, Ltd., 1910), Book III, § 51, s. 131–32.
- ^ Nutton, Vivian (1983) "Hastalık tohumları: Yunanlılardan Rönesans'a bulaşma ve enfeksiyonun bir açıklaması," Tıbbi geçmiş, 27 (1): 1–34; bkz. s. 10. Şuradan ulaşılabilir: U.S. National Library of Medicine, National Institutes of Health
- ^ Rastogi, Nalin; Rastogi, R (1985-01-01). "Eski Hindistan'da Cüzzam". Uluslararası Cüzzam ve Diğer Mikobakteriyel Hastalıklar Dergisi. 52 (4): 541–43. PMID 6399073.
- ^ Susruta; Bhishagratna, Kunja Lal (1907–1916). Orijinal Sanskrit metnine dayanan Sushruta samhita'nın İngilizce çevirisi. Kaviraj Kunja Lal Bhishagratna tarafından düzenlenmiş ve yayınlanmıştır. Tam ve kapsamlı bir giriş, farklı okumaların, notların, karşılaştırmalı görünümlerin, dizin, sözlük ve plakaların çevirisi ile. Gerstein – University of Toronto. Kalküta.
- ^ Hoernle, A.F.Rudolf (Ağustos Friedrich Rudolf) (1907). Eski Hindistan tıbbında yapılan çalışmalar. Gerstein – University of Toronto. Oxford: Clarendon Press'te.
- ^ Byrne, Joseph Patrick (2012). Kara Ölüm Ansiklopedisi. ABC-CLIO. s. 29. ISBN 978-1598842531.
- ^ Reid, Megan H. (2013). Law and Piety in Medieval Islam. Cambridge University Press. pp. 106, 114, 189–90. ISBN 978-1107067110.
- ^ Majeed, Azeem (22 December 2005). "How Islam changed medicine". BMJ. 331 (7531): 1486–87. doi:10.1136/bmj.331.7531.1486. ISSN 0959-8138. PMC 1322233. PMID 16373721.
- ^ Beretta M (2003). "Rönesans sırasında Lucretian atomizmi ve bulaşıcı hastalıkların yeniden canlanması". Medicina Nei Secoli. 15 (2): 129–54. PMID 15309812.
- ^ Moorhead Robert (Kasım 2002). "William Budd ve tifo ateşi". J R Soc Med. 95 (11): 561–64. doi:10.1258 / jrsm.95.11.561. PMC 1279260. PMID 12411628.
- ^ Isırgan D (2009). "İnsan davranış çeşitliliği üzerindeki ekolojik etkiler: son bulguların gözden geçirilmesi". Trendler Ecol. Evol. 24 (11): 618–24. doi:10.1016 / j.tree.2009.05.013. PMID 19683831.
- ^ Molnar, R. E., 2001, "Theropod paleopatoloji: literatür taraması": İçinde: Mesozoik Omurgalı YaşamıTanke, D. H. ve Carpenter, K., Indiana University Press, s. 337–63 tarafından düzenlenmiştir.
- ^ Caspermeyer, Joe (23 Eylül 2007). "Uzay uçuşunun bakterilerin hastalığa neden olma kabiliyetini değiştirdiği gösterilmiştir". Arizona Devlet Üniversitesi. Alındı 14 Eylül 2017.
- ^ Kim W, vd. (29 Nisan 2013). "Uzay uçuşu Pseudomonas aeruginosa'nın Biyofilm Oluşumunu Teşvik Ediyor". PLOS ONE. 8 (4): e6237. Bibcode:2013PLoSO ... 862437K. doi:10.1371 / journal.pone.0062437. PMC 3639165. PMID 23658630.
- ^ Dvorsky, George (13 Eylül 2017). "Endişe Verici Çalışma Bazı Bakterilerin Uzaydaki İlaçlara Neden Daha Dirençli Olduğunu Gösteriyor". Gizmodo. Alındı 14 Eylül 2017.
- ^ Doz, K .; Bieger-Dose, A .; Dillmann, R .; Gill, M .; Kerz, O .; Klein, A .; Meinert, H .; Nawroth, T .; Risi, S .; Stridde, C. (1995). "ERA-deney" uzay biyokimyası"" (PDF). Uzay Araştırmalarındaki Gelişmeler. 16 (8): 119–29. Bibcode:1995AdSpR..16..119D. doi:10.1016 / 0273-1177 (95) 00280-R. PMID 11542696.[kalıcı ölü bağlantı ]
- ^ Horneck G .; Eschweiler, U .; Reitz, G .; Wehner, J .; Willimek, R .; Strauch, K. (1995). "Uzaya biyolojik tepkiler: EURECA I üzerinde ERA'nın" Ekzobiyolojik Birimi "deneyinin sonuçları". Adv. Uzay Res. 16 (8): 105–18. Bibcode:1995AdSpR..16..105H. doi:10.1016 / 0273-1177 (95) 00279-N. PMID 11542695.
Dış bağlantılar
| Sınıflandırma |
|---|
- Avrupa Hastalık Önleme ve Kontrol Merkezi
- ABD Hastalık Kontrol ve Önleme Merkezleri,
- Amerika Bulaşıcı Hastalıklar Derneği (IDSA)
- Bulaşıcı Hastalık Endeksi Kanada Halk Sağlığı Kurumu (PHAC)
- Aşı Araştırma Merkezi Ortaya Çıkan ve Yeniden Ortaya Çıkan Bulaşıcı Hastalıklar için aşı araştırma klinik denemelerine ilişkin bilgiler.
- Enfeksiyon Bilgi Kaynağı
- Mikroplar ve Enfeksiyon (günlük)
- Yara yönetiminde yer alan Sağlık Uzmanları için bilgi kaynağı www.woundsite.info
- Tablo: Küresel bulaşıcı hastalıklardan ölümler, 2010 - Canadian Broadcasting Corp.


