Serotonin-norepinefrin geri alım inhibitörü - Serotonin–norepinephrine reuptake inhibitor
| Serotonin-norepinefrin geri alım inhibitörü | |
|---|---|
| İlaç sınıfı | |
 Duloksetin, bir SNRI örneği. | |
| Sınıf tanımlayıcıları | |
| Eş anlamlı | Seçici Serotonin-noradrenalin geri alım inhibitörü; SNaRI |
| Kullanım | Depresyon; Kaygı; Ağrı; Obezite; Menopoz semptomları |
| Biyolojik hedef | Serotonin taşıyıcısı; Norepinefrin taşıyıcı |
| Dış bağlantılar | |
| MeSH | D000068760 |
| Vikiveri'de | |
Serotonin-norepinefrin geri alım inhibitörleri (SNRI'ler) bir sınıftır antidepresan ilaçlar o tedavi majör depresif bozukluk (MDD), anksiyete bozuklukları, obsesif kompulsif bozukluk (OKB), sosyal fobi, Dikkat eksikliği hiperaktivite bozukluğu (DEHB), kronik nöropatik ağrı, fibromiyalji sendromu (FMS) ve menopoz semptomlar. SNRI'ler monoamin geri alım inhibitörleri; özellikle onlar engellemek yeniden alım nın-nin serotonin ve norepinefrin. Bunlar nörotransmiterler duygudurum düzenlemesinde önemli bir rol oynadığı düşünülmektedir. SNRI'ler, daha yaygın olarak kullanılanlarla karşılaştırılabilir. seçici serotonin geri alım inhibitörleri (SSRI'lar), yalnızca serotonin üzerinde etkili olur.
İnsan serotonin taşıyıcısı (SERT) ve norepinefrin taşıyıcı (NET) membran taşıma proteinleri serotonin ve norepinefrinin geri alımından sorumlu olanlar sinaptik yarık presinaptik sinir terminaline geri dönün. Serotonin ve norepinefrin geri alımının ikili inhibisyonu, daha geniş bir semptom yelpazesini tedavi ederek diğer antidepresan ilaçlara göre avantajlar sağlayabilir.[1] Özellikle eşlik eden kronik veya nöropatik ağrı.[2]
SNRI'ler, SSRI'lar ve norepinefrin geri alım inhibitörleri (NRI'lar), ikinci nesil antidepresanlar. Son yirmi yılda, ikinci nesil antidepresanlar, basitçe birinci nesil antidepresanların yerini aldı. trisiklik antidepresanlar (TCA'lar) ve monoamin oksidaz inhibitörleri (MAOI'ler), geliştirilmiş tolerans ve güvenlik profilleri nedeniyle MDB tedavisinde tercih edilen ilaçlar olarak.[3]
İlaçlar

Amerika Birleşik Devletleri'nde FDA onaylı sekiz SNRI vardır, venlafaksin 1993 yılında geliştirilen ilk ilaçtır ve levomilnacipran 2013 yılında geliştirilen en son ilaçtır. İlaçlar diğer tıbbi kullanımlarına, kimyasal yapılarına, yan etkilerine ve etki.[4]
SNRI'ler için onay yılları:[4]
- 1993: Venlafaksin
- 1998: Sibutramin
- 2004: Duloksetin
- 2008: Desvenlafaksin
- 2009: Milnacipran
- 2013: Levomilnacipran
| İlaç tedavisi | Marka adı | FDA Endikasyonları | Onay Yılı | Kimyasal yapı | Notlar |
|---|---|---|---|---|---|
| Atomoksetin | Strattera | 2002 | 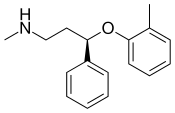 | Norepinefrin ağırlıklı bir SNRI'nin tedavisinde kullanılan DEHB ve etiket dışı, majör depresyon. 2002'de FDA tarafından onaylandı. Başlangıçta seçici olarak kabul edildi. norepinefrin geri alım inhibitörü, ancak daha sonra yapılan araştırmalar, serotoninin klinik dozajlarda geri alımını da önemli ölçüde engellediğini ortaya çıkardı.[6] | |
| Desvenlafaksin[7] | Pristiq Khedezla (ER) |
| 2007 |  | Venlafaksinin aktif metaboliti. Benzer şekilde çalıştığına inanılıyor, ancak bazı kanıtlar venlafaksin ve duloksetin ile karşılaştırıldığında daha düşük yanıt oranlarını gösteriyor. Mayıs 2008'de Wyeth tarafından tanıtıldı ve daha sonra onaylanan üçüncü SNRI oldu.[8] |
| Duloksetin[9] | Cymbalta Irenka |
| 2004 |  | Depresyon tedavisi için onaylandı ve nöropatik ağrı duloksetin, şiddetli alkol kullanımı veya kronik karaciğer hastalığı olan hastalarda kontrendikedir, çünkü duloksetin akut hastalığa yol açabilen bazı karaciğer enzimlerinin düzeylerini artırabilir. hepatit veya risk altındaki bazı hastalarda diğer hastalıklar. Şu anda, karaciğer hasarı riski, antidepresandan farklı olarak, yalnızca zaten risk altındaki hastalar için görünmektedir. nefazodon nadir de olsa sağlıklı hastalarda kendiliğinden karaciğer yetmezliğine neden olabilir.[13] Duloksetin ayrıca aşağıdakiler için onaylanmıştır: majör depresif bozukluk (MDD), genelleştirilmiş anksiyete bozukluğu (GAD), diyabetik nöropati, kronik kas-iskelet ağrısı, kronik dahil Kireçlenme ağrı ve kronik bel ağrısı.[11] Duloksetin ayrıca hepatik metabolizmaya uğrar ve hepatik sitokrom P450 enziminin inhibisyonuna neden olduğu gösterilmiştir. CYP 2D6.[14] Duloksetin, CYP 2D6 tarafından metabolize edilen diğer ilaçlarla birlikte alınmalıdır çünkü bu, potansiyel bir ilaç-ilaç etkileşimini hızlandırabilir.[14] |
| Levomilnacipran | Fetzima |
| 2013 | 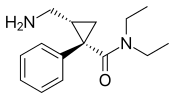 | Levorotasyon milnasipranın izomeri. Amerika Birleşik Devletleri ve Kanada'da depresyon tedavisi için geliştirilmekte olan ilaç, Temmuz 2013'te MDB tedavisi için FDA tarafından onaylandı. |
| Milnacipran | Ixel Savella Dürtücü |
| 1996 |  | Olarak gösterildi önemli ölçüde depresyon ve fibromiyalji tedavisinde etkilidir.[15] Gıda ve İlaç İdaresi (FDA), Ocak 2009'da Amerika Birleşik Devletleri'nde fibromiyaljinin tedavisi için milnasipran'ı onayladı, ancak şu anda bu ülkede depresyon için onaylanmadı. Milnacipran, birkaç yıldır Avrupa ve Asya'da ticari olarak mevcuttur. İlk olarak 1996'da Fransa'da tanıtıldı. |
| Sibutramin | Meridia | 1997 |  | Depresyon tedavisi için geliştirilen bir SNRI, yaygın bir şekilde bir iştah kesici için kilo kaybı amaçlar. Sibutramin, obezite tedavisi için 30 yıl sonra onaylanan ilk ilaç oldu.[17] Artmış kardiyovasküler olaylar ve felçlerle ilişkilendirilmiştir ve geri çekilmiş dahil olmak üzere birçok ülke ve bölgede pazardan Amerika Birleşik Devletleri 2010 yılında.[18] | |
| Tramadol | Ultram |
| 1977 | 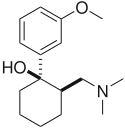 | Çift zayıf opioid ve SNRI. 1995 yılında FDA tarafından onaylandı, ancak Almanya 1977'den beri. İlaç akut ve kronik ağrıyı tedavi etmek için kullanılmaktadır. Bu amaç için özel olarak onaylanmasa da fibromiyalji tedavisinde etkinlik göstermiştir. İlaç ayrıca bir antidepresan olarak ve nöropatik ağrının tedavisi için araştırılmaktadır. Kimyasal yapı olarak venlafaksin ile ilgilidir. Bir opioid olması nedeniyle kötüye kullanım ve bağımlılık riski vardır, ancak diğer opioidlere (hidrokodon, oksikodon vb.) Kıyasla daha az kötüye kullanım potansiyeli, solunum depresyonu ve kabızlık vardır.[19] |
| Venlafaksin | Effexor | 1994 |  | İlk ve en sık kullanılan SNRI. Tarafından tanıtıldı Wyeth 1994'te. Venlafaksinin geri alım etkileri doza bağlıdır. Düşük dozlarda (<150 mg / gün), sadece serotonerjik geçişte etkilidir. Orta dozlarda (> 150 mg / gün), serotonerjik ve noradrenerjik sistemlere etki ederken, yüksek dozlarda (> 300 mg / gün) dopaminerjik nörotransmisyonu da etkiler.[22] Küçük dozlarda, venlafaksinin de tedavide etkili olduğu gösterilmiştir. vazomotor semptomlar (sıcak basmaları ve gece terlemeleri) menopozda olduğu kadar etkili olabilir. hormon değişim terapisi (HRT).[21] |
Tarih
1952'de, iproniazid, bir antimikobakteriyel ajan, sahip olduğu keşfedildi psikoaktif olası bir tedavi olarak araştırılan özellikler tüberküloz. Araştırmacılar, iproniazid verilen hastaların daha neşeli, daha iyimser ve fiziksel olarak daha aktif hale geldiğini belirtti. Gelişmesinden kısa bir süre sonra, iproniazid ve ilgili maddelerin serotoninin enzimatik parçalanmasını yavaşlattığı gösterilmiştir. dopamin ve enzimin inhibisyonu yoluyla norepinefrin monoamin oksidaz. Bu nedenle, bu tür ilaçlar monoamin oksidaz inhibitörleri veya MAOI'ler. Bu süre zarfında, belirgin şekilde farklı antidepresan ajanların geliştirilmesi de araştırıldı. İmipramin ilk klinik olarak yararlı oldu trisiklik antidepresan (TCA). İmipraminin çok sayıda nörotransmiter sistemini etkilediği ve norepinefrin ve serotonin geri alımını bloke ettiği bulunmuştur. sinaps bu nedenle bu nörotransmiterlerin seviyelerini arttırır. MAOI'lerin ve TCA'ların kullanımı, depresyon ama kullanımları nahoştu yan etkiler ve önemli güvenlik ve toksisite sorunlar.[23]
1960'lar ve 1970'ler boyunca katekolamin Duygu hipotezi ve depresyonla ilişkisi büyük ilgi gördü ve norepinefrin, serotonin ve dopamin gibi belirli nörotransmiterlerin azalmış seviyelerinin patogenez depresyon. Bu gelişmesine yol açtı fluoksetin, ilk SSRI. TCA'lar ve MAOI'lere kıyasla MDB'li hastalarda SSRI'ların gelişmiş güvenlik ve tolere edilebilirlik profili, depresyon tedavisinde bir başka önemli ilerlemeyi temsil ediyordu.[23]
1980'lerin sonlarından beri, SSRI'lar antidepresan ilaç pazarına hakim oldu. Günümüzde antidepresan ilaçlara daha geniş bir ilgi artmaktadır. etki mekanizmaları bu, etkililikte iyileştirmeler ve daha az yan etki sunabilir. 1993 yılında ABD pazarına yeni bir ilaç tanıtıldı. venlafaksin bir serotonin-norepinefrin geri alım inhibitörü.[20] Venlafaksin, yeni bir antidepresif madde sınıfında tanımlanan ilk bileşiktir. feniletilaminler. Bu maddeler, TCA ve diğer SSRI'larla ilgili değildir. Venlafaksin, serotonin, noradrenalinin nöronal geri alımını engeller ve daha az ölçüde, dopamin içinde Merkezi sinir sistemi. Diğer birkaç antidepresan ilacın aksine, venlafaksin, esas olarak müteakip bir norepinefrin geri alım inhibisyonuna bağlı olarak hızlı bir etki başlangıcına neden olabilir.[24] Şekil 1'deki zaman çizelgesine bakın.

Hareket mekanizması
Monoaminler, patofizyoloji depresyon. Norepinefrin ve serotonin gibi nörotransmiter konsantrasyonlarının yetersiz olması ve aşağı yönde değişikliklere yol açması nedeniyle semptomlar ortaya çıkabilir.[10][25] Depresyon ilaçları serotonin, norepinefrin ve dopaminin geçişini etkiler.[10] TCA'lar ve MAOI'ler gibi daha eski ve daha seçici olmayan antidepresanlar, geri alımını engeller veya metabolizma Beyindeki norepinefrin ve serotonin, daha yüksek nörotransmiter konsantrasyonlarına neden olur.[25] İkili etki mekanizmalarına sahip antidepresanlar, hem serotonin hem de norepinefrinin geri alımını inhibe eder ve bazı durumlarda, zayıf etkiyle dopamin geri alımını inhibe eder.[10]Antidepresanlar, muskarinik-kolinerjik, α gibi değişken nöronal reseptörleri etkiler.1- ve α2-adrenerjik ve H1-histaminerjik reseptörler ve sodyum kanalları içinde Kalp kası kalp iletiminin azalmasına yol açar ve kardiyotoksisite {kaynak gerekli}. Antidepresan ajanların seçiciliği, depresyon semptomlarını etkilediği düşünülen nörotransmiterlere dayanmaktadır.[26]Serotonin ve norepinefrinin geri alımını seçici olarak bloke eden ilaçlar, depresyonu etkili bir şekilde tedavi eder ve TCA'lardan daha iyi tolere edilir. TCA'lar çeşitli nörotransmiter reseptörleri üzerinde kapsamlı etkilere sahiptir, bu da tolere edilebilirlik eksikliğine ve toksisite riskinin artmasına neden olur.[27]
Trisiklik antidepresanlar

TCA'lar, ikili etki mekanizmasına sahip ilk ilaçlardı. Trisiklik ikincil amin antidepresanların etki mekanizması sadece kısmen anlaşılmıştır. TCA'ların norepinefrin geri alım taşıyıcıları ve serotonin geri alım taşıyıcıları üzerinde ikili inhibisyon etkileri vardır. Artan norepinefrin ve serotonin konsantrasyonları, bu taşıyıcı proteinlerin her ikisinin de inhibe edilmesiyle elde edilir. TCA'lar, SSRI'lara göre norepinefrin geri alım proteinleri için önemli ölçüde daha fazla afiniteye sahiptir. Bunun nedeni, ikincil amin TCA metabolitlerinin oluşumudur.[28][29]
Ek olarak, TCA'lar, adrenerjik reseptörler. Bu etkileşim, sinaptik yarıkların içinde veya yakınında norepinefrinin artan bulunabilirliği için kritik görünmektedir. İmipramin benzeri trisiklik antidepresanların eylemleri, norepinefrin taşınmasının inhibitörleri ve serotonin taşınmasının değişken blokajı olarak ilk ve sürekli eylemlerine karmaşık, ikincil uyarlamalara sahiptir.
Norepinefrin, postsinaptik α ve β adrenerjik reseptör alt tipleri ve presinaptik α ile etkileşime girer.2 otomatik alıcılar. Α2 reseptörler arasında presinaptik otomatik alıcılar noradrenerjik nöronların nörofizyolojik aktivitesini sınırlayan Merkezi sinir sistemi. Norepinefrin oluşumu, otomatik alıcılar hız sınırlayıcı enzim aracılığıyla tirozin hidroksilaz, azalmanın aracılık ettiği bir etki döngüsel AMP aracılı fosforilasyon -aktivasyonu enzim.[29] α2 reseptörler ayrıca hücre içi siklik AMP ekspresyonunun azalmasına neden olur ve bu da düz kas gevşeme veya azalmış salgı.[30]
TCA'lar bir olumsuz geribildirim presinaptik reseptörler üzerindeki etkileri yoluyla mekanizma. Azalmış nörotransmiter salınımı üzerindeki etkilerin olası bir açıklaması, reseptörler aktive ettikçe, nörotransmiter salımının inhibisyonunun meydana gelmesidir (voltaj kapılı Ca'nın baskılanması dahil)2+ G proteinine bağlı reseptörle işletilen K'nin akımları ve aktivasyonu+ akımlar). Bu tür mekanizma ile ajanların tekrar tekrar maruz kalması, nörotransmiter salınımının inhibisyonuna yol açar, ancak TCA'ların tekrar tekrar uygulanması, nihayetinde a2 reseptörler. duyarsızlaştırma Bu yanıtların% 90'ı endojen norepinefrine maruziyetin artmasına veya norepinefrin taşıma mekanizmalarının uzun süreli işgaline (allosterik etki yoluyla) bağlı olabilir. Adaptasyon, norepinefrinin presinaptik sentezinin ve salgılanmasının, sinaptik yarıklarda normal norepinefrin seviyelerine dönmesine veya hatta aşmasına izin verir. Genel olarak, TCA'lar tarafından indüklenen norepinefrin geri alımının inhibisyonu, nöron ateşleme oranlarının azalmasına yol açar (a2 oto alıcılar), metabolik aktivite ve nörotransmiterlerin salınımı.[29]
TCA'lar dopamin taşınmasını doğrudan engellemez, ancak dopamin taşınmasını dolaylı olarak engelleyerek dopaminerjik etkileri kolaylaştırabilir. beyin zarı.[29] Pek çok farklı reseptörü etkiledikleri için, TCA'lar yan etkilere, zayıf tolere edilebilirliğe ve artan toksisite riskine sahiptir.[27]
Seçici serotonin geri alım inhibitörleri
Seçici serotonin geri alım inhibitörleri (SSRI'lar) seçici olarak serotoninin geri alımını engeller ve yaygın olarak kullanılan bir antidepresan grubudur.[31] TCA'lara kıyasla artan reseptör seçiciliği ile, zayıf tolere edilebilirlik gibi istenmeyen etkiler önlenir.[29] Serotonin, adı verilen bir amino asitten sentezlenir. L-triptofan. Aktif taşımacılık sistem alımını düzenler triptofan karşısında Kan beyin bariyeri. Serotonerjik yollar beyinde iki ana şekilde sınıflandırılır: medial ve dorsal raphe'den yükselen projeksiyonlar ve beyindeki alçalan projeksiyonlar. kaudal raphe içine omurilik.
Seçici norepinefrin geri alım inhibitörleri
Noradrenerjik nöronlar, beyindeki iki ana bölgede bulunur. Bu bölgeler locus coeruleus ve yanal tegmental. SNRI'lerin uygulanmasıyla, sinaptik yarıkta artan norepinefrin konsantrasyonu nedeniyle lokus seruleus bölgesindeki nöronal aktivite indüklenir. Bu, aktivasyonuyla sonuçlanır α2 adrenerjik reseptörler,[25] tartışıldığı gibi, anlatıldığı gibi Önceden.
Tahliller, SNRI'lerin önemsiz bir mACh, α1 ve α2 adrenerjik veya H1 reseptörler.[26]
İkili serotonin ve norepinefrin geri alım inhibitörleri
İkili serotonin ve norepinefrin geri alım inhibisyonuna (SNRI'ler) sahip ajanlar bazen trisiklik olmayan serotonin ve norepinefrin geri alım inhibitörleri olarak adlandırılır. Klinik çalışmalar, hem norepinefrin hem de serotoninin sinaptik yarığındaki konsantrasyonu artıran bileşiklerin, depresyon tedavisinde tek etkili ajanlardan daha başarılı olduğunu göstermektedir, ancak veriler, SNRI'lerin depresyon için SSRI'lara göre daha etkili bir tedavi seçeneği olup olmadığı konusunda kesin değildir.[32][33][34] İkili yeniden alım inhibitörleri, TCA'lara kıyasla düşük yan etkilere sahip olan diğer nörotransmiterlerin nöronal reseptörlerinde düşük afiniteye sahiptir. Nontrisiklik antidepresanlar, tek başına SSRI'lara göre antidepresan yanıtta daha iyi etki ve etki başlangıç hızına sahiptir, bu da sinerjizmin antidepresan aktiviteye aracılık etmede etkili bir özellik olduğu izlenimini verir.
Trisiklik olmayan SNRI'ler, farmakokinetik, aktif metabolitlere metabolizma, inhibisyona dayanan birkaç önemli farklılığa sahiptir. CYP izoformlar, ilaç-ilaç etkileşimlerinin etkisi ve yarı ömür nontrisiklik SNRI'lerin.[28][35]
Etki mekanizmalarının tek bir aktif maddede kombinasyonu, psikofarmakoloji.[35]
Yapı aktivite ilişkisi (SAR)
Ariloksipropanamin iskele
Birkaç geri alım inhibitörü, bir ariloksipropanamin iskelesi içerir. Bu yapısal motif, biyojenik amin nakillerine yüksek afinite bağlanma potansiyeline sahiptir.[35] Bir ariloksipropanamin iskelesi içeren ilaçlar, ariloksi halkasının ikame modeline bağlı olan norepinefrin ve serotonin taşıyıcıları için seçicilik profiline sahiptir. Seçici NRI'lar ariloksi halkasının 2 'pozisyonunda bir ikame içerir, ancak SSRI'lar bir ikame ariloksi halkasının 4 'pozisyonunda. Atomoksetin, nisoksetin ve reboksetinin tümü 2 'konumunda bir ikame grubuna sahiptir ve seçici NRI'lardır, 4' konumunda bir ikame grubuna sahip bileşikler (fluoksetin ve paroksetin ) SSRI'lardır. Duloksetin, fenil grubu 2 've 3' pozisyonlarında kaynaşmıştır, bu nedenle ikili seçici norepinefrin ve serotonin geri alım engelleyici etkilere sahiptir ve her iki taşıyıcı için benzer potenslere sahiptir.[36] Doğası aromatik sübstitüent ayrıca, serotonin veya norepinefrin taşıyıcılarının inhibitörleri olarak bileşiklerin etkinliği ve seçiciliği üzerinde önemli bir etkiye sahiptir.[35]

Sikloalkanol etilamin iskele
Venlafaksin ve desvenlafaksin bir sikloalkanol etilamin iskelesi içerir. Elektron çekme doğasının arttırılması aromatik halka norepinefrin alımının daha güçlü bir inhibe edici etkisini sağlar ve serotonin taşıyıcısı üzerinde norepinefrin için seçiciliği geliştirir.[36] Sikloalkanol etilamin iskelesinin aromatik halkasında kloro, metoksi ve triflorometil ikame edicilerin etkileri test edildi. Sonuçlar, en güçlü elektron çekmenin m-triflorometil analoğu, norepinefrinin en güçlü inhibe edici etkisini ve serotonin alımına göre en fazla seçiciliği sergilemiştir.[36] WY-46824 piperazin içeren bir türev, norepinefrin ve dopamin geri alım inhibisyonu. Ek sentez ve testler, mükemmel seçicilik sergileyen ve depresyon, ağrı ve termoregülatör disfonksiyonun hayvan modellerinde etkili olan güçlü bir norepinefrin geri alım inhibitörü olan WAY-256805'i tanımladı.[37]

Milnacipran

Milnacipran yapısal olarak diğer SNRI'lardan farklıdır.[28] Taşıyıcı seviyesindeki milnasipran türevlerinin SAR değeri hala büyük ölçüde belirsizdir ve 1987'de bildirilen in vivo etkinliğe dayanmaktadır. Nikame grubu R'de milnasipran metilasyonu4 ve R5 norepinefrin ve serotonin aktivitesini azaltır.[38] İkame grupları R'de farklı ikincil amidler üzerine araştırmalar6 ve R7 π elektronlarının taşıyıcılar ve ligandlar arasındaki etkileşimde önemli bir rol oynadığını gösterdi. İkame R'deki bir fenil grubu6 norepinefrin taşıyıcıları üzerinde etki göstermiştir. R'deki ikame grupları6 ve R7 ile müttefik çift bağ, hem norepinefrin hem de serotonin taşıyıcıları üzerinde önemli ölçüde geliştirilmiş etki gösterdi.[38] Çalışmalar, ikame R'ye bir 2-metil grubu eklenmesinin3Norepinefrin ve serotonin taşıyıcılarındaki etki neredeyse ortadan kalktı. İkame grupları R'deki metil grupları1 ve R2 ayrıca norepinefrin ve serotonin taşıyıcılarındaki gücü ortadan kaldırır. Araştırmacılar, milnasipranın etil gruplarından birini bir alil kısmı ile değiştirmenin norepinefrin potensini artırdığını buldular.[39] farmakofor Milnasipran türevlerinin oranı hala büyük ölçüde belirsizdir.[38]
Milnasipranın yapısı, farmakoforunun önemli bir parçasıdır. Milnasipran cinsinden SAR'ın değiştirilmesi, stereokimya ve norepinefrin ve serotonin konsantrasyonunu etkiler. Milnacipran, bir Rasemik karışım. Milnasipranın etkileri, (1S,2R)-izomer ve fenil grubunun (1S,2R) -izomerin norepinefrin konsantrasyonu üzerinde olumsuz etkisi vardır.[39] Milnacipran düşük moleküler ağırlık Ve düşük lipofiliklik. Bu özelliklerinden dolayı milnasipran neredeyse ideal farmakokinetik insanlarda yüksek gibi biyoyararlanım, denekler arası düşük değişkenlik, sınırlı karaciğer enzim etkileşim, orta doku dağılımı ve oldukça uzun bir eliminasyon yarı ömrü. Milnacipran'ın ilaç-ilaç etkileşimi eksikliği sitokrom P450 Enzimlerin çekici bir özellik olduğu düşünülmektedir çünkü merkezi sinir sistemi ilaçlarının çoğu oldukça lipofiliktir ve esas olarak karaciğer enzimleri tarafından elimine edilir.[39]
SAR'ın gelecekteki gelişimi
Bir ariloksipropanamin iskelesinin uygulanması, bir dizi güçlü MAOI üretmiştir.[40] Duloksetinin geliştirilmesinden önce, ariloksipropanamin SAR'ın araştırılması, fluoksetin ve atomoksetinin tanımlanmasıyla sonuçlanmıştır. Aynı motif, reboksetinde sınırlandırıldığı yerde bulunabilir. morfolin halka sistemi. Reboksetindeki oksijenin yerini aldığı bazı çalışmalar yapılmıştır. kükürt ariltiyometil morfolin vermek için. Bazı ariltiyometil morfolin türevleri, güçlü serotonin ve norepinefrin geri alım inhibisyonu seviyelerini muhafaza eder. İkili serotonin ve norepinefrin geri alım inhibisyonu, ariltiyometil morfolin iskelesi için farklı enantiyomerlerde bulunur.[41] İkili serotonin ve norepinefrin geri alım inhibitör aktivitesine sahip olası ilaç adayları da piperazin, 3-amino-pirolidin ve benzilamin şablonlarından türetilmiştir.[42]
Klinik denemeler
Birkaç çalışma, serotonerjik ve noradrenerjik aktiviteyi birleştiren antidepresan ilaçların genellikle kendi başına serotonin geri alımına etki eden SSRI'lardan daha etkili olduğunu göstermiştir. Serotonerjik-noradrenerjik antidepresan ilaçlar, majör depresif bozukluğun (MDD) tedavisinde SSRI'lara kıyasla mütevazı bir etkinlik avantajına sahip olabilir,[43] ancak biraz daha az tolere edilir.[44] Spesifik MDB alt popülasyonlarında veya spesifik MDB semptomlarında, bu antidepresan ilaç sınıfları arasındaki olası etkililik farklılıklarını incelemek için daha fazla araştırmaya ihtiyaç vardır.
Klinik çalışmalardan elde edilen veriler, SNRI'lerin ağrı giderici özelliklere sahip olabileceğini göstermiştir. Merkezi sinir sistemindeki ağrı uyaranlarının algılanması ve iletilmesi tam olarak aydınlatılmamış olsa da, kapsamlı veriler ağrının modülasyonunda serotonin ve norepinefrinin rolünü desteklemektedir. İnsanlarda yapılan klinik araştırmalardan elde edilen bulgular, bu antidepresanların merkezi ve nöropatik ağrı koşullarında ağrıyı ve fonksiyonel bozukluğu azaltabileceğini göstermiştir. SNRI'lerin bu özelliği, diğer ağrı giderici ilaçların dozlarını azaltmak ve güvenlik sıklığını, sınırlı etkililiği ve tolere edilebilirlik sorunlarını azaltmak için kullanılabilir.[45]Klinik araştırma verileri, kısa süreli ve uzun süreli tedaviden sonra, YAB hastalarında SNRI duloksetinin ağrıyla ilişkili YAB semptomlarını azaltmada plasebodan önemli ölçüde daha etkili olduğunu göstermiştir. Bununla birlikte, bulgular, bu tür fiziksel ağrı semptomlarının nüks durumlarında yeniden ortaya çıktığını, bu da YAB hastalarında devam eden tedaviye ve eşzamanlı ağrılı fiziksel semptomlara işaret ettiğini göstermektedir.[46]
Belirteçler
SNRI'ler, aşağıdaki durumların tedavisi için test edilmiştir:
- Major depresif bozukluk (MDD)
- Travmatik stres bozukluğu sonrası (TSSB)
- Genelleştirilmiş anksiyete bozukluğu (GAD)
- Sosyal anksiyete bozukluğu (ÜZGÜN)
- Obsesif kompulsif bozukluk[47][48][49]
- Panik atak
- Nöropatik ağrı
- Fibromiyalji
- Kronik kas-iskelet ağrısı
Farmakoloji
Yönetim yolu
SNRI'ler, genellikle kapsüller veya tabletler şeklinde ağızdan verilir. İlaç seviyelerini etkilemeyen, ancak bazı yan etkilere yardımcı olabilecek SNRI'lerin sabah kahvaltı ile alınması tavsiye edilir.[50] Norepinefrin vücutta aktive edici etkilere sahiptir ve bu nedenle yatmadan alındığında bazı hastalarda uykusuzluğa neden olabilir.[51] SNRI'ler ayrıca genellikle hafif olan ve tedaviden birkaç hafta sonra kaybolan mide bulantısına da neden olabilir, ancak ilacı yiyecekle birlikte almak bunu hafifletmeye yardımcı olabilir.[52] İlaçlar genellikle sindirim sırasında vücuda yayılan ince kristal bir tozdur.
Dozaj
Dozajlar, söz konusu ilacın değişen potenslerinin yanı sıra her bir ilaç için çoklu kuvvetler nedeniyle kullanılan SNRI'ye bağlı olarak değişir.
Aksiyon modu
SNRI'ların en çok endike olduğu durum olan majör depresif bozukluğun esas olarak azalan serotonin seviyelerinden kaynaklandığı düşünülmektedir ve norepinefrin sinaptik yarıkta düzensiz sinyale neden oluyor. Göre monoamin hipotezi Monoamin nörotransmiterlerinin azalan konsantrasyonlarının depresif belirtilere yol açtığını öne süren depresyonun, aşağıdaki ilişkiler belirlendi: "Norepinefrin, anksiyete, dikkat ve yaşama ilginin yanı sıra uyanıklık ve enerji ile ilişkili olabilir; [eksikliği] anksiyeteye serotonin , takıntılar ve dürtüler ve dikkat, motivasyon, zevk ve ödül için dopamin ve yaşama ilgi. "[53] SNRI'ler şu şekilde çalışır: engelleyici yeniden alım nörotransmiterler serotonin ve norepinefrin. Bu artışla sonuçlanır hücre dışı serotonin ve norepinefrin konsantrasyonları ve sonuç olarak, nörotransmisyon. Venlafaksin, desvenlafaksin ve duloksetin de dahil olmak üzere çoğu SNRI, norepinefrine göre serotonin için birkaç kat daha seçicidir, milnasipran ise serotoninden üç kat daha fazla norepinefrin seçicidir. Bir antidepresanın etkili olabilmesi için norepinefrin seviyelerinin yükselmesinin gerekli olduğu düşünülmektedir. nöropatik ağrı, daha büyük olanla paylaşılan bir mülk trisiklik antidepresanlar (TCA'lar), ancak SSRI'larla değil.[54]
Son çalışmalar, depresyonun artan inflamatuar yanıtla bağlantılı olabileceğini göstermiştir.[55] bu nedenle SNRI'ler için ek bir mekanizma bulma girişimleri yapılmıştır. Çalışmalar, SNRI'lerin yanı sıra SSRI'ların üzerinde önemli antiinflamatuar etkiye sahip olduğunu göstermiştir. mikroglia[56] serotonin ve norepinefrin seviyeleri üzerindeki etkilerine ek olarak. Bu nedenle, daha önce anlaşılan mekanizma ile kombinasyon halinde hareket eden bu ilaçların ek bir mekanizmasının mevcut olması mümkündür. Bu bulguların arkasındaki sonuç, SNRI'lerin, beyin hasarını veya beynin şişmesinin bir sorun olduğu diğer herhangi bir hastalığı takiben potansiyel anti-enflamatuarlar olarak kullanılmasını önermektedir. Bununla birlikte, mekanizma ne olursa olsun, bu ilaçların endike oldukları hastalıkların tedavisinde etkinliği hem klinik hem de pratikte kanıtlanmıştır.[yanlış sentez? ]
Farmakodinamik
SNRI'lerin çoğu yan yana çalışır birincil metabolitler ve ikincil metabolitler serotonin, norepineferin ve marjinal miktarlarda dopamin geri alımını engellemek için. Örneğin, venlafaksin, birincil metabolitinin yanında çalışır. ÖBeyindeki serotonin ve norepinefrin geri alımını güçlü bir şekilde inhibe etmek için desmetilvenlafaksin. Kanıtlar ayrıca, dopamin ve norepineferinin, dopaminin norepinefrin geri alımıyla inaktivasyonuna bağlı olarak, birlikte taşıma şeklinde davrandığını da göstermektedir. ön korteks, beynin büyük ölçüde dopamin taşıyıcılarından yoksun bir bölgesi. SNRI'lerin bu etkisi, serotonin ve norepinefrin aktivitesindeki artışlara ek olarak, artmış dopamin nörotransmisyonu ile sonuçlanır.[57] Ayrıca, SNRI'ler son derece seçici oldukları için, diğer istenmeyen reseptörler üzerinde ölçülebilir etkileri yoktur. monoamin oksidaz inhibisyon.[58] Farmasötik testler, hem SNRI'lerin hem de SSRI'ların kullanımının önemli anti-inflamatuar etki oluşturabileceğini belirlemiştir. mikroglia aynı zamanda.[56][16][59][60][11][61]
Aktivite profilleri
| Bileşik | SERT | AĞ | ~ Oran (5-HT : NE) | ||
|---|---|---|---|---|---|
| Kben | IC50 | Kben | IC50 | ||
| Venlafaksin | 7.8 | 145 | 1,920 | 1420 | 30:1 |
| Des-venlafaksin | 40.2 | 47.3 | 558.4 | 531.3 | 14:1 |
| Duloksetin | 0.07 | 3.7 | 1.17 | 20 | 10:1 |
| Atomoksetin | 87[63] | 5.4 [63] | 0.06:1 (1:16) | ||
| Milnacipran | 8.44 | 151 | 22 | 68 | 1.6:1 |
| Levo-milnasipran | 11.2 | 19.0 | 92.2 | 10.5 | 1:2 |
| Tüm Kben ve IC50 değerler nM. 5-HT/NE oran IC'ye dayalı50 değerleri SERT ve AĞ.[62] | |||||
Farmakokinetik
Yarı ömrü venlafaksin yaklaşık 5 saattir ve günde bir kez dozlama ile kararlı durum konsantrasyonuna, aktif metaboliti desvenlafaksin daha uzun sürmesine rağmen yaklaşık 3 gün sonra ulaşılır.[60] Yarı ömrü desvenlafaksin yaklaşık 11 saattir ve kararlı durum konsantrasyonlarına 4 ila 5 gün sonra ulaşılır.[59] Yarı ömrü duloksetin yaklaşık 12 saattir (aralık: 8-17 saat) ve kararlı duruma yaklaşık 3 gün sonra ulaşılır.[11] Milnacipran yaklaşık 6 ila 8 saatlik bir yarı ömre sahiptir ve kararlı durum seviyelerine 36 ila 48 saat içinde ulaşılır.[61]
Kontrendikasyonlar
SNRI'ler, alan hastalarda kontrendikedir. MAOI'ler artan risk nedeniyle son iki hafta içinde serotonin sendromu hayati tehlike oluşturabilir.[65] Bir SNRI ile birleştirildiğinde artan serotonin sendromu riski nedeniyle kaçınılması gereken diğer ilaçlar ve maddeler şunlardır: antidepresanlar, anti-konvülzanlar, analjezikler, antiemetik ajanlar, anti-migren ilaçları, metilen mavisi, linezolid, Lityum, St.John's worts, coşku, ve l.s.d..[65] Serotonin sendromunun belirtileri ve semptomları şunları içerir: hipertermi, sertlik, miyoklonus, değişen yaşamsal belirtilerle birlikte otonomik istikrarsızlık ve deliryum ve komaya ilerleyen aşırı ajitasyon içeren zihinsel durum değişiklikleri.[11]
Artan etkiler nedeniyle norepinefrin seviyeleri ve dolayısıyla daha yüksek noradrenerjik aktivite, önceden var olan hipertansiyon, SNRI'larla tedaviden önce kontrol edilmeli ve tedavi boyunca kan basıncı periyodik olarak izlenmelidir.[66] Duloksetin ayrıca karaciğer yetmezliği vakaları ile ilişkilendirilmiştir ve kronik alkol kullanımı veya karaciğer hastalığı olan hastalara reçete edilmemelidir. Çalışmalar, Duloxetine'nin artabileceğini bulmuştur karaciğer fonksiyon testleri normal üst sınırlarının üç katı.[67] Muzdarip hastalar koroner arter hastalığı SNRI'lerin kullanımına dikkat etmelidir.[68] Ayrıca, bazı SNRI'ların obezite üzerindeki etkileri nedeniyle, Anoreksiya nervoza veya bulimia SNRI'ler reçete edilmemelidir.[16] Duloksetin ve milnasipran da kontrol edilemeyen dar açılı glokomlu hastalarda kontrendikedir, çünkü bunların insidansını arttırdığı gösterilmiştir. midriyazis.[11][61]
Yan etkiler
SNRI'ler ve SSRI'lar serotonin seviyelerini yükseltmek için benzer şekillerde hareket ettiklerinden, değişen derecelerde de olsa birçok yan etkiyi paylaşırlar. En yaygın yan etkiler mide bulantısı / kusma, terleme, iştahsızlık, baş dönmesi, baş ağrısı, intihar düşüncelerinde artış ve cinsel işlev bozukluğudur.[69] Norepinefrin seviyelerinin yükselmesi bazen anksiyeteye, nabızın hafifçe yükselmesine ve yüksek kan basıncına neden olabilir. Bununla birlikte, reboksetin ve desipramin gibi norepinefrin seçici antidepresanlar, anksiyete bozukluklarını başarılı bir şekilde tedavi etmiştir.[70] Hipertansiyon ve kalp hastalığı riski taşıyan kişiler kan basıncını izlemelidir.[16][59][60][11][61] Mide rahatsızlığının yan etkileri, SNRI'leri yiyecekle birlikte alarak azaltılabilir.
Cinsel İşlev Bozukluğu
SNRI'ler, SSRI'lara benzer şekilde, erektil disfonksiyon, azalmış libido, cinsel işlev bozukluğu gibi çeşitli cinsel işlev bozukluğuna neden olabilir. Anhedonia, ve anorgazmi.[71][72][73] İki yaygın cinsel yan etki, cinsiyete olan ilginin azalması (libido) ve doruğa ulaşma güçlüğüdür (anorgazmi ), SSRI'lara kıyasla SNRI'lerde genellikle biraz daha hafiftir.[74] Cinsel işlev bozukluğunu yönetmek için araştırmalar, cinsel ilişkiye geçmenin veya Bupropion veya ekleyerek PDE5 İnhibitörü cinsel işlev bozukluğunun semptomlarında azalma var.[75] Çalışmalar, PDE5 İnhibitörlerinin, örneğin Sildenafil (Viagra), tadalafil (Cialis), vardenafil (Levitra) ve Avanafil (Stendra), erkeklerde kadınlardan daha etkili olduğu gösterilse de, bazen erektil disfonksiyon da dahil olmak üzere cinsel işlev bozukluğunu azaltmaya yardımcı oldu.[75]
Serotonin Sendromu
SNRI'lerin ciddi ancak nadir görülen bir yan etkisi, vücuttaki aşırı serotoninin neden olduğu serotonin sendromudur. Serotonin sendromuna, SSRI'lar veya SNRI'ler gibi birden fazla serotonerjik ilaç alınması neden olabilir. Serotonin sendromuna katkıda bulunan diğer ilaçlar arasında MAO inhibitörleri, linezolid, tedizolid, metilen mavisi, prokarbazin, amfetaminler, klomipramin ve daha fazlası bulunur.[76] Serotonin sendromunun erken belirtileri mide bulantısı, kusma, ishal, terleme, ajitasyon, kafa karışıklığı, kas sertliği, genişlemiş göz bebekleri, hipertermi, sertlik ve tüylerim diken diken olabilir. Daha şiddetli semptomlar arasında ateş, nöbetler, düzensiz kalp atışı, deliryum ve koma bulunur.[77][78][11] Belirti veya semptomlar ortaya çıkarsa, serotonerjik ajanlarla tedaviyi derhal bırakın.[77] Bir MAO inhibitörü kullanmadan önce serotonerjik ajanın 4 ila 5 yarılanma ömrünün yıkanması önerilir.[79]
Kanama
Bazı çalışmalar, trombosit agregasyonunun bozulması ve trombosit serotonin düzeylerinin tükenmesi nedeniyle özellikle venlafaksin olmak üzere üst gastrointestinal kanama riskleri olduğunu göstermektedir.[80][81] SSRI'lara benzer şekilde, SNRI'ler ile etkileşime girebilir antikoagülanlar, sevmek warfarin. Şu anda, SSRI'ların SNRI'lardan daha yüksek kanama riskine sahip olduğuna dair daha fazla kanıt vardır.[80] Çalışmalar, yüksek dozlarda SNRI'ler veya SSRI'lar kullanılırken dikkatli olunmasını önermektedir. steroid olmayan antiinflamatuar ilaçlar (NSAID'ler), gibi ibuprofen veya naproksen üst GI kanama riskinin artması nedeniyle.[34]
Önlemler
Bir SNRI rejiminin başlatılması
Norepinefrin ve serotonin geri alım inhibisyonundan üretilen noradrenerjik aktivitede aşırı değişiklikler nedeniyle, SNRI rejimine yeni başlayan hastalara, vücudun ilacın etkilerine alışmasına izin vermek için genellikle beklenen son dozlarından daha düşük dozlar verilir. Hasta, herhangi bir yan etki olmaksızın düşük dozlarda devam ettiğinden, hasta, zararlı yan etkiler olmaksızın semptomlarda iyileşme görene kadar doz aşamalı olarak artırılır.[82]
Kesilme sendromu
SSRI'larda olduğu gibi, bir SNRI'nin aniden kesilmesi genellikle para çekme veya "kesilme sendromu ", durumları içerebilir kaygı ve diğer semptomlar. Bu nedenle, bir SNRI'yi sonlandırmak isteyen kullanıcıların, bir profesyonel gözetiminde dozu yavaşça azaltmaları önerilir. Kesilme sendromunun belirgin şekilde daha kötü olduğu bildirilmiştir. venlafaksin diğer SNRI'larla karşılaştırıldığında. Gibi, gibi Tramadol venlafaksin ile ilgilidir, aynı koşullar geçerlidir.[83] Bu muhtemelen venlafaksinin nispeten kısa olmasından kaynaklanmaktadır. yarı ömür ve bu nedenle, durdurulduğunda hızlı temizlik. Bazı durumlarda, kesilme semptomlarını azaltmak için venlafaksin'den uzun etkili bir SSRI olan fluoksetine geçiş ve ardından fluoksetinin azaltılması önerilebilir.[84][85] Bir SNRI'nin aniden kesilmesinden çekilmenin belirtileri ve semptomları arasında baş dönmesi, anksiyete, uykusuzluk, mide bulantısı, terleme ve uyuşukluk ve halsizlik gibi grip benzeri semptomlar bulunur.[86]
Aşırı doz
Nedenleri
SNRI'larda aşırı doz, ilaç kombinasyonlarından veya ilacın kendisinin aşırı miktarlarından kaynaklanabilir. Venlafaksin doz aşımında duloksetin veya SSRI'lardan marjinal olarak daha toksiktir.[16][59][60][11][61][87] Birden fazla serotonerjik ajan veya etkileşen ajan alan hastalarda doz aşımı riski artar.
Semptomlar
Karma ilaç etkileşimi veya tek başına ilaç olsun, SNRI aşırı dozunun semptomları, alınan ilacın miktarına ve bireylerin SNRI tedavisine duyarlılığına bağlı olarak yoğunluk ve insidans açısından farklılık gösterir. Olası semptomlar şunları içerebilir:[11]
Yönetim
Overdose is usually treated symptomatically, especially in the case of serotonin syndrome, which requires treatment with cyproheptadine and temperature control based on the progression of the serotonin toxicity.[88] Patients are often monitored for vitals and airways cleared to ensure that they are receiving adequate levels of oxygen. Another option is to use activated carbon in the GI tract in order to absorb excess neurotransmitter.[11] It is important to consider drug interactions when dealing with overdose patients, as separate symptoms can arise.
Comparison to SSRIs
Because SNRIs were developed more recently than SSRIs, there are relatively few of them. However, the SNRIs are among the most widely used antidepressants today. In 2009, Cymbalta and Effexor were the 11th- and 12th-most-prescribed branded drugs in the United States, respectively. This translates to the 2nd- and 3rd-most-common antidepressants, behind Lexapro (essitalopram ), an SSRI.[89] In some studies, SNRIs demonstrated slightly higher antidepressant efficacy than the SSRIs (response rates 63.6% versus 59.3%).[43] However, in one study essitalopram had a superior efficacy profile to venlafaxine.[90]
Özel popülasyonlar
Gebelik
Currently, no antidepressants are FDA approved during pregnancy. All SSRIs and SNRIs are Category C, except paroxetine, which is Category D since it has shown association with congenital heart disorders.[91] Use of antidepressants during pregnancy may result in fetus abnormalities affecting functional development of the brain and behavior.[91] Untreated depression may also affect birth outcomes, so it is recommended to discuss options with a provider to weigh the risks and benefits.
Pediatri
SSRIs and SNRIs have been shown to be effective in treating major depressive disorder and anxiety in pediatric populations.[92] However, there is a risk of increased suicidality in pediatric populations for treatment of major depressive disorder, especially with venlafaxine.[92] Fluoxetine is the only antidepressant that is approved for child/adolescent major depressive disorder.[93]
Geriatri
Most antidepressants, including SNRIs, are safe and effective in the geriatric population. Decisions are often based on co-morbid conditions, drug interactions, and patient tolerance. Due to differences in body composition and metabolism, starting doses are often half that of the recommended dose for younger adults.[94]
Ayrıca bakınız
- Monoamin geri alım inhibitörü
- List of antidepressants
- Serotonin salıcı ajan
- Selective Serotonin Reuptake Inhibitor (SSRI)
- Uyuşturucu yoksunluğu
- Serotonin sendromu
- Cinsel işlev bozukluğu
Referanslar
- ^ Cashman JR, Ghirmai S (October 2009). "Inhibition of serotonin and norepinephrine reuptake and inhibition of phosphodiesterase by multi-target inhibitors as potential agents for depression". Biyorganik ve Tıbbi Kimya. 17 (19): 6890–7. doi:10.1016/j.bmc.2009.08.025. PMID 19740668.
- ^ Wright, Megan E.; Rizzolo, Denise (March 2017). "An update on the pharmacologic management and treatment of neuropathic pain". Journal of the American Academy of PAs. 30 (3): 13–17. doi:10.1097/01.JAA.0000512228.23432.f7. ISSN 1547-1896. PMID 28151738.
- ^ Spina E, Santoro V, D'Arrigo C (Temmuz 2008). "İkinci kuşak antidepresanlarla klinik olarak ilgili farmakokinetik ilaç etkileşimleri: bir güncelleme". Clinical Therapeutics. 30 (7): 1206–27. doi:10.1016 / S0149-2918 (08) 80047-1. PMID 18691982.
- ^ a b Hillhouse TM, Porter JH (February 2015). "A brief history of the development of antidepressant drugs: from monoamines to glutamate". Deneysel ve Klinik Psikofarmakoloji. 23 (1): 1–21. doi:10.1037/a0038550. PMC 4428540. PMID 25643025.
- ^ "Strattera (atomoxetine) Capsules for Oral Use. Full Prescribing Information" (PDF). Lilly USA, LLC, Indianapolis, IN 46285, USA. Alındı 29 Ağustos 2016.
- ^ Ding YS, Naganawa M, Gallezot JD, Nabulsi N, Lin SF, Ropchan J, et al. (Şubat 2014). "Clinical doses of atomoxetine significantly occupy both norepinephrine and serotonin transports: Implications on treatment of depression and ADHD". NeuroImage. 86: 164–71. doi:10.1016/j.neuroimage.2013.08.001. PMID 23933039.
- ^ a b Deecher DC, Beyer CE, Johnston G, Bray J, Shah S, Abou-Gharbia M, Andree TH (August 2006). "Desvenlafaxine succinate: A new serotonin and norepinephrine reuptake inhibitor". The Journal of Pharmacology and Experimental Therapeutics. 318 (2): 657–65. doi:10.1124/jpet.106.103382. PMID 16675639.
- ^ a b Perry R, Cassagnol M (June 2009). "Desvenlafaxine: a new serotonin-norepinephrine reuptake inhibitor for the treatment of adults with major depressive disorder". Clinical Therapeutics. 31 Pt 1 (1): 1374–404. doi:10.1016/j.clinthera.2009.07.012. PMID 19698900.
- ^ Iyengar S, Webster AA, Hemrick-Luecke SK, Xu JY, Simmons RM (November 2004). "Efficacy of duloxetine, a potent and balanced serotonin-norepinephrine reuptake inhibitor in persistent pain models in rats". The Journal of Pharmacology and Experimental Therapeutics. 311 (2): 576–84. doi:10.1124/jpet.104.070656. PMID 15254142.
- ^ a b c d Hunziker ME, Suehs BT, Bettinger TL, Crismon ML (August 2005). "Duloxetine hydrochloride: a new dual-acting medication for the treatment of major depressive disorder". Clinical Therapeutics. 27 (8): 1126–43. doi:10.1016/j.clinthera.2005.08.010. PMID 16199241.
- ^ a b c d e f g h ben j k "Cymbalta (duloxetine delayed-release) Capsules for Oral Use. Full Prescribing Information" (PDF). Lilly USA, LLC, Indianapolis, IN 46285, USA. Alındı 29 Ağustos 2016.
- ^ "Yentreve (duloxetine hydrochloride) Hard Gastro-Resistant Capsules. Summary of Product Characteristics" (PDF). Avrupa İlaç Ajansı. Alındı 29 Ağustos 2016.
- ^ "Nefazodone Hydrochloride Tablets. Full Prescribing Information". DailyMed. Teva Pharmaceuticals USA, Inc. North Wales, PA 19454. September 2015. Alındı 2 Eylül 2016.
- ^ a b Frampton JE, Plosker GL (2007). "Duloxetine: a review of its use in the treatment of major depressive disorder". CNS İlaçları. 21 (7): 581–609. doi:10.2165/00023210-200721070-00004. PMID 17579500.
- ^ a b Morishita S, Arita S (February 2003). "The clinical use of milnacipran for depression". Avrupa Psikiyatrisi. 18 (1): 34–5. doi:10.1016/S0924-9338(02)00003-2. PMID 12648895.
- ^ a b c d e "Meridia (sibutramine hydrochloride monohydrate) Capsules C-IV. Full Prescribing Information (archived label)". Abbott Laboratories, North Chicago, IL 60064, USA. Alındı 2 Eylül 2016.
- ^ Luque CA, Rey JA (April 2002). "The discovery and status of sibutramine as an anti-obesity drug". Avrupa Farmakoloji Dergisi. 440 (2–3): 119–28. doi:10.1016/S0014-2999(02)01423-1. PMID 12007530.
- ^ Rockoff JD, Dooren JC (October 8, 2010). "Abbott Pulls Diet Drug Meridia Off US Shelves". Wall Street Journal. Alındı 8 Ekim 2010.
- ^ Keating GM (2006). "Tramadol sustained-release capsules". İlaçlar. 66 (2): 223–30. doi:10.2165/00003495-200666020-00006. PMID 16451094.
- ^ a b Gutierrez MA, Stimmel GL, Aiso JY (August 2003). "Venlafaxine: a 2003 update". Clinical Therapeutics. 25 (8): 2138–54. doi:10.1016/s0149-2918(03)80210-2. PMID 14512125.
- ^ a b Joffe H, Guthrie KA, LaCroix AZ, Reed SD, Ensrud KE, Manson JE, et al. (Temmuz 2014). "Low-dose estradiol and the serotonin-norepinephrine reuptake inhibitor venlafaxine for vasomotor symptoms: a randomized clinical trial". JAMA Dahiliye. 174 (7): 1058–66. doi:10.1001/jamainternmed.2014.1891. PMC 4179877. PMID 24861828.
- ^ Redrobe JP, Bourin M, Colombel MC, Baker GB (July 1998). "Dose-dependent noradrenergic and serotonergic properties of venlafaxine in animal models indicative of antidepressant activity". Psikofarmakoloji. 138 (1): 1–8. doi:10.1007/s002130050638. PMID 9694520.
- ^ a b Lieberman JA (2003). "History of the Use of Antidepressants in Primary Care" (PDF). Primary Care Companion J Clin Psychiatry. 5 (S7): 6–10.
- ^ Ruelas EG, Diaz-Martinez A, Ruiz RM, Study TV, Group C (1997). "An open assessment of the acceptability, efficacy, and tolerance of venlafaxine in usual care settings". Current Therapeutic Research. 58 (9): 609–630. doi:10.1016/S0011-393X(97)80088-4.
- ^ a b c Grandoso L, Pineda J, Ugedo L (May 2004). "Comparative study of the effects of desipramine and reboxetine on locus coeruleus neurons in rat brain slices". Nörofarmakoloji. 46 (6): 815–23. doi:10.1016/j.neuropharm.2003.11.033. PMID 15033341.
- ^ a b Brunello N, Mendlewicz J, Kasper S, Leonard B, Montgomery S, Nelson J, et al. (October 2002). "The role of noradrenaline and selective noradrenaline reuptake inhibition in depression" (PDF). Avrupa Nöropsikofarmakoloji. 12 (5): 461–75. doi:10.1016/s0924-977x(02)00057-3. PMID 12208564.
- ^ a b Stahl SM, Grady MM, Moret C, Briley M (September 2005). "SNRIs: their pharmacology, clinical efficacy, and tolerability in comparison with other classes of antidepressants". CNS Spektrumları. 10 (9): 732–47. doi:10.1017/S1092852900019726. PMID 16142213.
- ^ a b c Lemke TL, Williams DA, Roche VF, Zito SW (2008). Foye´s principles of medicinal chemistry (6. baskı). USA: Lippincott Williams & Wilkins. pp. 547–67, 581–582.
- ^ a b c d e Brunton, L.L.; Lazo, J.S.; Parker, K.L., eds. (2006). Goodman & Gilman's: The Pharmacological Basis of Therapeutics (11 ed.). New York: McGraw-Hill.
- ^ Silverthorn, D.U., ed. (2007). İnsan fizyolojisi (4 ed.). San Francisco: Pearson. s. 383–384.
- ^ Nutt DJ, Forshall S, Bell C, Rich A, Sandford J, Nash J, Argyropoulos S (July 1999). "Mechanisms of action of selective serotonin reuptake inhibitors in the treatment of psychiatric disorders". Avrupa Nöropsikofarmakoloji. 9 Suppl 3: S81-6. doi:10.1016/S0924-977X(99)00030-9. PMID 10523062.
- ^ Santarsieri, Daniel; Schwartz, Thomas L (2015-10-08). "Antidepressant efficacy and side-effect burden: a quick guide for clinicians". Drugs in Context. 4: 212290. doi:10.7573/dic.212290. ISSN 1745-1981. PMC 4630974. PMID 26576188.
- ^ Clevenger, Steven S.; Malhotra, Devvrat; Dang, Jonathan; Vanle, Brigitte; IsHak, Waguih William (2018). "The role of selective serotonin reuptake inhibitors in preventing relapse of major depressive disorder". Therapeutic Advances in Psychopharmacology. 8 (1): 49–58. doi:10.1177/2045125317737264. ISSN 2045-1253. PMC 5761909. PMID 29344343.
- ^ a b Zeind, Caroline; Carvalho (2018). Applied Therapeutics: The Clinical Use of Drugs, 11e. Wolters Kluwer. pp. 1813–1833. ISBN 9781496318299.
- ^ a b c d Boot J, Cases M, Clark BP, Findlay J, Gallagher PT, Hayhurst L, et al. (Şubat 2005). "Discovery and structure-activity relationships of novel selective norepinephrine and dual serotonin/norepinephrine reuptake inhibitors". Biyorganik ve Tıbbi Kimya Mektupları. 15 (3): 699–703. doi:10.1016/j.bmcl.2004.11.025. PMID 15664840.
- ^ a b c Mahaney PE, Vu AT, McComas CC, Zhang P, Nogle LM, Watts WL, et al. (Aralık 2006). "Synthesis and activity of a new class of dual acting norepinephrine and serotonin reuptake inhibitors: 3-(1H-indol-1-yl)-3-arylpropan-1-amines". Biyorganik ve Tıbbi Kimya. 14 (24): 8455–66. doi:10.1016/j.bmc.2006.08.039. PMID 16973367.
- ^ Mahaney PE, Gavrin LK, Trybulski EJ, Stack GP, Vu TA, Cohn ST, et al. (Temmuz 2008). "Structure-activity relationships of the cycloalkanol ethylamine scaffold: discovery of selective norepinephrine reuptake inhibitors". Tıbbi Kimya Dergisi. 51 (13): 4038–49. doi:10.1021/jm8002262. PMID 18557608.
- ^ a b c Chen C, Dyck B, Fleck BA, Foster AC, Grey J, Jovic F, et al. (Şubat 2008). "Studies on the SAR and pharmacophore of milnacipran derivatives as monoamine transporter inhibitors". Biyorganik ve Tıbbi Kimya Mektupları. 18 (4): 1346–9. doi:10.1016/j.bmcl.2008.01.011. PMID 18207394.
- ^ a b c Tamiya J, Dyck B, Zhang M, Phan K, Fleck BA, Aparicio A, et al. (Haziran 2008). "Identification of 1S,2R-milnacipran analogs as potent norepinephrine and serotonin transporter inhibitors". Biyorganik ve Tıbbi Kimya Mektupları. 18 (11): 3328–32. doi:10.1016/j.bmcl.2008.04.025. PMID 18445525.
- ^ Vu AT, Cohn ST, Terefenko EA, Moore WJ, Zhang P, Mahaney PE, et al. (Mayıs 2009). "3-(Arylamino)-3-phenylpropan-2-olamines as a new series of dual norepinephrine and serotonin reuptake inhibitors". Biyorganik ve Tıbbi Kimya Mektupları. 19 (9): 2464–7. doi:10.1016/j.bmcl.2009.03.054. PMID 19329313.
- ^ Boot JR, Brace G, Delatour CL, Dezutter N, Fairhurst J, Findlay J, et al. (Kasım 2004). "Benzothienyloxy phenylpropanamines, novel dual inhibitors of serotonin and norepinephrine reuptake". Biyorganik ve Tıbbi Kimya Mektupları. 14 (21): 5395–9. doi:10.1016/j.bmcl.2004.08.005. PMID 15454233.
- ^ Fish PV, Deur C, Gan X, Greene K, Hoople D, Mackenny M, et al. (Nisan 2008). "Design and synthesis of morpholine derivatives. SAR for dual serotonin & noradrenaline reuptake inhibition". Biyorganik ve Tıbbi Kimya Mektupları. 18 (8): 2562–6. doi:10.1016/j.bmcl.2008.03.050. PMID 18387300.
- ^ a b Papakostas GI, Thase ME, Fava M, Nelson JC, Shelton RC (December 2007). "Are antidepressant drugs that combine serotonergic and noradrenergic mechanisms of action more effective than the selective serotonin reuptake inhibitors in treating major depressive disorder? A meta-analysis of studies of newer agents". Biyolojik Psikiyatri. 62 (11): 1217–27. doi:10.1016/j.biopsych.2007.03.027. PMID 17588546.
- ^ Nemeroff CB, Thase ME (2007). "A double-blind, placebo-controlled comparison of venlafaxine and fluoxetine treatment in depressed outpatients". Psikiyatrik Araştırmalar Dergisi. 41 (3–4): 351–9. doi:10.1016/j.jpsychires.2005.07.009. PMID 16165158.
- ^ Marks DM, Shah MJ, Patkar AA, Masand PS, Park GY, Pae CU (December 2009). "Serotonin-norepinephrine reuptake inhibitors for pain control: premise and promise". Güncel Nörofarmakoloji. 7 (4): 331–6. doi:10.2174/157015909790031201. PMC 2811866. PMID 20514212.
- ^ Beesdo K, Hartford J, Russell J, Spann M, Ball S, Wittchen HU (December 2009). "The short- and long-term effect of duloxetine on painful physical symptoms in patients with generalized anxiety disorder: results from three clinical trials". Anksiyete Bozuklukları Dergisi. 23 (8): 1064–71. doi:10.1016/j.janxdis.2009.07.008. PMID 19643572.
- ^ "International OCD Foundation | Medications for OCD". Uluslararası OKB Vakfı. Alındı 2020-04-18.
- ^ Publishing, Harvard Health. "Ask Dr. Rob about OCD". Harvard Sağlık. Alındı 2020-04-18.
- ^ Sansone, Randy A.; Sansone, Lori A. (2011). "SNRIs Pharmacological Alternatives for the Treatment of Obsessive Compulsive Disorder?". Klinik Nörobilimde Yenilikler. 8 (6): 10–14. ISSN 2158-8333. PMC 3140892. PMID 21779536.
- ^ Troy, S. M.; Parker, V. P.; Hicks, D. R.; Pollack, G. M.; Chiang, S. T. (October 1997). "Pharmacokinetics and effect of food on the bioavailability of orally administered venlafaxine". Journal of Clinical Pharmacology. 37 (10): 954–961. doi:10.1002/j.1552-4604.1997.tb04270.x. ISSN 0091-2700. PMID 9505987.
- ^ Wichniak A, Wierzbicka A, Walęcka M, Jernajczyk W (August 2017). "Effects of Antidepressants on Sleep". Güncel Psikiyatri Raporları. 19 (9): 63. doi:10.1007/s11920-017-0816-4. PMC 5548844. PMID 28791566.
- ^ "Helpful for chronic pain in addition to depression". Mayo Kliniği. Alındı 2019-10-24.
- ^ Nutt DJ (2008). "Relationship of neurotransmitters to the symptoms of major depressive disorder". Klinik Psikiyatri Dergisi. 69 Suppl E1: 4–7. PMID 18494537.
- ^ Sindrup SH, Otto M, Finnerup NB, Jensen TS (June 2005). "Antidepressants in the treatment of neuropathic pain". Temel ve Klinik Farmakoloji ve Toksikoloji. 96 (6): 399–409. doi:10.1111/j.1742-7843.2005.pto_96696601.x. PMID 15910402.
- ^ Shelton RC, Miller AH (2011). "Inflammation in depression: is adiposity a cause?". Klinik Sinirbilimde Diyaloglar. 13 (1): 41–53. PMC 3181969. PMID 21485745.
- ^ a b Tynan RJ, Weidenhofer J, Hinwood M, Cairns MJ, Day TA, Walker FR (March 2012). "A comparative examination of the anti-inflammatory effects of SSRI and SNRI antidepressants on LPS stimulated microglia". Beyin, Davranış ve Bağışıklık. 26 (3): 469–79. doi:10.1016/j.bbi.2011.12.011. PMID 22251606.
- ^ http://stahlonline.cambridge.org/prescribers_drug.jsf?page=9781107675025c127.html.therapeutics&name=Venlafaxine&title=Therapeutics
- ^ Lambert O, Bourin M (November 2002). "SNRIs: mechanism of action and clinical features". Nöroterapötiklerin Uzman Değerlendirmesi. 2 (6): 849–58. doi:10.1586/14737175.2.6.849. PMID 19810918.
- ^ a b c d "Pristiq (desvenlafaxine) Extended-Release Tablets, for Oral Use. Full Prescribing Information". Wyeth Pharmaceuticals, Inc. A subsidiary of Pfizer, Inc. Philadelphia, PA 19101. July 2016. Alındı 2 Eylül 2016.
- ^ a b c d "Effexor XR (venlafaxine) Extended-Release Capsules. Full Prescribing Information". Wyeth Pharmaceuticals, Inc. A subsidiary of Pfizer, Inc. Philadelphia, PA 19101. August 2015. Alındı 2 Eylül 2016.
- ^ a b c d e "Savella (milnacipran HCl) Tablets. Full Prescribing Information". Allergan USA, Inc. Irvine, CA 92612. August 2016. Alındı 2 Eylül 2016.
- ^ a b Raouf M, Glogowski AJ, Bettinger JJ, Fudin J (August 2017). "Serotonin-norepinephrine reuptake inhibitors and the influence of binding affinity (Ki) on analgesia". Klinik Eczacılık ve Terapötikler Dergisi. 42 (4): 513–517. doi:10.1111/jcpt.12534. PMID 28503727.
- ^ a b c Upadhyaya HP, Desaiah D, Schuh KJ, Bymaster FP, Kallman MJ, Clarke DO, et al. (Mart 2013). "A review of the abuse potential assessment of atomoxetine: a nonstimulant medication for attention-deficit/hyperactivity disorder". Psikofarmakoloji. Springer Nature. 226 (2): 189–200. doi:10.1007/s00213-013-2986-z. PMC 3579642. PMID 23397050.
- ^ Roth BL, Driscol J (Dec 2012). "PDSP Kben Veri tabanı". Psikoaktif İlaç Tarama Programı (PDSP). Chapel Hill'deki North Carolina Üniversitesi ve Amerika Birleşik Devletleri Ulusal Ruh Sağlığı Enstitüsü. Alındı 7 Temmuz 2018.
- ^ a b Boyer EW, Shannon M (March 2005). "The serotonin syndrome". New England Tıp Dergisi. 352 (11): 1112–20. doi:10.1056/NEJMra041867. PMID 15784664.
- ^ Zhong, Zhuoyuan; Wang, Limin; Wen, Xiaojun; Liu, Yunyun; Fan, Yafei; Liu, Zhonglin (2017-11-07). "A meta-analysis of effects of selective serotonin reuptake inhibitors on blood pressure in depression treatment: outcomes from placebo and serotonin and noradrenaline reuptake inhibitor controlled trials". Nöropsikiyatrik Hastalık ve Tedavi. 13: 2781–2796. doi:10.2147/NDT.S141832. ISSN 1176-6328. PMC 5683798. PMID 29158677.
- ^ McIntyre RS et al. The hepatic safety profile of duloxetine: a review. Expert Opin Drug Metab Toxicol. 2008;4(3):281–285.
- ^ Mladěnka, Přemysl; Applová, Lenka; Patočka, Jiří; Costa, Vera Marisa; Remiao, Fernando; Pourová, Jana; Mladěnka, Aleš; Karlíčková, Jana; Jahodář, Luděk; Vopršalová, Marie; Varner, Kurt J. (July 2018). "Comprehensive review of cardiovascular toxicity of drugs and related agents". Tıbbi Araştırma İncelemeleri. 38 (4): 1332–1403. doi:10.1002/med.21476. ISSN 0198-6325. PMC 6033155. PMID 29315692.
- ^ "SNRI Antidepressants". poison.org. Alındı 2019-10-21.
- ^ Versiani M, Cassano G, Perugi G, Benedetti A, Mastalli L, Nardi A, Savino M (January 2002). "Reboxetine, a selective norepinephrine reuptake inhibitor, is an effective and well-tolerated treatment for panic disorder". Klinik Psikiyatri Dergisi. 63 (1): 31–7. doi:10.4088/jcp.v63n0107. PMID 11838623.
- ^ "Cymbalta Package Insert" (PDF).
- ^ "Effexor XR Prescribing Information".
- ^ Olivier JD, Olivier B (2019-09-01). "Antidepressants and Sexual Dysfunctions: a Translational Perspective". Current Sexual Health Reports. 11 (3): 156–166. doi:10.1007/s11930-019-00205-y. ISSN 1548-3592.
- ^ Clayton AH, Montejo AL (2006). "Major depressive disorder, antidepressants, and sexual dysfunction". Klinik Psikiyatri Dergisi. 67 Suppl 6: 33–7. PMID 16848675.
- ^ a b Jing E, Straw-Wilson K (July 2016). "Sexual dysfunction in selective serotonin reuptake inhibitors (SSRIs) and potential solutions: A narrative literature review". The Mental Health Clinician. 6 (4): 191–196. doi:10.9740/mhc.2016.07.191. PMC 6007725. PMID 29955469.
- ^ "Serotonin syndrome: Preventing, recognizing, and treating it". www.mdedge.com. Alındı 2019-11-21.
- ^ a b Frank C (July 2008). "Recognition and treatment of serotonin syndrome". Kanadalı Aile Hekimi. 54 (7): 988–92. PMC 2464814. PMID 18625822.
- ^ "SNRI Antidepressants". poison.org. Alındı 2019-10-23.
- ^ Tint, Aung; Haddad, Peter M; Anderson, Ian M (2008-05-01). "The effect of rate of antidepressant tapering on the incidence of discontinuation symptoms: a randomised study". Psikofarmakoloji Dergisi. 22 (3): 330–332. doi:10.1177/0269881107081550. ISSN 0269-8811. PMID 18515448.
- ^ a b Cochran KA, Cavallari LH, Shapiro NL, Bishop JR (August 2011). "Bleeding incidence with concomitant use of antidepressants and warfarin". Terapötik İlaç İzleme. 33 (4): 433–8. doi:10.1097/FTD.0b013e318224996e. PMC 3212440. PMID 21743381.
- ^ Cheng YL, Hu HY, Lin XH, Luo JC, Peng YL, Hou MC, et al. (Kasım 2015). "Use of SSRI, But Not SNRI, Increased Upper and Lower Gastrointestinal Bleeding: A Nationwide Population-Based Cohort Study in Taiwan". İlaç. 94 (46): e2022. doi:10.1097/MD.0000000000002022. PMC 4652818. PMID 26579809.
- ^ "Duloxetine: Drug Information". Güncel. Alındı 28 Haziran 2012.
- ^ Perahia DG, Pritchett YL, Kajdasz DK, Bauer M, Jain R, Russell JM, et al. (Ocak 2008). "A randomized, double-blind comparison of duloxetine and venlafaxine in the treatment of patients with major depressive disorder". Psikiyatrik Araştırmalar Dergisi. 42 (1): 22–34. doi:10.1016/j.jpsychires.2007.01.008. PMID 17445831.
- ^ Wilson E, Lader M (December 2015). "A review of the management of antidepressant discontinuation symptoms". Therapeutic Advances in Psychopharmacology. 5 (6): 357–68. doi:10.1177/2045125315612334. PMC 4722507. PMID 26834969.
- ^ Fava GA, Benasi G, Lucente M, Offidani E, Cosci F, Guidi J (2018). "Withdrawal Symptoms after Serotonin-Noradrenaline Reuptake Inhibitor Discontinuation: Systematic Review" (PDF). Psikoterapi ve Psikosomatik. 87 (4): 195–203. doi:10.1159/000491524. PMID 30016772.
- ^ Fava, Giovanni A.; Benasi, Giada; Lucente, Marcella; Offidani, Emanuela; Cosci, Fiammetta; Guidi, Jenny (2018). "Withdrawal Symptoms after Serotonin-Noradrenaline Reuptake Inhibitor Discontinuation: Systematic Review". Psikoterapi ve Psikosomatik. 87 (4): 195–203. doi:10.1159/000491524. hdl:2158/1132671. ISSN 0033-3190. PMID 30016772.
- ^ Taylor D, Lenox-Smith A, Bradley A (June 2013). "A review of the suitability of duloxetine and venlafaxine for use in patients with depression in primary care with a focus on cardiovascular safety, suicide and mortality due to antidepressant overdose". Therapeutic Advances in Psychopharmacology. 3 (3): 151–61. doi:10.1177/2045125312472890. PMC 3805457. PMID 24167687.
- ^ Simon, Leslie V.; Hashmi, Muhammad F.; Keenaghan, Michael (2019), "Serotonin Syndrome", StatPearlsStatPearls Yayıncılık, PMID 29493999, alındı 2019-11-21
- ^ "2009 Top 200 branded drugs by total prescriptions" (PDF). SDI/Verispan, VONA, full year 2009. www.drugtopics.com. Arşivlenen orijinal (PDF) 14 Temmuz 2011'de. Alındı 6 Nisan 2011.
- ^ Llorca PM, Fernandez JL (April 2007). "Escitalopram in the treatment of major depressive disorder: clinical efficacy, tolerability and cost-effectiveness vs. venlafaxine extended-release formulation". Uluslararası Klinik Uygulama Dergisi. 61 (4): 702–10. doi:10.1111/j.1742-1241.2007.01335.x. PMID 17394446.
- ^ a b Dubovicky, Michal; Belovicova, Kristína; Csatlosova, Kristína; Bogi, Eszter (September 2017). "Risks of using SSRI / SNRI antidepressants during pregnancy and lactation". Interdisciplinary Toxicology. 10 (1): 30–34. doi:10.1515/intox-2017-0004. ISSN 1337-6853. PMC 6096863. PMID 30123033.
- ^ a b Strawn, Jeffrey R.; Mills, Jeffrey A.; Sauley, Beau A.; Welge, Jeffrey A. (April 2018). "The Impact of Antidepressant Dose and Class on Treatment Response in Pediatric Anxiety Disorders: A Meta-Analysis". Amerikan Çocuk ve Ergen Psikiyatrisi Akademisi Dergisi. 57 (4): 235–244.e2. doi:10.1016/j.jaac.2018.01.015. ISSN 0890-8567. PMC 5877120. PMID 29588049.
- ^ Emslie, Graham J.; Heiligenstein, John H.; Wagner, Karen Dineen; Hoog, Sharon L.; Ernest, Daniel E.; Brown, Eileen; Nilsson, Mary; Jacobson, Jennie G. (October 2002). "Fluoxetine for acute treatment of depression in children and adolescents: a placebo-controlled, randomized clinical trial". Amerikan Çocuk ve Ergen Psikiyatrisi Akademisi Dergisi. 41 (10): 1205–1215. doi:10.1097/00004583-200210000-00010. ISSN 0890-8567. PMID 12364842.
- ^ Mulsant, Benoit H.; Blumberger, Daniel M.; Ismail, Zahinoor; Rabheru, Kiran; Rapoport, Mark J. (August 2014). "A systematic approach to the pharmacotherapy of geriatric major depression". Geriatrik Tıp Klinikleri. 30 (3): 517–534. doi:10.1016/j.cger.2014.05.002. ISSN 0749-0690. PMC 4122285. PMID 25037293.
