Dekompresyon teorisi - Decompression theory

Dekompresyon teorisi transferinin incelenmesi ve modellenmesidir. atıl gaz bileşeni solunum gazları akciğerlerdeki gazdan dokulara ve ortam basıncındaki değişikliklere maruz kalma sırasında geri. Su altı dalışı ve basınçlı hava çalışması durumunda, bu çoğunlukla yerel yüzey basıncından daha büyük ortam basınçlarını içerir,[1] ancak astronotlar, yüksek irtifa dağcıları ve deniz seviyesi basıncına maruz kalmayan uçaklardaki yolcular,[2][3] genellikle standart deniz seviyesi atmosfer basıncından daha düşük ortam basınçlarına maruz kalırlar. Her durumda, dekompresyonun neden olduğu semptomlar önemli bir basınç düşüşünden sonra nispeten kısa saatler veya ara sıra günler sırasında veya içinde meydana gelir.[4]
"Dekompresyon" terimi, Ortam basıncı organizma tarafından deneyimlenir ve hem basınç ve çözünmüş asal gazların elimine edilmesine izin verme süreci Dokular basınçtaki bu azalma sırasında ve sonrasında. Dokular tarafından gaz alımı çözünmüş durumdadır ve eliminasyon aynı zamanda gazın da çözünmesini gerektirir, ancak ortam basıncında yeterli bir azalma dokularda kabarcık oluşumuna neden olabilir, bu da doku hasarına ve dekompresyon olarak bilinen semptomlara yol açabilir. hastalık ve ayrıca gazın atılmasını geciktirir.[1]
Dekompresyon modellemesi, ortam basıncındaki değişiklikler sırasında ve sonrasında organizmada gaz giderme ve kabarcık oluşum mekanizmasını açıklamaya ve tahmin etmeye çalışır,[5] ve sahada dekompresyon için kabul edilebilir derecede düşük risk ve makul ölçüde uygulanabilir prosedürleri tahmin etmeye çalışan matematiksel modeller sağlar.[6]Hem deterministik hem de olasılıksal modeller kullanılmıştır ve halen kullanılmaktadır.
Dekompresyon fizyolojisi

Gaz ortam basıncında solunur ve bu gazın bir kısmı kan ve diğer sıvılarda çözünür. İnert gaz, dokularda çözünen gaz, içindeki gaz ile denge durumuna gelene kadar alınmaya devam edilir. akciğerler, (görmek: "doygunluk dalışı ") veya ortam basıncı, dokularda çözünen inert gazlar denge durumundan daha yüksek bir konsantrasyona gelene kadar düşürülür ve tekrar yayılmaya başlar.[1]
Gazların sıvılardaki emilimi, çözünürlük Spesifik sıvıdaki spesifik gazın, geleneksel olarak ölçülen gaz konsantrasyonu kısmi basıncı ve sıcaklık.[1] Dekompresyon teorisi çalışmasında, dokularda çözünen gazların davranışı araştırılır ve zaman içindeki basınç değişimleri için modellenir.[7]
Çözündükten sonra, çözünmüş gazın dağıtımı şu şekilde olabilir: yayılma, toplu akışının olmadığı çözücü, veya tarafından perfüzyon çözücünün (kan) dalgıcın vücudu etrafında dolaştığı, gazın daha düşük yerel bölgelere yayılabildiği konsantrasyon. Solunum gazında belirli bir kısmi basınçta yeterli süre verildiğinde, dokulardaki konsantrasyon, çözünürlük, difüzyon hızı ve perfüzyona bağlı bir oranda stabilize olacak veya doyacaktır.[1]
Solunum gazındaki inert gazın konsantrasyonu dokulardan herhangi birinin altına düşerse, gazın dokulardan solunum gazına geri dönme eğilimi olacaktır. Bu olarak bilinir gaz çıkışı ve dekompresyon sırasında, ortam basıncındaki azalma veya solunum gazındaki bir değişiklik, ciğerlerdeki inert gazın kısmi basıncını azalttığı zaman meydana gelir.[1]
Herhangi bir dokudaki birleşik gaz konsantrasyonları, basınç ve gaz bileşiminin geçmişine bağlı olacaktır. Denge koşulları altında, oksijen dokularda metabolize edildiğinden ve üretilen karbondioksit çok daha fazla çözünür olduğundan, çözünmüş gazların toplam konsantrasyonu ortam basıncından daha az olacaktır. Bununla birlikte, ortam basıncında bir azalma sırasında, basınç düşüş hızı, gazın difüzyon ve perfüzyonla elimine edilebildiği hızı aşabilir ve konsantrasyon çok yükselirse, aşırı doymuş ortamda kabarcık oluşumunun meydana gelebileceği bir aşamaya ulaşabilir. Dokular. Bir baloncuğun içindeki gazların basıncı, ortam basıncının birleşik dış basınçlarını ve kabarcık-sıvı arayüzündeki yüzey gerilimini aştığında, kabarcıklar büyür ve bu büyüme dokulara zarar verebilir. Bu hasarın neden olduğu belirtiler şu şekilde bilinir: Dekompresyon hastalığı.[1]
Gerçek difüzyon ve perfüzyon oranları ve gazların belirli dokulardaki çözünürlüğü genel olarak bilinmemektedir ve önemli ölçüde değişir. Bununla birlikte, gerçek durumu az ya da çok yaklaştıran matematik modeller önerilmiştir ve bu modeller, belirli bir basınca maruz kalma profili için semptomatik kabarcık oluşumunun meydana gelip gelmeyeceğini tahmin etmek için kullanılır.[7]Dekompresyon, canlı dokularda gaz çözünürlüğü, kısmi basınçlar ve konsantrasyon gradyanları, difüzyon, toplu taşıma ve kabarcık mekaniğinin karmaşık bir etkileşimini içerir.[6]
Çözünmüş faz gaz dinamiği
Çözünürlük sıvılardaki gazların oranı, çözücü sıvının ve çözünen maddenin doğasından etkilenir,[8] sıcaklık,[9] basınç,[10][11] ve çözücüde diğer çözünen maddelerin varlığı.[12] Difüzyon daha küçük, daha hafif moleküllerde daha hızlıdır, bunun en uç örneği helyumdur. Helyumun difüzivitesi nitrojenden 2,65 kat daha hızlıdır.[13] konsantrasyon gradyanı, difüzyon tahrik mekanizması için bir model olarak kullanılabilir.[14] Bu bağlamda, inert gaz, olmayan bir gazı ifade eder. metabolik olarak aktif. Atmosferik azot (N2) en yaygın örnektir ve helyum (He), yaygın olarak kullanılan diğer inert gazdır. dalgıçlar için nefes karışımları.[15] Atmosferik nitrojen, deniz seviyesinde yaklaşık 0,78 barlık bir kısmi basınca sahiptir. Hava alveoller akciğerlerin% 'si doymuş su buharı (H2O) ve karbon dioksit (CO2), bir metabolik ürün kan tarafından verilir ve daha az içerir oksijen (Ö2) Metabolik kullanım için bir kısmı kan tarafından alındığı için atmosferik havadan daha fazla. Ortaya çıkan kısmi nitrojen basıncı yaklaşık 0,758 bardır.[16]
Atmosferik basınçta vücut Dokular bu nedenle normalde 0.758 bar'da (569 mmHg) nitrojen ile doyurulur. Artmış ortamda derinlikten kaynaklanan basınçlar veya habitat basınçlandırması, bir dalgıcın akciğerleri artan basınçta solunum gazı ile doldurulur ve bileşen gazların kısmi basınçları orantılı olarak artar.[7] Akciğerlerdeki solunum gazından çıkan inert gazlar, alveolar kılcal damarlar ve vücudun etrafına dağıtılır. sistemik dolaşım olarak bilinen süreçte perfüzyon.[7] Çözünen materyaller, kanda tek başına difüzyonla dağıtılacaklarından çok daha hızlı taşınır.[17] Sistemik kılcal damarlardan, çözünmüş gazlar hücre zarları boyunca ve sonunda dengeye ulaşabileceği dokulara yayılır. Bir dokuya kan akışı ne kadar fazlaysa, yeni kısmi basınçta gazla dengeye o kadar hızlı ulaşacaktır.[7][17] Bu dengeye doyma.[7] Sürtünme, basit bir ters üstel denklemi takip ediyor gibi görünüyor. Bir dokunun değişen kısmi basınçta çözünmüş gaz kapasitesindeki farkın% 50'sini alması veya bırakması için geçen süre, o doku ve gaz için yarı zaman olarak adlandırılır.[18][19]
Gaz, akciğerlerdeki kısmi basıncı kanla ilgili dokulardan daha düşük bir konsantrasyonda bir konsantrasyon gradyanına neden olacak şekilde yeterince düşene kadar dokularda çözünmüş olarak kalır. Kandaki konsantrasyon, komşu dokudaki konsantrasyonun altına düştüğünde, gaz dokudan dışarı kana yayılacak ve daha sonra akciğerlere geri taşınacak ve burada akciğer gazına yayılacak ve daha sonra ekshalasyonla elimine edilecektir. . Ortam basıncı azalması sınırlıysa, bu desatürasyon çözünmüş fazda gerçekleşecektir, ancak ortam basıncı yeterince düşürülürse, hem kanda hem de diğer aşırı doymuş dokularda kabarcıklar oluşabilir ve büyüyebilir.[7] Bir dokuda çözünen tüm gazın kısmi basıncı doku üzerindeki toplam ortam basıncını aştığında aşırı doyurulur,[20] ve kabarcık oluşumu olasılığı vardır.[7]
Dalgıcın soluduğu gazın kısmi basınçlarının toplamı, akciğer gazındaki kısmi basınçların toplamı ile mutlaka dengelenmelidir. Alveollerde gaz nemlendirilmiş ve venöz kandan karbondioksit kazanmıştır. Oksijen ayrıca arteriyel kana da yayılır ve alveollerdeki kısmi oksijen basıncını düşürür. Alveollerdeki toplam basıncın ortam basıncı ile dengelenmesi gerektiğinden, bu seyreltme, normal atmosfer basıncında havada yaklaşık 758 mb (569 mmHg) etkili bir kısmi nitrojen basıncı ile sonuçlanır.[21] Kararlı bir durumda, dokular solunum karışımının inert gazları tarafından doyurulduğunda, metabolik süreçler daha az çözünür oksijenin kısmi basıncını azaltır ve onu suda önemli ölçüde daha çözünür olan karbondioksit ile değiştirir. Tipik bir dokunun hücrelerinde, kısmi oksijen basıncı düşerken, kısmi karbondioksit basıncı yükselecektir. Bu kısmi basınçların (su, oksijen, karbondioksit ve nitrojen) toplamı, solunum gazının toplam basıncından daha azdır. Bu önemli bir doygunluk açığıdır ve aşırı doygunluğa karşı bir tampon ve kabarcıkların çözülmesi için bir itici güç sağlar.[21] Deneyler, doymamışlık derecesinin, sabit bileşimin solunan karışımı için basınçla doğrusal olarak arttığını ve solunum karışımındaki inert gaz fraksiyonuyla doğrusal olarak azaldığını göstermektedir.[22] Sonuç olarak, doymamışlık derecesini maksimize etme koşulları, mümkün olan en düşük inert gaz fraksiyonuna sahip bir solunum gazıdır - yani, izin verilen maksimum kısmi basınçta saf oksijendir. Bu doygunluk açığı aynı zamanda doğal doymamışlık olarak da adlandırılır, "Oksijen penceresi ".[23] veya kısmi basınç boşluğu.[24]
Mikro çekirdeklerin yeri veya kabarcıkların başlangıçta oluştuğu yer bilinmemektedir.[25] Dekompresyon modellerine kabarcık oluşumu ve büyüme mekanizmalarının dahil edilmesi, modelleri daha biyofiziksel hale getirebilir ve daha iyi ekstrapolasyona izin verebilir.[25] Kabarcık büyümesi için çözünmüş gaz için doku ve dolaşım kabarcıkları arasındaki ve çoklu kabarcıklar arasındaki rekabette akış koşulları ve perfüzyon oranları baskın parametrelerdir.[25]
Kabarcık mekaniği
Bir baloncuğun oluşması için yüzeydeki kuvvetlerin dengesi gereklidir. Toplamı Ortam basıncı ve yüzeyin dışına uygulanan doku bozulmasına bağlı basınç, yüzey gerilimi Kabarcık ve çevresi arasındaki arayüzdeki sıvının miktarı, balonun içindeki basınçla dengelenmelidir. Bu, gazın kabarcığa ve balondan net difüzyonundan dolayı içerideki gazların kısmi basınçlarının toplamıdır. Kabarcık üzerindeki kuvvet dengesi, bir katman tarafından değiştirilebilir. yüzey aktif Temiz bir kabarcık üzerindeki yüzey geriliminin hızla çökmesine neden olacağı bir boyutta bir mikro kabarcığı stabilize edebilen moleküller ve bu yüzey tabakası, geçirgenlik öyle ki, eğer kabarcık yeterince sıkıştırılırsa, difüzyon geçirimsiz hale gelebilir.[26] Kabarcığın dışındaki çözücü doymuşsa veya doymamışsa, kısmi basınç balondakinden daha az olacaktır ve yüzey gerilimi, iç basıncı yüzey eğriliğiyle doğru orantılı olarak artırarak kabarcıktan difüzyonu artırmak için bir basınç gradyanı sağlayacaktır. , etkili bir şekilde "gazın balondan dışarı doğru sıkıştırılması" ve kabarcık ne kadar küçük olursa o kadar hızlı sıkışacaktır. Bir gaz kabarcığı, yalnızca çevreleyen çözücü yüzey geriliminin üstesinden gelmek için yeterince aşırı doymuşsa veya yüzey tabakası yüzey geriliminin üstesinden gelmek için yeterli reaksiyon sağlıyorsa sabit basınçta büyüyebilir.[26] Yeterince küçük olan temiz kabarcıklar, aşırı doygunluk düşükse yüzey gerilimi nedeniyle çökecektir. Yarı geçirgen yüzeylere sahip kabarcıklar, basınca, yüzey katmanının bileşimine ve süperdoymaya bağlı olarak belirli bir yarıçapta stabilize olur veya kritik yarıçaptan daha büyükse, süresiz olarak büyümeye devam eder.[27] Kanda veya diğer dokularda kabarcık oluşumu meydana gelebilir.[28]
Bir çözücü, çözelti içinde aşırı doymuş bir gaz yükü taşıyabilir. Solventin büyük kısmındaki solüsyondan kabarcıklar oluşturup çıkmayacağı bir dizi faktöre bağlı olacaktır. Yüzey gerilimini azaltan veya gaz moleküllerini emen veya yerel olarak gazın çözünürlüğünü azaltan veya bir sıvıda statik basınçta yerel bir azalmaya neden olan bir şey, kabarcık çekirdeklenmesi veya büyümesiyle sonuçlanabilir. Bu, sıvılarda hız değişimlerini ve türbülansı ve katı ve yarı katılarda yerel çekme yüklerini içerebilir. Lipitler ve diğerleri hidrofobik yüzeyler yüzey gerilimini azaltabilir (kan damarı duvarları bu etkiye sahip olabilir). Dehidrasyon, diğer çözünen maddelerin daha yüksek konsantrasyonu ve gazı tutmak için daha az çözücü nedeniyle bir dokudaki gaz çözünürlüğünü azaltabilir.[29] Başka bir teori, mikroskobik kabarcık çekirdeklerin canlı dokular da dahil olmak üzere sulu ortamda her zaman var olduğunu varsayar. Bu kabarcık çekirdekleri, süspansiyonda kalacak kadar küçük, ancak çökmeye direnecek kadar güçlü olan küresel gaz fazlarıdır; stabiliteleri, yüzey geriliminin etkisine direnen yüzey aktif moleküllerden oluşan elastik bir yüzey tabakası tarafından sağlanır.[30]
Bir mikro kabarcık oluştuğunda, dokular yeterince aşırı doymuşsa büyümeye devam edebilir. Kabarcık büyüdükçe, çevreleyen dokuyu bozabilir ve hücrelere zarar verebilir ve ağrıya neden olan sinirler üzerinde baskıya neden olabilir veya bir kan damarını tıkayarak kan akışını kesebilir ve normalde damar tarafından perfüze edilen dokularda hipoksiye neden olabilir.[31]
Gaz moleküllerini toplayan bir kabarcık veya bir nesne varsa, bu gaz molekülleri topluluğu, iç basıncın birleşik yüzey gerilimini ve dış basıncı aştığı bir boyuta ulaşabilir ve kabarcık büyüyecektir.[32] Çözücü yeterince aşırı doymuşsa, gazın baloncuğa difüzyonu, çözeltiye geri yayılma hızını aşacaktır ve bu fazla basınç, yüzey geriliminden kaynaklanan basınçtan daha büyükse, kabarcık büyümeye devam edecektir. Bir kabarcık büyüdüğünde, yüzey gerilimi azalır ve iç basınç düşer, bu da gazın daha hızlı yayılmasına ve daha yavaş yayılmasına izin verir, böylece kabarcık olumlu bir geri besleme durumunda büyür veya küçülür. Kabarcık büyüdükçe büyüme hızı azalır, çünkü yüzey alanı yarıçapın karesi olarak artarken, yarıçapın küpü olarak hacim artar. Yükselme sırasında hidrostatik basıncın düşmesi nedeniyle dış basınç azalırsa, kabarcık da büyür ve tersine, artan bir dış basınç, balonun büzülmesine neden olur, ancak sıkıştırmaya dirençli bir yüzey tabakası olması durumunda tamamen ortadan kaldırılmasına neden olmayabilir. var.[32]
Dekompresyon kabarcıkları, çoğunlukla gaz konsantrasyonunun en yüksek olduğu sistemik kılcal damarlarda, sıklıkla aktif uzuvları boşaltan damarları besleyenlerde oluşuyor gibi görünmektedir. Arteriyel kan son zamanlarda aşırı gazı akciğerlere salma fırsatına sahip olduğundan, ortam basıncındaki düşüşün çok hızlı olmaması koşuluyla genellikle arterlerde oluşmazlar. Damarlarda kalbe geri taşınan kabarcıklar, bir kanal aracılığıyla sistemik dolaşıma aktarılabilir. patent foramen ovale Bu septal defekti olan dalgıçlarda, daha sonra vücudun herhangi bir yerinde kılcal damarların tıkanma riski vardır.[33]
Damarlarda kalbe geri taşınan kabarcıklar kalbin sağ tarafına geçecek ve oradan normalde pulmoner dolaşıma girecek ve alveollerin etrafındaki akciğer kılcal damarlarından geçecek veya hapsolacaktır. solunum gazına çok yakın, burada gaz kabarcıklardan kılcal ve alveolar duvarlardan akciğerdeki gaza yayılacaktır. Bu kabarcıklar tarafından bloke edilen akciğer kılcal damarlarının sayısı nispeten azsa, dalgıç semptom göstermeyecek ve hiçbir doku hasar görmeyecektir (akciğer dokuları difüzyonla yeterince oksijenlenir).[34] Akciğer kılcal damarlarından geçecek kadar küçük olan kabarcıklar, yüzey gerilimi ve çevreleyen kandaki düşük konsantrasyona difüzyonun bir kombinasyonu nedeniyle çözülebilecek kadar küçük olabilir, ancak Değişken Geçirgenlik Modeli çekirdeklenme teorisi, kabarcıkların çoğunun geçtiğini ima eder. pulmoner dolaşım, kılcal damarlardan geçmek için yeterli gazı kaybedecek ve geri dönüştürülmüş ancak stabil çekirdekler olarak sistemik dolaşıma geri dönecektir.[35] Dokular içinde oluşan kabarcıklar, uygun bir konsantrasyon gradyanı anlamına gelen difüzyon ile yerinde ortadan kaldırılmalıdır.[34]
İzobarik karşı difüzyon (ICD)
İzobarik karşı difüzyon, ortam basıncında değişiklik olmaksızın, dış ortam gazının veya solunan gazın bileşimindeki bir değişikliğin neden olduğu gazların zıt yönlerde difüzyonudur. Bir dalıştan sonra dekompresyon sırasında bu, solunum gazında bir değişiklik yapıldığında veya dalgıç, solunum gazından farklı olan gaz dolu bir ortama geçtiğinde meydana gelebilir.[36] Bir dekompresyon fenomeni tam olarak konuşulmasa da, dekompresyon sırasında ortaya çıkabilen ve çevresel basınçta değişiklik olmaksızın kabarcıkların oluşmasına veya büyümesine neden olabilen bir komplikasyondur. Bu fenomenin iki biçimi Lambertsen tarafından tanımlanmıştır:[37][36]
Yüzeysel ICD (Kararlı Durumda İzobarik Karşı Difüzyon olarak da bilinir)[38] dalgıcın soluduğu inert gaz, vücudu çevreleyen inert gaza göre vücuda daha yavaş yayıldığında oluşur.[37][36][38] Bunun bir örneği, bir helioks ortamında hava solumaktır. Heliokstaki helyum cilde hızla yayılırken, nitrojen kılcal damarlardan cilde ve vücudun dışına daha yavaş yayılır. Ortaya çıkan etki, yüzeysel dokuların belirli bölgelerinde süperdoyma ve inert gaz kabarcıklarının oluşmasına neden olur.[36]
Derin Doku ICD (Geçici İzobarik Karşı Difüzyon olarak da bilinir)[38] dalgıç tarafından sırayla farklı inert gazlar solunduğunda oluşur.[37] Hızla yayılan gaz dokuya daha yavaş yayılan gazın doku dışına taşınmasından daha hızlı taşınır.[36] Bu, dalgıçlar bir nitrojen karışımından bir helyum karışımına geçerken veya hidrelioks soluyan doymuş dalgıçlar bir helioks karışımına geçtiğinde meydana gelebilir.[36][39]
Doolette ve Mitchell'in İç Kulak Dekompresyon Hastalığı (IEDCS) üzerine yaptığı çalışma, iç kulağın yaygın (örneğin Bühlmann) algoritmalarıyla iyi modellenemeyebileceğini gösteriyor. Doolette ve Mitchell, teknik dalışta yükselişte trimix'ten nitroks'a geçerken yaygın olduğu gibi, helyum bakımından zengin bir karışımdan nitrojen bakımından zengin bir karışıma geçişin, iç kulakta inert gazın geçici bir aşırı doygunluğuna neden olabileceğini ve bunun sonucunda IEDCS.[40] Solunum gazı geçişlerinin helyum bakımından zengin karışımlardan nitrojen bakımından zengin karışımlara geçişlerinin ya derin (nitrojen narkozu dikkate alınarak) ya da dekompresyondan kaynaklanan maksimum süperdoyma süresinden kaçınmak için sığ olarak dikkatlice planlanması gerektiğini öne sürüyorlar. Oksijen toksisitesi dikkate alınarak güvenli bir şekilde tolere edilebilen en büyük solunan oksijen kısmi basıncının solunması sırasında da anahtarlar yapılmalıdır.[40]
Dekompresyon hastalığı
Sistemik kılcal damarlarda oluşan vasküler kabarcıklar, akciğer kılcal damarlarında sıkışarak bunları geçici olarak bloke edebilir. Bu şiddetliyse, "boğulma" adı verilen belirti ortaya çıkabilir.[33] Dalgıcın bir patent foramen ovale (veya a şant pulmoner dolaşımda), kabarcıklar içinden geçebilir ve arteryel kana girmek için pulmoner dolaşımı atlayabilir. Bu kabarcıklar arteriyel plazmada emilmezse ve sistemik kılcal damarlara yerleşmezse, oksijenli kanın bu kılcal damarlar tarafından sağlanan dokulara akışını engeller ve bu dokular oksijenden yoksun kalır. Moon ve Kisslo (1988) şu sonuca varmıştır: "Kanıtlar, ciddi nörolojik DCI veya erken başlangıçlı DCI riskinin dalgıçlarda PFO aracılığıyla sağdan sola şant ile dinlendiğini gösteriyor. Şu anda, PFO'ya dair hiçbir kanıt yoktur hafif veya geç başlangıçlı virajlarla ilgilidir. "[41]
Diğer dokularda ve kan damarlarında kabarcıklar oluşur.[33] İnert gaz, dokular arasında kabarcık çekirdeklerine yayılabilir. Bu durumda, kabarcıklar dokuya zarar verebilir ve kalıcı olarak zarar verebilir. Kabarcıklar büyüdükçe ağrıya neden olarak büyüdükçe sinirleri de sıkıştırabilir.[34][42]
Ekstravasküler veya otokton[a] kabarcıklar genellikle eklemler, tendonlar ve kas kılıfları gibi yavaş dokularda oluşur. Doğrudan genişleme, serbest bırakılmasıyla doku hasarına neden olur. histaminler ve bunların ilişkili etkileri. Biyokimyasal hasar, mekanik etkiler kadar veya onlardan daha önemli olabilir.[34][33][43]
Kan ve dokular arasında çözünmüş gazların değişimi, özellikle heterojen dokularda perfüzyonla ve daha az ölçüde difüzyonla kontrol edilir. Kan akışının dokulara dağılımı değişkendir ve çeşitli etkilere tabidir. Akış yerel olarak yüksek olduğunda, bu alana perfüzyon hakimdir ve akış düşük olduğunda difüzyon hakimdir. Akışın dağılımı, ortalama arter basıncı ve lokal vasküler direnç tarafından kontrol edilir ve arter basıncı, kardiyak output ve toplam vasküler dirence bağlıdır. Temel vasküler direnç, sempatik sinir sistemi tarafından kontrol edilir ve metabolitler, sıcaklık ve lokal ve sistemik hormonlar, duruma göre önemli ölçüde değişebilen ikincil ve sıklıkla lokalize etkilere sahiptir. Soğuk sudaki periferik vazokonstriksiyon, titreme başlayana kadar oksijen tüketimini artırmadan genel ısı kaybını azaltır; bu noktada, vazokonstriksiyon devam edebilirse de oksijen tüketimi artacaktır.[33]
Basınca maruz kalma ve dekompresyon sırasında solunan gazın bileşimi, belirli bir basınca maruz kalma profili için inert gaz alımı ve eliminasyonunda önemlidir. Dalış için solunan gaz karışımları tipik olarak havanınkinden farklı bir nitrojen gaz fraksiyonuna sahip olacaktır. Her bir bileşen gazının kısmi basıncı, herhangi bir derinlikte havadaki nitrojenden farklı olacaktır ve her bir inert gaz bileşeninin alımı ve ortadan kaldırılması, zaman içindeki gerçek kısmi basınçla orantılıdır. Karışık solunum gazlarının kullanılmasının en önemli iki nedeni, oksijenle seyreltilerek nitrojen kısmi basıncının düşürülmesidir. Nitroks karışımlar, öncelikle basınca maruz kalma sırasında nitrojen alım oranını düşürmek için ve helyumun (ve bazen diğer gazların) nitrojen yerine kullanılması narkotik etkiler yüksek kısmi basınca maruz kalma altında. Helyum ve nitrojen oranlarına bağlı olarak bu gazlara Heliox nitrojen yoksa veya Trimix, gerekli oksijenle birlikte nitrojen ve helyum varsa.[44][45] Azot yerine kullanılan inert gazlar, canlı dokularda yerini aldıkları nitrojene göre farklı çözünürlük ve difüzyon özelliklerine sahiptir. Örneğin, nitrojen için en yaygın inert gaz seyreltici ikame maddesi, canlı dokuda önemli ölçüde daha az çözünür olan helyumdur.[46] aynı zamanda nispeten küçük boyutu ve kütlesi nedeniyle daha hızlı yayılır O atom ile karşılaştırıldığında N2 molekül.[47]
Cilde ve yağa kan akışı, deri ve çekirdek sıcaklıktan etkilenir ve dinlenen kas perfüzyonu, kasın kendisinin sıcaklığı tarafından kontrol edilir. Egzersiz sırasında çalışan kaslara artan akış, genellikle böbrekler, dalak ve karaciğer gibi diğer dokulara azalmış akışla dengelenir.[33] Soğuk suda kaslara kan akışı da daha düşüktür, ancak egzersiz kasları sıcak tutar ve cilt soğuduğunda bile akışı yüksek tutar. Normalde egzersiz sırasında yağa kan akışı artar, ancak bu soğuk suya daldırma ile engellenir. Soğuğa adaptasyon, genellikle soğuk suya daldırma ile ortaya çıkan aşırı vazokonstriksiyonu azaltır.[33] Perfüzyon dağılımındaki varyasyonlar, respiratuar inert gaz değişimini mutlaka etkilemez, ancak bazı gazlar, perfüzyondaki değişiklikler tarafından lokal olarak tutulabilir. Soğuk bir ortamda dinlenmek deriden, yağdan ve kastan inert gaz alışverişini azaltırken, egzersiz gaz değişimini artıracaktır. Dekompresyon sırasında egzersiz, kabarcıkların olmaması koşuluyla dekompresyon süresini ve riskini azaltabilir, ancak kabarcıklar varsa riski artırabilir.[33] İnert gaz değişimi, sıcak olan ve iç içe geçme aşamasında derinlemesine egzersiz yapan ve dekompresyon sırasında dinlenen ve soğuk olan dalgıç için en az elverişlidir.[33]
Dekompresyon riskini etkileyebilecek diğer faktörler arasında oksijen konsantrasyonu, karbondioksit seviyeleri, vücut pozisyonu, vazodilatörler ve konstriktörler, pozitif veya negatif basınçlı solunum sayılabilir.[33] ve dehidrasyon (kan hacmi).[48] Dekompresyon hastalığına karşı bireysel duyarlılık, belirli bir nedene atfedilebilecek bileşenlere ve rasgele görünen bileşenlere sahiptir. Rastgele bileşen, ardışık dekompresyonları zayıf bir duyarlılık testi yapar.[33] Obezite ve yüksek serum lipid seviyeleri, bazı çalışmalarda risk faktörleri olarak ilişkilendirilmiştir ve risk yaşla birlikte artmaktadır.[49] Başka bir çalışma, yaşlı deneklerin henüz bilinmeyen nedenlerden dolayı genç deneklerden daha fazla balonlaşma eğiliminde olduğunu, ancak kilo, vücut yağı veya cinsiyet ve kabarcıklar arasında hiçbir eğilim tespit edilmediğini ve bazı insanların neden kabarcık oluşturma olasılığının daha yüksek olduğu sorusunu gösterdi diğerlerine göre belirsizliğini koruyor.[50]
Dekompresyon modeli kavramları


Dekompresyon modellemesi için oldukça farklı iki kavram kullanılmıştır. Birincisi, çözünmüş gazın çözünmüş fazdayken elimine edildiğini ve asemptomatik dekompresyon sırasında kabarcıkların oluşmadığını varsayar. Deneysel gözlemle desteklenen ikincisi, asemptomatik dekompresyonların çoğunda kabarcıkların oluştuğunu ve gaz eliminasyonunun hem çözünmüş hem de kabarcık aşamalarını dikkate alması gerektiğini varsayar.[32]
Erken dekompresyon modelleri, çözünmüş faz modellerini kullanma eğilimindeydi ve bunları semptomatik kabarcık oluşumu riskini azaltmak için az çok keyfi faktörlerle ayarladı. Çözünmüş faz modelleri iki ana gruptadır. Değişken gaz emme oranlarına (yarı zamanlı) sahip birkaç bölmenin birbirinden bağımsız olarak var olduğu düşünülen paralel bölme modelleri ve sınırlayıcı durum, belirli bir maruz kalma profili için en kötü durumu gösteren bölme tarafından kontrol edilir. Bu bölmeler kavramsal dokuları temsil eder ve belirli organik dokuları temsil etmeyi amaçlamaz, yalnızca organik dokular için olasılıklar aralığını temsil eder. İkinci grup, gazın diğerine ulaşmadan önce bir bölmeden yayıldığı varsayıldığı seri bölmeler kullanır.[51] Seri bölmeli modelde yeni bir varyasyon, Goldman birbirine bağlı bölme modelidir (ICM).[52]
Daha yeni modeller, tabloların hesaplanmasını kolaylaştırmak ve daha sonra bir dalış sırasında gerçek zamanlı tahminlere izin vermek için basitleştirilmiş modellerle kabarcık dinamiklerini modellemeye çalışır. Kabarcık dinamiklerini tahmin etmek için kullanılan modeller çeşitlidir ve çözünmüş faz modellerinden çok daha karmaşık olmayan modellerden, önemli ölçüde daha fazla hesaplama gücü gerektirenlere kadar çeşitlilik gösterir.[53]
Çeşitli hipotezlere karşılık gelen matematiksel modellerin yorumları önerilmiş olmasına rağmen, dekompresyon modellerinin hiçbirinin fizyolojik süreçlerin doğru bir temsili olduğu gösterilemez. Bunların tümü, gerçekliği az ya da çok tahmin eden yaklaşık değerlerdir ve yalnızca toplanan deneysel verilere karşı kalibrasyon sınırları dahilinde kabul edilebilir şekilde güvenilirdir.[54]
Uygulama aralığı
İdeal dekompresyon profili, kabarcıkların oluşmasına neden olmadan bir dokudan inert gazın giderilmesi için mümkün olan en büyük gradyanı oluşturur,[55] ve çözünmüş faz dekompresyon modelleri, kabarcık oluşumunun önlenebileceği varsayımına dayanmaktadır. Bununla birlikte, bunun pratik olarak mümkün olup olmadığı kesin değildir: bazı dekompresyon modelleri, kararlı kabarcık mikronükleuslarının her zaman var olduğunu varsayar.[30] Kabarcık modelleri kabarcıkların olacağını varsayar, ancak tolere edilebilir bir toplam gaz fazı hacmi vardır.[30] veya tolere edilebilir bir gaz kabarcığı boyutu,[56] ve bu toleransları hesaba katmak için maksimum eğimi sınırlayın.[30][56]
Dekompresyon modelleri ideal olarak, durmaksızın yukarı çıkış limitleri dahilindeki kısa dalışlardan, aşırı pozlamalı dalışlar ve tekrarlayan dalışlar dahil olmak üzere tüm pratik uygulanabilirlik aralığında dekompresyon sekme dalışlarından, gaz anahtarları dahil alternatif solunum gazlarından kaynaklanan riskleri doğru bir şekilde tahmin etmelidir. sabit PO2, dalış profilindeki varyasyonlar ve doygunluk dalışları. Bu genellikle geçerli değildir ve çoğu model, olası derinlik ve zaman aralığının bir bölümü ile sınırlıdır. Ayrıca, belirli bir solunum gazları aralığı ile sınırlıdır ve bazen hava ile sınırlıdır.[57]
Dekompresyon tablolarının tasarımındaki temel bir problem, tek bir dalışı ve yükselişi yöneten basitleştirilmiş kuralların, bazı doku baloncukları halihazırda mevcut olduğunda geçerli olmamasıdır, çünkü bunlar, inert gaz eliminasyonunu geciktirecek ve eşdeğer dekompresyon dekompresyon hastalığına neden olabilir.[57] Tekrarlayan dalış, tek bir dalışta çoklu çıkış ve yüzey dekompresyon prosedürleri DCS için önemli risk faktörleridir.[55] Bunlar, kısmen sonraki dalışlara veya bir testere dişi profilinin son yükselişine taşınabilen nispeten yüksek bir gaz fazı hacminin gelişmesine atfedilmiştir.[6]
Dekompresyon modellerinin işlevi, Doppler ultrasonik kabarcık detektörlerinin mevcudiyetiyle değişmiştir ve artık sadece dekompresyon hastalığının semptomatik oluşumunu sınırlamak değil, aynı zamanda asemptomatik post-dalış venöz gaz kabarcıklarını da sınırlamaktır.[25] Yüzeye çıktıktan hemen sonra asemptomatik dalgıçlarda Doppler ölçümü ile venöz kabarcıkların tanımlanmasından bu yana, çözünmüş faz modellerinde bir dizi ampirik modifikasyon yapılmıştır.[58]
Doku bölmeleri
Çözüme yönelik bir girişim, vücudun farklı bölgelerinin gazı farklı oranlarda emdiğini ve ortadan kaldırdığını varsayan çok doku modellerinin geliştirilmesiydi. Bunlar, doygunluk oranını tanımlamak için hızlı ve yavaş olarak adlandırılan varsayımsal dokulardır. Her doku veya bölmenin farklı bir yarı ömrü vardır. Gerçek dokuların doyması daha fazla veya daha az zaman alacaktır, ancak modellerin yararlı bir sonuç elde etmek için gerçek doku değerlerini kullanmasına gerek yoktur. 1-16 doku bölmeli modeller[59] dekompresyon tabloları oluşturmak için kullanılmıştır ve dalış bilgisayarları 20 bölmeye kadar kullanılmış.[60]
- Örneğin: Yüksek lipit içerik daha fazla miktarda nitrojen alabilir, ancak çoğu zaman zayıf bir kan kaynağına sahiptir. Bunların dengeye ulaşması daha uzun sürer ve hızlı olarak tanımlanan çözünmüş gaz için iyi bir kan kaynağı ve daha az kapasitesi olan dokulara kıyasla yavaş olarak tanımlanır.
Hızlı dokular gazı nispeten hızlı emer, ancak genellikle çıkış sırasında hızlı bir şekilde serbest bırakır. Hızlı bir doku, normal bir spor dalışı sırasında doymuş hale gelebilirken, yavaş bir doku, potansiyel gaz kapasitesinin yalnızca küçük bir bölümünü emmiş olabilir. Araştırmacılar, her bölmedeki seviyeleri ayrı ayrı hesaplayarak daha etkili algoritmalar oluşturabilirler. Ek olarak, her bölme, diğerlerinden daha fazla veya daha az aşırı doygunluğu tolere edebilir. Son form karmaşık bir modeldir, ancak çok çeşitli dalışlara uygun algoritmaların ve tabloların oluşturulmasına izin veren bir modeldir. Tipik bir dalış bilgisayarı 8-12 doku modeline sahiptir ve yarım kez 5 dakika ile 400 dakika arasında değişir.[60] Bühlmann masaları Yarım kez 4 dakika ile 640 dakika arasında değişen 16 doku içeren bir algoritma kullanın.[59]
Dokuların seri olduğu varsayılabilir, çözünmüş gazın farklı çözünürlük özelliklerine sahip olan diğerine ulaşmak için bir doku boyunca yayılması gerektiği, paralel olarak, her bir dokuya giren ve çıkan difüzyonun diğerlerinden bağımsız olduğu kabul edilir. sayısal olarak karmaşık hale gelen seri ve paralel doku kombinasyonları.[52]
Sürtünme modeli
Bir dokunun yarılanma süresi, dokunun değişen bir kısmi basınçta çözünmüş gaz kapasitesindeki farkın% 50'sini alması veya bırakması için geçen süredir. Ardışık her devre için doku, ½, ¾, 7/8, 15/16, 31/32, 63/64 vb. Dizideki kümülatif farkın yarısını yeniden alır veya serbest bırakır.[19] Doku bölmesinin yarım süreleri 1 dakika ile en az 720 dakika arasında değişir.[61] Belirli bir doku bölmesi, farklı çözünürlüklere ve difüzyon oranlarına sahip gazlar için farklı yarı sürelere sahip olacaktır. Ingassing is generally modeled as following a simple inverse exponential equation where saturation is assumed after approximately four (93.75%) to six (98.44%) half-times depending on the decompression model.[18][62][63]This model may not adequately describe the dynamics of outgassing if gas phase bubbles are present.[64][65]
Outgassing models
For optimised decompression the driving force for tissue desaturation should be kept at a maximum, provided that this does not cause symptomatic tissue injury due to bubble formation and growth (symptomatic decompression sickness), or produce a condition where diffusion is retarded for any reason.[66]
There are two fundamentally different ways this has been approached. The first is based on an assumption that there is a level of supersaturation which does not produce symptomatic bubble formation and is based on empirical observations of the maximum decompression rate which does not result in an unacceptable rate of symptoms. This approach seeks to maximise the concentration gradient providing there are no symptoms, and commonly uses a slightly modified exponential half-time model. The second assumes that bubbles will form at any level of supersaturation where the total gas tension in the tissue is greater than the ambient pressure and that gas in bubbles is eliminated more slowly than dissolved gas.[63] These philosophies result in differing characteristics of the decompression profiles derived for the two models: The critical supersaturation approach gives relatively rapid initial ascents, which maximize the concentration gradient, and long shallow stops, while the bubble models require slower ascents, with deeper first stops, but may have shorter shallow stops. This approach uses a variety of models.[63][67][68][66][69]
The critical supersaturation approach
J.S. Haldane originally used a critical pressure ratio of 2 to 1 for decompression on the principle that the saturation of the body should at no time be allowed to exceed about double the air pressure.[70] This principle was applied as a pressure ratio of total ambient pressure and did not take into account the partial pressures of the component gases of the breathing air. His experimental work on goats and observations of human divers appeared to support this assumption. However, in time, this was found to be inconsistent with incidence of decompression sickness and changes were made to the initial assumptions. This was later changed to a 1.58:1 ratio of nitrogen partial pressures.[71]
Further research by people such as Robert Workman suggested that the criterion was not the ratio of pressures, but the actual pressure differentials. Applied to Haldane's work, this would suggest that the limit is not determined by the 1.58:1 ratio but rather by the critical difference of 0.58 atmospheres between tissue pressure and ambient pressure. Most tables today, including the Bühlmann tables, are based on the critical difference model.[72]
At a given ambient pressure, the M-value is the maximum value of absolute inert gas pressure that a tissue compartment can take without presenting symptoms of decompression sickness. M-values are limits for the tolerated gradient between inert gas pressure and ambient pressure in each compartment. Alternative terminology for M-values include "supersaturation limits", "limits for tolerated overpressure", and "critical tensions".[67][73]
Gradient factors are a way of modifying the M-value to a more muhafazakar value for use in a decompression algorithm. The gradient factor is a percentage of the M-value chosen by the algorithm designer, and varies linearly between the maximum depth of the specific dive and the surface. They are expressed as a two number designation, where the first number is the percentage of the deep M-value, and the second is a percentage of the shallow M-value.[68] The gradient factors are applied to all tissue compartments equally and produce an M-value which is linearly variable in proportion to ambient pressure.[68]
- For example: A 30/85 gradient factor would limit the allowed supersaturation at depth to 30% of the designer's maximum, and to 85% at the surface.
In effect the user is selecting a lower maximum supersaturation than the designer considered appropriate. Use of gradient factors will increase decompression time, particularly in the depth zone where the M-value is reduced the most. Gradient factors may be used to force deeper stops in a model which would otherwise tend to produce relatively shallow stops, by using a gradient factor with a small first number.[68]
The no-supersaturation approach
Göre termodinamik model of Hugh LeMessurier and Brian Andrew Hills, this condition of optimum driving force for outgassing is satisfied when the ambient pressure is just sufficient to prevent phase separation (bubble formation).[69]
Bu yaklaşımın temel farkı, kabarcık oluşumunun beklendiği sınırlama noktası olarak dekompresyondan sonra her gaz için dokudaki kısmi gaz gerilimlerinin toplamıyla mutlak ortam basıncını eşitlemektir.[69]
Model, oksijen kısmi basıncındaki metabolik azalmaya bağlı olarak dokulardaki doğal doymamışlığın, kabarcık oluşumuna karşı tampon sağladığını ve ortam basıncındaki azalmanın bu doymamışlık değerini aşmaması kaydıyla dokunun güvenli bir şekilde dekomprese edilebileceğini varsaymaktadır. Açıkça, doymamışlığı arttıran herhangi bir yöntem, daha hızlı dekompresyona izin verecektir, çünkü konsantrasyon gradyanı, kabarcık oluşumu riski olmaksızın daha büyük olacaktır.[69]
The natural unsaturation increases with depth, so a larger ambient pressure differential is possible at greater depth, and reduces as the diver surfaces. Bu model, daha yavaş yükselme hızlarına ve daha derin ilk duruşlara yol açar, ancak ortadan kaldırılacak daha az kabarcık fazı gazı olduğundan daha kısa sığ duruşlara yol açar.[69]
The critical volume approach
Kritik hacim kriteri, dokularda biriken toplam gaz fazı hacmi kritik bir değeri aştığında, DCS'nin belirti veya semptomlarının ortaya çıkacağını varsayar. Bu varsayım, doppler kabarcık algılama anketleri tarafından desteklenmektedir. Bu yaklaşımın sonuçları, büyük ölçüde kullanılan kabarcık oluşumuna ve büyüme modeline, özellikle de kabarcık oluşumunun dekompresyon sırasında pratik olarak önlenebilir olup olmadığına bağlıdır.[32]
Bu yaklaşım, pratik dekompresyon profilleri sırasında, canlı dokular da dahil olmak üzere sulu ortamda her zaman var olan stabil mikroskobik kabarcık çekirdeklerinin büyümesi olacağını varsayan dekompresyon modellerinde kullanılır.[66]
Etkili dekompresyon, toplam kabarcık birikimini kabul edilebilir bir semptomatik olmayan kritik değerle sınırlarken, toplam yukarı çıkış süresini en aza indirecektir. Kabarcık büyümesinin ve ortadan kaldırılmasının fiziği ve fizyolojisi, kabarcıkların çok küçükken yok edilmesinin daha verimli olduğunu göstermektedir. Kabarcık fazını içeren modeller, sadece çözünmüş faz gazını dikkate alan modellere kıyasla, kabarcık büyümesini azaltmanın ve erken eliminasyonu kolaylaştırmanın bir yolu olarak daha yavaş çıkışlar ve daha derin ilk dekompresyon duruşları ile dekompresyon profilleri üretmiştir.[74]
Residual inert gas
Gas bubble formation has been experimentally shown to significantly inhibit inert gas elimination.[16][75]A considerable amount of inert gas will remain in the tissues after a diver has surfaced, even if no symptoms of decompression sickness occur. This residual gas may be dissolved or in sub-clinical bubble form, and will continue to outgas while the diver remains at the surface. If a repetitive dive is made, the tissues are preloaded with this residual gas which will make them saturate faster.[76][77]
In repetitive diving, the slower tissues can accumulate gas day after day, if there is insufficient time for the gas to be eliminated between dives. This can be a problem for multi-day multi-dive situations. Multiple decompressions per day over multiple days can increase the risk of decompression sickness because of the build up of asymptomatic bubbles, which reduce the rate of off-gassing and are not accounted for in most decompression algorithms.[78] Consequently, some diver training organisations make extra recommendations such as taking "the seventh day off".[79]
Decompression models in practice
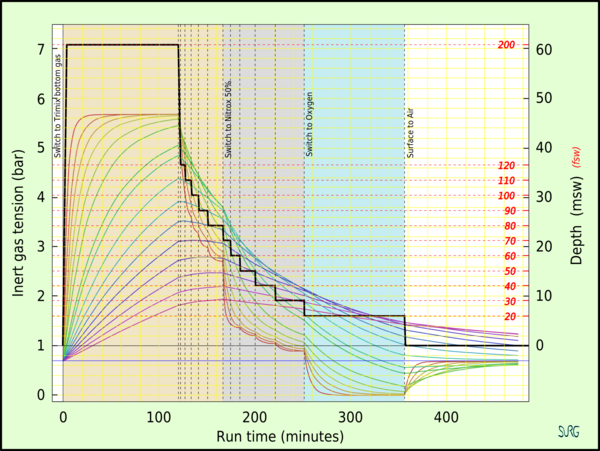
Deterministik modeller
Deterministik decompression models are a rule based approach to calculating decompression.[80] These models work from the idea that "excessive" aşırı doygunluk çeşitliliğinde Dokular is "unsafe" (resulting in dekompresyon hastalığı ). The models usually contain multiple depth and tissue dependent rules based on mathematical models of idealised tissue compartments. Yok amaç mathematical way of evaluating the rules or overall risk other than comparison with empirical test results. The models are compared with experimental results and reports from the field, and rules are revised by nitel yargı and curve fitting so that the revised model more closely predicts observed reality, and then further observations are made to assess the reliability of the model in extrapolations into previously untested ranges. The usefulness of the model is judged on its accuracy and reliability in predicting the onset of symptomatic decompression sickness and asymptomatic venous bubbles during ascent.[80]
It may be reasonably assumed that in reality, both perfusion transport by blood circulation, and diffusion transport in tissues where there is little or no blood flow occur. The problem with attempts to simultaneously model perfusion and diffusion is that there are large numbers of variables due to interactions between all of the tissue compartments and the problem becomes intractable. A way of simplifying the modelling of gas transfer into and out of tissues is to make assumptions about the limiting mechanism of dissolved gas transport to the tissues which control decompression. Assuming that either perfusion or diffusion has a dominant influence, and the other can be disregarded, can greatly reduce the number of variables.[66]
Perfusion limited tissues and parallel tissue models
The assumption that perfusion is the limiting mechanism leads to a model comprising a group of tissues with varied rates of perfusion, but supplied by blood of approximately equivalent gas concentration. It is also assumed that there is no gas transfer between tissue compartments by diffusion. This results in a parallel set of independent tissues, each with its own rate of ingassing and outgassing dependent on the rate of blood flowing through the tissue. Gas uptake for each tissue is generally modelled as an exponential function, with a fixed compartment half-time, and gas elimination may also be modelled by an exponential function, with the same or a longer half time, or as a more complex function, as in the exponential-linear elimination model.[76]
The critical ratio hypothesis predicts that the development of bubbles will occur in a tissue when the ratio of dissolved gas partial pressure to ambient pressure exceeds a particular ratio for a given tissue. The ratio may be the same for all tissue compartments or it may vary, and each compartment is allocated a specific critical supersaturation ratio, based on experimental observations.[18]
John Scott Haldane kavramını tanıttı half times to model the uptake and release of nitrogen into the blood. He suggested 5 tissue compartments with half times of 5, 10, 20, 40 and 75 minutes.[18] In this early hypothesis it was predicted that if the ascent rate does not allow the inert gas partial pressure in each of the hypothetical tissues to exceed the environmental pressure by more than 2:1 bubbles will not form.[70] Basically this meant that one could ascend from 30 m (4 bar) to 10 m (2 bar), or from 10 m (2 bar) to the surface (1 bar) when saturated, without a decompression problem. To ensure this a number of decompression stops were incorporated into the ascent schedules. The ascent rate and the fastest tissue in the model determine the time and depth of the first stop. Thereafter the slower tissues determine when it is safe to ascend further.[70] This 2:1 ratio was found to be too conservative for fast tissues (short dives) and not conservative enough for slow tissues (long dives). The ratio also seemed to vary with depth.[81] Haldane's approach to decompression modeling was used from 1908 to the 1960s with minor modifications, primarily changes to the number of compartments and half times used. The 1937 US Navy tables were based on research by O. D. Yarbrough and used 3 compartments: the 5- and 10-minute compartments were dropped. In the 1950s the tables were revised and the 5- and 10-minute compartments restored, and a 120-minute compartment added.[82]
1960'larda Robert D. Workman of U.S. Navy Experimental Diving Unit (NEDU) reviewed the basis of the model and subsequent research performed by the US Navy. Tables based on Haldane's work and subsequent refinements were still found to be inadequate for longer and deeper dives. Workman proposed that the tolerable change in pressure was better described as a critical pressure difference, and revised Haldane's model to allow each tissue compartment to tolerate a different amount of supersaturation which varies with depth. He introduced the term "M-value" to indicate the maximum amount of supersaturation each compartment could tolerate at a given depth and added three additional compartments with 160, 200 and 240-minute half times. Workman presented his findings as an equation which could be used to calculate the results for any depth and stated that a linear projection of M-values would be useful for computer programming.[82]
A large part of Albert A. Bühlmann 's research was to determine the longest half time compartments for Nitrogen and Helium, and he increased the number of compartments to 16. He investigated the implications of decompression after diving at altitude and published decompression tables that could be used at a range of altitudes. Bühlmann used a method for decompression calculation similar to that proposed by Workman, which included M-values expressing a linear relationship between maximum inert gas pressure in the tissue compartments and ambient pressure, but based on absolute pressure, which made them more easily adapted for altitude diving.[83] Bühlmann's algorithm was used to generate the standard decompression tables for a number of sports diving associations, and is used in several personal decompression computers, sometimes in a modified form.[83]
B.A. Hills and D.H. LeMessurier studied the empirical decompression practices of Okinawan inci dalgıçları içinde Torres boğazı and observed that they made deeper stops but reduced the total decompression time compared with the generally used tables of the time. Their analysis strongly suggested that bubble presence limits gas elimination rates, and emphasized the importance of inherent unsaturation of tissues due to metabolic processing of oxygen. This became known as the thermodynamic model.[69] More recently, recreational technical divers developed decompression procedures using deeper stops than required by the decompression tables in use. These led to the RGBM and VPM bubble models.[84] A deep stop was originally an extra stop introduced by divers during ascent, at a greater depth than the deepest stop required by their computer algorithm. There are also computer algorithms that are claimed to use deep stops, but these algorithms and the practice of deep stops have not been adequately validated.[85]
A "Pyle dur " is a deep stop named after Richard Pyle, an early advocate of deep stops,[86] at the depths halfway between the bottom and the first conventional decompression stop, and halfway between the previous Pyle stop and the deepest conventional stop, provided the conventional stop is more than 9 m shallower. A Pyle stop is about 2 minutes long. The additional ascent time required for Pyle stops is included in the dive profile before finalising the decompression schedule.[87] Pyle found that on dives where he stopped periodically to vent the swim-bladders of his fish specimens, he felt better after the dive, and based the deep stop procedure on the depths and duration of these pauses.[85] The hypothesis is that these stops provide an opportunity to eliminate gas while still dissolved, or at least while the bubbles are still small enough to be easily eliminated, and the result is that there will be considerably fewer or smaller venous bubbles to eliminate at the shallower stops as predicted by the thermodynamic model of Hills.[88]
- For example, a diver ascends from a maximum depth of 60 metres (200 ft), where the ambient pressure is 7 bars (100 psi), to a decompression stop at 20 metres (66 ft), where the pressure is 3 bars (40 psi). The first Pyle stop would take place at the halfway pressure, which is 5 bars (70 psi) corresponding to a depth of 40 metres (130 ft). The second Pyle stop would be at 30 metres (98 ft). A third would be at 25 metres (82 ft) which is less than 9 metres (30 ft) below the first required stop, and therefore is omitted.[87][89]
The value and safety of deep stops additional to the decompression schedule derived from a decompression algorithm is unclear. Decompression experts have pointed out that deep stops are likely to be made at depths where ingassing continues for some slow tissues, and that the addition of deep stops of any kind should be included in the hyperbaric exposure for which the decompression schedule is computed, and not added afterwards, so that such ingassing of slower tissues can be taken into account.[85] Deep stops performed during a dive where the decompression is calculated in real-time are simply part of a multi-level dive to the computer, and add no risk beyond that which is inherent in the algorithm.
There is a limit to how deep a "deep stop" can be. Some off-gassing must take place, and continued on-gassing should be minimised for acceptably effective decompression. The "deepest possible decompression stop" for a given profile can be defined as the depth where the gas loading for the leading compartment crosses the ambient pressure line. This is not a useful stop depth - some excess in tissue gas concentration is necessary to drive the outgassing diffusion, however this depth is a useful indicator of the beginning of the decompression zone, in which ascent rate is part of the planned decompression.[90]
Tarafından yapılan bir çalışma DAN in 2004 found that the incidence of high-grade bubbles could be reduced to zero providing the nitrogen concentration of the most saturated tissue was kept below 80 percent of the allowed M value and that an added deep stop was a simple and practical way of doing this, while retaining the original ascent rate.[84]
Diffusion limited tissues and the "Tissue slab", and series models
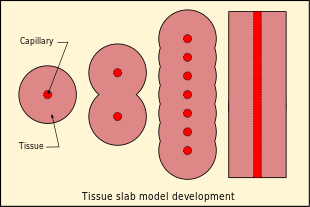
The assumption that diffusion is the limiting mechanism of dissolved gas transport in the tissues results in a rather different tissue compartment model. In this case a series of compartments has been postulated, with perfusion transport into one compartment, and diffusion between the compartments, which for simplicity are arranged in series, so that for the generalised compartment, diffusion is to and from only the two adjacent compartments on opposite sides, and the limit cases are the first compartment where the gas is supplied and removed via perfusion, and the end of the line, where there is only one neighbouring compartment.[83] The simplest series model is a single compartment, and this can be further reduced to a one-dimensional "tissue slab" model.[83]
Bubble models
Kabarcık decompression models are a rule based approach to calculating decompression based on the idea that microscopic bubble nuclei always exist in water and tissues that contain water and that by predicting and controlling the bubble growth, one can avoid decompression sickness. Most of the bubble models assume that bubbles will form during decompression, and that mixed phase gas elimination occurs, which is slower than dissolved phase elimination. Bubble models tend to have deeper first stops to get rid of more dissolved gas at a lower supersaturation to reduce the total bubble phase volume, and potentially reduce the time required at shallower depths to eliminate bubbles.[30][56][88]
Decompression models that assume mixed phase gas elimination include:
- The arterial bubble decompression model of the French Tables du Ministère du Travail 1992[56]
- The U.S. Navy Exponential-Linear (Thalmann) algorithm used for the 2008 US Navy air decompression tables (among others)[83]
- Hennessy's combined perfusion/diffusion model of the BSAC'88 tables
- The Varying Permeability Model (VPM) developed by D.E. Yount and others at the University of Hawaii[30]
- The Reduced Gradient Bubble Model (RGBM) developed by Bruce Wienke at Los Alamos National Laboratory[88]
Probabilistic models
Olasılık decompression models are designed to calculate the risk (or probability) of dekompresyon hastalığı (DCS) occurring on a given decompression profile.[80] These models can vary the dekompresyon duruşu depths and times to arrive at a final decompression schedule that assumes a specified probability of DCS occurring. The model does this while minimizing the total decompression time. This process can also work in reverse allowing one to calculate the probability of DCS for any decompression schedule.
Goldman Interconnected Compartment Model
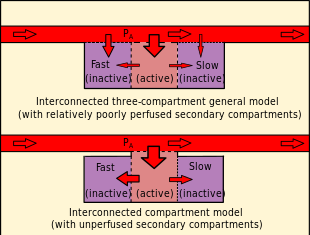
In contrast to the independent parallel compartments of the Haldanean models, in which all compartments are considered risk bearing, the Goldman model posits a relatively well perfused "active" or "risk-bearing" compartment in series with adjacent relatively poorly perfused "reservoir" or "buffer" compartments, which are not considered potential sites for bubble formation, but affect the probability of bubble formation in the active compartment by diffusive inert gas exchange with the active compartment.[52][91] During compression, gas diffuses into the active compartment and through it into the buffer compartments, increasing the total amount of dissolved gas passing through the active compartment. During decompression, this buffered gas must pass through the active compartment again before it can be eliminated. If the gas loading of the buffer compartments is small, the added gas diffusion through the active compartment is slow.[91] The interconnected models predict a reduction in gas washout rate with time during decompression compared with the rate predicted for the independent parallel compartment model used for comparison.[52]
The Goldman model differs from the Kidd-Stubbs series decompression model in that the Goldman model assumes linear kinetics, where the K-S model includes a quadratic component, and the Goldman model considers only the central well-perfused compartment to contribute explicitly to risk, while the K-S model assumes all compartments to carry potential risk. The DCIEM 1983 model associates risk with the two outermost compartments of a four compartment series.[52] The mathematical model based on this concept is claimed by Goldman to fit not only the Navy square profile data used for calibration, but also predicts risk relatively accurately for saturation profiles. A bubble version of the ICM model was not significantly different in predictions, and was discarded as more complex with no significant advantages. The ICM also predicted decompression sickness incidence more accurately at the low-risk recreational diving exposures recorded in DAN's Project Dive Exploration data set. The alternative models used in this study were the LE1 (Linear-Exponential) and straight Haldanean models.[91] The Goldman model predicts a significant risk reduction following a safety stop on a low-risk dive[92] and significant risk reduction by using nitrox (more so than the PADI tables suggest).[93]
Doygunluk dekompresyonu
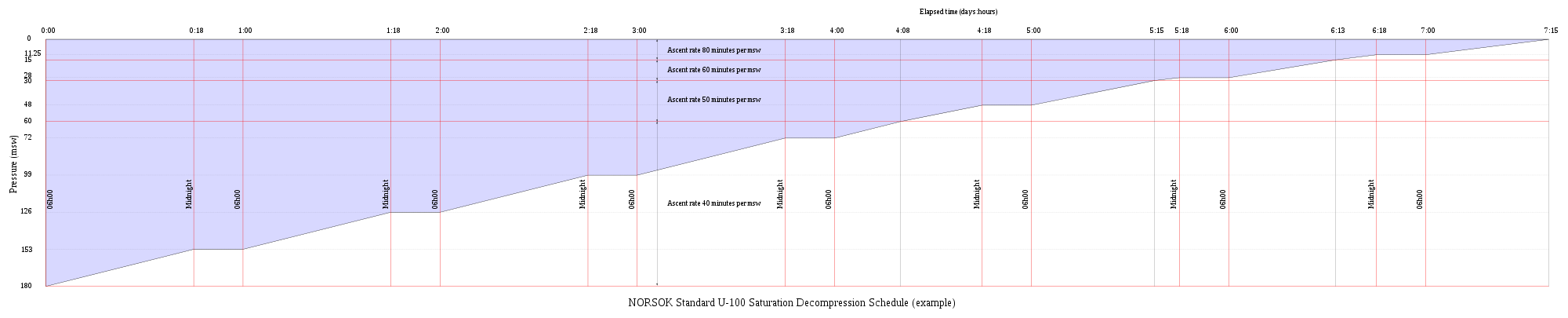
Saturation decompression is a physiological process of transition from a steady state of full saturation with inert gas at raised pressure to standard conditions at normal surface atmospheric pressure. It is a long process during which inert gases are eliminated at a very low rate limited by the slowest affected tissues, and a deviation can cause the formation of gas bubbles which can produce decompression sickness. Most operational procedures rely on experimentally derived parameters describing a continuous slow decompression rate, which may depend on depth and gas mixture.[94]
In saturation diving all tissues are considered saturated and decompression which is safe for the slowest tissues will theoretically be safe for all faster tissues in a parallel model. Direct ascent from air saturation at approximately 7 msw produces venous gas bubbles but not symptomatic DCS. Deeper saturation exposures require decompression to saturation schedules.[95]
The safe rate of decompression from a saturation dive is controlled by the partial pressure of oxygen in the inspired breathing gas.[96] The inherent unsaturation due to the oksijen penceresi allows a relatively fast initial phase of saturation decompression in proportion to the oxygen partial pressure and then controls the rate of further decompression limited by the half-time of inert gas elimination from the slowest compartment.[97] However, some saturation decompression schedules specifically do not allow an decompression to start with an upward excursion.[98] Neither the excursions nor the decompression procedures currently in use (2016) have been found to cause decompression problems in isolation, but there appears to be significantly higher risk when excursions are followed by decompression before non-symptomatic bubbles resulting from excursions have totally resolved. Starting decompression while bubbles are present appears to be the significant factor in many cases of otherwise unexpected decompression sickness during routine saturation decompression.[99]
Application of a bubble model in 1985 allowed successful modelling of conventional decompressions, altitude decompression, no-stop thresholds, and saturation dives using one setting of four global nucleation parameters.[100]
Research continues on saturation decompression modelling and schedule testing. In 2015 a concept named Extended Oxygen Window was used in preliminary tests for a modified saturation decompression model. This model allows a faster rate of decompression at the start of the ascent to utilise the inherent unsaturation due to metabolic use of oxygen, followed by a constant rate limited by oxygen partial pressure of the breathing gas. The period of constant decompression rate is also limited by the allowable maximum oxygen fraction, and when this limit is reached, decompression rate slows down again as the partial pressure of oxygen is reduced. The procedure remains experimental as of May 2016. The goal is an acceptably safe reduction of overall decompression time for a given saturation depth and gas mixture.[94]
Validation of models
It is important that any theory be validated by carefully controlled testing procedures. As testing procedures and equipment become more sophisticated, researchers learn more about the effects of decompression on the body. Initial research focused on producing dives that were free of recognizable symptoms of decompression sickness (DCS). With the later use of Doppler ultrasound testing, it was realized that bubbles were forming within the body even on dives where no DCI signs or symptoms were encountered. This phenomenon has become known as "silent bubbles". The US Navy 1956 tables were based on limits determined by external DCS signs and symptoms. Later researchers were able to improve on this work by adjusting the limitations based on Doppler testing. However the US Navy CCR tables based on the Thalmann algorithm also used only recognisable DCS symptoms as the test criteria.[101][102] Since the testing procedures are lengthy and costly, it is common practice for researchers to make initial validations of new models based on experimental results from earlier trials. This has some implications when comparing models.[103]
Güncel araştırma
Research on decompression continues. Data is not generally available on the specifics, however Divers Alert Network (DAN) has an ongoing vatandaş bilimi based programme run by DAN (Europe) which gathers data from volunteer eğlence dalgıçları for analysis by DAN research staff and other researchers. This research is funded by subscription fees of DAN Europe members.[104] The Diving Safety Laboratory is a database to which members can upload dive profiles from a wide range of dive computers converted to a standard format and other data about the dive.[105] Data on hundreds of thousands of real dives is analysed to investigate aspects of diving safety.[106] The large amounts of data gathered is used for probabilistic analysis of decompression risk. The data donors can get immediate feedback in the form of a simple risk analysis of their dive profiles rated as one of three nominal levels of risk (high, medium and low) based on comparison with Bühlmann ZH16c M-values computed for the same profile.
Listed projects (not all directly related to decompression) include:[107]
- Gathering data on vascular gas bubbles and analysis of the data
- Identification of optimised ascent profile
- Investigating the causes of unexplained diving incidents
- Stress in recreational diving
- Correlation between patent foramen ovale (PFO) and risk of decompression illness
- Diving with astım ve diyabet and managing the associated risk
- Physiology and pathophysiology of breath-hold
- Hypothermia and diving
- Headache and diving
- Blood changes associated with diving
- Decompression risk of air travel after diving
- Physiological effects of rebreather diving
- Effects of decompression stress on endothelial stem cells and blood cells
- Early decompression stress biomarkers
- The effects of normobaric oxygen on blood and in DCI first aid
Practical effectiveness of models
Bubble models for decompression were popular among technical divers in the early 2000s, although there was little data to support the effectiveness of the models in practice. Since then, several comparative studies have indicated relatively larger numbers of venous gas emboli after decompression based on bubble models, and one study reported a higher rate of decompression sickness. The deeper decompression stops earlier in the ascent appear to be less effective at controlling bubble formation than the hypotheses suggested. This failure may be due to continued ingassing of slower tissues during the extended time at greater depth, resulting in these tissues being more supersaturated at shallower depths. The optimal decompression strategy for deep bounce dives remains unknown (2016).[108]
The practical efficacy of gas switches from helium based diluent to nitrox for accelerating decompression has not been demonstrated convincingly. These switches increase risk of inner ear decompression sickness due to counterdiffusion effects.[108]
Teaching of decompression theory and tables
Decompression is an area where you discover that, the more you learn, the more you know that you really don't know what is going on. For behind the "black-and-white" exactness of table entries, the second-by-second countdowns of dive computers, and beneath the mathematical purity of decompression models, lurks a dark and mysterious physiological jungle that has barely been explored.
— Karl E. Huggins, 1992[109]
Exposure to the various theories, models, tables and algorithms is needed to allow the diver to make educated and knowledgeable decisions regarding their personal decompression needs.[110] Temel dekompresyon teorisi ve dekompresyon tablolarının kullanımı, ticari dalgıçlar için eğitimin teori bileşeninin bir parçasıdır.[111] ve dekompresyon tablolarına dayalı dalış planlaması ve dekompresyon uygulaması ve saha yönetimi dalış süpervizörünün işinin önemli bir parçasıdır.[112][113] Rekreasyon dalgıçları, sertifika veren kuruluşun her sertifika için eğitim standardında belirttiği ölçüde dekompresyon teorisi ve uygulaması konusunda eğitilir. Bu, dalgıcın giriş seviyesindeki dalgıçlar için dekompresyon zorunluluğundan kaçınmasına, kişisel dalış bilgisayarları, dekompresyon yazılımı ve ileri teknik dalgıçlar için tablolar aracılığıyla çeşitli dekompresyon algoritmalarının kullanımındaki yeterliliğine izin verecek kadar basit bir genel bakıştan farklılık gösterebilir.[72] Dekompresyon teorisinin ayrıntılı olarak anlaşılması, ne ticari ne de rekreasyonel dalgıçlar için genellikle gerekli değildir.
Ayrıca bakınız
- Dekompresyon (dalış) - Hiperbarik maruziyetten sonra su altı dalgıçları üzerindeki ortam basıncının azaltılması ve dalgıç dokularından çözünmüş gazların giderilmesi
- Dekompresyon uygulaması – Techniques and procedures for safe decompression of divers
- Dekompresyon hastalığı - Çevreleyen basıncın düşürülmesi sırasında kabarcık oluşturan dokularda çözünmüş gazların neden olduğu bozukluk
- Dekompresyon araştırma ve geliştirme tarihi - Dalış dekompresyon tarihindeki önemli olayların kronolojik listesi.
Notlar
- 1. ^ a autochthonous: formed or originating in the place where found
Referanslar
- ^ a b c d e f g US Navy 2008, Vol 1 Chpt. 3 Sec. 9.3
- ^ Van Liew, HD; Conkin, J. (2007). A start toward micronucleus-based decompression models: Altitude decompression. Undersea and Hyperbaric Medical Society, Inc. Annual Scientific Meeting, 14–16 June 2007. Ritz-Carlton Kapalua Maui, Hawaii (http://www.uhms.org ). Alındı 26 Kasım 2015.
- ^ "Altitude-induced Decompression Sickness" (PDF). Federal Havacılık İdaresi. Alındı 21 Şubat 2012.
- ^ US Navy 2008, Cilt. 5 Chpt. 20 Sect. 3.1
- ^ Gorman, Des. "Decompression theory" (PDF). Avustralya Kraliyet Donanması. Alındı 9 Şubat 2016.
- ^ a b c Wienke, B.R. "Decompression theory" (PDF). Alındı 9 Şubat 2016.
- ^ a b c d e f g h Huggins 1992, chpt. 1
- ^ Young, C.L.; Battino, R.; Clever, H.L. (1982). "The solubility of gases in liquids" (PDF). Alındı 9 Şubat 2016.
- ^ Hill, John W.; Petrucci, Ralph H. (1999). Genel Kimya (2. baskı). Prentice Hall.
- ^ Henry, W. (1803). "Experiments on the quantity of gases absorbed by water, at different temperatures, and under different pressures". Phil. Trans. R. Soc. Lond. 93: 29–274. doi:10.1098/rstl.1803.0004.
- ^ P. Cohen, ed. (1989). The ASME handbook on Water Technology for Thermal Power Systems. Amerikan Makine Mühendisleri Derneği. s. 442.
- ^ Kasture, A.V. (Ekim 2008). "5. Solubility of pharmaceuticals: Factors affecting solubility". Pharmaceutical Chemistry - I. Pragati Books Pvt. Ltd. s. 5.3. ISBN 9788185790121. Alındı 7 Mart 2016.
- ^ Burton, Steve (December 2004). "Isobaric Counter Diffusion". ScubaEngineer. Alındı 3 Şubat 2011.
- ^ Huggins 1992, chpt. 9-page 6
- ^ "15: Mixed gas and oxygen diving". The NOAA Diving Manual: Diving for Science and Technology (resimli ed.). DIANE Yayıncılık. 1992. s. 15.1. ISBN 9781568062310. Alındı 8 Mart 2016.
- ^ a b Hills, Brian A (1978). "Effect of decompression per se on nitrogen elimination". J Appl Physiol. 45 (6): 916–921. doi:10.1152/jappl.1978.45.6.916. PMID 730597.
- ^ a b Pittman, RN (2011). "Chapter 2: The Circulatory System and Oxygen Transport". Regulation of Tissue Oxygenation. San Rafael (CA): Morgan & Claypool Life Sciences.
- ^ a b c d Huggins 1992, chpt. 2
- ^ a b Bookspan, Jolie (June 2005). "Are Tissue Halftimes Real?". DAN Mediucal articles. Divers Alert Network. Alındı 8 Mart 2016.
- ^ Huggins 1992, chpt. 1 page 7
- ^ a b Hills, Brian A (1978). "A fundamental approach to the prevention of decompression sickness". South Pacific Underwater Medicine Society Journal. 8 (2): 20–47. ISSN 0813-1988. OCLC 16986801. Alındı 31 Ekim 2011.
- ^ Wienke 2002, s. 10
- ^ Behnke, Albert R (1967). "The isobaric (oxygen window) principle of decompression". Trans. Third Marine Technology Society Conference, San Diego. The New Thrust Seaward. Washington DC: Marine Technology Society. Alındı 19 Haziran 2010.
- ^ Van Liew, Hugh D; Conkin, J; Burkard, ME (1993). "Oksijen penceresi ve dekompresyon kabarcıkları: tahminler ve önemi". Havacılık, Uzay ve Çevre Tıbbı. 64 (9): 859–65. ISSN 0095-6562. PMID 8216150.
- ^ a b c d Papadopoulou, Virginie; Robert J. Eckersley; Costantino Balestra; Thodoris D. Karapantsios; Meng-Xing Tang (2013). "A critical review of physiological bubble formation in hyperbaric decompression". Kolloid ve Arayüz Bilimindeki Gelişmeler. Elsevier. 191-192 (191–192): 22–30. doi:10.1016/j.cis.2013.02.002. hdl:10044/1/31585. PMID 23523006.
- ^ a b Yount 1991, s. 131.
- ^ Yount 1991, s. 132.
- ^ Hills BA (March 1992). "A hydrophobic oligolamellar lining to the vascular lumen in some organs". Denizaltı Biomed Res. 19 (2): 107–20. PMID 1561717. Alındı 31 Ekim 2011.
- ^ Tikuisis, P (1993). "Theoretical considerations for in vivo nucleation of bubbles". Abstract of the Undersea and Hyperbaric Medical Society, Inc. Annual Scientific Meeting held July 7–10, 1993. World Trade and Convention Centre, Halifax, Nova Scotia, Canada. Denizaltı ve Hiperbarik Tıp Derneği, Inc. Alındı 8 Mart 2016.
- ^ a b c d e f Yount 1991.
- ^ Campbell, Ernest S. (1997). "Decompression Illness in Sports Divers: Part I". Medscape Orthopaedics & Sports Medicine eJournal, 1(5). Orange Beach, Ala.: Medscape Portals, Inc. Archived from orijinal 29 Ocak 2010. Alındı 14 Mart 2016.
- ^ a b c d Yount, David E. (2002). "Dekompresyon teorisi - Kabarcık modelleri: VPM'yi dalışa uygulama" (PDF). Dalış Bilimi. Derin Okyanus Dalışı. s. 8. Alındı 11 Mart 2016.
- ^ a b c d e f g h ben j k Vann, Richard D (1989). Vann, Richard D (ed.). The Physiological Basis of Decompression: An overview. Proceedings of the thirty-eighth undersea and hyperbaric medical society workshop. Bethesda, Maryland: Undersea and Hyperbaric Medical Society. s. 1–10. Alındı 12 Mart 2016.
- ^ a b c d Stephenson, Jeffrey (2016). "Pathophysiology, treatment and aeromedical retrieval of SCUBA – related DCI". Askeri ve Gazi Sağlığı Dergisi. Australasian Military Medicine Association. 17 (3). ISSN 1839-2733.
- ^ Yount 1991, pp. 131,136.
- ^ a b c d e f Lambertson, Christian J (1989). Vann, RD. (ed.). Relations of isobaric gas counterdiffusion and decompression gas lesion diseases. The Physiological Basis of Decompression. 38th Undersea and Hyperbaric Medical Society Workshop UHMS Publication Number 75(Phys)6-1-89. Alındı 10 Ocak 2010.
- ^ a b c Hamilton & Thalmann 2003, s. 477–478.
- ^ a b c D'Aoust, BG; White, R; Swanson, H; Dunford, RG; Mahoney, J (1982). Differences in Transient and Steady State Isobaric Counterdiffusion. Report to the Office of Naval Research (Bildiri). Alındı 10 Ocak 2010.
- ^ Masurel, G; Gutierrez, N; Giacomoni, L (1987). "Hydrogen dive and decompression". Abstract of the Undersea and Hyperbaric Medical Society, Inc. Annual Scientific Meeting held May 26–30, 1987. The Hyatt Regency Hotel, Baltimore, Maryland. Denizaltı ve Hiperbarik Tıp Derneği, Inc. Alındı 14 Mart 2016.
- ^ a b Doolette, David J; Mitchell, Simon J (Haziran 2003). "İç kulak dekompresyon hastalığı için biyofiziksel temel". Uygulamalı Fizyoloji Dergisi. 94 (6): 2145–50. doi:10.1152 / japplphysiol.01090.2002. PMID 12562679.
- ^ Ay, Richard E; Kisslo, Joseph (1998). "PFO and decompression illness: An update". South Pacific Underwater Medicine Society Journal. 28 (3). ISSN 0813-1988. OCLC 16986801. Arşivlenen orijinal 5 Ağustos 2009. Alındı 31 Ekim 2011.
- ^ Staff (May 2014). "Pathophysiology". Medscape İlaçları ve Hastalıkları. Medscape. pp. Organ involvement associated with decompression sickness. Alındı 8 Mart 2016.
- ^ Kitano, Motoo (1995). "Pathological Aspects of Decompression Sicknes". 南太平洋海域調査研究報告=Occasional papers, Volume 25.鹿児島大学: 47–59. hdl:10232/16803.
- ^ Brubakk, A. O .; T. S. Neuman (2003). Bennett ve Elliott'ın fizyolojisi ve dalış tıbbı (5. Rev bas.). Amerika Birleşik Devletleri: Saunders Ltd. s. 800. ISBN 0-7020-2571-2.
- ^ Gernhardt, ML (2006). Lang, MA; Smith, NE (editörler). "300 FSW'ye Yüzey Tedarikli Karışık Gaz Dalışı için Biyomedikal ve Operasyonel Hususlar". İleri Bilimsel Dalış Çalıştayı Bildirileri. Washington, DC: Smithsonian Enstitüsü. Arşivlenen orijinal 5 Ağustos 2009. Alındı 21 Ekim 2013.
- ^ Scharlin, P.; Battino, R.; Silla, E.; Tuñón, I.; Pascual-Ahuir, J. L. (1998). "Solubility of gases in water: Correlation between solubility and the number of water molecules in the first solvation shell". Saf ve Uygulamalı Kimya. 70 (10): 1895–1904. doi:10.1351/pac199870101895. S2CID 96604119.
- ^ Clifford A. Hampel (1968). The Encyclopedia of the Chemical Elements. New York: Van Nostrand Reinhold. s. 256–268. ISBN 0-442-15598-0.
- ^ Williams, S.T.; Prior, F; Bryson, P.J. (2005). "Haematocrit change in recreational Scuba divers following single dive exposure".
- ^ Mouret, GML (2006). "Obesity and diving". Güney Pasifik Sualtı Tıbbı Derneği Dergisi. Victoria, Australia: South Pacific Underwater Medicine Society. Alındı 8 Mart 2016.
- ^ Bookspan, J (Mayıs 2003). "İnsanlarda yüksek irtifada endojen gaz fazı oluşumunun tespiti". Spor ve Egzersizde Tıp ve Bilim. 35 (5): S164. doi:10.1097/00005768-200305001-00901. Alındı 7 Mayıs 2012.
- ^ Huggins 1992, chpt. 4
- ^ a b c d e Goldman, Saul (19 Nisan 2007). "Tüplü dalışta dekompresyon hastalığı olasılığını tahmin etmek için yeni bir biyofiziksel model sınıfı". Uygulamalı Fizyoloji Dergisi. 103 (2): 484–493. doi:10.1152 / japplphysiol.00315.2006. PMID 17446410.
- ^ Kuch, Benjamin; Buttazzo, Giorgio; Sieber, Arne (2011). "Düşük güçlü bir mikro denetleyicide uygulama için optimize edilmiş kabarcık modeli tabanlı dekompresyon algoritması" (PDF). International Journal of the Society for Underwater Technology. Sualtı Teknolojisi Derneği. 29 (4): 195–202. doi:10.3723 / ut.29.195. Alındı 14 Mart 2016.
- ^ Huggins 1992, Giriş. sayfa 2
- ^ a b Gorman, Desmond F; Pearce, A; Webb, RK (1988). "1987 Kraliyet Adelaide Hastanesi'nde tedavi edilen disbarik hastalık, bir faktör analizi". South Pacific Underwater Medicine Society Journal. 18 (3): 95–101.
- ^ a b c d Imbert, JP; Paris, D; Hugon, J (2004). Dekompresyon Tablo Hesaplamaları için Arteriyel Kabarcık Modeli (PDF). EUBS 2004. Fransa: Divetech.
- ^ a b Gorman, Des F (1989). "Dekompresyon tabloları: kullanımları ve sorunları". South Pacific Underwater Medicine Society Journal. 19 (3): 111–113. Alındı 31 Ekim 2011.
- ^ Huggins, Karl E. (1981). Doppler Ultrasonik Kabarcık Algılama ile Belirlenen Dekompresyonsuz Sınırlara Dayalı Yeni Dekompresyonsuz Tablolar. Rapor # MICHU-SG-81-205 (Bildiri). Michigan Sea Grant Koleji Programı.
- ^ a b Bühlmann Albert A. (1984). Dekompresyon-Dekompresyon Hastalığı. Berlin New York: Springer-Verlag. ISBN 978-0-387-13308-9.
- ^ a b Blogg, S.L .; M.A. Lang; A. Møllerløkken, editörler. (2012). "Dalış Bilgisayarlarının Doğrulanması Çalıştayı". Avrupa Sualtı ve Baromedikal Derneği Sempozyumu, 24 Ağustos 2011. Gdansk. Trondheim: Norveç Bilim ve Teknoloji Üniversitesi. Alındı 7 Mart 2013.
- ^ Yount 1991, s. 137.
- ^ "Dalış Bilgisayarları ve Dalış Simülasyonları". LogoDalış. Alındı 11 Mart 2016.
- ^ a b c Maiken, Eric (1995). "Bölüm I: arka plan ve teori. Kabarcık fiziği". Kabarcık Dekompresyon Stratejileri. Alındı 11 Mart 2016.
- ^ Wienke, Bruce R. (1990). Michael A. Lang; Glen H. Egstrom (editörler). "Faz dinamikleri ve dalış" (PDF). AAUS Güvenli Yükselişlerin Biyomekaniği Çalıştayı Bildirileri. Costa Mesa CA .: Amerikan Sualtı Bilimi Akademisi. s. 13–29. Alındı 8 Mart 2016.
- ^ Yount, David E. (1990). Michael A. Lang; Glen H. Egstrom (editörler). "Kabarcık oluşumunun fiziği" (PDF). AAUS Güvenli Yükselişlerin Biyomekaniği Çalıştayı Bildirileri. Costa Mesa CA .: Amerikan Sualtı Bilimi Akademisi. s. 13–29. Alındı 8 Mart 2016.
- ^ a b c d Wienke, BR (1989). "Doku gazı değişim modelleri ve dekompresyon hesaplamaları: bir inceleme". Denizaltı Biyomedikal Araştırma. Denizaltı ve Hiperbarik Tıp Derneği, Inc. 16 (1): 53–89. PMID 2648656. Alındı 7 Mart 2016.
- ^ a b Baker Erik (1998). "M değerlerini anlamak". Batık. 3 (3): 23–27.
- ^ a b c d Anttila, Matti. "Gradyan Faktörleri". Alındı 2 Mayıs 2012.
- ^ a b c d e f LeMessurier, H; Hills, B.A. (1965). "Dekompresyon Hastalığı. Torres Boğazı dalış teknikleri üzerine yapılan bir çalışmadan ortaya çıkan bir termodinamik yaklaşım". Hvalradets Skrifter. 48: 54–84.
- ^ a b c Boykot, AE; Damant, GCC; Haldane, John Scott (1908). "Basınçlı hava hastalığının önlenmesi". Hijyen Dergisi. 8 (3): 342–443. doi:10.1017 / S0022172400003399. PMC 2167126. PMID 20474365. Arşivlenen orijinal 24 Mart 2011 tarihinde. Alındı 30 Mayıs 2010.
- ^ Huggins 1992, chpt. 3 sayfa 2
- ^ a b Beresford, M .; Southwood, P. (2006). CMAS-ISA Normoxic Trimix Kılavuzu (4. baskı). Pretoria, Güney Afrika: CMAS Eğitmenleri Güney Afrika.
- ^ İşçi, Robert D (1957). "Hava doygunluğu dekompresyon tablolarının hesaplanması". Donanma Deneysel Dalış Birimi Teknik Raporu. NEDU-RR-11-57. Arşivlenen orijinal 18 Eylül 2011'de. Alındı 31 Ekim 2011.
- ^ Yount, David E .; Hoffman, DC (1984). Bachrach A.J .; Matzen, M.M. (eds.). "Dekompresyon teorisi: dinamik bir kritik hacim hipotezi" (PDF). Sualtı fizyolojisi VIII: Sualtı fizyolojisi üzerine sekizinci sempozyum bildirileri. Bethesda: Denizaltı Tıp Derneği. s. 131–146. Arşivlenen orijinal (PDF) 13 Mart 2016 tarihinde. Alındı 12 Mart 2016.
- ^ Kindwall, Eric P; Baz, A; Lightfoot, EN; Lanphier, Edward H; Seireg, A (1975). "Dekompresyon sırasında insanda azot giderimi". Denizaltı Biyomedikal Araştırma. 2 (4): 285–297. ISSN 0093-5387. OCLC 2068005. PMID 1226586. Arşivlenen orijinal 27 Temmuz 2011'de. Alındı 31 Ekim 2011.
- ^ a b Berghage, TE (1978). "Dekompresyon Teorisi". Savunma Bakanlığı ve Savunma Teknik Bilgi Merkezi. Alındı 8 Mart 2016.
- ^ Huggins 1992
- ^ Lang, Michael A; Vann Richard D (1991). AAUS Tekrarlayan Dalış Çalıştayı Bildirileri. Duke Üniversitesi, Durham, NC: Amerikan Sualtı Bilimleri Akademisi. s. 339. Alındı 31 Ekim 2011.
- ^ Cole, Bob (2008). "Dalgıç Davranışı - Mikro-kabarcık Kontrolü". SAA Buhlmann Derin Durdurma Sistemi El Kitabı. Alt Su Derneği. sayfa 4–2. ISBN 978-0-9532904-8-2.
SAA, vücudunuzun gazdan çıkmasına ve normal bir düzeye dönmesine izin vermek için en az yedinci gün izin almanızı önerir.
- ^ a b c Doolette David J (2005). "Belirleyici ve olasılıklı dekompresyon modellerinin geliştirilmesi ve test edilmesi". South Pacific Underwater Medicine Society Journal. 35 (1). Alındı 10 Ocak 2012.
- ^ Huggins 1992, Chpt. 3 sayfa 2-3
- ^ a b Huggins 1992, Chpt. 3
- ^ a b c d e Huggins 1992, Chpt. 4
- ^ a b Bennett, Peter B; Alessandro Marroni; Frans J. Cronjé (2004). "Derin Duraklar: Başka Bir Güvenlik Marjında Bir Güvenlik Durdurma Yapısının Yarı Derinliğinin Yarısını Ekleyebilir mi?". Alert Diver. Divers Alert Network (Mayıs / Haziran 2004).
- ^ a b c Denoble, Petar (Kış 2010). "Derin duraklar". Alert Diver. Dalgıç Uyarı Ağı. Alındı 3 Ağustos 2015.
- ^ "Decoweenie Kılavuzu" (PDF). decoweenie.com. Arşivlenen orijinal (PDF) 6 Eylül 2008'de. Alındı 26 Eylül 2008.
- ^ a b Pyle Richard L (1997). "Derin güvenlik duraklarının önemi: Dekompresyon dalışlarından yükselme modellerini yeniden düşünmek". South Pacific Underwater Medicine Society Journal (Yeniden basıldı: Deep Tech). 27 (2). Alındı 31 Ekim 2011.
- ^ a b c Wienke 2002
- ^ Pyle, Richard L (27 Eylül 2007). "Derin Dekompresyon Dururları". Bishop Müzesi. Alındı 9 Eylül 2009.
- ^ Baker, Erik C. "Derin Duraklarla İlgili Kafa Karışıklığı Giderme'" (PDF). Alındı 4 Ağustos 2015.
- ^ a b c Goldman, Saul; Goldman, Ethel (2010). "Yakında yakınınızdaki bir Dalış Bilgisayarına geliyor" (PDF). Alert Diver (Avrupa Sürümü). Roseto degli Abruzzi, İtalya: DAN Europe (4. çeyrek, 2010): 4–8.
- ^ Goldman, Saul; Goldman, Ethel (2014). "Durmak ya da durmamak ve neden?" (PDF). Alert Diver. DAN Güney Afrika. 6 (2): 34–37. ISSN 2071-7628. Alındı 10 Eylül 2014.
- ^ Goldman, Saul (23 Eylül 2013). "SAUL'un PADI dalış tabloları ile ilişkisi". Modern dekompresyon. Alındı 10 Eylül 2014.
- ^ a b Kot, Jacek; Sicko, Zdzislaw; Doboszynski, Tadeusz (2015). "Hava ve Nitroks Kullanarak Doygunluk Dekompresyonlarını Programlamak için Genişletilmiş Oksijen Penceresi Konsepti". PLOS ONE. 10 (6): 1–20. Bibcode:2015PLoSO..1030835K. doi:10.1371 / journal.pone.0130835. PMC 4482426. PMID 26111113.
- ^ Eckenhoff, R.G .; Osborne, SF; Parker, JW; Bondi, KR (1986). "Sığ hava doygunluğundan doğrudan çıkış". Denizaltı Biyomedikal Araştırma. Denizaltı ve Hiperbarik Tıp Derneği, Inc. 13 (3): 305–16. PMID 3535200. Alındı 5 Nisan 2016.
- ^ Vann, R.D. (Mart 1984). "Doygunluk Dalışlarından Dekompresyon". 3. yıllık Kanada Okyanus Teknolojisi Kongresi Bildirileri. Toronto Kanada. s. 175–186. Alındı 5 Nisan 2016.
- ^ Doboszynski, T; Sicko, Z; Kot, J (2012). "Hava, nitroks, helioks ve trimix doygunluk maruziyetlerinden sonra oksijenle çalışan dekompresyon". Denizaltı ve Hiperbarik Tıp Derneği Dergisi. Denizaltı ve Hiperbarik Tıp, Inc. Alındı 5 Nisan 2016.
- ^ Personel (Nisan 2009). NORSOK Standard U-100: İnsanlı su altı operasyonları (3. baskı). Lysaker, Norveç: Standartlar Norveç.
- ^ Flook Valerie (2004). Doygun dalışta gezi tabloları - mevcut İngiltere uygulamasının dekompresyon etkileri ARAŞTIRMA RAPORU 244 (PDF). Aberdeen Birleşik Krallık: Sağlık ve Güvenlik Yöneticisi için Unimed Scientific Limited tarafından hazırlanmıştır. ISBN 0-7176-2869-8. Alındı 27 Kasım 2013.
- ^ Hoffman, D.C .; Yount, DE (1985). "Küçük kabarcık helyum dekompresyon tabloları". Denizaltı ve Hiperbarik Tıp Derneği, Inc. Yıllık Bilimsel Toplantısı Özeti. Denizaltı ve Hiperbarik Tıp Derneği, Inc. Alındı 5 Nisan 2016.
- ^ Thalmann 1984, s. 24
- ^ Thalmann 1985, s. 5
- ^ Huggins 1992, Chpt. 10
- ^ Personel. "DAN Research Hakkında". DAN Europe web sitesi. DAN Europe. Alındı 13 Şubat 2016.
- ^ Personel. "Dalış Profilinizi Gönderin". DAN Europe web sitesi. DAN Europe. Alındı 13 Şubat 2016.
- ^ Personel. "DAN Araştırma Dalıcısı Olun". DAN Europe web sitesi. DAN Europe. Alındı 13 Şubat 2016.
- ^ Personel. "Projelerimiz". DAN Europe web sitesi. Alındı 13 Şubat 2016.
- ^ a b Mitchell, Simon J. (2016). Pollock, KB; Satıcılar, SH; Godfrey, JM (editörler). Dekompresyon Bilimi: Kritik Gaz Değişimi (PDF). Rebreathers ve Bilimsel Dalış. NPS / NOAA / DAN / AAUS Bildirileri 16–19 Haziran 2015 Çalıştayı. Wrigley Deniz Bilimleri Merkezi, Catalina Adası, CA. s. 163–1 74.
- ^ Huggins 1992, Giriş sayfası 3
- ^ Huggins 1992, Giriş sayfası 2
- ^ "Uluslararası Dalgıç Eğitimi Sertifikası: Dalgıç Eğitim Standartları" (PDF) (4. revizyon). IDSA. Ekim 2009. Arşivlenen orijinal (PDF) 3 Mart 2016 tarihinde. Alındı 14 Mart 2016. Erişim tarihi 13 Eylül 2013
- ^ Personel (2002). Paul Williams (ed.). Dalış Süpervizörünün El Kitabı (IMCA D 022 Mayıs 2000, Mayıs 2002 yazı dizisini içeren). Carlyle House, 235 Vauxhall Bridge Road, Londra SW1V 1EJ, İngiltere: Uluslararası Deniz Müteahhitleri Birliği. ISBN 978-1-903513-00-2.CS1 Maint: konum (bağlantı)
- ^ ABD Donanması 2008
Kaynaklar
- Hamilton, Robert W; Thalmann, Edward D (2003). "10.2: Dekompresyon Uygulaması". Brubakk, Alf O; Neuman, Tom S (editörler). Bennett ve Elliott'ın fizyolojisi ve dalış tıbbı (5. Revize ed.). Amerika Birleşik Devletleri: Saunders. s. 455–500. ISBN 978-0-7020-2571-6. OCLC 51607923.
- Huggins, Karl E. (1992). "Dekompresyon dinamikleri atölyesi". Michigan Üniversitesinde Verilen Ders. Alındı 10 Ocak 2012.
- Thalmann, E.D. (1984). "ABD Donanması su altı dekompresyon bilgisayarında kullanılmak üzere dekompresyon algoritmalarının Faz II testi". Donanma Uzm. Dalış Birimi Arş. Bildiri. 1–84. Alındı 16 Mart 2008.
- Thalmann, E.D. (1985). "Helyum Dalışında Sabit Oksijen Kısmi Basıncı için Dekompresyon Algoritmasının Geliştirilmesi". Donanma Uzm. Dalış Birimi Arş. Bildiri. 1–85. Alındı 16 Mart 2008.
- ABD Donanması (2008). ABD Donanması Dalış Kılavuzu, 6. revizyon. Amerika Birleşik Devletleri: ABD Deniz Deniz Sistemleri Komutanlığı. Alındı 15 Haziran 2008.
- Wienke, Bruce R; O'Leary, Timothy R (13 Şubat 2002). "Azaltılmış gradyan balon modeli: Dalış algoritması, temeli ve karşılaştırmaları" (PDF). Tampa, Florida: NAUI Teknik Dalış Operasyonları. Alındı 25 Ocak 2012.
- Yount, DE (1991). Hans-Jurgen, K; Harper Jr, DE (editörler). "Jelatin, kabarcıklar ve kıvrımlar". International Pacifica Scientific Diving ..., (American Academy of Underwater Sciences Onbirth Annual Scientific Diving Symposium'un Bildirileri 25-30 Eylül 1991'de Gerçekleştirildi. University of Hawaii, Honolulu, Hawaii). Alındı 25 Ocak 2012.
daha fazla okuma
- Ball, R; Himm, J; Homer, LD; Thalmann, ED (1995). "Kabarcık evriminin zaman akışı dekompresyon hastalığı riskini açıklıyor mu?". Denizaltı ve Hiperbarik Tıp. 22 (3): 263–280. ISSN 1066-2936. PMID 7580767.
- Gerth, Wayne A; Doolette, David J. (2007). "VVal-18 ve VVal-18M Thalmann Algoritması - Hava Dekompresyon Tabloları ve Prosedürleri". Navy Deneysel Dalış Ünitesi, TA 01-07, NEDU TR 07-09. Alındı 27 Ocak 2012.
- Gribble, M. de G. (1960); Dekompresyon hastalığının Yüksek İrtifa ve Yüksek Basınç sendromlarının bir karşılaştırması, Br. J. Ind. Med., 1960, 17, 181.
- Hills. B. (1966); Dekompresyon hastalığına termodinamik ve kinetik bir yaklaşım. Tez
- Lippmann, John; Mitchell, Simon (2005). Dalışta Daha Derin (2. baskı). Melbourne, Avustralya: J L Publications. ISBN 0-9752290-1-X.
- Parker, E. C .; S.S. Survanshi; P.K. Weathersby ve E.D. Thalmann (1992). "İstatistik Tabanlı Dekompresyon Tabloları VIII: Doğrusal Üstel Kinetik". Deniz Tıbbi Araştırma Enstitüsü Raporu. 92-73. Alındı 16 Mart 2008.
- Powell, Mark (2008). Dalgıçlar için Deco. Southend-on-Sea: Aquapress. ISBN 978-1-905492-07-7.
